文档内容
第十一单元技能过关训练
可能用到相对原子质量 H:1 O:16 Na:23
一、选择题(每小题1分,共10分,每小题只有一个选项符合题意)
1.下列几组物质按酸、碱、盐顺序排列的是 ( )
A.KNO、NaOH、HCl B.Ca(OH)、HCl、NaCl
3 2
C.HSO、NaCO、Ba(OH) D.HNO、KOH、CuSO
2 4 2 3 2 3 4
2.张聪同学的午餐如下,其中富含蛋白质的食品是
A.大米饭 B.鱼香肉丝 C.炒白菜 D.酸菜粉丝汤
3.下列化肥属于复合肥的是 ( )
A.NHHPO B. NaNO C.KSO D.NHHCO
4 2 4 3 2 4 4 3
4.下列做法符合环保要求的是 ( )
A.造纸厂的碱性污水直接排放到小河中
B.炼铁厂的废气中含有大量的CO未经处理直接排放到空气中
C.农业上合理高效地使用农药、化肥
D.使用过的干电池直接丢入垃圾堆中
5.食品安全关系人民健康,下列食品属于安全食品的是
A.添加瘦肉精饲养的猪肉 B.用化工原料染色的馒头
C.用甲醛浸泡过的毛肚 D.加碳酸氢钠焙制的糕点
6.“羊毛出在羊身上”,羊毛的主要成分是 ( )
A.纤维素 B.脂肪 C.蛋白质 D.糖类
7.下列各组溶液,相互能发生反应的是 ( )
①碳酸钠和氯化钙 ②氢氧化钾和盐酸 ③硫酸和氯化钠
④碳酸钠和氯化钠 ⑤氯化钠和氢氧化钙
A.①② B.④⑤ C.③⑤ D.①③
8.下列叙述中,正确的是 ( )
A.酸和碱中都一定含有氢、氧两种元素
B.能跟碱反应生成盐和水的化合物不一定是酸
C.有盐参加的反应都是复分解反应
D.生成盐和水的反应都是中和反应
9.下列几组物质中能按照右边关系图进行转化的一组是(→表示反应一步完成)( )
1物质 A B C D
X FeO C CaCO Cu
2 3 3
Y Fe CO CaO CuO
Z FeCl CO Ca(OH) Cu(OH)
2 2 2 2
10.要将待提纯的物质中杂质(括号内为杂质)除去,所用试剂和方法均正确的是 ( )
选项 待提纯物质 选用试剂 操作方法
A CuCl(FeCl) 铜片 过滤
2 2
B CaO(CaCO) 盐酸 蒸发
3
C Cu(Fe) 硫酸铜溶液 过滤,洗涤
D FeCl 溶液(盐酸) 氢氧化钠溶液 过滤,洗涤
3
二、填空题(本题包括6个小题,每空1分,共16分)
11.河南烩面配料(面粉、羊肉、食盐、青菜等)中含有的营养素有
(写两种)。加碘食盐所含Kl03中I显 价。
12.化学与生活有密切的联系。糖类、油脂、蛋白质和维生素都是人类基本营养物质。
下表为某品牌燕麦片标签中的一部分。
每 100 g 含 糖类 油脂 蛋白质 维 生 素钙 镁 钠 锌
有 C
营养成分 7.6 g 7.8 g 7.4 g 18 mg 201 mg 18.2 mg 30.8 mg 8.1 mg
请回答下列问题:
(1)燕麦片的营养成分中能与水反应生成氨基酸的营养物质是 ;人体必需的微量元素是
。
(2)维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至
沸腾,红色消失。因此,烹调富含维生素C的食物(如蔬菜)时,应该注意 ;
在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点 。
13. (1)我们穿的衣服通常是由纤维织成的,常见的纤维有棉花、羊毛、涤纶等。用灼烧
法可初步鉴别三种纤维,给三种纤维编号后,分别灼烧产生的气味如下:
纤维编号 ① ② ③
灼烧时的气味 特殊气味 烧纸气味 烧焦羽毛气味
则羊毛、棉花的编号分别为(填序号,下同) _ 。
(2)加酶洗衣粉易除去衣物上的汗渍、血迹及油渍。现有下列衣料:
①羊毛织品 ②棉花织品 ③化纤布料 ④蚕丝织品。
其中不宜用加酶洗衣粉洗涤的是 。
14. 通过学习化学肥料的有关知识,我们知道铵盐是氮肥中的一类。请你写出一种铵盐的化学式
2,请你用简单的化学方法来鉴别某种化肥是氮肥 。
15. 氢氧化钾是我国古代纺织业常用作漂洗的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼
烧后的固体(主要成分是氧化钙)与草木灰(主要成分是碳酸钾)在水中相互作用,生成氢
氧化钾。请按要求用化学方程式表述上述有关反应。
(1)分解反应 ,
(2)化合反应 ,
(3)复分解反应 。
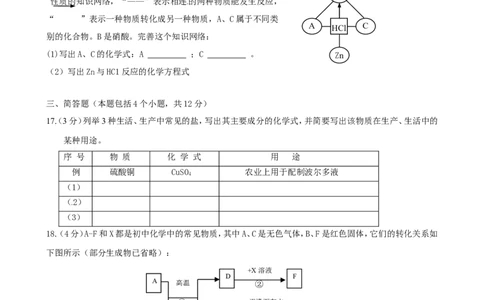
16.构建知识网络是一种重要的学习方法。下图是关于盐酸化学
B
性质的知识网络,“——”表示相连的两种物质能发生反应,
“ ”表示一种物质转化成另一种物质,A、C属于不同类
A HCl C
别的化合物。B是硝酸。完善这个知识网络:
(1)写出A、C的化学式:A ;C 。 Zn
(2)写出Zn与HC1反应的化学方程式
三、简答题(本题包括4个小题,共12分)
17(. 3分)列举3种生活、生产中常见的盐,写出其主要成分的化学式,并简要写出该物质在生产、生活中的
某种用途。
序 号 物 质 化 学 式 用 途
例 硫酸铜 CuSO 农业上用于配制波尔多液
4
(1)
(2)
(3)
18.(4分)A-F和X都是初中化学中的常见物质,其中A、C是无色气体,B、F是红色固体,它们的转化关系如
下图所示(部分生成物已省略):
+X溶液
D F
A 高温 ②
⑴写出反应①的化学方程式 ① + 澄 清 石 灰 水 。
B C E
⑵写出反应②的化学方程式 ,该反应属于 (填
写基本反应类型)反应。
⑶含D的生产、生活用品腐蚀的过程,实际上是D与空气中的 发生化学反应的过程。
19.(3分)在化学实验中,常常依据反应伴随的现象来确定反应是否发生。请按要求写出化学方程式。
(1)反应中伴有发光、放热现象。
3阳离子阴 离子 NO 3 - SO 4 2- OH-
(2)加热某种固体(或固体混合物),反应后 K+ 溶 溶 溶
固体质量减小。 Na+ 溶 溶 溶
Cu2+ 溶 溶 不溶
(3)根据右表写出有沉淀生成的复分解反应。
20.(2分)有三瓶无色透明的液体,分别是碳酸钠溶液、氢氧化钠溶液和氯化钠溶液,请
设计一个实验方案把这三瓶液体区分开来,写出实验操作步骤、现象和结论。
四、综合应用题(共12分)
21.实验室里有一瓶常用的无色液体试剂,因保管不当造成标签破损
(如图所示),其残缺的标签中只剩下“Na”和“10%”字样。 Na
10%
小强和小华同学对此很兴趣,决定对其成分进行探究。
【提出问题】该瓶试剂到底是什么物质的溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是( )
A.酸 B.碱 C.盐
【查阅资料】 I.初中化学中常见的含钠化合物有:NaCl, NaOH ,NaCO ,NaHCO。
2 3 3
II.NaCO和NaHCO的水溶液都呈碱性。
2 3 3
Ⅲ.测定室温(200C)时,四种物质的溶解度数据如下:
物质 NaCl NaOH NaCO NaHCO
2 3 3
溶解度g 36 109 215 9.6
【得出结论】小华根据试剂瓶标签上标注的溶质质量分数为10%和上表中的溶解度数据判
断,这瓶试剂不可能是 溶液。
【作出猜想】①可能是NaCl溶液;②可能是NaCO溶液;③可能是 溶液;
2 3
【设计方案并实验】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则这瓶试剂 不可能是 溶液。
(2)小强为了判断该溶液是NaOH溶液还是NaCO溶液,他又进行了如下实验:
2 3
操作步骤 实验现象 结论及化学方程式
取样于品试管中,滴加 产生大量的气泡 相应的化学方程式:
把产生的气体通入澄清石灰水中 猜想②正确
【拓展与应用】请你选择与小强不同的试剂来鉴别NaOH溶液和NaCO溶液,你选择
2 3
溶液。
【综合计算】运用侯氏制碱法制取的纯碱中可能含有少量的氯化钠。现取含有氯化钠杂质的纯碱样品25g放
4入烧杯中,向烧杯中加入167g水使样品全部溶解,再向烧杯中加入100g氯化钙溶液,恰好完全反应,然后过
滤,称得滤液的质量为272g。试计算:纯碱样品中氯化钠的
质量分数?
5参考答案
一、选择题(共计10分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D B A C D C A B B C
二、填空题(共计16分)
11. 蛋白质、糖类等 ; +5
12.(1)蛋白质 ;锌 ;(2)温度不能过高;食醋 。
13.(1)③②;(2)①④ 。
14.NHCl ;(其他合理答案均可) 取少量该化肥与少量熟石灰粉末共同混合、研磨。
4
如果有刺激性气味产生,则是铵盐,否则不是铵盐。
15.(1)CaCO 高温 CaO + CO↑ ; (2)CaO + HO == Ca(OH) ;
3 2 2 2
(3)KCO + Ca(OH) == CaCO↓+ 2KOH 。
2 3 2 3
16.(1)A:NaOH;C:FeO (其他合理答案均可) (2)Zn + 2HCl === ZnCl + H↑
2 3 2 2
三、简答题(共计12分)
17.(1)食盐;NaCl;作生活中的调味品。(1分)
(2)纯碱;NaCO;用于制造玻璃、造纸等。(1分)
2 3
(3)碳酸氢铵;NHHCO;农业上用作化肥。(1分)(其他合理答案均可)
4 3
18.⑴3CO + FeO 高温 2Fe +3 CO (1分) ⑵ Fe + CuSO = FeSO + Cu (1分)
2 3 2 4 4
置换 (1分) ⑶ 氧气和水(写化学式也可) (1分)
19.(1)C + O 点燃 CO (1分) (2)2KMnO △ KMnO +MnO + O↑(1分)
2 2 4 2 4 2 2
(3)CuSO+2NaOH= Cu(OH)↓+ NaSO (1分) (其他合理答案均可)
4 2 2 4
20.(1)分别取少量三种溶液置于三支试管中,然后分别滴加酚酞试液,如果溶液呈红色者
是NaCO 和NaOH,不变色者是NaCl。 (1分)
2 3
(2)再重新另取呈红色两种溶液少许置于二支试管中,然后分别滴加澄清石灰水,有浑
浊出现者是NaCO ,无现象者是NaOH 。 (1分)
2 3
四、综合应用题(计算4分,其余每空1分,共12分)
【交流讨论】 A 【得出结论】NaHCO 【作出猜想】NaOH
3
【设计方案并实验】(1)NaCl
(2)
操作步骤 实验现象 结论及化学方程式
稀盐酸 NaCO+2HCl==2NaCl+HO+CO↑
2 3 2 2
白色沉淀
【拓展与应用】可溶性的钙盐或可溶性的钡盐。 (以上每空1分)
【综合计算】 (4分)
6解:设25g纯碱样品中NaCO 的质量为X,则生成的碳酸钙质量为:
2 3
25g+167g+100g-272g = 20g ……………………………… (1分)
NaCO + CaCl== CaCO ↓+ 2NaCl ……………………………… (1分)
2 3 2 3
106 100
X 20g
106/X=100/20g X=21.2g ……………………………… (1分)
纯碱样品中NaCl的质量分数=25g -21.2g/ 25g×100%=15.2% ………(1分)
答:略
7