文档内容
二轮复习:中考化学探究性试验及计算
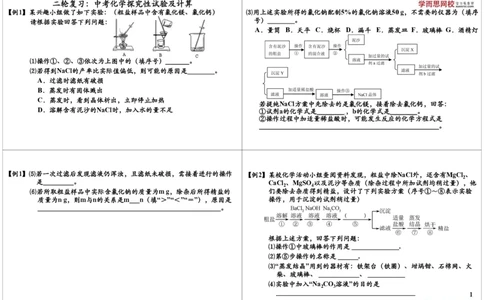
【例1】某兴趣小组做了如下实验:(粗盐样品中含有氯化镁、氯化钙) ⑶用上述实验所得的氯化钠配制5%的氯化钠溶液50 g,不需要的仪器为(填序
请根据实验回答下列问题:
号)________。
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒精灯
⑴操作①、②、③依次为上图中的(填序号)_______。
⑵若得到NaCl的产率比实际值偏低,则可能的原因是________。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.蒸发时,看到晶体析出,立即停止加热
若提纯NaCl方案中先除去的是氯化镁,接着除去氯化钙,回答:
D.溶解含有泥沙的NaCl时,加入水的量不足 ①试剂a的化学式是________ ,b的化学式是________。
②操作过程中加适量稀盐酸时,可能发生反应的化学方程式是
_____________________________________________________。
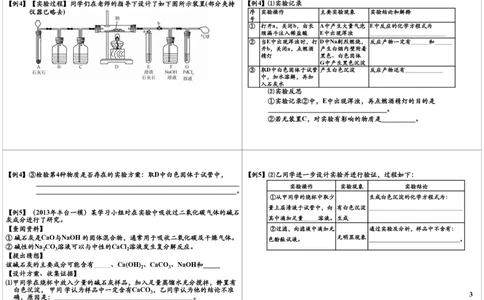
【例1】⑸若一次过滤后发现滤液仍浑浊,且滤纸未破损,需接着进行的操作 【例2】某校化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl 、
2
是_________。 CaCl 、MgSO 以及泥沙等杂质(除杂过程中所加试剂均稍过量),他
2 4
⑹若所取粗盐样品中实际含氯化钠的质量为m g,除杂后所得精盐的 们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验
质量为n g,则m与n的关系是m___n(填“>”“<”“=”),原因是 操作,用于沉淀的试剂稍过量)
______________________________________________________。
根据上述方案,回答下列问题:
⑴操作①中玻璃棒的作用是______________.
⑵第⑤步操作的名称是______.
⑶“蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火
柴、玻璃棒、____________、___________
⑷实验中加入“Na CO 溶液”的目的是
2 3
_________________________________________
1
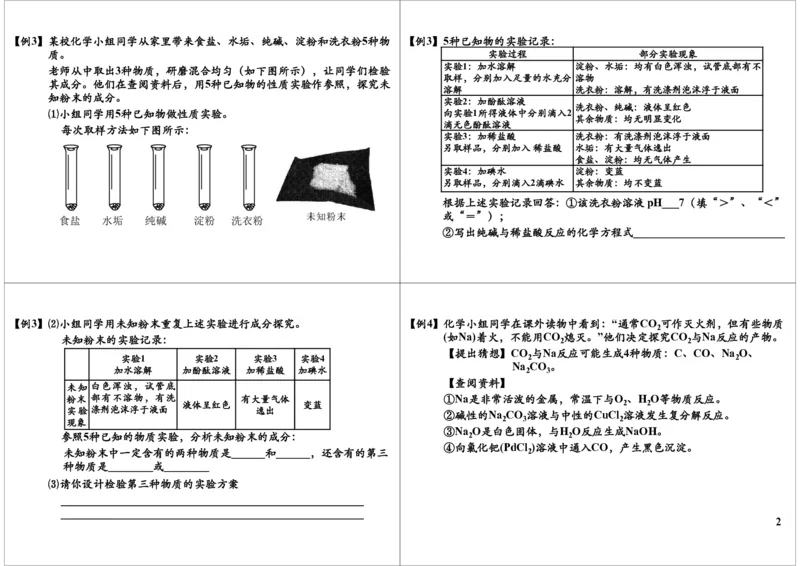
QQ 1426912393【例3】某校化学小组同学从家里带来食盐、水垢、纯碱、淀粉和洗衣粉5种物 【例3】5种已知物的实验记录:
质。 实验过程 部分实验现象
老师从中取出3种物质,研磨混合均匀(如下图所示),让同学们检验 实验1:加水溶解 淀粉、水垢:均有白色浑浊,试管底部有不
取样,分别加入足量的水充分 溶物
其成分。他们在查阅资料后,用5种已知物的性质实验作参照,探究未
溶解 洗衣粉:溶解,有洗涤剂泡沫浮于液面
知粉末的成分。
实验2:加酚酞溶液
洗衣粉、纯碱:液体呈红色
⑴小组同学用5种已知物做性质实验。 向实验1所得液体中分别滴入2
其余物质:均无明显变化
滴无色酚酞溶液
每次取样方法如下图所示:
实验3:加稀盐酸 洗衣粉:有洗涤剂泡沫浮于液面
另取样品,分别加入稀盐酸 水垢:有大量气体逸出
食盐、淀粉:均无气体产生
实验4:加碘水 淀粉:变蓝
另取样品,分别滴入2滴碘水 其余物质:均不变蓝
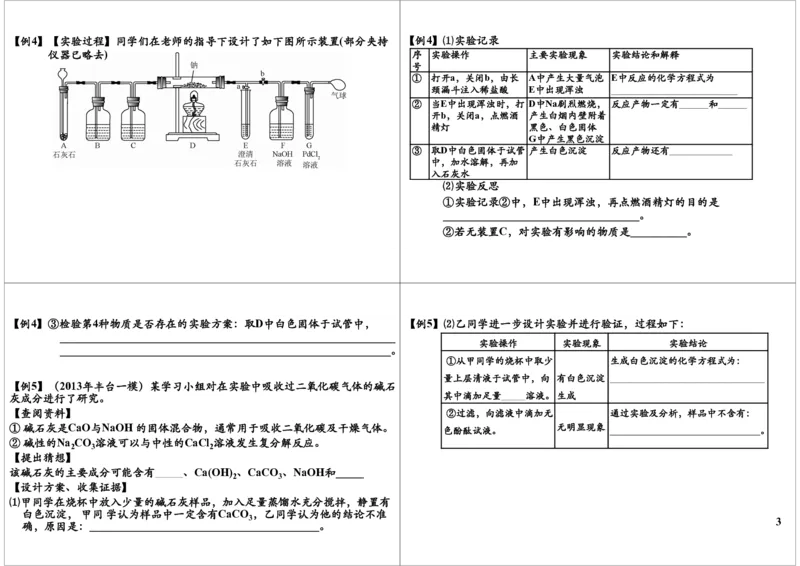
根据上述实验记录回答:①该洗衣粉溶液pH___7(填“>”、“<”
或“=”);
②写出纯碱与稀盐酸反应的化学方程式___________________________
【例3】⑵小组同学用未知粉末重复上述实验进行成分探究。 【例4】化学小组同学在课外读物中看到:“通常CO 可作灭火剂,但有些物质
2
未知粉末的实验记录:
(如Na)着火,不能用CO
2
熄灭。”他们决定探究CO
2
与Na反应的产物。
【提出猜想】CO 与Na反应可能生成4种物质:C、CO、Na O、
实验1 实验2 实验3 实验4 2 2
Na CO 。
加水溶解 加酚酞溶液 加稀盐酸 加碘水 2 3
【查阅资料】
未知 白色浑浊,试管底
粉末 部有不溶物,有洗 有大量气体 ①Na是非常活泼的金属,常温下与O 、H O等物质反应。
液体呈红色 变蓝 2 2
实验 涤剂泡沫浮于液面 逸出 ②碱性的Na CO 溶液与中性的CuCl 溶液发生复分解反应。
2 3 2
现象
③Na O是白色固体,与H O反应生成NaOH。
参照5种已知的物质实验,分析未知粉末的成分: 2 2
④向氯化钯(PdCl )溶液中通入CO,产生黑色沉淀。
未知粉末中一定含有的两种物质是______和______,还含有的第三 2
种物质是________或________
⑶请你设计检验第三种物质的实验方案
______________________________________________________
______________________________________________________
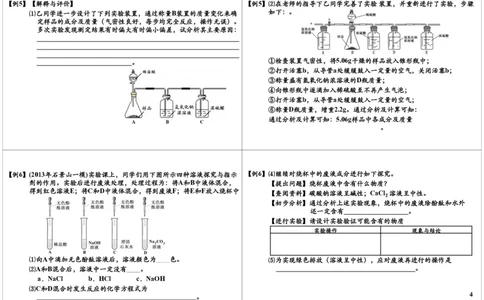
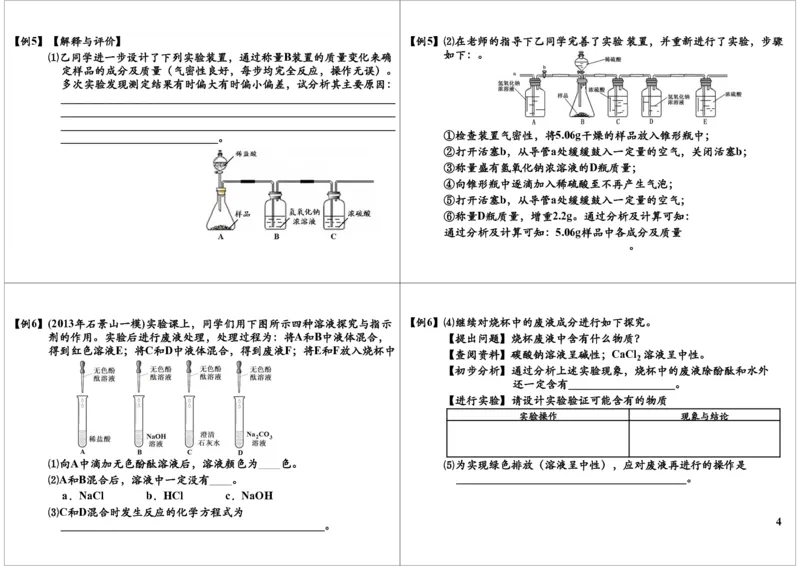
2【例4】【实验过程】同学们在老师的指导下设计了如下图所示装置(部分夹持 【例4】⑴实验记录
仪器已略去) 序 实验操作 主要实验现象 实验结论和解释
号
① 打开a,关闭b,由长 A中产生大量气泡 E中反应的化学方程式为
颈漏斗注入稀盐酸 E中出现浑浊 __________________________
② 当E中出现浑浊时,打 D中Na剧烈燃烧, 反应产物一定有______和______
开b,关闭a,点燃酒 产生白烟内壁附着
精灯 黑色、白色固体
G中产生黑色沉淀
③ 取D中白色固体于试管 产生白色沉淀 反应产物还有_____________
中,加水溶解,再加
入石灰水
⑵实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是
___________________________________。
②若无装置C,对实验有影响的物质是__________。
【例4】③检验第4种物质是否存在的实验方案:取D中白色固体于试管中, 【例5】⑵乙同学进一步设计实验并进行验证,过程如下:
____________________________________________________________
实验操作 实验现象 实验结论
___________________________________________________________。
①从甲同学的烧杯中取少 生成白色沉淀的化学方程式为:
量上层清液于试管中,向 有白色沉淀 ________________________________
【例5】(2013年丰台一模)某学习小组对在实验中吸收过二氧化碳气体的碱石
灰成分进行了研究。 其中滴加足量 溶液。生成
【查阅资料】 ②过滤,向滤液中滴加无 通过实验及分析,样品中不含有:
①碱石灰是CaO与NaOH的固体混合物,通常用于吸收二氧化碳及干燥气体。 色酚酞试液。 无明显现象 _______________________________。
②碱性的Na CO 溶液可以与中性的CaCl 溶液发生复分解反应。
2 3 2
【提出猜想】
该碱石灰的主要成分可能含有 、Ca(OH) 、CaCO 、NaOH和_____
2 3
【设计方案、收集证据】
⑴甲同学在烧杯中放入少量的碱石灰样品,加入足量蒸馏水充分搅拌,静置有
白色沉淀,甲同学认为样品中一定含有CaCO ,乙同学认为他的结论不准
3 3
确,原因是:_________________________________________。【例5】【解释与评价】 【例5】⑵在老师的指导下乙同学完善了实验装置,并重新进行了实验,步骤
⑴乙同学进一步设计了下列实验装置,通过称量B装置的质量变化来确 如下:。
定样品的成分及质量(气密性良好,每步均完全反应,操作无误)。
多次实验发现测定结果有时偏大有时偏小偏差,试分析其主要原因:
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________。 ①检查装置气密性,将5.06g干燥的样品放入锥形瓶中;
②打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
③称量盛有氢氧化钠浓溶液的D瓶质量;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤打开活塞b,从导管a处缓缓鼓入一定量的空气;
⑥称量D瓶质量,增重2.2g。通过分析及计算可知:
通过分析及计算可知:5.06g样品中各成分及质量
。
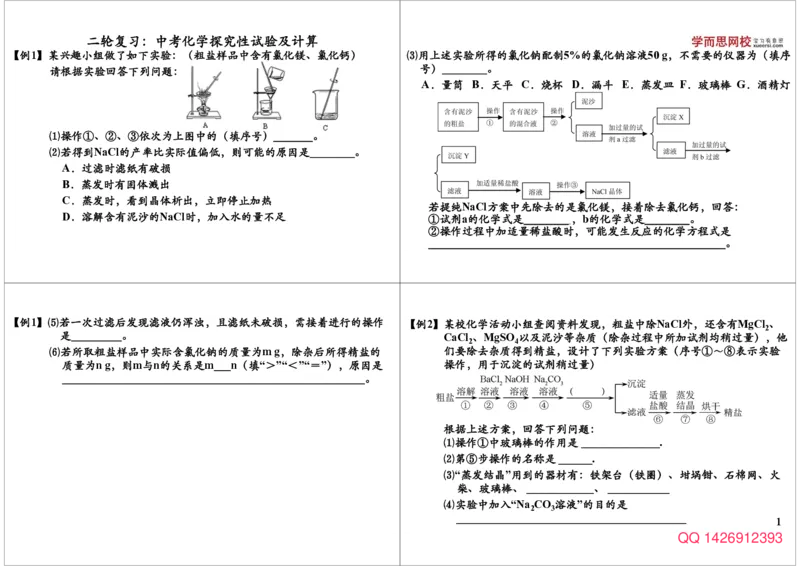
【例6】(2013年石景山一模)实验课上,同学们用下图所示四种溶液探究与指示 【例6】⑷继续对烧杯中的废液成分进行如下探究。
剂的作用。实验后进行废液处理,处理过程为:将A和B中液体混合, 【提出问题】烧杯废液中含有什么物质?
得到红色溶液E;将C和D中液体混合,得到废液F;将E和F放入烧杯中
【查阅资料】碳酸钠溶液呈碱性;CaCl 溶液呈中性。
2
【初步分析】通过分析上述实验现象,烧杯中的废液除酚酞和水外
还一定含有___________________。
【进行实验】请设计实验验证可能含有的物质
实验操作 现象与结论
⑴向A中滴加无色酚酞溶液后,溶液颜色为 色。 ⑸为实现绿色排放(溶液呈中性),应对废液再进行的操作是
⑵A和B混合后,溶液中一定没有 。 _________________________________________。
a.NaCl b.HCl c.NaOH
⑶C和D混合时发生反应的化学方程式为
4
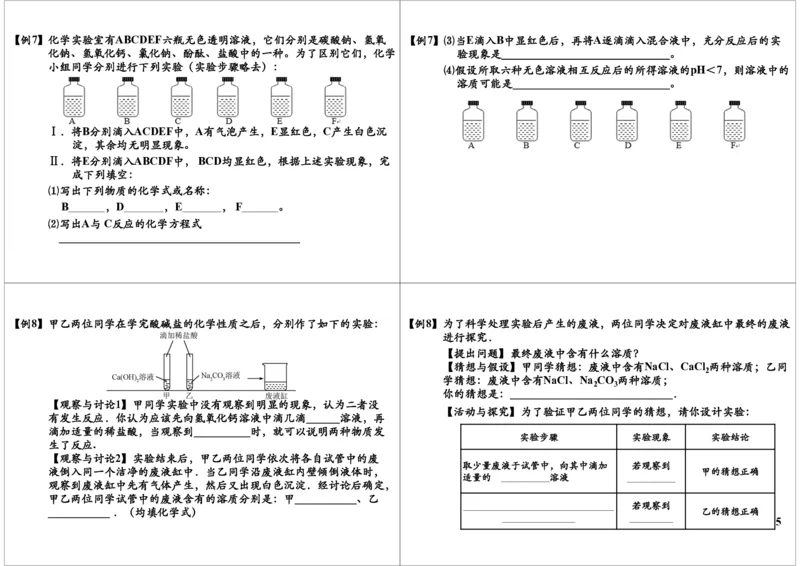
_______________________________________________。【例7】化学实验室有ABCDEF六瓶无色透明溶液,它们分别是碳酸钠、氢氧 【例7】⑶当E滴入B中显红色后,再将A逐滴滴入混合液中,充分反应后的实
化钠、氢氧化钙、氯化钠、酚酞、盐酸中的一种。为了区别它们,化学 验现象是______________________________。
小组同学分别进行下列实验(实验步骤略去): ⑷假设所取六种无色溶液相互反应后的所得溶液的pH<7,则溶液中的
溶质可能是____________________________。
Ⅰ.将B分别滴入ACDEF中,A有气泡产生,E显红色,C产生白色沉
淀,其余均无明显现象。
Ⅱ.将E分别滴入ABCDF中,BCD均显红色,根据上述实验现象,完
成下列填空:
⑴写出下列物质的化学式或名称:
B ,D ,E ,F 。
⑵写出A与C反应的化学方程式
___________________________________________
【例8】甲乙两位同学在学完酸碱盐的化学性质之后,分别作了如下的实验: 【例8】为了科学处理实验后产生的废液,两位同学决定对废液缸中最终的废液
进行探究.
【提出问题】最终废液中含有什么溶质?
【猜想与假设】甲同学猜想:废液中含有NaCl、CaCl 两种溶质;乙同
2
学猜想:废液中含有NaCl、Na CO 两种溶质;
2 3
你的猜想是:_____________________________.
【观察与讨论1】甲同学实验中没有观察到明显的现象,认为二者没
【活动与探究】为了验证甲乙两位同学的猜想,请你设计实验:
有发生反应.你认为应该先向氢氧化钙溶液中滴几滴______溶液,再
滴加适量的稀盐酸,当观察到__________时,就可以说明两种物质发
实验步骤 实验现象 实验结论
生了反应.
【观察与讨论2】实验结束后,甲乙两位同学依次将各自试管中的废
取少量废液于试管中,向其中滴加 若观察到
液倒入同一个洁净的废液缸中.当乙同学沿废液缸内壁倾倒液体时, 甲的猜想正确
适量的 __________溶液 __________
观察到废液缸中先有气体产生,然后又出现白色沉淀.经讨论后确定,
甲乙两位同学试管中的废液含有的溶质分别是:甲___________、乙
_______________________________ 若观察到
___________ .(均填化学式) 乙的猜想正确
_______________ _________
5【例9】有的化学反应伴随明显现象,有的化学反应则没有明显现象。某兴趣小 【例9】方案三:向NaOH溶液中滴加酚酞试液,溶液显红色,再滴加稀盐酸,
组同学为证明NaOH与稀盐酸能发生化学反应,从不同角度设计了如下 若红色消失,则证明NaOH与稀盐酸发生了化学反应。实验中,同学们
方案,并进行实验。 发现了一个意外现象:
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸并不断振荡, 向NaOH溶液中滴入酚酞试液,溶液变红,片刻,红色消失。同学们对
同时测定溶液的pH,若测得溶液的pH (填序号),则证明NaOH 此进行了探究。
与稀盐酸发生了化学反应。 猜想 实验操作 实验现象 结论与解释
①可能是红色溶液 用煮沸过的蒸馏水 溶液变成红 红色消失的现
a.逐渐增大并≥7 b.逐渐减小并≤7 c.始终不变并等于7
与空气中的O 发生 配制上述NaOH溶液,色,片刻, 象与空气中的
2
方案二:化学反应通常伴随能量的变化,可借助反应前后的温度变化来 了反应,使红色消 在液面上方滴些植 红色消失。 O 无关。
2
判断是否发生了反应。某同学在不使用温度计的情况下,通过右图所示 失。 物油,冷却后加入
装置进行实验,观察到红墨水向右移动。有的同学提 酚酞试液。
②可能是NaOH溶液 溶液变红色,红色消失的现
出,该现象不足以证明NaOH与稀盐酸发生了化学反 取少量Na CO 溶液,
与空气中CO 反应生 2 3 一段时间后 象与空气中的
2 向其中滴入酚酞试
应,他的理由是: 成了Na CO ,使红 红色不消失。CO 无关。
2 3 液。 2
①_________________________________; 色消失。
②_________________________________。
【例9】⑴在验证猜想①的实验中“煮沸”和“滴入植物油”的目的是
________________________________。
⑵该小组同学通过查阅资料得知:当选用溶质的质量分数大于10%的
氢氧化钠溶液时,就会出现上述意外现象。请你设计实验证明:上
述方案中红色消失是NaOH溶液中溶质的质量分数过大所致。你的
实验方案是
__________________________________________________________
__________________________________________________________
________________________________________________。
6