文档内容
第二单元 我们周围的空气
课题1 空 气
一、空气成分的研究史
法国科学家 最早运用天平作为研究化学的工具,用定量的方法
研究了空气的成分,第一次明确提出了“空气是由氧气和氮气组成的”。
二、空气中氧气成分的测定:
1、装置图(见书P27)
2、实验现象:①、
②、(过一会儿白烟消失,装置冷却到室温后打开弹簧夹)烧杯内的水倒流入集气瓶,约占瓶
子容积的 。
3、实验结论:说明空气不是单一的物质;氧气约占空气总体积的1/5。
点燃
4、原理:表达式:磷(P) + 氧气(O) 五氧化二磷(PO)
2 2 5
化学方程式:
5、注意事项:A、所用的红磷必须 ,如果红磷过少则氧气没有全部消
耗完
B、要等集气瓶(装置) 后才能打开弹簧夹
C、装置的气密性要好(否则测量结果偏小)
D、要先夹住橡皮管,然后再点红磷(否则测量结果 )。
思考:可否换用木炭、硫等物质?
答:
三、空气的主要成分(按体积分数):氮气(N) ,氧气
2
(O) (氮气比氧气约为4:1),稀有气体 ,二
2
氧化碳(CO) ,其它气体和杂质0.03%
2
四、物质的分类:纯净物和混合物
1、纯净物:由 物质组成的。
2、混合物: 物质组成的。这些物质相互间没有发生化学反应,各物质
都保持各自的性质。
五、空气是一种宝贵的资源
1、氮气:无色、无味的气体, 于水,不燃烧也不支持燃烧,不能供给呼
吸,化学性质不活泼。
2、稀有气体:无色、无味的气体,通电时能发出不同颜色的光,化学性质很不活泼。
氧气的用途 ①动植物呼吸②医疗急救③金属切割④炼钢⑤宇宙航行等
氮气的用途 ①作保护气②食品充氮作防腐剂等
稀有气体的用途 ①作保护气②制多种用途的电光源等
六、空气的污染及防治。
1、 造成空气污染的物质:有害气体( , ,
,))和烟尘。
2、污染来源:空气中的有害物质来自化石燃料的燃烧,工厂排放的废气及汽车排放的尾气。
3、被污染的空气带来的危害:损害人体健康、影响作物生长、破坏生态平衡。
存在的环境问题: (二氧化碳含量过多引起)、
(飞机的尾气、氟里昂的排放)、 (由二氧化硫、二氧化氮引起)。
4、防止空气污染的措施:加强大气质量监测,改善环境状态、植树造林、使用清洁能源。
课题2 氧气一、氧气的物理性质
1、色、味、态:通常情况下,是 的气体;
2、密度:标准状况下,密度为1.429g/L, 。(可用向上排空法)
3、溶解性:氧气 。(可用排水法收集),
4、三态变化:降温后,氧气可以变为 的液体,甚至
, 状固体。
二、氧气的化学性质(很活泼)
(一)与非金属(碳、硫、磷)的反应
1、木炭(黑色固体)燃烧
实验现象:在氧气中:剧烈燃烧,发出 ,放出热量,生成一种无色无味
气体,该气体能使 变浑浊。
点燃
文字表达式:碳(C)+ 氧气(O) 二氧化碳(CO)
2 2
化学方程式
2、硫粉(淡黄色)燃烧:
实验现象:在空气中:发出微弱的 火焰;放出热量、生成一种带
有 气味的气体。
在氧气中: 发出明亮的 的火焰, 放出热量、生成一种带
有 气味的气体。
点燃
文字表达式 硫(S) + 氧气(O) 二氧化硫(SO )
2 2
化学方程式
实验时,要在瓶底装少量水(吸收 ,防止污染空气)。
3、红磷(暗红色固体)的燃烧
实验现象:在氧气中:剧烈燃烧,发出白光,放出热量,生成大量的白烟
点燃
文字表达式:磷(P)+ 氧气(O) 五氧化二磷(PO)
2 2 5
化学方程式:
注意:五氧化二磷(PO)是固体,不是气体
2 5
(二)与金属(镁、铁)的反应
1、镁带(银白色固体)燃烧
实验现象:在空气中,剧烈燃烧,发出 ,放出热量,生
成 固体。
点燃
文字表达式:镁(Mg)+ 氧气(O) 氧化镁(MgO)
2
化学方程式:
2、铁丝(银白色固体)燃烧
实验现象:在氧气中,剧烈燃烧, ,放出热量,生成一
种 。点燃
文字表达式:铁(Fe) + 氧气(O) 四氧化三铁(Fe O)
2 3 4
化学方程
注意:集气瓶底部 ,防止生成的固体物质溅落瓶底,致使集气
瓶炸裂。铁丝在 中不能燃烧。
(三)其他物质与氧气的反应
某些物质在一些条件下,与氧气发生缓慢的氧化反应,称为 。缓慢氧
化也放热。
如:动植物新陈代谢, , 、酒醋的酿造、农家肥
的腐熟等等。
总结:
1、氧气是一种化学性质比较活泼的气体,在一定的条件下,能与许多物质发生反应并放出大
量的热。在这些反应中,氧气提供氧,称为 。氧气具
有 。
2、物质在氧气中燃烧程度比空气中燃烧要剧烈。说明物质燃烧程度,与氧气的浓度大小成正
比;
3、物质燃烧时有的有火焰,有的会发光,有的会冒烟。一般来说,气体燃烧会有火焰产生;固
体直接燃烧,产生光或者火星。生成物有固体时,一般都会产生烟。
三、氧气的用途
(1)、供给呼吸:医疗上急救病人,登山、潜水、航空、宇航提供呼吸;
(2)、 :炼钢、气焊与气接、液氧炸弹、火箭助燃剂
四、反应类型:
①:化合反应:由 或 的物质生成另一种物质
的反应。(简称“多合一”)
②:分解反应:由 反应物生成两种或两种以上其他物质的反应。简称:
“一变多”)
③:氧化反应:物质与氧发生的化学反应。(注意:是“氧”而不只是限于“氧气”)有氧气参
加的反应一定属于氧化反应。氧化反应不一定是化合反应(石蜡的燃烧生成了水和二氧化碳
两种物质),化合反应不一定是氧化反应。
课题3 实验室制取氧气
一、氧气的工业制法(分离液态空气法)
原理:利用液态氧和液态氮的沸点不同。——是物理变化
具体过程:
氮气 沸点低(—196℃),先蒸发出来
降温加压 蒸发
空 气 液态空气
液态氧 沸点较高(—183℃)
装入天蓝色钢瓶
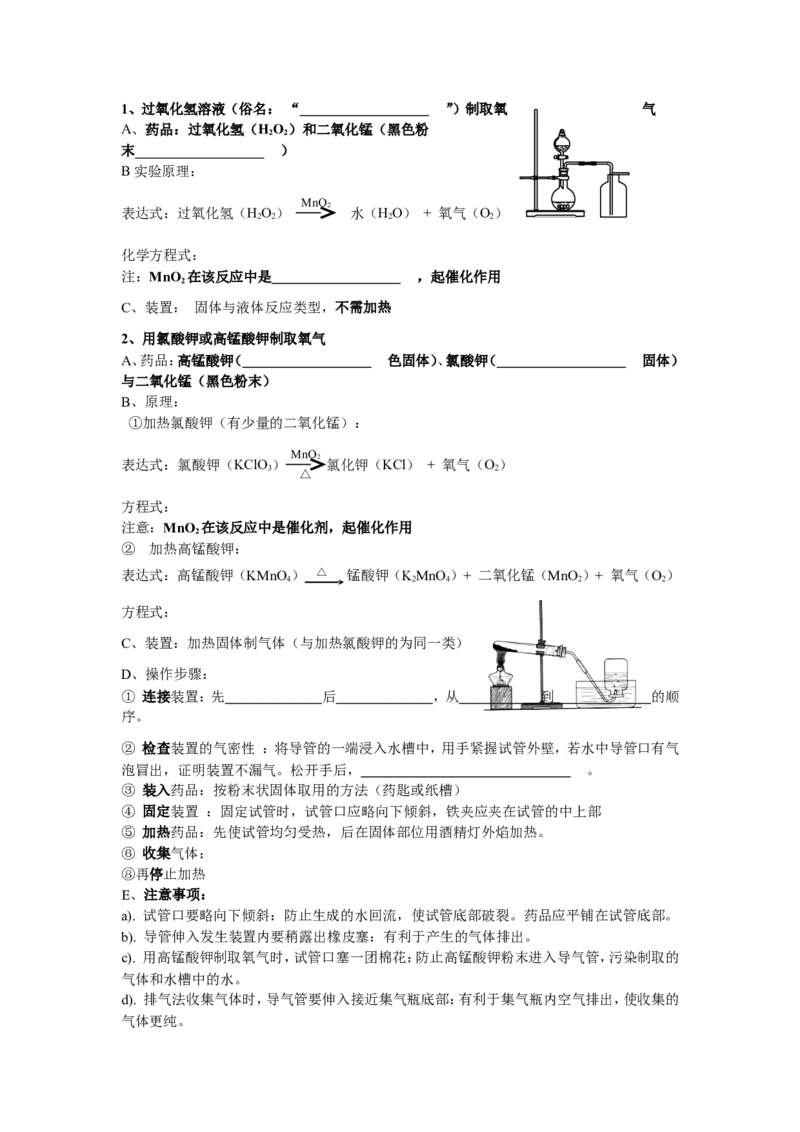
二、氧气的实验室制法(是化学变化)1、过氧化氢溶液(俗名: “ ”)制取氧 气
A、药品:过氧化氢(HO)和二氧化锰(黑色粉
2 2
末 )
B实验原理:
MnO
2
表达式:过氧化氢(HO) 水(HO) + 氧气(O)
2 2 2 2
化学方程式:
注:MnO 在该反应中是 ,起催化作用
2
C、装置: 固体与液体反应类型,不需加热
2、用氯酸钾或高锰酸钾制取氧气
A、药品:高锰酸钾( 色固体)、氯酸钾( 固体)
与二氧化锰(黑色粉末)
B、原理:
①加热氯酸钾(有少量的二氧化锰):
MnO
2
表达式:氯酸钾(KClO) 氯化钾(KCl) + 氧气(O)
3 △ 2
方程式:
注意:MnO 在该反应中是催化剂,起催化作用
2
② 加热高锰酸钾:
表达式:高锰酸钾(KMnO ) △ 锰酸钾(KMnO )+ 二氧化锰(MnO )+ 氧气(O)
4 2 4 2 2
方程式:
C、装置:加热固体制气体(与加热氯酸钾的为同一类)
D、操作步骤:
① 连接装置:先 后 ,从 到 的顺
序。
② 检查装置的气密性 :将导管的一端浸入水槽中,用手紧握试管外壁,若水中导管口有气
泡冒出,证明装置不漏气。松开手后, 。
③ 装入药品:按粉末状固体取用的方法(药匙或纸槽)
④ 固定装置 :固定试管时,试管口应略向下倾斜,铁夹应夹在试管的中上部
⑤ 加热药品:先使试管均匀受热,后在固体部位用酒精灯外焰加热。
⑥ 收集气体:
⑧再停止加热
E、注意事项:
a). 试管口要略向下倾斜:防止生成的水回流,使试管底部破裂。药品应平铺在试管底部。
b). 导管伸入发生装置内要稍露出橡皮塞:有利于产生的气体排出。
c). 用高锰酸钾制取氧气时,试管口塞一团棉花:防止高锰酸钾粉末进入导气管,污染制取的
气体和水槽中的水。
d). 排气法收集气体时,导气管要伸入接近集气瓶底部:有利于集气瓶内空气排出,使收集的
气体更纯。e). 实验结束后,先将导气管移出水面,然后熄灭酒精灯:防止水槽中的水倒流,炸裂试管。
三、催化剂:
1、概念:在化学反应中能 其他物质的反应速率,但本身
的 和 在反应前后不变的物质。
注意:①催化剂不能改变生成物的质量
②催化剂不是反应物也不是生成物
③一种催化剂只针对某一反应。不同的反应,催化剂可能不同
④某一反应的催化剂可能不只一种