文档内容
化学模拟试题 ( 二 )
[时间:60分钟 满分:50分]
可能用到的相对原子量:Ca-40 O-16 C-12 Na-23 Cl-35.5 N-14[来源:Z_xx_k.Com]
一、选择题(下列各题的四个选项中只有一个符合题意。共15小题,每小题1分,共15分)[来源:学。科。网]
1.下列变化中属于化学变化的是( )
A.榨取果汁 B.粉碎废纸
C.切割玻璃 D.燃放烟花
2.PM 是指大气中直径小于或等于2.5微米的颗粒物。PM 漂浮在空中,进入人体肺泡,对健康影响很大。PM 属
2.5 2.5 2.5
于下列空气污染物中的( )
A.可吸入颗粒物 B.一氧化碳
C.二氧化硫 D.二氧化氮
3.空气成分中体积分数最大的是( )
A.氧气 B.氮气
C.二氧化碳 D.稀有气体
4.把下列物质分别加入水中,充分搅拌后不能得到溶液的是( )
A.蔗糖 B.氯化钠
C.酒精 D.花生油
5.在生活中的下列说法合理的是( )
A.草木灰的主要成分是碳酸钾,碳酸钾是复合肥料
B.家中门把手表面涂防锈油来防锈
C.用浓氢氧化钠溶液中和沾到皮肤上的浓硫酸
D.元素的化学性质与该元素原子的最外层电子数目关系最密切
6.下列对O、CO、SO 、MnO 四种物质组成的说法正确的是( )
2 2 2 2
A.都含有氧分子 B.都含有两个氧原子
C.都含有氧元素 D.都是氧化物
7.有三瓶失去标签的无色溶液,只知道它们分别是稀盐酸、澄清石灰水和氯化钠溶液中的一种。下列四种试剂中,
能将上述三种无色溶液一次鉴别出来的是( )
A.NaCO 溶液 B.MgCl 溶液
2 3 2
C.KNO 溶液 D.酚酞溶液
3
8.已知2A+3B===C+3D,用足量的A和49 g B恰好完全反应,其生成57 g C和1 g D,若B的相对分子质量为
98,则A的相对分子质量为( )
A.16 B.27 C.44 D.56
9.把一定质量的锌粉放入Cu(NO ) 溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生,根据以上现象,下
3 2
列判断滤渣中的成分正确的是( )
A.只有Cu
B.只有Zn
C.一定有Zn和Cu
D.一定有Cu,可能有Zn
10.对下列几种化学符号说法正确的是( )
①N ②Na+ ③ ④PO ⑤KClO
2 5 3
A.表示物质组成的化学式有①④⑤
B.表示阳离子的有②③C.④中数字“5”表示五氧化二磷中有5个氧原子
D.⑤中各元素的质量比为1∶1∶3
11.为比较X、Y、Z三种金属活动性顺序,进行如下实验。实验结论正确的是( )
图M2-1
A.X>Y>Z B.Z>Y>X
C.Y>X,Y>Z D.X>Y,Z>Y
12.下列实验方案中设计不合理的是( )
A.用灼烧闻气味的方法区分羊毛纤维与棉纤维
B.用燃着的木条区分二氧化碳和氮气
C.用磁铁吸引区分铁丝和铝丝
D.用水区分氢氧化钠和硝酸铵固体
13.硝酸钾在不同温度时的溶解度数据如下表,下列说法错误的是( )
温度/℃ 0 20 40 60 80 100
169[
31.6[
110[ 来源:
来
来源: 学_科
溶解度/g 13.3 源:Z_x 63.9 246
学科 _网
x_k.Co
网] Z_X_
m]
X_K]
A.硝酸钾的溶解度受温度影响较大
B.60 ℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11∶21
C.20 ℃时,10 g水中加入5 g硝酸钾充分溶解后再加入5 g水,前后溶质的质量分数不变
D.将溶质质量分数为28%的硝酸钾溶液从60 ℃降温至20 ℃,没有晶体析出
14.在pH=10的水溶液中,下列各组离子能大量共存的是( )
A.Fe2+、Ca2+、CO2-
3
B.Na+、SO 2-、Cl-
4
C.Ba2+、H+、Cl-
D.Ag+、NH +、NO -
4 3
15.下列说法正确的是( )
A.用50 g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需加水20 g
B.图书室、资料室着火时,应立即用泡沫灭火器灭火
C.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液[来源:学科网]
D.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
二、填空与简答题(本题2个小题,共10分)
16.(5分)用化学用语填空:
(1)地壳中含量最多的金属元素________。
(2)2个铜离子________。
(3)2个二氧化硫分子________。
(4)改良酸性土壤的碱________。
(5)用于人工降雨的干冰________。
17.(5分)按要求回答下列问题。
(1)“物质的性质与其用途密切相关”。例如:铜用于制导线是因为其具有良好的延展性和________性;一氧化碳的性质决定了一氧化碳在钢铁冶炼中的作用,请用化学方程式表示高炉炼铁的原理:________________________________。
(2)目前人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和____________;为减少污染,提高煤的利用率,
可将其转化为可燃性气体,此过程可认为是碳和水的反应,其微观示意图如图M2-2所示。
图M2-2
该反应的基本类型为________反应,生成物C和D的分子个数比为________。
三、实验与探究题(本题3个小题,共18分)
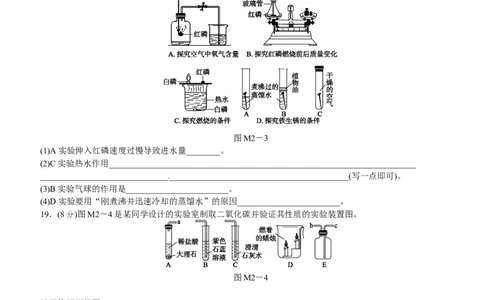
18.(4分)结合图M2-3所示实验回答有关问题。
图M2-3
(1)A实验伸入红磷速度过慢导致进水量________。
(2)C实验热水作用________________________________________________________________________
________________________________________________________________________(写一点即可)。
(3)B实验气球的作用是________________________。
(4)D实验要用“刚煮沸并迅速冷却的蒸馏水”的原因________________________。
19.(8分)图M2-4是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。
图M2-4
请回答下列问题。
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管________(填“b”或“c”)相连接。检验E装置中二氧化
碳已收集满的方法是______________________________________________________________________。
(2)将A、B装置连接,观察到的现象是____________________________________。
(3) 将 A 、 C 装 置 连 接 , 可 验 证 二 氧 化 碳 与 氢 氧 化 钙 反 应 , 该 反 应 的 化 学 方 程 式 为 ___
_____________________________________________________________________
________________________________________________________________________。
(4)用E装置收集满一瓶二氧化碳气体,取下双孔橡皮塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的
现 象 是 __________________________________________ , 这 些 现 象 说 明 二 氧 化 碳 具 有 的 物 理 性 质 是
__________________________;化学性质是________________、__________________。
20.(6分)在化学实验室,小刚和小强意外发现实验桌上有一瓶敞口放置的氢氧化钠固体,他们对这瓶氢氧化钠固体
是否变质进行了如下实验探究:[提出问题] 这瓶氢氧化钠固体是否变质?
氢氧化钠露置在空气中会发生变质。变质的原因是______________________________(用化学方程式表示)。
[实验探究] 为检验这瓶氢氧化钠固体是否变质,小刚和小强设计了如下实验方案。
小刚:取少量样品加适量蒸馏水配成溶液,滴入几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有
变质。
小强:取少量样品加适量蒸馏水配成溶液后,滴入适量澄清石灰水,若观察到有白色沉淀生成,证明该瓶氢氧化钠
固体已经变质。
你认为上述实验方案错误的是________。理由是________________________________________________。[来
源:Z#xx#k.Com]
请你设计另外一个方案,证明该瓶氢氧化钠固体已经变质,并完成以下实验报告:
实验步骤 实验现象及结论
______________________________________
______________________________________
__________________________________[来
__________________________________
源:学&科&网Z&X&X&K]
______________________________________
______________________________________
__________________________________
__________________________________
______________________________________
______________________________________
__________________________________
__________________________________
[交流反思] 在实验室里氢氧化钠需要密封保存。药品密封保存的原因很多,请你写出浓硫酸需要密封保存的原因:
____________________________________________。
四、计算与分析题(共7分)
21.在氯化钙与氯化钠的固体混合物中加入一定量的水,全部溶解后得到50 g溶液,向该溶液中加入溶质质量分数
一定的碳酸钠溶液50 g,恰好完全反应后过滤,得到白色固体5 g。求:
(1)白色沉淀的相对分子质量为________。
(2)所加碳酸钠溶液的溶质质量分数。[来源:Z,xx,k.Com]
(3)恰好完全反应所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
参考答案
1.D 2.A 3.B 4.D 5.D 6.C 7.A 8.B 9.C 10.B 11.A 12.B 13.D 14.B 15.C
16.(1)Al (2)2Cu2+ (3)2SO (4)Ca(OH) (5)CO
2 2 2
17.(1)导电 Fe O+3CO=====2Fe+3CO
2 3 2
(2)天然气 置换 1∶1
18.(1)偏大 (2)提供温度(或隔绝氧气)
(3)密封、缓冲,防止红磷燃烧放热使胶塞弹开
(4)除去溶解于水中的氧气
[解析] (1)若实验中若伸入红磷速度过慢,会使瓶内的一部分空气逸出,导致装置内的气压减小较大,会使测定氧气
的结果偏大;(2)实验C中热水的作用是:供给铜片上白磷燃烧所需要的热量,同时让水中白磷隔绝空气;(3)B实验中气
球的作用是提供密闭环境,且起缓冲作用,防止红磷燃烧放热使胶塞弹开;(4)温度越高,气体的溶解度越小,煮沸并迅速
冷却的蒸馏水,可将水中的氧气除去。
19.(1)c 将燃着的木条放到集气瓶口的b导管处,木条熄灭,证明集气瓶里已收集满二氧化碳
(2)溶液由紫色变成红色(3)CO+Ca(OH) ===CaCO ↓+HO
2 2 3 2
(4)燃着的蜡烛由低到高依次熄灭 密度比空气大 不燃烧 不支持燃烧
20.[提出问题] 2NaOH+CO===Na CO+HO
2 2 3 2
[实验探究] 小刚 氢氧化钠溶液、碳酸钠溶液都显碱性,都能使无色酚酞溶液变红
取少量样品加入过量稀盐酸中 有气泡产生,证明该瓶氢氧化钠固体已经变质
[交流反思] 浓硫酸有吸水性,易吸收空气中的水蒸气,而导致溶液变稀
21.(1)100
解:(2)由题意得知,CaCO 的质量为5 g,
3
设原混合物中碳酸钠的质量为x,生成氯化钠的质量为y,消耗氯化钙的质量为z。[来源:学_科_网Z_X_X_K]
NaCO+CaCl ===CaCO ↓+2NaCl
2 3 2 3
106 111 100 117
x z 5 g y
= x=5.3 g
= y=5.85 g
= z=5.55 g
所加碳酸钠溶液的溶质质量分数为×100%=10.6%。
(3)设原固体混合物的质量是m。
所以×100%=10%。
m=9.2 g
答:(2)所加碳酸钠溶液的溶质质量分数为10.6%;
(3)原固体混合物的质量是9.2 g。