文档内容
化学模拟试题 ( 五 )
[时间:60分钟 满分:50分]
可能用到的相对原子量:H-1 O-16 Cu-64 Na-23 Cl-35.5
一、选择题(下列各题的四个选项中只有一个符合题意。共15小题,每小题1分,共15分)
1.我们生活在不断变化的物质世界中,下列变化属于物理变化的是( )
A.蜡烛的燃烧
B.二氧化碳使澄清石灰水变浑浊
C.铁钉在潮湿的空气中生锈
D.磁悬浮列车中液氮制冷
2.下列物质的用途中,利用其化学性质的是( )
A.铜用于制作电线
B.熟石灰用于改良酸性土壤
C.干冰用于人工降雨
D.金刚石用于切割大理石
3.绘制出世界上第一张元素周期表的科学家是( )
A.门捷列夫 B.拉瓦锡
C.道尔顿 D.张青莲
4.下列措施中,不利于节能减排和改善环境的是( )
A.开发太阳能、风能
B.工业废水处理后排放
C.推广乙醇汽油
D.焚烧秸秆
5.对照实验是研究物质性质的一种重要方法,下列不是用来作对照实验的是( )
图M5-1
6.实验室制取氧气必须满足的条件是( )
A.一定要加入催化剂
B.反应物中一定有液体
C.反应物中一定有含氧化合物 [来源:学.科.网]
D.反应一定需要加热
7.氢气作为21世纪极具开发前景的新能源之一,理由是( )
①燃烧热值高 ②原料资源丰富 ③贮存和运输时安全性高 ④燃烧产物无污染
A.①②③ B.①②④C.②③④ D.①③④
8.下列物质不需要密封保存的是( )
A.浓硫酸 B.生石灰
C.浓氨水 D.石灰石
9.KPO 既能促进农作物根系发达,又能使其茎秆粗壮,它属于( )
3 4
A.氮肥 B.复合肥
C.钾肥 D.磷肥
10.下列关于实验现象的描述,正确的是( )
A.硫在氧气中燃烧时,发出微弱的淡蓝色火焰
B.棉线在空气中燃烧时,有烧焦羽毛气味
C.细铁丝在氧气中燃烧时,火星四射,生成黑色固体
D.红磷在空气中燃烧时,产生白色烟雾
11.图M5-2为三条溶解度曲线,当溶液接近饱和时,分别采用降低温度、蒸发溶剂、增加溶质的方法,
图M5-2
均可变为饱和溶液的物质是( )
A.a、b溶液 [来源:Zxxk.Com]
B.b、c溶液
C.c溶液
D.a溶液[来源:Z_xx_k.Com]
12.世界卫生组织把铝确定为食物污染源之一。铝的下列用途必须加以控制的是( )
A.用铝合金制门窗
B.用铝合金作飞机材料
C.用金属铝制的易拉罐装碳酸饮料
D.用金属铝制电线[来源:Zxxk.Com]
13.下列各组溶液中,在混合时酸都是过量的,反应完全后,无沉淀生成的是( )
A.Ca(OH) 、NaCO、HCl B.AgNO、FeCl 、HNO
2 2 3 3 3 3
C.BaCl 、KCO、HSO D.BaCl 、KOH、HSO
2 2 3 2 4 2 2 4
14.在CuCl 和MgCl 的混合液中,加入过量的锌粉充分反应后,过滤留在滤纸上的物质是( )
2 2
A.Zn B.Cu
C.Zn和Cu D.Cu和Mg
15.下列各组转化中,一定条件下均能一步实现的组合是( )
图M5-3
A.①② B.②③ C.①③ D.①②③
二、填空与简答题(本题2个小题,共10分)
16.(6分)化学就在我们身边。请用相关的化学知识回答下列问题。
(1)生活中硬水软化的方法为________。
(2)泡茶时,为将茶叶与茶水分离,可在茶杯内装上纱网,该设计利用的化学实验操作原理是________。
(3)补锌可服用葡萄糖酸锌(C H O Zn)口服液,其中属于微量元素的是________。
12 22 14(4)化石燃料是不可再生能源,可利用和开发的新能源有____________(填一种即可)。
(5)人呼吸产生的CO 若不能及时排出,滞留在血液中会使血液的pH________(填“变大”“变小”或“不变”)。
2
(6)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO 和Mg(OH) ]。下列物质能清洗瓶内水垢的是
3 2
____________(填序号)。
①酒 ②食醋 ③苏打水
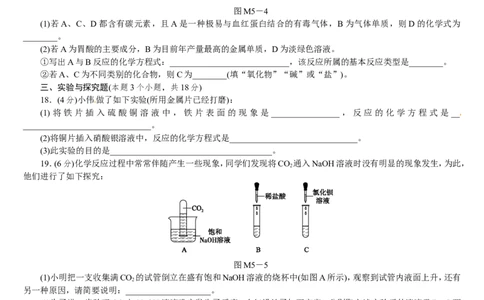
17.(4分)A、B、C、D为初中化学常见的物质,它们之间的转化关系如图M5-4所示(其中“→”表示转化关系)。
图M5-4
(1)若A、C、D都含有碳元素,且A是一种极易与血红蛋白结合的有毒气体,B为气体单质,则D的化学式为
________。
(2)若A为胃酸的主要成分,B为目前年产量最高的金属单质,D为淡绿色溶液。
①写出A与B反应的化学方程式:____________________________,该反应所属的基本反应类型是________。
②若A、C为不同类别的化合物,则C为________(填“氧化物”“碱”或“盐”)。
三、实验与探究题(本题3个小题,共18分)
18.(4分)小伟做了如下实验(所用金属片已经打磨):
(1)将铁片插入硫酸铜溶液中 ,铁片表面的现象是________________,反应的化学方程式是__
______________________________。
(2)将铜片插入硝酸银溶液中,反应的化学方程式是______________________________。
(3)此实验的目的是______________________________________。
19.(6分)化学反应过程中常常伴随产生一些现象,同学们发现将CO 通入NaOH溶液时没有明显的现象发生,为此,
2
他们进行了如下探究:
图M5-5
(1)小明把一支收集满CO 的试管倒立在盛有饱和NaOH溶液的烧杯中(如图A所示),观察到试管内液面上升,还有
2
另一种原因,请简要说明:____________________。
(2)为了进一步验证CO 与NaOH溶液确实发生了反应,小红设计了如下方案:分别取上述实验后的溶液于B、C两
2
支试管中,向试管 B 中滴加足量的稀盐酸,观察到的现象是______________,反应的化学方程式为
____________________________________。向试管B中滴加氯化钡溶液,观察到的现象是________________,反应的化
学方程式为__________________________________。虽然实验的现象不同,但都能证明CO 与NaOH溶液确实发生了化
2
学反应。
(3)实验过程中需要吸收CO 时,大多会选择NaOH溶液,但是,检验CO 时常常选择新配制的澄清石灰水,请简要
2 2
解释原因:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
20.(8分)实验室有一瓶久置的NaOH溶液,为检验是否变质并确定溶液中溶质是什么,兴趣小组设计实验并进行验
证。
(1)请你用化学方程式写出NaOH溶液变质的原因: ____________________________________________。[提出问题] 待测液中的溶质是什么?
[查阅资料] 氯化钙溶液呈中性。
(2)[作出猜想] 猜想一:NaOH;猜想二:NaCO;猜想三:________________。
2 3
(3)[设计方案] 实验方案(一):取少量待测溶液于试管中,向其中滴加无色酚酞溶液,若溶液变红,则待测溶液没有变
质,猜想一正确。该方案是否合理________,理由是____________________________________。
实验方案(二):取少量待测溶液于试管中,先加足量的澄清石灰水,再加无色酚酞,若观察到先有白色沉淀产生,后
有溶液变红的现象,猜想三正确。发生的化学反应方程式为__________________________________。某同学提出异议,
原因是________________________________________________________________________。
实验方案(三):取少量待测溶液于试管中,先向其中加入足量的 CaCl 溶液,再加入无色酚酞,若观察到
2
__________________________________的现象,则说明猜想三正确。[来源:Zxxk.Com]
[实验结论] 该溶液为部分变质的NaOH溶液。
[反思交流] CO 与NaOH溶液反应没有明显现象,除了选用试剂验证产物碳酸钠的存在能证明两者发生反应外,是
2
否有其他办法证明两者反应呢?
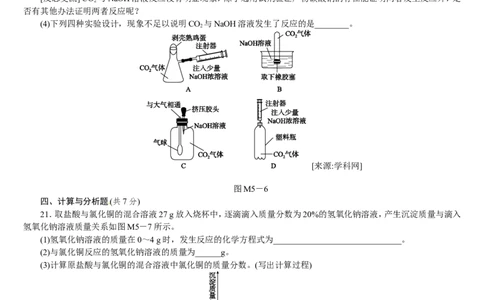
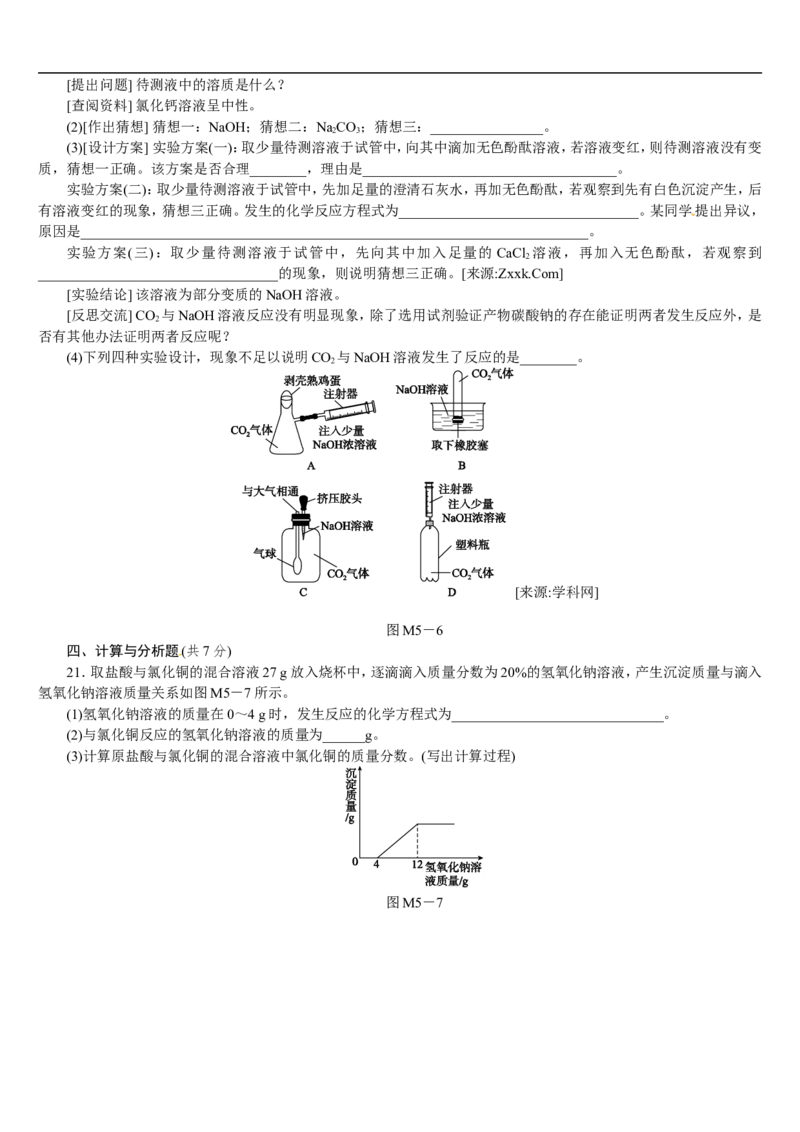
(4)下列四种实验设计,现象不足以说明CO 与NaOH溶液发生了反应的是________。
2
[来源:学科网]
图M5-6
四、计算与分析题(共7分)
21.取盐酸与氯化铜的混合溶液27 g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入
氢氧化钠溶液质量关系如图M5-7所示。
(1)氢氧化钠溶液的质量在0~4 g时,发生反应的化学方程式为______________________________。
(2)与氯化铜反应的氢氧化钠溶液的质量为______g。
(3)计算原盐酸与氯化铜的混合溶液中氯化铜的质量分数。(写出计算过程)
图M5-7[来源:学科网]
参考答案
1.D 2.B 3.A 4.D 5.B 6.C 7.B 8.D 9.B 10.C 11.A 12.C 13.A 14.C 15.D
16.(1)煮沸 (2)过滤 (3)Zn (4)太阳能等
(5)变小 (6)②
17.(1)CO (2)①2HCl+Fe===FeCl +H ↑
2 2 2
置换反应 ②盐
18.(1)有红色物质析出 Fe +CuSO ===FeSO+Cu
4 4
(2)Cu+2AgNO===Cu(NO )+2Ag
3 3 2
(3)探究铁、铜和银三种金属的活动性顺序
19.(1)二氧化碳被水溶解了
(2)有气泡产生 NaCO+2HCl===2NaCl+HO+CO↑ 有白色沉淀产生
2 3 2 2
NaCO+BaCl ===BaCO ↓+2NaCl
2 3 2 3
(3)氢氧化钠的溶解度比氢氧化钙大,二氧化碳能使澄清石灰水变浑浊,所以除去二氧化碳常用氢氧化钠溶液,而检
验二氧化碳一定要用澄清石灰水[来源:学|科|网Z|X|X|K]
20.(1)2NaOH+CO===Na CO+HO [来源:Z#xx#k.Com]
2 2 3 2
(2)NaOH和NaCO
2 3[来源:Zxxk.Com](3)不合理 变质后的溶液也显碱性,都能使指示剂变色
NaCO+Ca(OH) ===CaCO ↓+ 2NaOH
2 3 2 3
碳酸钠与氢氧化钙反应后能生成氢氧化钠,所以不能证明原溶液中是否有NaOH
有白色沉淀生成,加入酚酞后溶液变红
(4)B
21.(1)HCl+NaOH===NaCl+HO (2)8
2
(3)解:设原盐酸与氯化铜的混合溶液中氯化铜的质量为x。
CuCl +2NaOH===Cu(OH) ↓+2NaCl
2 2
135 80
x 8 g×20%
= x=2.7 g
所以原盐酸与氯化铜的混合溶液中氯化铜的质量分数为×100%=10%。
答:原盐酸与氯化铜的混合溶液中氯化铜的质量分数为10%。