文档内容
九年级学生学业质量调查分析与反馈
化学部分 (70 分)
友情提醒:
化学试题共分第Ⅰ卷和第Ⅱ卷两部分,请将本试卷答案按规定填入答题纸相应的位置
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Mg—24 S—32 Fe—56
一、选择题(本题共15题,每小题只有一个选项符合题意,每题2分,共30分。请将各小题
的选项涂在答题卡上)
1.下列自然资源的利用过程中,发生了化学变化的是( )
A.海水晒盐 B.铁矿石炼铁
C.风力发电 D.太阳能供暖
2. 头发的成分能反映一个人的健康状况。根据分析证明:健康人的头发每克约含铁
130mg、锌167~172mg、铝5mg、硼7mg等。这里的铁、锌、铝、硼是指( )
A.元素 B.原子
C.分子 D.单质
3.下列物质的俗名、化学式和物质分类有错误的一组是( )
A.生石灰 CaO 氧化物 B.水银 Hg 单质
C.纯碱 NaOH 碱 D.酒精 C HOH 有机物
2 5
4. 根据右图的信息判断,下列说法错误的是( )
A.硫原子的相对原子质量为32.07 g
B.硫原子的核电荷数为16
C.硫元素属于非金属元素
D.在化学反应中,硫原子容易得到电子
5.粗盐提纯实验的部分操作如图所示,其中错误的是( )
7
号证试考
名姓
级班
校学
镇乡
……………………………………………线……………………………封……………………………密……………………………………………A.取一定量粗盐 B.溶解 C.过滤 D.蒸发
6.厨房中的下列物质放入足量的水中,充分搅拌,能形成溶液的是( )
A.白糖 B.冰块 C.面粉 D.食用油
7.下列实验现象描述错误的是( )
A.镁带在空气中燃烧发出耀眼的白光
B.打开浓盐酸的瓶盖,瓶口出现白烟
C.硫粉在氧气中燃烧,发出蓝紫色火焰
D.电解水时正极产生的气体体积比负极产生的气体体积少
8. 下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而增大的是( )
A.浓盐酸 B.稀硫酸 C.浓硫酸 D.氢氧化钠溶液
9.下列各组物质分别加入足量的水中,能得到无色透明溶液的是( )
A.KNO、NaCl、NaSO B.NaCO、HCl、AgNO
3 2 4 2 3 3
C.CuSO 、KCl 、Ba(NO ) D.MgCl 、NaOH、NH Cl
4 3 2 2 4
10.根据生活经验和所学知识判断,下列做法不合理的是( )
A.用电器短路着火,立即切断电源
B.在冰箱里放入活性炭,除去冰箱里异味
C.室内烤火取暖,放一盆水防止CO中毒
D.处理油锅起火,用锅盖盖灭
11. 善于梳理化学知识,能使你头脑更聪明。以下有错误的一组是( )
化学变化中的能量变化 保护好我们的环境
A B
蜡烛燃烧—放热反应 保护空气—减少有害气体的排放
碳还原二氧化碳—吸热反应 爱护水资源—合理使用农药、化肥
化学符号的含义 日常生活经验
C D
2N—2个氮元素
—氧的化合价为-1
硬水变为软水—生活中常用煮沸的方法
鉴别羊毛、涤纶—点燃嗅闻气味
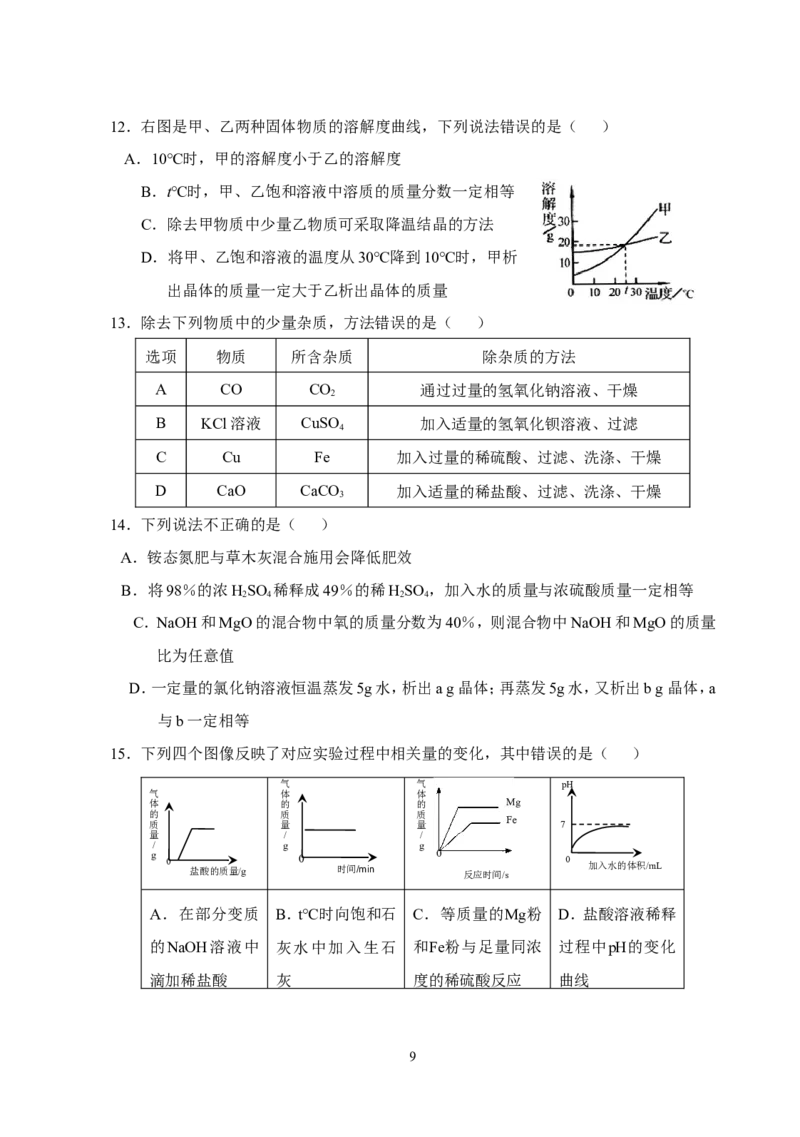
812.右图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( )
A.10℃时,甲的溶解度小于乙的溶解度
B.t℃时,甲、乙饱和溶液中溶质的质量分数一定相等
C.除去甲物质中少量乙物质可采取降温结晶的方法
D.将甲、乙饱和溶液的温度从30℃降到10℃时,甲析
出晶体的质量一定大于乙析出晶体的质量
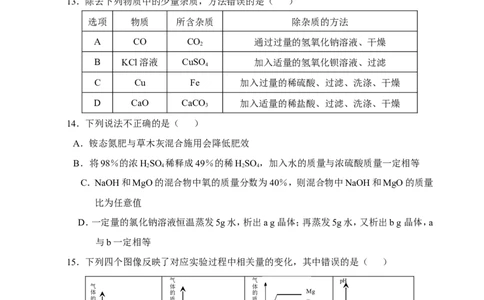
13.除去下列物质中的少量杂质,方法错误的是( )
选项 物质 所含杂质 除杂质的方法
A CO CO 通过过量的氢氧化钠溶液、干燥
2
B KCl溶液 CuSO 加入适量的氢氧化钡溶液、过滤
4
C Cu Fe 加入过量的稀硫酸、过滤、洗涤、干燥
D CaO CaCO 加入适量的稀盐酸、过滤、洗涤、干燥
3
14.下列说法不正确的是( )
A.铵态氮肥与草木灰混合施用会降低肥效
B.将98%的浓HSO 稀释成49%的稀HSO ,加入水的质量与浓硫酸质量一定相等
2 4 2 4
C.NaOH和MgO的混合物中氧的质量分数为40%,则混合物中NaOH和MgO的质量
比为任意值
D.一定量的氯化钠溶液恒温蒸发5g水,析出a g晶体;再蒸发5g水,又析出b g 晶体,a
与b一定相等
15.下列四个图像反映了对应实验过程中相关量的变化,其中错误的是( )
气 气 pH
气 体 体
体 的 的 Mg
的 质 质
质 量 量 Fe 7
量 / /
/ g g
g 0 盐酸的质量/g 0 时间/min 0 反应时间/s 0 加入水的体积/mL
A.在部分变质 B.t℃时向饱和石 C.等质量的Mg粉 D.盐酸溶液稀释
的NaOH溶液中 灰水中加入生石 和Fe粉与足量同浓 过程中pH的变化
滴加稀盐酸 灰 度的稀硫酸反应 曲线
9二、非选择题(本题共4小题,共40分)
16.(9分)化学就在我们身边,请用所学的化学知识填空。
(1)现有四种物质,选择相应物质的字母填空:
A.不锈钢 B.食盐 C.干冰 D.熟石灰
①可用于厨房调味品的是 ▲ ; ②可用于人工降雨的是 ▲ ;
③可用于制造医疗器械的是 ▲ ; ④可用于中和酸性土壤的是 ▲ 。
(2)“五一”期间,同学们为了感受大自然,相约到永丰生态园野炊。
①小明准备的物品有:一次性筷子、保鲜袋、铁锅、菜刀等,这些用品中由有机
合成材料制成的是 ▲ ;
②小红采购食物时,已购买了食盐、矿泉水、羊肉、土豆和黄油,从营养均衡的
角度看,还需采购富含 ▲ (填营养元素的名称)的食物;
③小青切完菜后,为了防止菜刀生锈,她将菜刀 ▲ ;
④小强烧烤食物时,将燃烧的木材架空的目的 ▲ ;
⑤小芳清洗餐具时使用了洗洁精,利用了其 ▲ 作用将餐具洗得更洁净。
17.(12分)实验室利用下图所示装置进行相关实验,请回答问题:
分液漏斗
②
c d
注射器 a
水 5
①
b
A B C D E F
(1)写出有标号仪器的名称:① ▲ ;② ▲ 。
(2)若用B装置制取氧气,B中发生反应的化学方程式是 ▲ 。
(3)老师提出可用碳酸钠粉末与稀盐酸制取二氧化碳,其反应的化学方程为 ▲ 。
为了完成该实验,你认为最合适的发生装置是 ▲ (填A、B或C),该装置的
最大优点是 ▲。
(4)小明用D装置测量产生的CO气体的体积。量筒中凹液面的最低处与图E中 ▲
2
(填a或b)处保持水平,读出体积为6.0ml。实验发现,产生二氧化碳的实际体积
▲ (填大于、等于或小于) 6.0ml,其理由是 ▲ 。
(5)小红用图F验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水
10或二氧化碳,应该采取的实验操作顺序是 ▲ (填序号,可重复选用)。
①从d端通氮气
②从c端通二氧化碳
③从分液漏斗中滴加适量水
④将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
18.(6分)某小组同学将BaCl 溶液与HSO 溶液混合,将反应后的液体过滤,并探究滤液
2 2 4
的成分,请你参与探究并回答相关问题。
【问题与发现】Ⅰ.BaCl 溶液与HSO 溶液混合,发生反应的化学方程式是: ▲ 。
2 2 4
Ⅱ.滤液里的溶质是什么?
【猜想与假设】
猜想1:滤液里的溶质只有HCl;
猜想2:滤液里的溶质有HCl和HSO ;
2 4
猜想3:滤液里的溶质有HCl和 ▲ 。
【探究与验证】
实验操作 现 象 结 论
甲 取少量滤液,加入少量锌粒 有气泡产生 猜想2成立
乙 取少量滤液,加入少量的NaSO 溶液 ▲ 猜想3成立
2 4
【反思与评价】经过小组讨论,分析出 ▲ _(填甲或乙)的结论是错误的,应该将药
品更换成 ▲ (填序号)。
A.AgNO 溶液 B.Ba(NO ) 溶液 C.NaCO 溶液 D.
3 3 2 2 3
Mg
19.(13分)医学上经常用硫酸亚铁糖衣片给贫血患者补铁。某兴趣小组的同学对糖衣片中
硫酸亚铁晶体的制备和组成产生了兴趣并对其进行探究。
探究Ⅰ:利用实验室的废水回收铜、制备硫酸亚铁晶体。
红色固体
适量稀硫酸
实验室含硫酸 固体甲
铝、硫酸亚铁、过量铁 ②
硫酸铜的废水 硫酸亚铁溶液 硫酸亚铁晶体
①
溶液乙
(1)步骤①的化学方程式是 ▲ 。
11(2)固体甲中含有的物质是 ▲ (填化学式,下同) ;红色固体是 ▲ ;溶液乙中的
溶质是 ▲ 。
探究Ⅱ:硫酸亚铁晶体(FeSO•xHO)的化学式。
4 2
【查阅资料】
(1)无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体。
(2)硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解产生金属氧化物和气态非
金属氧化物。
【进行实验】
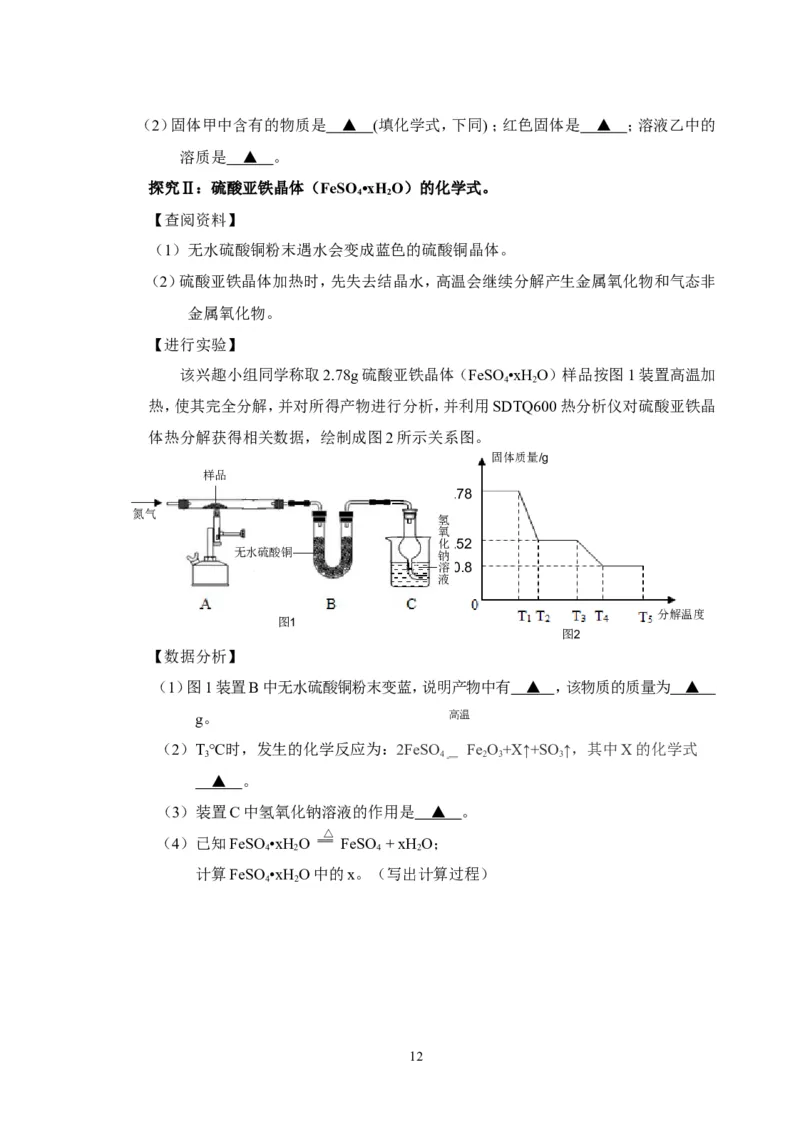
该兴趣小组同学称取2.78g硫酸亚铁晶体(FeSO •xH O)样品按图1装置高温加
4 2
热,使其完全分解,并对所得产物进行分析,并利用SDTQ600热分析仪对硫酸亚铁晶
体热分解获得相关数据,绘制成图2所示关系图。
固体质量/g
样品
2.78
氮气
氢
氧
化1.52
无水硫酸铜 钠
溶0.8
液
分解温度
图1
图2
【数据分析】
(1)图1装置B中无水硫酸铜粉末变蓝,说明产物中有 ▲ ,该物质的质量为 ▲
g。 高温
(2)T℃时,发生的化学反应为:2FeSO Fe O+X↑+SO↑,其中X的化学式
3 4 2 3 3
▲ 。
(3)装置C中氢氧化钠溶液的作用是 ▲ 。
△
(4)已知FeSO •xH O FeSO + xH O;
4 2 4 2
计算FeSO •xH O中的x。(写出计算过程)
4 2
12【交流讨论】实验中要持续通入氮气,否则测出的x值会 ▲ (填偏大、偏小或不
变)。
13九年级化学参考答案(70分)
说明:
1.物质的名称、仪器名称和化学专业术语方面出现错别字,该空不给分。
2.化学方程式的书写,凡写错化学式或漏写反应物、生成物的,该方程式不得分;未配平的,
扣该方程式一半分;化学方程式配平正确,反应条件、沉淀、气体符号漏写或错写的,每
错一处,扣1分;化学式书写全部正确,配平及条件、符号等累计扣分不超过该方程式的
一半分。
3.凡出现与本答案不同的其他合理答案,可参照标准给分。
一、选择题:(每小题2分,共30分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 B A C A C A B D A C C D D D B
二、非选择题:(本题共4小题,每空1分,化学方程式每空2分,19计算3分,共40分)
16.(9分)
(1)① B ② C ③ A ④ D
(2)①保鲜袋 ②维生素 ③洗净擦干等
④增大与空气的接触面积或燃烧更充分 ⑤乳化
17.(12分)
(1) ① 铁架台 ②长颈漏斗
MnO
2 (2)2H O 2H O + O ↑;
2 2 2 2
(3)Na CO +2 HCl == 2NaCl +H O +CO ↑; C;
2 3 2 2
能控制液体的添加量
(4)a ; 大于; 二氧化碳能溶于水
(5)④②①③②
18.(6分)
【问题与发现】BaCl +H SO =BaSO ↓+2HCl
2 2 4 4
【猜想与假设】BaCl
2
【探究与验证】产生白色沉淀
14【反思与评价】甲; B
19.(13分)
探究Ⅰ:(1)Fe+CuSO =FeSO +Cu
4 4
(2)Fe和Cu; Cu ; FeSO 和Al (SO )
4 2 4 3
探究Ⅱ:
【数据分析】
(1)H 0; 1.26
2
(2)SO
2
(3)吸收二氧化硫和三氧化硫,防止污染空气
(4)方法一:
△
FeSO •xH O = FeSO + xH O
4 2 4 2
152+18x 18x
2.78g 1.26g
(152+18x)/ 2.78g = 18x/ 1.26g
解得x=7
方法二:
△
FeSO •xH O = FeSO + xH O
4 2 4 2
152 18x
1.52g 1.26g
152/ 1.52g=18x/ 1.26g
解得x=7
【交流讨论】偏小
15