文档内容
第五章 化工生产中的重要非金属元素
第一节 硫及其化合物
第一课时 硫和二氧化硫
[明确学习目标] 1.了解硫的性质和用途。2.掌握SO 的化学性质及检验方法。
2
学会设计实验验证SO 的还原性及漂白性。3.了解SO 的主要性质。
2 3
学生自主学习
硫
1.硫的物理性质
(1) □ 黄 色晶体,质脆。
(2)溶解性: □ 难溶 于水, □ 微溶 于酒精, □ 易溶 于CS 。
2
2.硫的化学性质
硫在空气中燃烧:□S+O =====SO 。
2 2
硫与一些单质的反应:
S+Fe□=====FeS
S+2Cu□=====Cu S
2
S+H □=====H S
2 2
硫的氧化物
1.二氧化硫
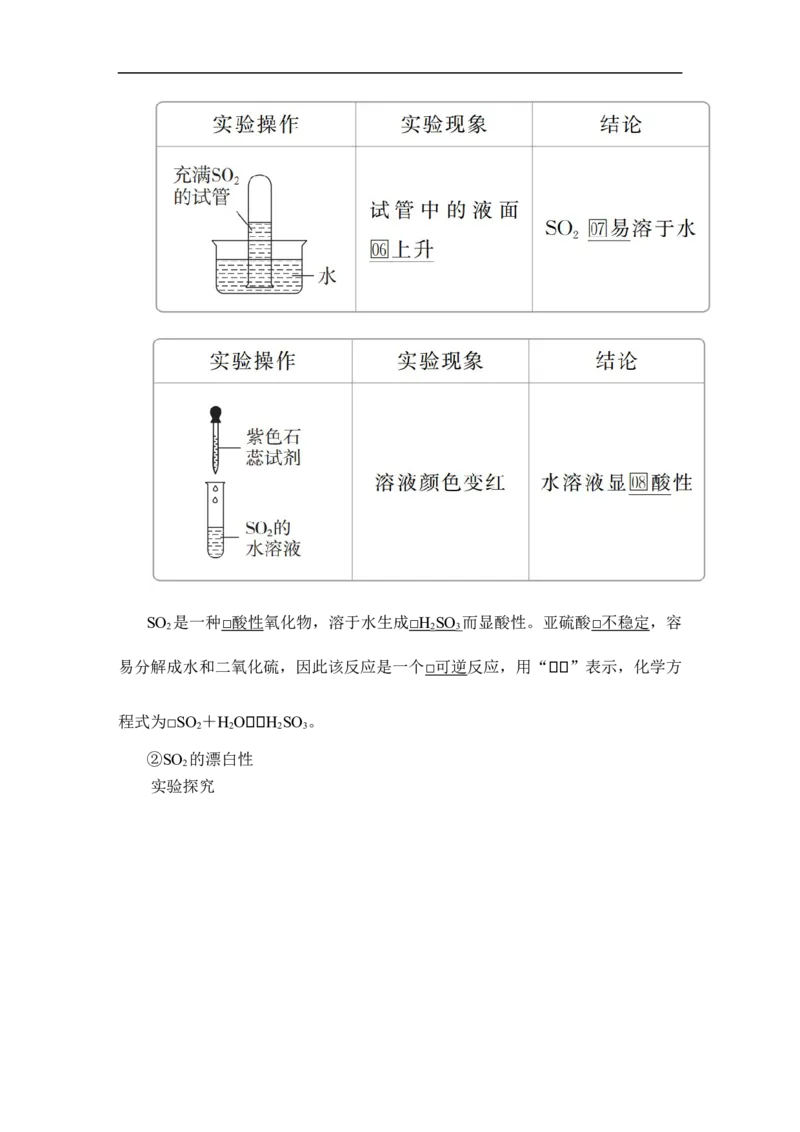
(1)物理性质
(2)化学性质
①SO 与水的反应
2
实验探究SO 是一种 □ 酸性 氧化物,溶于水生成 □ H SO 而显酸性。亚硫酸 □ 不稳定 ,容
2 2 3
易分解成水和二氧化硫,因此该反应是一个 □ 可逆 反应,用“”表示,化学方
程式为□SO +H OH SO 。
2 2 2 3
②SO 的漂白性
2
实验探究③SO 与O 反应的化学方程式为□2SO +O ((((2SO 。
2 2 2 2 3
(3)SO 的用途
2
①漂白纸浆、毛、丝、草帽辫等。
②用于 □ 杀菌、消毒 。
2.三氧化硫
SO 具有酸性氧化物的通性:
3
能溶于水形成硫酸:□SO +H O===H SO 。
3 2 2 4
1.试管壁上有硫附着时应如何洗涤?
提示:依据物理性质,可以用CS 来洗涤。
2
2.如何鉴别SO 和CO 两种气体?可以用澄清石灰水吗?
2 2
提示:鉴别方法:①根据SO 具有刺激性气味鉴别。
2
②根据SO 能使品红溶液褪色鉴别。
2
③根据SO 能使酸性KMnO 溶液或溴水褪色鉴别。
2 4
不能用澄清石灰水鉴别,二者现象相同。
课堂互动探究知识点一 硫的性质
1.硫的还原性
硫在空气中燃烧,发出淡蓝色火焰,同时有刺激性气味的气体产生。硫在氧
气中燃烧时,发出明亮的蓝紫色火焰。
2.硫的氧化性
硫单质的氧化性较弱,与变价金属反应时,一般只能生成低价态金属硫化物,
如S+Fe=====FeS。
1 下列说法中正确的是( )
A.硫是一种难溶于水的黄色晶体
B.硫与金属反应时作氧化剂,与非金属反应时作还原剂
C.硫与铁反应时生成硫化铁
D.硫在空气中燃烧有SO 生成
3
[批注点拨]
[答案] A
[练1] 下列说法正确的是( )
A.硫质脆,微溶于酒精和二硫化碳
B.硫与氢气反应,体现了硫的还原性
C.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
D.从硫的化合价角度分析,单质硫既具有氧化性又具有还原性
答案 D[练2] 不能由两种单质直接化合而成的是( )
A.FeCl B.Na S C.CuS D.SO
3 2 2
答案 C
解析 S与Cu反应生成的是Cu S,而非CuS。
2
硫化氢
(1)物理性质
颜色 状态 气味 毒性
无色 气体 臭鸡蛋气味 剧毒
(2)化学性质
①H S可以在氧气中燃烧
2
O 不足时:2H S+O =====2S↓+2H O;
2 2 2 2
O 足量时:2H S+3O =====2SO +2H O。
2 2 2 2 2
②H S溶于水形成氢硫酸,澄清的氢硫酸放置一段时间会变浑浊,这是因为
2
氢硫酸会和溶解在水中的 O 缓慢反应,产生不溶于水的单质硫:2H S+
2 2
O ===2S↓+2H O。
2 2
③硫化物遇到酸时会产生硫化氢
Na S+2HCl===H S↑+2NaCl。
2 2
知识点二 硫的氧化物
SO 的化学性质
2
(1)SO 的氧化性和还原性
2
SO 中硫元素的化合价为+4价,处于中间价态,既有氧化性又有还原性,
2
主要表现为还原性。
①氧化性
与H S反应:2H S+SO ===3S+2H O。
2 2 2 2
②还原性
SO 除了与O 反应外,还会与酸性 KMnO 溶液、氯水、溴水等反应:5SO
2 2 4 2
+2KMnO +2H O===K SO +2MnSO +2H SO ,从而使KMnO 溶液褪色;
4 2 2 4 4 2 4 4
SO +Cl +2H O===2HCl+H SO ,从而使氯水褪色;
2 2 2 2 4
SO +Br +2H O===2HBr+H SO ,从而使溴水褪色。
2 2 2 2 4
(2)SO 具有酸性氧化物的通性
2①与碱性氧化物(如CaO)反应生成盐
SO +CaO===CaSO 。
2 3
②与碱反应生成盐和水
与NaOH溶液的反应:
SO 少量:2NaOH+SO ===Na SO +H O;
2 2 2 3 2
SO 过量:NaOH+SO ===NaHSO 。
2 2 3
与Ca(OH) 溶液的反应:
2
SO 少量:Ca(OH) +SO ===CaSO ↓+H O;
2 2 2 3 2
SO 过量:Ca(OH) +2SO ===Ca(HSO ) 。
2 2 2 3 2
故不能用澄清石灰水鉴别SO 与CO 。
2 2
(3)二氧化硫与氯水漂白性的比较
①原理比较
②应用举例2 下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、KMnO 溶液、石蕊
2 4
溶液褪色
B.能使品红褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、Na O 都能使红墨水褪色,其原理相同
2 2 2
D.盐酸能使滴有酚酞的NaOH溶液褪色,所以盐酸也有漂白性
[批注点拨]
[解析] SO 能使品红溶液褪色,利用了其漂白性,使溴水、高锰酸钾溶液
2
褪色,利用其还原性,SO 不能使石蕊溶液褪色,A错误;使品红溶液褪色的可
2能是SO 、Cl 、H O 、O 等,B正确;活性炭具有吸附性,SO 利用其和有色物
2 2 2 2 3 2
质的结合,漂白粉和过氧化钠利用其氧化性,原理不同,C错误;盐酸和NaOH
发生中和反应,D错误。
[答案] B
[练3] 下列实验能证明一定有二氧化硫存在的是( )
①能使澄清石灰水变浑浊
②能使湿润的蓝色石蕊试纸变红
③能使品红溶液褪色
④通入足量的氢氧化钠溶液再加 BaCl 溶液有白色沉淀产生,该沉淀溶于稀
2
盐酸
⑤通入溴水能使溴水褪色,再滴加Ba(NO ) 溶液有白色沉淀产生
3 2
A.都能 B.都不能 C.③④⑤ D.只有⑤
答案 D
解析 ①使澄清石灰水变浑浊的也可能是 CO ,错误;②使湿润的蓝色石蕊
2
试纸变红的也可能是CO 、HCl等酸性气体,错误;③使品红溶液褪色的也可能
2
是Cl ,错误;④也可能是CO ,错误;⑤使溴水褪色,证明该气体有还原性,
2 2
再加Ba(NO ) 溶液产生白色沉淀为BaSO ,该气体一定为SO ,正确。
3 2 4 2
[练4] 下列溶液中能够区别SO 和CO 的是( )
2 2
①澄清石灰水 ②H S溶液 ③KMnO 溶液 ④氯水 ⑤品红溶液
2 4
A.①②③ B.②③④
C.②③④⑤ D.全部
答案 C
解析 SO 和CO 都属于酸性氧化物,都能与澄清石灰水反应生成不溶性的
2 2
盐,出现白色沉淀,气体过量时沉淀都会溶解生成酸式盐,所以不能用石灰水来
区别;SO 能将H S氧化成硫单质,能看到黄色沉淀生成,而 CO 不能;SO 能
2 2 2 2被KMnO 溶液和氯水氧化,从而使溶液褪色,且 SO 具有漂白性,能使品红溶
4 2
液褪色,而CO 没有这些性质。所以可用②③④⑤来区别SO 和CO 。
2 2 2
SO 和CO 都能使澄清石灰水变浑浊,若通入的气体过量,则沉淀都会消
2 2
失,故不能用澄清石灰水[或Ba(OH) ]鉴别SO 和CO 。通常用以下方法鉴别。
2 2 2
检验CO 、SO 同时存在的实验设计流程
2 2规律方法
(1)二氧化硫的三种“褪色”:
①二氧化硫能使品红溶液褪色表现漂白性;
②使溴水、氯水及酸性高锰酸钾溶液褪色体现还原性;
③使滴有酚酞的氢氧化钠溶液褪色说明其水溶液呈酸性。
(2)SO 不能漂白紫色石蕊溶液。
2
(3)检验SO 气体的方法是将气体通入品红溶液,溶液褪色后加热又恢复到红
2
色。
本课归纳总结
1.硫在O 中燃烧生成SO 。
2 2
2.SO 是酸性氧化物,可与碱、碱性氧化物反应。
2
SO +2NaOH===Na SO +H O,SO +CaO===CaSO 。
2 2 3 2 2 3
3.SO 具有还原性,可被O 、氯水、溴水、酸性KMnO 溶液等氧化剂氧化。
2 2 4
2SO +O ((((2SO ,SO +Cl +2H O===2HCl+H SO 。
2 2 3 2 2 2 2 4
4.SO 具有漂白性,可与某些有色物质(品红、草帽辫等)化合生成无色不稳
2
定的化合物,受热后又恢复原色。
5.SO 是一种酸性氧化物,可与碱性氧化物、碱反应。
3
学习效果检测
1.能实现下列物质间直接转化的元素是( )单质――→氧化物――→酸或碱――→盐
A.铝 B.硫 C.铜 D.铁
答案 B
解析 硫可依次发生以下反应:S+O =====SO 、SO +H OH SO 、
2 2 2 2 2 3
H SO +2NaOH===Na SO +2H O,Al O 、CuO、Fe O 均不可与水反应。
2 3 2 3 2 2 3 3 4
2.(双选)下列几种溶液既能鉴别CO 和SO ,又能除去CO 中的SO 的是(
2 2 2 2
)
A.溴水 B.酸性KMnO
4
C.饱和NaHCO 溶液 D.澄清石灰水
3
答案 AB
解析 CO 与溴水、酸性KMnO 溶液均不反应;SO 能与溴水或酸性KMnO
2 4 2 4
溶液发生氧化还原反应,使之颜色褪去或变浅,这样既检验了 SO 的存在,又除
2
去了SO ,饱和NaHCO 溶液虽然能除去SO ,但没有明显现象,不能检验 SO
2 3 2 2
的存在,澄清石灰水能与CO 反应,也能与SO 反应,且现象相同,不能用来鉴
2 2
别CO 和SO 。
2 2
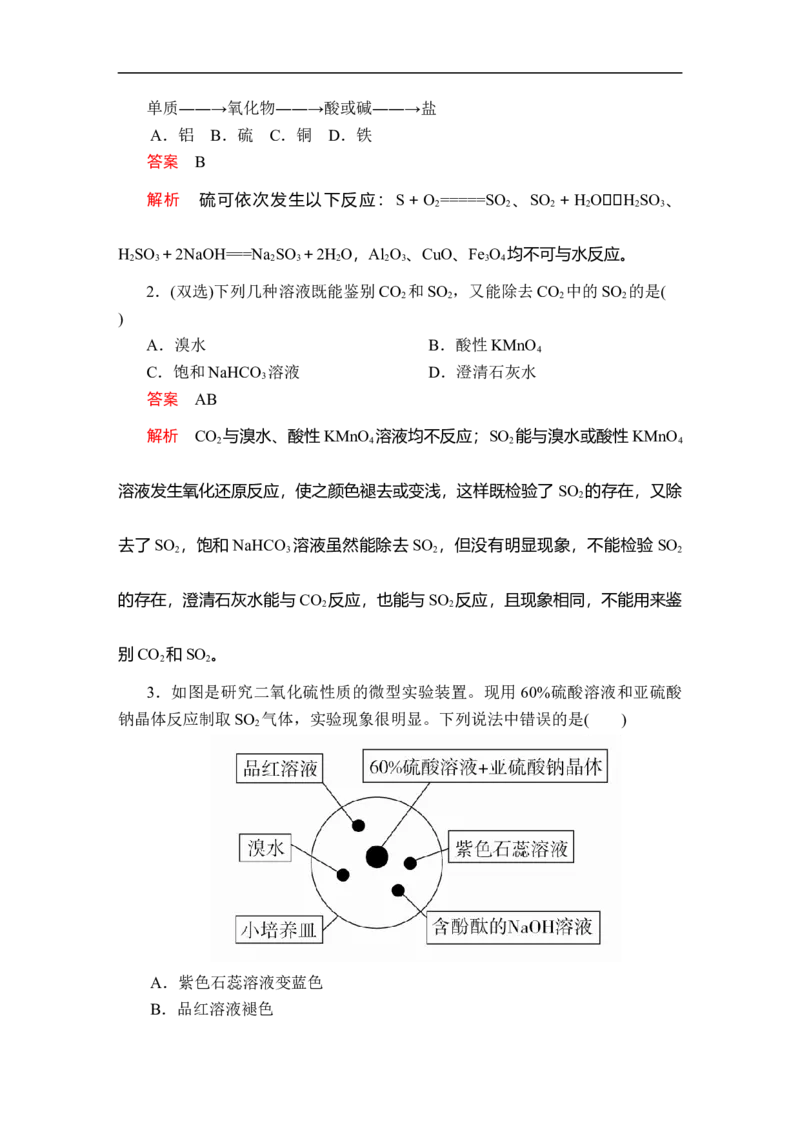
3.如图是研究二氧化硫性质的微型实验装置。现用 60%硫酸溶液和亚硫酸
钠晶体反应制取SO 气体,实验现象很明显。下列说法中错误的是( )
2
A.紫色石蕊溶液变蓝色
B.品红溶液褪色C.溴水橙色褪去
D.含酚酞的NaOH溶液红色变浅
答案 A
解析 SO 与H O反应生成H SO ,H SO 具有酸性,能使紫色石蕊溶液变
2 2 2 3 2 3
红。
4.在括号中填写二氧化硫在下列反应中表现的性质。
A.氧化性 B.还原性
C.漂白性 D.酸性氧化物
(1)SO +Br +2H O===2HBr+H SO ( )
2 2 2 2 4
(2)SO +2H S===3S+2H O( )
2 2 2
(3)SO +2NaOH===Na SO +H O( )
2 2 3 2
(4)SO +Ca(OH) ===CaSO ↓+H O( )
2 2 3 2
答案 (1)B (2)A (3)D (4)D
解析 (1)SO →SO,说明SO 具有还原性。
2 2
(2)SO 使H S中的S被氧化为S,说明具有氧化性。
2 2
(3)(4)SO 与NaOH、Ca(OH) 反应生成盐和水,这些是酸性氧化物的性质。
2 2
5.A、B两种气体都是大气的主要污染物,国家《环境保护法》规定严禁
未经处理就把它们排放到空气中。A是一种单质,其水溶液具有杀菌消毒作用,
B的氧化物用于葡萄酒的酿制过程中。请写出下列变化的化学方程式:
(1)A用于工业上制取漂白粉:______________________________________。
(2)B的水溶液露置在空气中酸性增强:______________________________。
(3)A、B都能分别使品红溶液褪色,但等体积的二者溶于水后的溶液混合后
却不能使品红溶液褪色且溶液酸性增强:______________________。
答案 (1)2Cl +2Ca(OH) ===CaCl +Ca(ClO) +2H O
2 2 2 2 2
(2)2H SO +O ===2H SO
2 3 2 2 4
(3)SO +Cl +2H O===H SO +2HCl
2 2 2 2 4
解析 由题给信息可推知:A为Cl ,B为SO 。
2 2
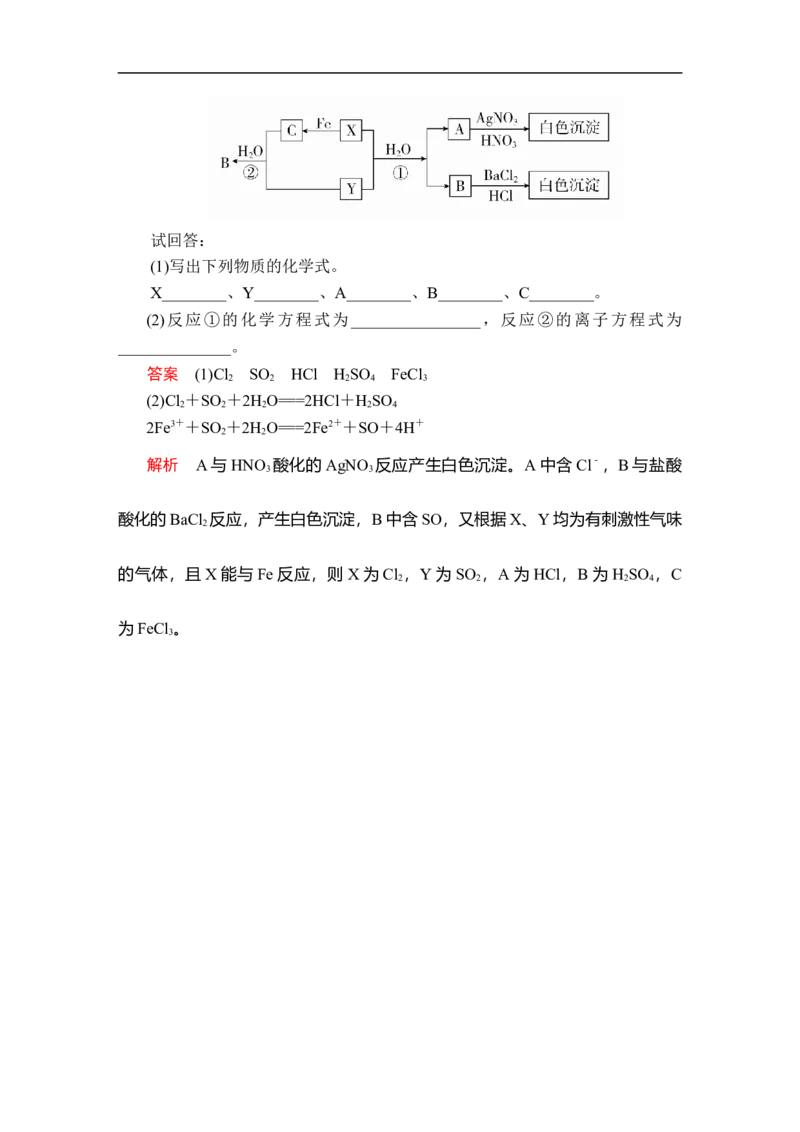
6.已知X、Y都是有刺激性气味的气体,其中 X为黄绿色,Y为无色。有
以下转化关系,部分产物未标出。试回答:
(1)写出下列物质的化学式。
X________、Y________、A________、B________、C________。
(2)反应①的化学方程式为________________,反应②的离子方程式为
______________。
答案 (1)Cl SO HCl H SO FeCl
2 2 2 4 3
(2)Cl +SO +2H O===2HCl+H SO
2 2 2 2 4
2Fe3++SO +2H O===2Fe2++SO+4H+
2 2
解析 A与HNO 酸化的AgNO 反应产生白色沉淀。A中含Cl-,B与盐酸
3 3
酸化的BaCl 反应,产生白色沉淀,B中含SO,又根据X、Y均为有刺激性气味
2
的气体,且X能与Fe反应,则X为Cl ,Y为SO ,A为HCl,B为H SO ,C
2 2 2 4
为FeCl 。
3