文档内容
平顶山市 2012—2013 学年第一学期期末调研考试
九年级化学
相对原子质量:H-1 C-12 O-16 N-14 Si-28 Ca-40
一、选择题(本大题共有10小题,每小题只有一个选项符合题意,请将其字母标号填在下表
相应的空格内。每题1分,共10分)
题号 1 2 3 4 5 6 7 8 9 10
答案
1.下列各物质的变化中,属于化学变化的是
A.矿石粉碎 B.汽油挥发 C.酒精燃烧 D.水结成冰
2.小亮同学在某次测验中写出了下列物质的化学式,其中完全正确的是
A.氯化钠 Nacl B.碳酸钠 Na2CO3 C.高锰酸钾 KmnO D.碳酸钙 CaCO
4 3
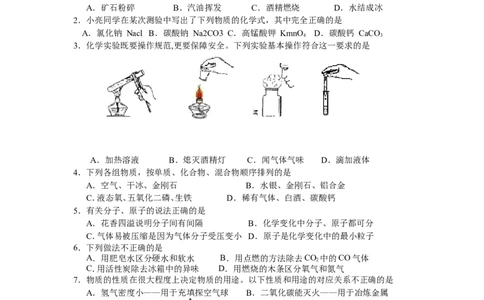
3.化学实验既要操作规范,更要保障安全。下列实验基本操作符合这一要求的是
A.加热溶液 B.熄灭酒精灯 C.闻气体气味 D.滴加液体
4.下列各组物质,按单质、化合物、混合物顺序排列的是
A.空气、干冰、金刚石 B.水银、金刚石、铝合金
C.液态氧、五氧化二磷、生铁 D.稀有气体、白酒、碳酸钙
5.有关分子、原子的说法正确的是
A.花香四溢说明分子间有间隔 B.化学变化中分子、原子都可分
C.气体易被压缩是因为气体分子受压变小 D.原子是化学变化中的最小粒子
6.下列做法不正确的是
A.用肥皂水区分硬水和软水 B.用点燃的方法除去CO 中的CO气体
2
C.用活性炭除去冰箱中的异味 D.用燃烧的木条区分氧气和氮气
7.物质的性质在很大程度上决定物质的用途。以下性质和用途的对应关系不正确的是
A.氢气密度小——用于充填探空气球 B.二氧化碳能灭火——用于冶炼金属
C.金属钨的熔点高——可作灯丝 D.氧气能供给呼吸——用于医疗急救
8.在化学反应MnO +4HCl MnCl +2HO+Cl↑中,化合价降低的元素是
2 2 2 2
A.Mn B.O C.H D.Cl
9.小明用“三”对初中所学化学知识进行了归纳总结,其中正确的是
A.大气污染产生的环境问题有“三种”:温室效应、臭氧层破坏、水体富营养化
B.不显电性的微粒有“三种”:质子、中子、电子
C.一般燃烧必须同时满足“三点”:可燃物、与氧气或空气接触、温度达到着火点
D.过滤操作用到的仪器只有“三种”:漏斗、烧杯、铁架台
10.1.6g某物质完全燃烧后生成4.4gCO 和3.6gHO,关于该物质的组成有以下论断:
2 2
①一定含C、H;②一定不含O;③可能含O;④一定含O;⑤分子中C、H的原子数之比
1为1∶2;⑥分子中C、H的原子数之比为1∶4。其中正确的是
A.①④⑤ B.①③⑥ C.①②⑤ D.①②⑥
二、填空题(本题包括6个小题,每空1分,共16分)
11.请在①氢气、②石墨、③干冰、④氦气、⑤氮气、⑥氧气几种物质中选
择适当物质填空(填序号):可以作制冷剂的是 ;空气中含量最多
的是_____;铅笔中含有的成分是 ;可供人呼吸的是 。
12.生活离不开化学,化学与生活息息相关。
(1)右图的净水装置中,活性炭的主要作用是_______(填字母序号)。
A.沉淀 B.过滤 C.吸附 D.消毒
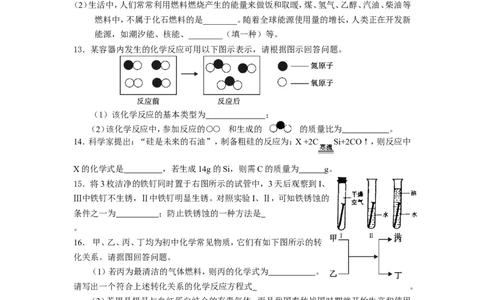
(2)生活中,人们常常利用燃料燃烧产生的能量来做饭和取暖,煤、氢气、乙醇、汽油、柴油等
燃料中,不属于化石燃料的是________。随着全球能源使用量的增长,人类正在开发新
能源,如潮汐能、核能、________(填一种)等。
13.某容器内发生的化学反应可用以下图示表示,请根据图示回答问题。
(1)该化学反应的基本类型为 ;
(2)该化学反应中,参加反应的○○ 和生成的 的质量比为 。
14.科学家提出:“硅是未来的石油”,制备粗硅的反应为:X +2C Si+2CO↑,则反应中
X的化学式是 ,若生成14g的Si,则需C的质量为 g。
15.将3枚洁净的铁钉同时置于右图所示的试管中,3天后观察到I、
Ⅲ中铁钉不生锈,Ⅱ中铁钉明显生锈。对照实验I、Ⅱ,可知铁锈蚀的
条件之一为 ;防止铁锈蚀的一种方法是
。
16. 甲、乙、丙、丁均为初中化学常见物质,它们有如下图所示的转
化关系。请据图回答问题。
(1)若丙为最清洁的气体燃料,则丙的化学式为 。
请写出一个符合上述转化关系的化学反应方程式 。
(2)若甲是极易与血红蛋白结合的有毒气体,丙是我国春秋战国时期就开始生产和使用
的一种金属。请写出一个符合上述转化关系的化学反应方程式
。
三、简答题 (本题包括4个小题,共14分)
17.(2分)下面是我们在课堂或实验室常做的两个对比实验。通过这两个实验,你分别得出
的结论是:甲 ;
乙 ____ ____ 。
2甲 乙
18.(4分)(1)生活中某同学发现铝制品“不生锈”,而铁制品易生锈,便认为金属铁比铝性
质活泼。你认为他的观点是否正确?请解释铝制品“不生锈”的原因。
(2)二氧化碳作灭火剂已有百年历史,当液体二氧化碳从储存容器中喷出后,会由液体迅
速汽化成气体,从而扑灭火灾。请说明用液体CO 灭火的原理。
2
19.(4分)学习知识的目的之一是分析和解决实际的问题。
(1)为防止资源浪费,燃烧时通常将煤块变为粉末状,其原因是 。
(2)在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体。制取轻质碳酸钙粉末是用
净化后的石灰乳(主要成分为氢氧化钙)与二氧化碳作用,制取过程中发生反应的化学
方程式为 。
(3)镁条在氧气中燃烧后,生成物的质量比原来镁条的质量增大,其原因 是
。
(4)CaCl 溶液和NaHCO 溶液反应生成CaCO 。为表示这个反应写出了下列两个化学方程
2 3 3
式:① CaCl + NaHCO CaCO ↓+ NaCl + HCl;
2 3 3
② CaCl + 2NaHCO CaCO ↓+ 2NaCl + CO ↑+ H O。
2 3 3 2 2
有同学认为化学方程式①不合理,请你简述其理由: 。
20.(4分)A~F分别是氢气、氧气、氮气、一氧化碳、二氧化碳、甲烷六种气体中的一种,请回
答下列问题。
(1)C与D在B中燃烧均能生成F,其中C中两种元素的质量比为3:1。
(2)在一定条件下,A和D反应能生成C和水。
请根据(1)和(2)推断:D为 ,E为 。
A与B反应的化学方程式为 ;C与B反应的化学方程式为
。
四、综合应用题 (共10分)
21.(8分)某实验小组对“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(NaO)颗
2 2
粒的装置”感到非常好奇,设计实验进行探究。
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】① 人呼出的气体中主要成分是N、O、CO 和水蒸气等。
2 2 2
② CO
2
+ 2NaOH Na
2
CO
3
+ H
2
O。
【提出猜想】过氧化钠与人呼出的N 或CO 或水蒸气反应并生成氧气。
2 2
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
过氧化钠 燃着木条
(1)实验操作如右图所示。 缓缓通入N
2
3(2)实验现象及结论:观察到 现象,可判断
过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。其中A装置的作用是________,发生
的变化是________变化(填写“物理”或“化学”)。
(2)实验现象及结论:带火星的木条复燃;过氧
化钠与水蒸气发生反应并生成氧气。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。
(1)同学们在老师的指导下设计了如下图所示装置。
(2)实验步骤及记录
①检查装置的气密性,向装置中加入药品。
②打开分液漏斗活塞,向A装置中缓慢加入稀盐
酸。A装置中观察到的现象有
,则A装置中发生反应的化
学方程式为 。
③一段时间后用带火星的木条在D内进行检验。带火星的木条复燃。过氧化钠与二氧化碳
反应并生成氧气。
【实验反思】
(1)根据实验Ⅱ和Ⅲ,过氧化钠与二氧化碳或水蒸气反应后,除生成氧气外还产生了另一
种物质,该物质是________(填“单质”或“化合物”)。
(2)某同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反
应,你认为他的理由是 。
【计算】本实验中,若提供22gCO 气体,则需要含CaCO 90%的大理石多少克?(结果保留
2 3
一位小数)
4平顶山市 2012—2013 学年第一学期期末调研考试
九年级化学参考答案及评分标准
说明:1.考生给出其他合理答案可比照给分。
2.方程式中化学式错不给分,不配平扣0.5分,其他(如必要的反应条件、状态符号
等)见错扣0.5分且共扣0.5分
一、选择题(每小题1分,共10分)
1.C 2.D 3.B 4.C 5.D 6.B 7.B 8.A 9.C 10.D
二、填空题(本题包括6个小题,每空1分,共16分)
11.③ ⑤ ② ⑥
12.(1)C (2)氢气、乙醇 , 太阳能(或风能、地热能等)
13.(1)化合反应 (2)8∶23
14.SiO 12
2
15.(1)有水存在(其他答案合理也可);保持铁制品表面洁净干燥(其他答案合理也可)
16.(1) H Zn+2HCl=ZnCl +H ↑等(2)3CO+Fe O 2Fe+3CO 等
2 2 2 2 3 2
三、简答题 (本题包括4个小题,共14分)
17.(2分) 甲:隔绝氧气(或空气)能灭火 等 乙:二氧化碳能溶于水
18.(4分)(1)该同学观点不正确(1分);因为铝在常温下易与氧气反应(0.5分),表面形成致
密的氧化物薄膜,阻止内层的铝进一步被氧化(0.5分),所以铝制品“不生锈”。(叙述合理即
可)
(2)液体二氧化碳喷出时,汽化吸热使环境温度降低(1分)。产生的不燃烧、不支持燃烧
的气体笼罩在可燃物周围,使可燃物与空气隔绝(1分)。(叙述合理即可)
19.(4分,每问1分)
(1)增大与氧气(或空气)的接触面积,使其充分燃烧
(2)CO + Ca(OH) ===CaCO ↓+ H O
2 2 3 2
(3)生成的氧化镁质量等于镁条质量与参加反应的氧气质量之和
(4) CaCO 和HCl不能同时存在(或CaCO 和HCl能反应)
3 3
20.(4分,每空1分)(1)D:一氧化碳(或CO);E:氮气(或N)
2
(2)2H + O
点燃
2H O CH + 2O
点燃
2H O + CO
2 2 2 4 2 2 2
四、综合应用题 (共10分,计算3分,其余每空1分)
21.(10分)
实验Ⅰ:燃着木条熄灭
实验Ⅱ:提供水蒸气 物理
实验Ⅲ:有气泡冒出,固体逐渐减少 CaCO
3
+ 2HCl CaCl
2
+ H
2
O + CO
2
↑
实验反思:(1)化合物
(2)二氧化碳中混有水蒸气,而水蒸气与过氧化钠反应也生成氧气
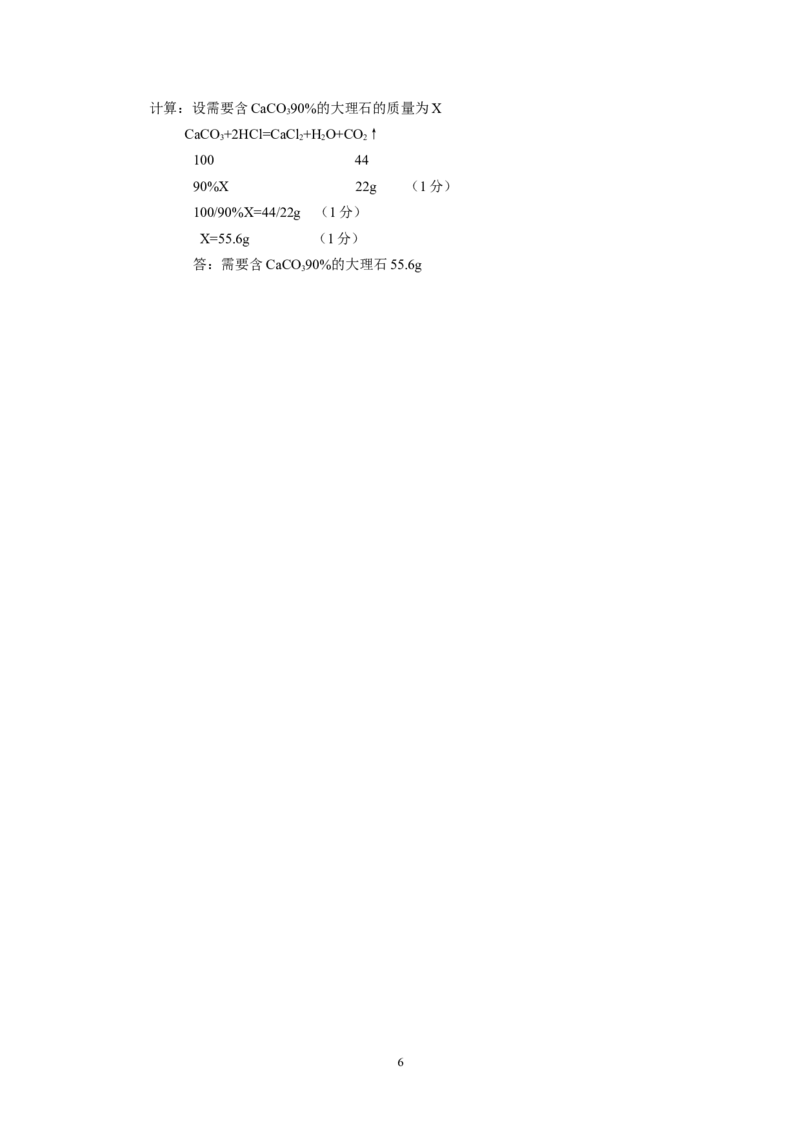
5计算:设需要含CaCO 90%的大理石的质量为X
3
CaCO +2HCl=CaCl +HO+CO↑
3 2 2 2
100 44
90%X 22g (1分)
100/90%X=44/22g (1分)
X=55.6g (1分)
答:需要含CaCO 90%的大理石55.6g
3
6