文档内容
第四章 章末测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
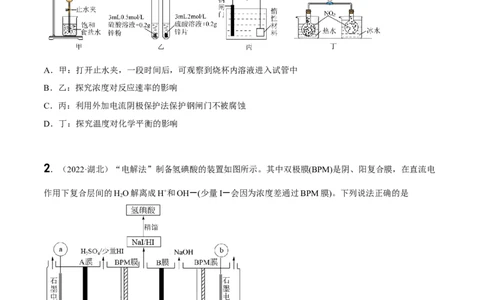
1.(2022·山东·济南市章丘区第四中学高二期中)下列实验装置不能达到实验目的的是
A.甲:打开止水夹,一段时间后,可观察到烧杯内溶液进入试管中
B.乙:探究浓度对反应速率的影响
C.丙:利用外加电流阴极保护法保护钢闸门不被腐蚀
D.丁:探究温度对化学平衡的影响
2
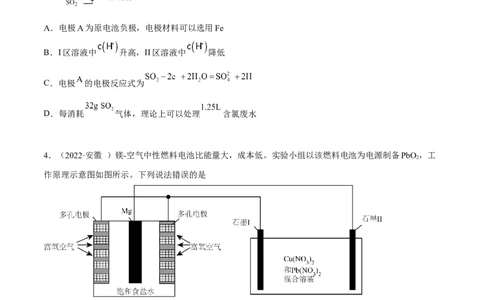
.(2022·湖北)“电解法”制备氢碘酸的装置如图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电
作用下复合层间的HO解离成H+和OH-(少量I-会因为浓度差通过BPM膜)。下列说法正确的是
2
A.a极的电势比b极的低
B.A、B膜均为阳离子交换膜
C.若撤去A膜,对该电解池的工作无影响
D.电解过程中,图中三处HSO 溶液的c(HSO )均不变
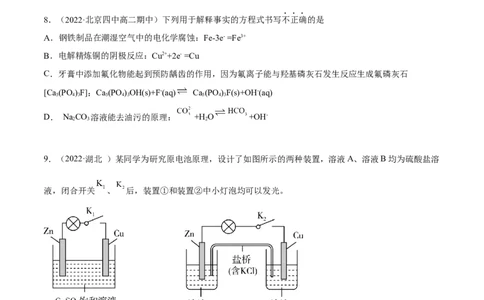
2 4 2 43.(2022·湖北 )某科研小组设计如图所示的原电池装置制取硫酸并处理含氯废水 [
]。下列有关说法正确的是
A.电极A为原电池负极,电极材料可以选用Fe
B.I区溶液中 升高,II区溶液中 降低
C.电极 的电极反应式为
D.每消耗 气体,理论上可以处理 含氯废水
4.(2022·安徽 )镁-空气中性燃料电池比能量大,成本低。实验小组以该燃料电池为电源制备PbO ,工
2
作原理示意图如图所示。下列说法错误的是
A.采用多孔电极有利于增大接触面积和氧气扩散
B.工作时,电源的正极反应式为
C.工作时,Pb2+在石墨II电极上失去电子
D.外电路中流过2mole-,理论上生成1molPbO
2
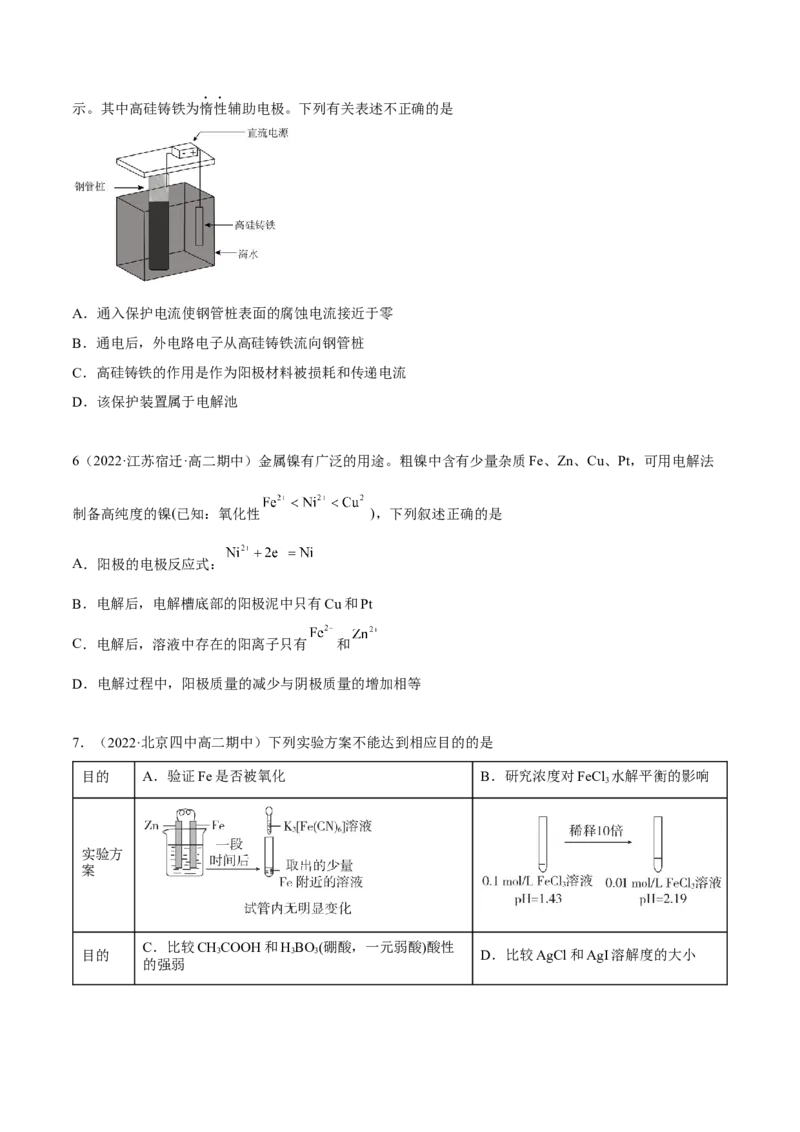
5.(2022·江苏宿迁·高二期中)支撑海港码头基础的钢管桩,常用外加电流法进行防腐,工作原理如图所示。其中高硅铸铁为惰性辅助电极。下列有关表述不正确的是
A.通入保护电流使钢管桩表面的腐蚀电流接近于零
B.通电后,外电路电子从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为阳极材料被损耗和传递电流
D.该保护装置属于电解池
6(2022·江苏宿迁·高二期中)金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法
制备高纯度的镍(已知:氧化性 ),下列叙述正确的是
A.阳极的电极反应式:
B.电解后,电解槽底部的阳极泥中只有Cu和Pt
C.电解后,溶液中存在的阳离子只有 和
D.电解过程中,阳极质量的减少与阴极质量的增加相等
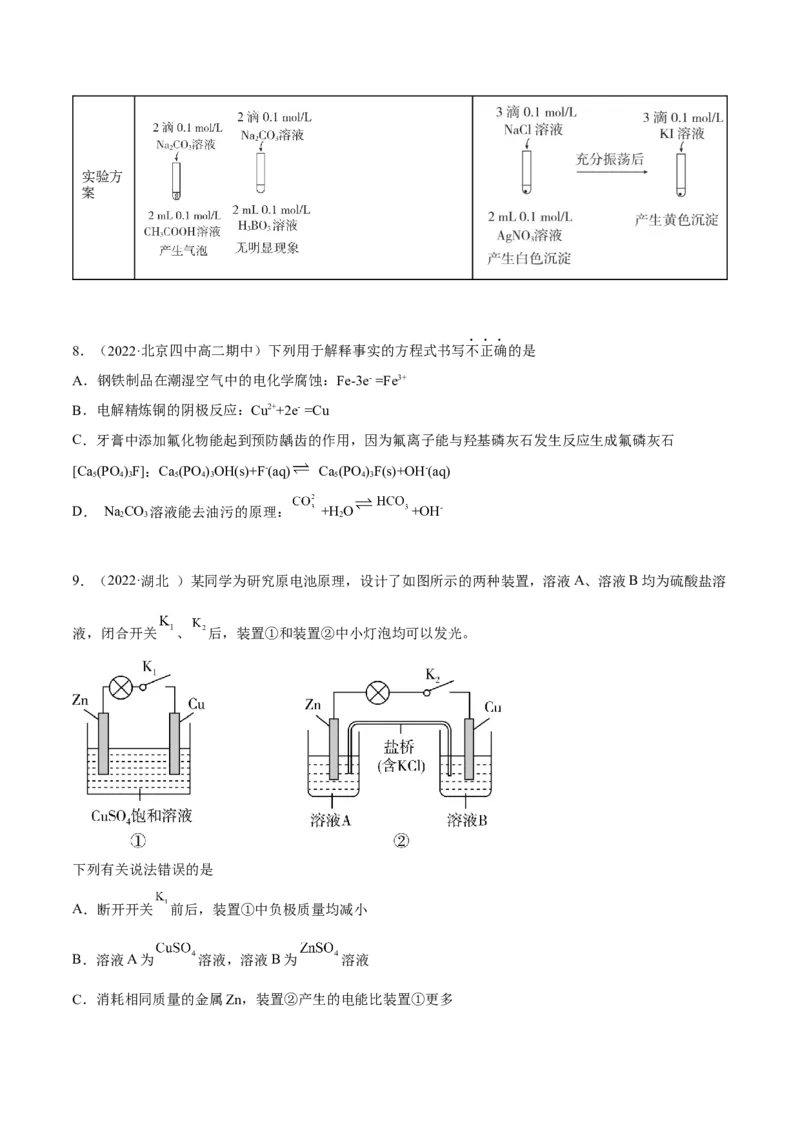
7.(2022·北京四中高二期中)下列实验方案不能达到相应目的的是
目的 A.验证Fe是否被氧化 B.研究浓度对FeCl 水解平衡的影响
3
实验方
案
C.比较CHCOOH和HBO(硼酸,一元弱酸)酸性
目的 3 3 3 D.比较AgCl和AgI溶解度的大小
的强弱实验方
案
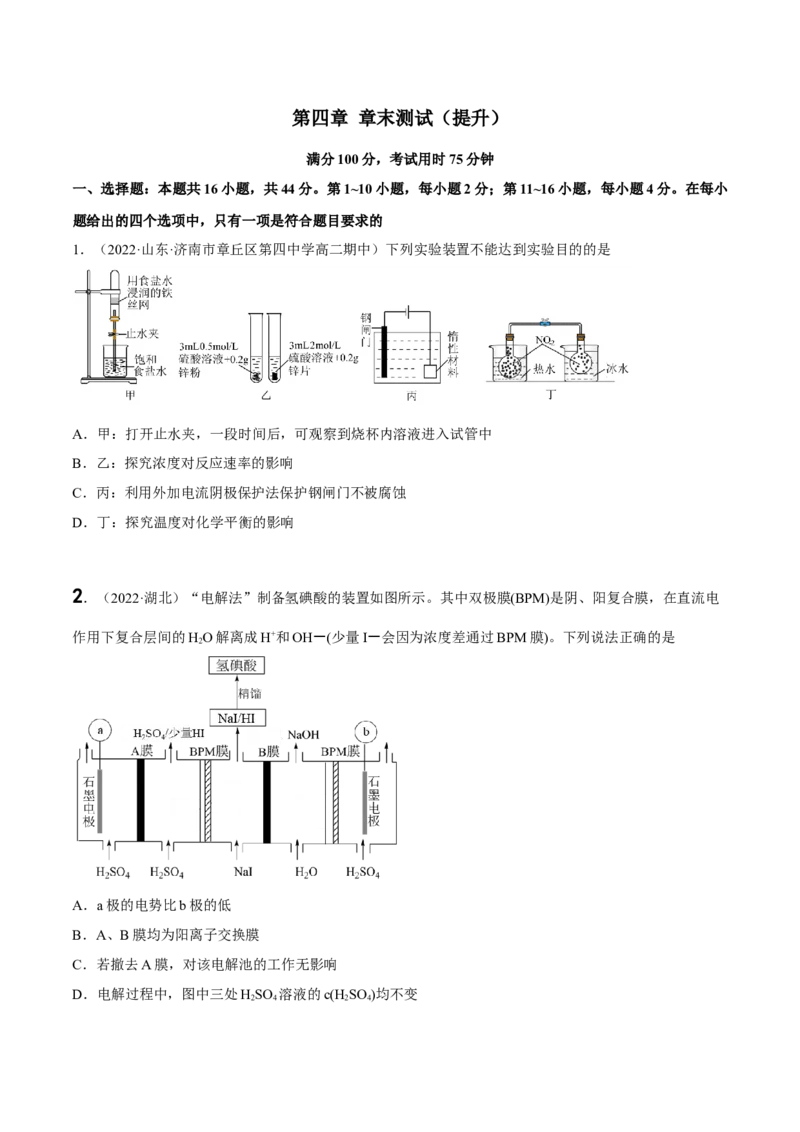
8.(2022·北京四中高二期中)下列用于解释事实的方程式书写不正确的是
A.钢铁制品在潮湿空气中的电化学腐蚀:Fe-3e- =Fe3+
B.电解精炼铜的阴极反应:Cu2++2e- =Cu
C.牙膏中添加氟化物能起到预防龋齿的作用,因为氟离子能与羟基磷灰石发生反应生成氟磷灰石
[Ca (PO )F]:Ca (PO )OH(s)+F-(aq) Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3 5 4 3
D. NaCO 溶液能去油污的原理: +H O +OH-
2 3 2
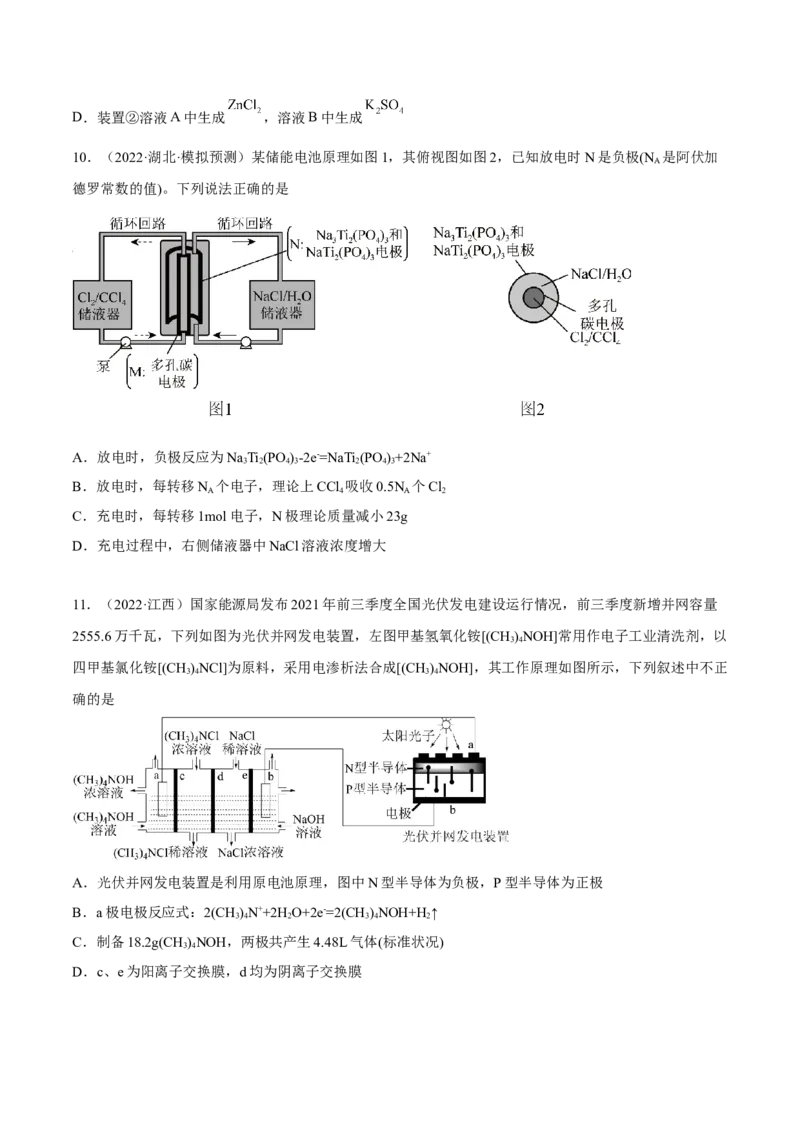
9.(2022·湖北 )某同学为研究原电池原理,设计了如图所示的两种装置,溶液A、溶液B均为硫酸盐溶
液,闭合开关 、 后,装置①和装置②中小灯泡均可以发光。
下列有关说法错误的是
A.断开开关 前后,装置①中负极质量均减小
B.溶液A为 溶液,溶液B为 溶液
C.消耗相同质量的金属Zn,装置②产生的电能比装置①更多D.装置②溶液A中生成 ,溶液B中生成
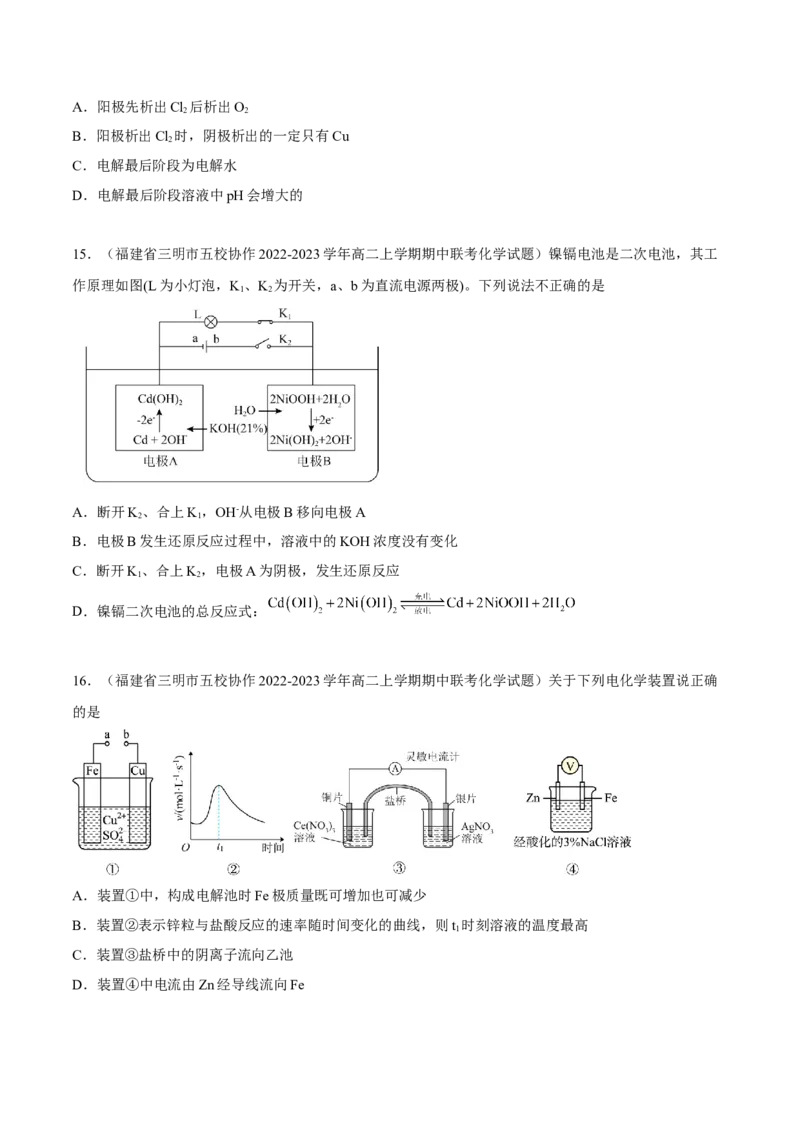
10.(2022·湖北·模拟预测)某储能电池原理如图1,其俯视图如图2,已知放电时N是负极(N 是阿伏加
A
德罗常数的值)。下列说法正确的是
A.放电时,负极反应为NaTi (PO )-2e-=NaTi(PO )+2Na+
3 2 4 3 2 4 3
B.放电时,每转移N 个电子,理论上CCl 吸收0.5N 个Cl
A 4 A 2
C.充电时,每转移1mol电子,N极理论质量减小23g
D.充电过程中,右侧储液器中NaCl溶液浓度增大
11.(2022·江西)国家能源局发布2021年前三季度全国光伏发电建设运行情况,前三季度新增并网容量
2555.6万千瓦,下列如图为光伏并网发电装置,左图甲基氢氧化铵[(CH )NOH]常用作电子工业清洗剂,以
3 4
四甲基氯化铵[(CH )NCl]为原料,采用电渗析法合成[(CH )NOH],其工作原理如图所示,下列叙述中不正
3 4 3 4
确的是
A.光伏并网发电装置是利用原电池原理,图中N型半导体为负极,P型半导体为正极
B.a极电极反应式:2(CH)N++2H O+2e-=2(CH )NOH+H ↑
3 4 2 3 4 2
C.制备18.2g(CH )NOH,两极共产生4.48L气体(标准状况)
3 4
D.c、e为阳离子交换膜,d均为阴离子交换膜12(2022·浙江·宁波市北仑中学高二期中)下列关于金属的腐蚀与防护说法正确的是
A.图①中往Fe电极区滴入2滴K[Fe(CN) ],产生蓝色沉淀
3 6
B.图②中铁丝容易生成Fe O·xH O
2 3 2
C.图③中M可用石墨代替
D.图④中若电源断开,闸门易发生吸氧腐蚀
13.(2022·黑龙江)我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s—SnLi可提高电催化制甲
酸盐的产率,同时释放电能,实验原理如图所示。下列说法错误的是
A.放电时,负极电极反应式为
B.使用催化剂 或者 均能加快化学反应速率,且能有效减少副产物 的生成
C.若电池工作 ,维持电流强度为 ,理论上消耗 的质量为 (已知 )
D.充电时,阳极电极周围 降低
14.(福建省三明市五校协作2022-2023学年高二上学期期中联考化学试题)某溶液中含有两种溶质
CuSO 和NaCl,它们的物质的量之比为2:1,用石墨作电极电解该混合溶液时,下列叙述不正确的是
4A.阳极先析出Cl 后析出O
2 2
B.阳极析出Cl 时,阴极析出的一定只有Cu
2
C.电解最后阶段为电解水
D.电解最后阶段溶液中pH会增大的
15.(福建省三明市五校协作2022-2023学年高二上学期期中联考化学试题)镍镉电池是二次电池,其工
作原理如图(L为小灯泡,K、K 为开关,a、b为直流电源两极)。下列说法不正确的是
1 2
A.断开K、合上K,OH-从电极B移向电极A
2 1
B.电极B发生还原反应过程中,溶液中的KOH浓度没有变化
C.断开K、合上K,电极A为阴极,发生还原反应
1 2
D.镍镉二次电池的总反应式:
16.(福建省三明市五校协作2022-2023学年高二上学期期中联考化学试题)关于下列电化学装置说正确
的是
A.装置①中,构成电解池时Fe极质量既可增加也可减少
B.装置②表示锌粒与盐酸反应的速率随时间变化的曲线,则t 时刻溶液的温度最高
1
C.装置③盐桥中的阴离子流向乙池
D.装置④中电流由Zn经导线流向Fe二.非选择题:共56分。
17.(14分)(2022·广东·广州市第十六中学高二期中)按照要求回答下列问题。
(1)工业上,在强碱性条件下用电解法除去废水中的 ,装置如图所示,依次发生的反应有:
i.
ii.
iii.
①a为电源_______极。
②通电过程中溶液pH不断_______(填“增大”“减小”或“不变”)。
③除去0.1mol ,外电路中至少需要转移_______mol电子。
④为了使电解池连续工作,需要不断补充_______、_______。(填化学式)
(2)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中的 的反应
原理如图所示。
①作负极的物质是_______。
②正极的电极反应式是_______。
(3)通过 传感器可监测 的含量,其工作原理示意图如图所示。①Pt电极上发生的是_______反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式:_______。
18.(15分)(2022·四川·遂宁中学高二期中)两位同学均想利用原电池反应检测金属的活动性顺序,两
人均使用镁片和铝片作电极,甲同学将电极放入2mol/L H SO 溶液A中,乙同学将电极放入6mol/L NaOH
2 4
溶液B中,如图:
(1)原电池中的能量转化过程是将_______。
(2)A中正极的电极反应式为_______,电子的流向是由_______(填“Al→Mg或Mg→Al”)。
(3)B中负极为_______(填元素符号)。
(4)由此实验得出的下列结论中,正确的是_______(填字母)。
A.镁的金属性不一定比铝的金属性强
B.该实验说明金属活动性顺序已过时,已没有实用价值
C.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
D.上述实验证明了“直接利用金属活动性顺序判断原电池中的正负极”这种做法不可靠
(5)两位同学继续用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电
键K时,观察到电流计的指针发生了偏转。
请回答下列问题:①A电极的电极反应式为_______。
②一段时间后,丙池中F电极上出现的现象是_______。
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O 的体积为_______mL(标准状况)。
2
19.(13分)(2022·江苏·马坝高中高二期中)完成下列问题
(1)工厂烟气(主要污染物 、 )直接排放会造成空气污染,需处理后才能排放。用 氧化。 氧化过
程中部分反应的能量变化如图所示。
①已知 。则 转化为 的热化学方程式为_______。
②其他条件不变时,增加 , 氧化 的反应几乎不受影响,其可能原因是_______。
(2)利用如图1装置可将 转化为 ,变废为宝,分别在两极通入 和 ,溶液中 向_______极
(填“A”或“B”)移动,则该电池总反应方程式为_______。(3)利用电解法处理含氮氧化物的废气。实验室模拟电解法吸收NO,装置如图2所示(均为石墨电极),电解
过程中NO转化为硝酸,请写出阳极的电极反应式为_______;电解总反应方程式为_______。
20.(14分)(2022·福建·南靖县第一中学高二期中)应用电化学原理,回答下列问题。
(1)甲中电流计指针偏移时,盐桥(装含琼脂的饱和 溶液)中离子移动的方向:_______离子移向硫酸锌
溶液。(2)乙中正极反应式为_______;若将 换成 ,则负极反应式为_______。
(3)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池_______极相连接。
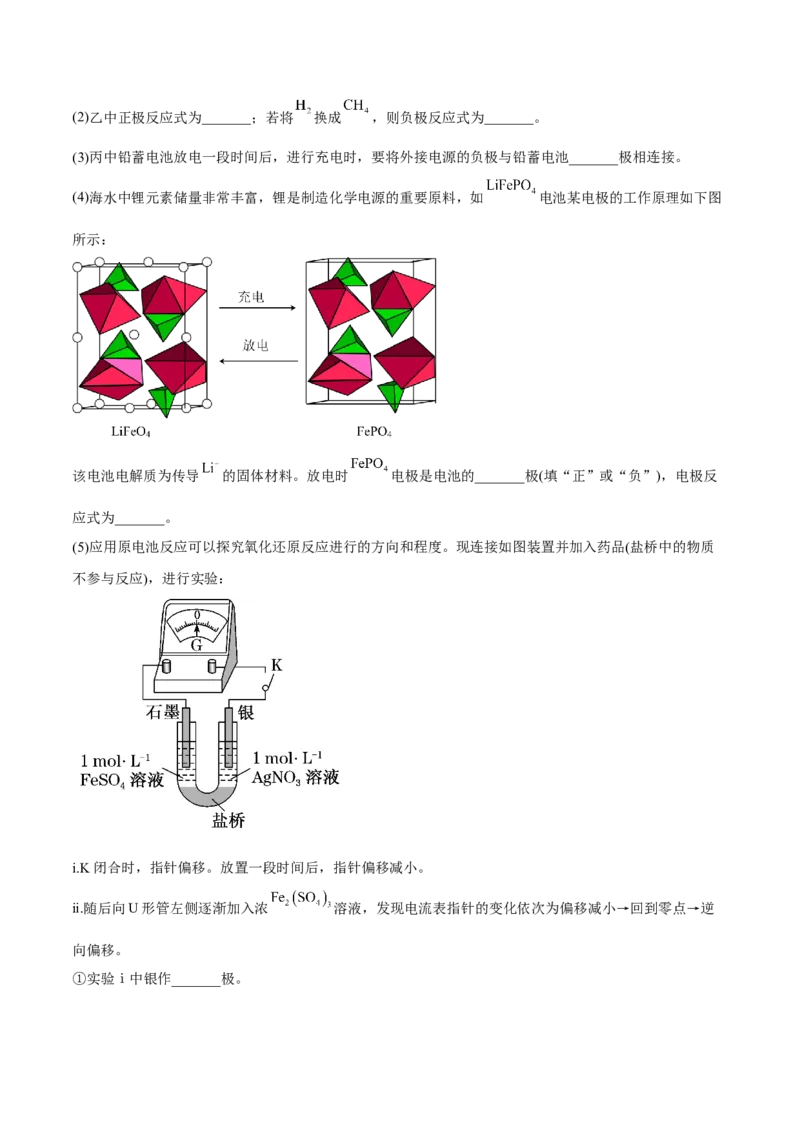
(4)海水中锂元素储量非常丰富,锂是制造化学电源的重要原料,如 电池某电极的工作原理如下图
所示:
该电池电解质为传导 的固体材料。放电时 电极是电池的_______极(填“正”或“负”),电极反
应式为_______。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。现连接如图装置并加入药品(盐桥中的物质
不参与反应),进行实验:
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U形管左侧逐渐加入浓 溶液,发现电流表指针的变化依次为偏移减小→回到零点→逆
向偏移。
①实验ⅰ中银作_______极。②综合实验i、ii的现象,得出 和 反应的离子方程式是_______。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育