文档内容
题型八 综合计算题)
类型1 文字叙述型
1.(2016黄冈)200g稀硫酸与13g锌恰好完全反应,反应后所得溶液的质量是多少?
2.(2016资阳)某食用纯碱中含有少量的氯化钠,为测定该纯碱中碳酸钠(Na CO)的含量,
2 3
现取该纯碱样品12.5g,加入150.0g稀盐酸溶液恰好完全反应,测得反应后溶液总质量变成
158.1g。计算:
(1)反应中产生CO 的质量为________。
2
(2)纯碱样品中NaCO 的质量分数。
2 3
3.(2016云南)为测定某硫酸溶液中溶质的质量分数,化学小组同学取10g该硫酸溶液,
向其中加入21.2gBaCl 溶液,二者恰好完全反应,过滤后称得滤液的质量为28.87g。请计算:
2
(温馨提示:HSO +BaCl ===BaSO ↓+2HCl)
2 4 2 4
(1)反应后生成沉淀的质量是________g。
(2)该硫酸溶液中溶质的质量分数。(计算结果精确到0.1%)
类型2 坐标曲线型
4.(2016咸宁)某学习小组在实验室中用加热KClO 和MnO 混合物的方法制取O ,反应
3 2 2
过程中固体质量变化如图所示,请计算。
(1)制取O 的质量是________g。
2
(2)原混合物中KClO 的质量分数。(写出计算过程,计算结果精确到0.1%)
3第4题图
[来源:Z.xx.k.Com]
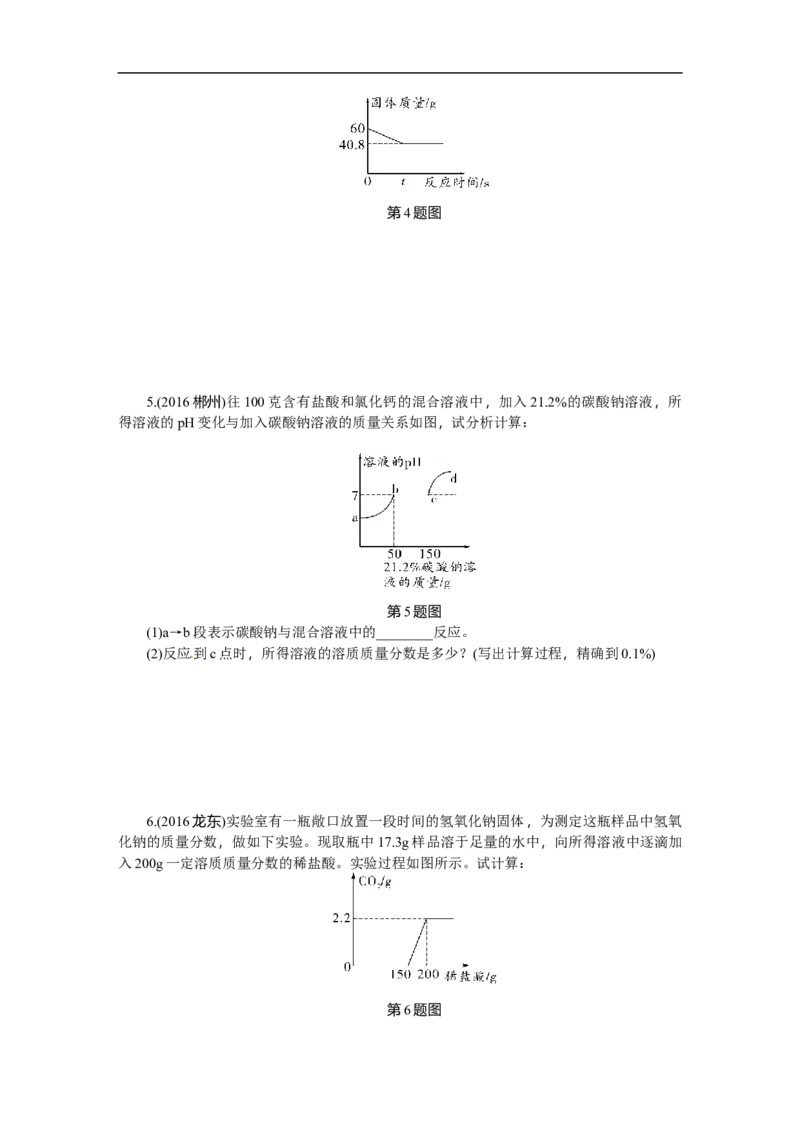
5.(2016郴州)往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所
得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
第5题图
(1)a→b段表示碳酸钠与混合溶液中的________反应。
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)
[来源:学科网ZXXK]
6.(2016龙东)实验室有一瓶敞口放置一段时间的氢氧化钠固体,为测定这瓶样品中氢氧
化钠的质量分数,做如下实验。现取瓶中17.3g样品溶于足量的水中,向所得溶液中逐滴加
入200g一定溶质质量分数的稀盐酸。实验过程如图所示。试计算:
第6题图(1)恰好完全反应时,产生气体的质量是________g。
(2)所加稀盐酸中的溶质的质量分数是多少?
(3)样品中氢氧化钠的质量分数是多少?(结果保留一位小数)
类型3 表格数据型
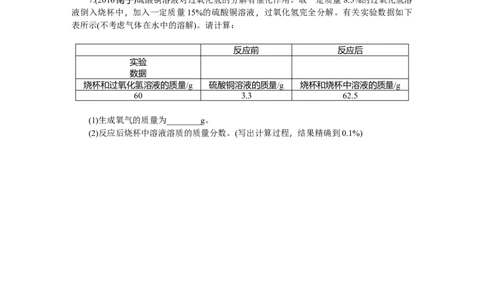
7.(2016南宁)硫酸铜溶液对过氧化氢的分解有催化作用。取一定质量8.5%的过氧化氢溶
液倒入烧杯中,加入一定质量15%的硫酸铜溶液,过氧化氢完全分解。有关实验数据如下
表所示(不考虑气体在水中的溶解)。请计算:
反应前 反应后
实验
数据
烧杯和过氧化氢溶液的质量/g 硫酸铜溶液的质量/g 烧杯和烧杯中溶液的质量/g
60 3.3 62.5
(1)生成氧气的质量为________g。
(2)反应后烧杯中溶液溶质的质量分数。(写出计算过程,结果精确到0.1%)
8.(2016遂宁)某校学习小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石
灰石样品10g加入烧杯中,再把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石
灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应):
实验次数 第1次 第2次 第3次 第4次
加入稀盐酸的质量/g 20 20 20 20
剩下固体的质量/g 7 4 2.6 m
分析表中数据,完成下列问题:
(1)表中m的数值为________。
(2)该石灰石样品中碳酸钙的质量分数为________。(3)计算第一次实验反应结束后所得溶液中溶质的质量分数(计算结果精确到0.1%)。
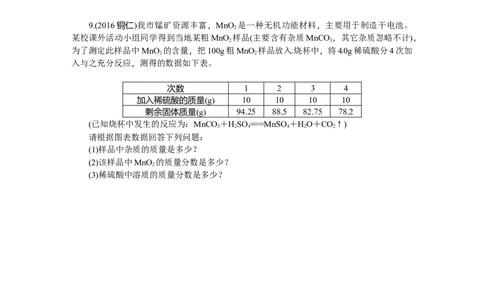
9.(2016铜仁)我市锰矿资源丰富,MnO 是一种无机功能材料,主要用于制造干电池。
2
某校课外活动小组同学得到当地某粗MnO 样品(主要含有杂质MnCO ,其它杂质忽略不计),
2 3
为了测定此样品中MnO 的含量,把100g粗MnO 样品放入烧杯中,将40g稀硫酸分4次加
2 2
入与之充分反应,测得的数据如下表。
次数 1 2 3 4
加入稀硫酸的质量(g) 10 10 10 10
剩余固体质量(g) 94.25 88.5 82.75 78.2
(已知烧杯中发生的反应为:MnCO +HSO ===MnSO +HO+CO↑)
3 2 4 4 2 2
请根据图表数据回答下列问题:
(1)样品中杂质的质量是多少?
(2)该样品中MnO 的质量分数是多少?
2
(3)稀硫酸中溶质的质量分数是多少?
类型4 图片、标签型
10.(2016百色)草木灰是农家肥料,其主要成分是碳酸钾。某化学兴趣小组进行如下实
验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你
回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为________。
(2)反应生成的气体质量为________g。
(3)稀盐酸中溶质质量分数是多少?第10题图
11.(2016江西)小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”
(杂质不参加反应)。操作过程如下:
第11题图
请计算:
(1)20g样品中碳酸钠的质量为________g。
(2)反应后所得滤液中氢氧化钠的质量分数为多少?(写出计算过程)
(3)将200g滤液浓缩成制作“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发
水________g。
类型5 图表综合型
12.(2016广东)过氧化钙(CaO)是一种环境友好的化工原料,工农业生产中用作漂白剂、
2
种子消毒剂及鱼类运输时的制氧剂等。过氧化钙与水反应方程式为:2CaO +
22HO===2Ca(OH) +O↑。
2 2 2
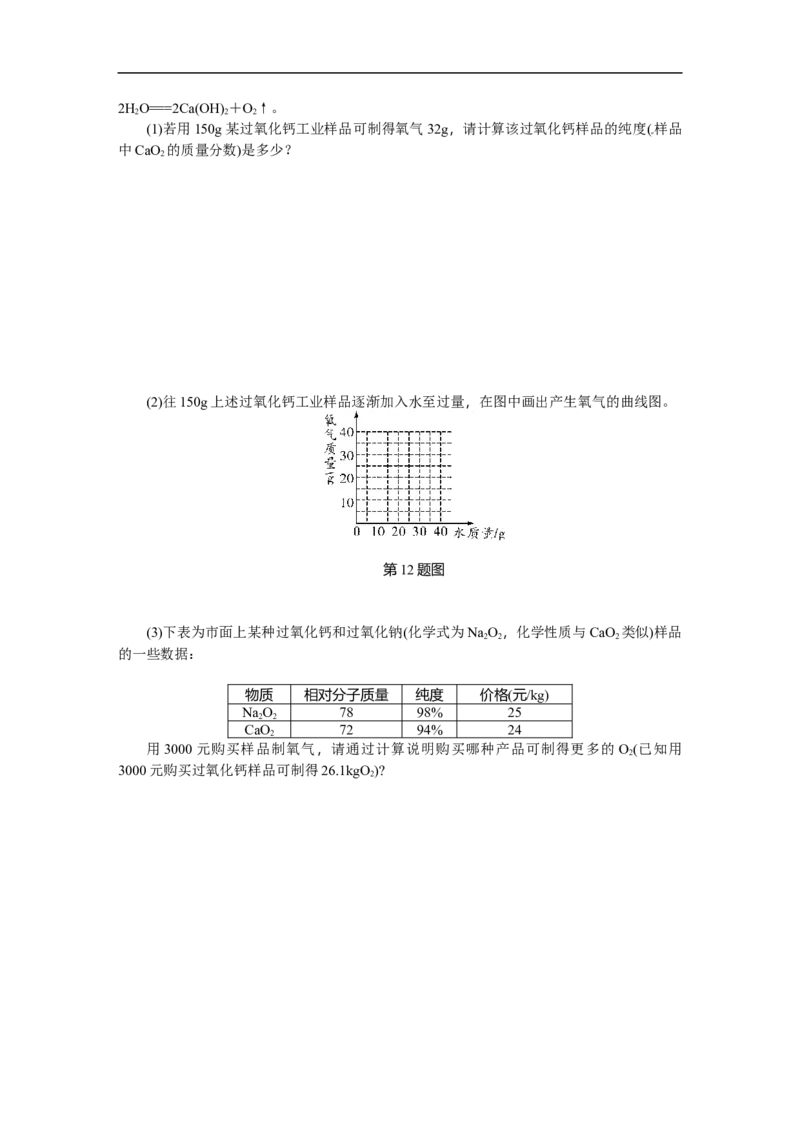
(1)若用150g某过氧化钙工业样品可制得氧气32g,请计算该过氧化钙样品的纯度(样品
中CaO 的质量分数)是多少?
2
[来源:学.科.网Z.X.X.K]
(2)往150g上述过氧化钙工业样品逐渐加入水至过量,在图中画出产生氧气的曲线图。
第12题图
(3)下表为市面上某种过氧化钙和过氧化钠(化学式为NaO,化学性质与CaO 类似)样品
2 2 2
的一些数据:
物质 相对分子质量 纯度 价格(元/kg)
NaO 78 98% 25
2 2
CaO 72 94% 24
2
用3000元购买样品制氧气,请通过计算说明购买哪种产品可制得更多的O(已知用
2
3000元购买过氧化钙样品可制得26.1kgO )?
2题型八 综合计算题
1. 解:设生成氢气的质量为x
Zn+HSO === ZnSO+H↑
2 4 4 2
65 2
13 g x
=
解得:x=0.4 g
则所得溶液的质量为:200 g+13 g-0.4 g=212.6 g
答:所得溶液的质量为212.6 g。
2. (1)4.4 g
(2)解:设纯碱样品碳酸钠的质量为x
NaCO+2HCl=== 2NaCl+CO↑+HO
2 3 2 2
106 44
x 4.4 g
= x=10.6 g
纯碱样品中碳酸钠的质量分数为×100%=84.8%
答:纯碱样品中碳酸钠的质量分数为84.8%。
3. (1)2.33
(2)解:设硫酸溶液中溶质的质量为x
HSO +BaCl === BaSO↓+2HCl
2 4 2 4
98 233
x 2.33 g
= x=0.98 g
硫酸溶液中溶质的质量分数为×100%=9.8%
答:硫酸溶液中溶质的质量分数为9.8%。
4. (1)19.2
(2)解:设原混合物中氯酸钾的质量为x
2KClO===== 2KCl+3O↑
3 2
245 96
[来源:Zxxk.Com]
x 19.2 g
=
x=49 g
原混合物中氯酸钾的质量分数为×100%≈81.7%
答:原混合物中氯酸钾的质量分数约为81.7%。
5. (1)盐酸
(2)解:设碳酸钠与盐酸反应生成氯化钠的质量为x,生成二氧化碳的质量为y
NaCO+2HCl=== 2NaCl+HO+CO↑
2 3 2 2
106 117 44
50 g×21.1% x y
= x=11.7 g
= y=4.4 g
设碳酸钠与氯化钙反应生氯化钠的质量为a,生成碳酸钙的质量为b
NaCO+CaCl === 2NaCl+CaCO ↓
2 3 2 3
106 117 100(150 g-50 g)×21.2% a b
= a=23.4 g
= b=20 g
反应到c点时,所得溶液的溶质质量分数为
×100%≈15.6%
答:反应到c点时,所得溶液的溶质质量分数约为15.6%。
6. (1)2.2
解:设与碳酸钠反应的稀盐酸溶质质量为x,样品中碳酸钠的质量为y
NaCO+2HCl === 2NaCl+HO+CO↑
2 3 2 2
106 73 44
y x 2.2 g
= x=3.65 g
= y=5.3 g
(2)稀盐酸溶质的质量分数为×100%=7.3%
(3)样品中氢氧化钠的质量分数为×100%≈69.4%
答:(2)所加稀盐酸中的溶质的质量分数是 7.3%。(3)样品中氢氧化钠的质量分数约为
69.4%。
7. (1)0.8
(2)解:设过氧化氢溶液的质量为x
2HO ===== 2HO+O↑
2 2 2 2
68 32
8.5%×x 0.8 g
=
x=20 g
反应后烧杯中溶液溶质的质量分数为×100%=2.2%
答:反应后烧杯中溶液溶质的质量分数为2.2%。
8. (1)2.6 (2)74%
(3)解:设第一次加入稀盐酸充分反应后生成氯化钙的质量为x,生成二氧化碳的质量为
y
CaCO +2HCl === CaCl +HO+CO↑
3 2 2 2
100 111 44
10 g-7 g x y
= =
解得:x=3.33 g y=1.32 g
第一次实验反应结束后所得溶液中溶质的质量分数=×100%≈15.4%
答:第一次实验反应结束后溶液中溶质质量分数约为15.4%。
9. 解:(1)杂质的质量为100 g-78.2 g=21.8 g
(2)该样品中二氧化锰的质量分数为×100%=78.2%
(3)设稀硫酸中溶质的质量分数为 x,由图表数据可知每10 g稀硫酸恰好与5.75 g的
MnCO 完全反应,则
3
MnCO + HSO === MnSO + HO + CO↑
3 2 4 4 2 2
115 98
5.75 g 10 g×x
= x=49%答:稀硫酸中溶质的质量分数为49%。
10. (1)13∶2∶8 (2)8.8
(3)解:设与碳酸钾反应的HCl的质量为x
KCO+2HCl=== 2KCl+CO↑+HO
2 3 2 2
73 44
x 8.8 g
= 解得:x=14.6 g
所以稀盐酸的溶质质量分数为×100%=14.6%
答:稀盐酸的溶质质量分数为14.6%。
11. (1)10.6
(2)解:设反应后生成氢氧化钠的质量为x
NaCO+Ca(OH) === CaCO ↓+2NaOH
2 3 2 3
106 80
10.6 g x
= x=8 g
所得滤液中氢氧化钠的质量分数为×100%=4%
答:反应后所得滤液中氢氧化钠的质量分数为4%。
(3)120
12. (1)解:设样品中CaO 的质量为x
2
2CaO+2HO=== 2Ca(OH) +O↑
2 2 2 2
144 32
x 32 g
= x=144 g
过氧化钙样品中CaO 的质量分数为 ×100%=96%
2
答:该过氧化钙样品的纯度是96%。
(2)
(3)3000元可购买的NaO 质量为×98%=117.6 kg
2 2
设生成氧气的质量为y
2NaO+2HO=== 4NaOH+O↑
2 2 2 2
156 32
117.6 kg y
=
y≈24.1 kg<26.1 kg
因此购买过氧化钙样品可制得更多的氧气。