文档内容
碳和碳的氧化物-一氧化碳还原氧化铁的
实验重难点梳理及常考题型
M =29
空气
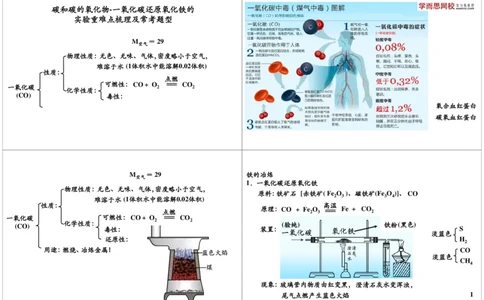
物理性质:无色、无味、气体,密度略小于空气,
难溶于水 (1体积水中能溶解0.02体积)
性质:
点燃
可燃性:CO+ O CO
一氧化碳 2 2
化学性质:
(CO) 毒性:
氧合血红蛋白
碳氧血红蛋白
M =29 铁的冶炼
空气
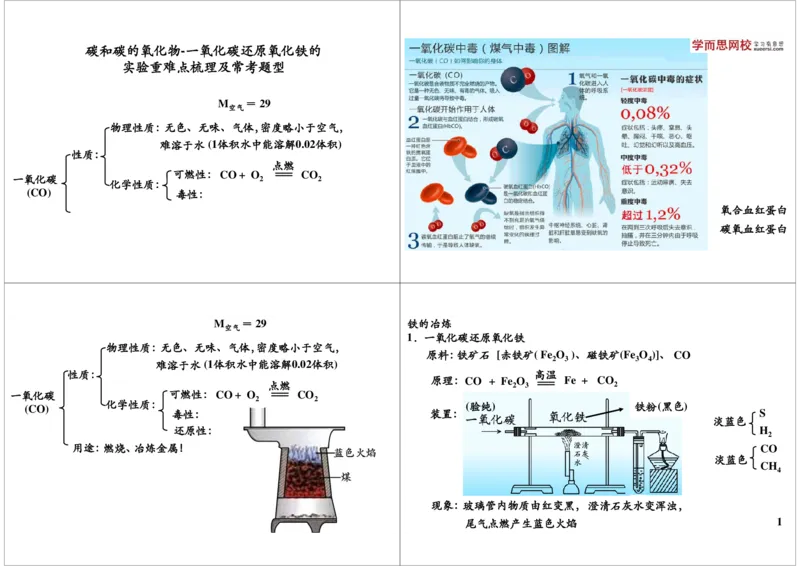
1.一氧化碳还原氧化铁
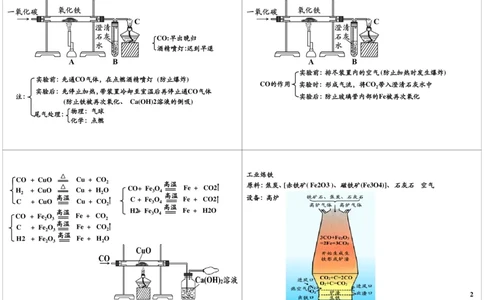
物理性质:无色、无味、气体,密度略小于空气,
原料:铁矿石 [赤铁矿( Fe O )、磁铁矿(Fe O )]、 CO
2 3 3 4
难溶于水 (1体积水中能溶解0.02体积)
性质: 高温
原理:CO + Fe O Fe + CO
点燃 2 3 2
一氧化碳 可燃性:CO+ O CO
2 2
(CO) 化学性质: (验纯) 铁粉(黑色)
毒性: 装置: S
淡蓝色
还原性: H
2
用途:燃烧、冶炼金属! CO
淡蓝色
CH
4
现象:玻璃管内物质由红变黑,澄清石灰水变浑浊,
尾气点燃产生蓝色火焰 1CO:早出晚归
酒精喷灯:迟到早退
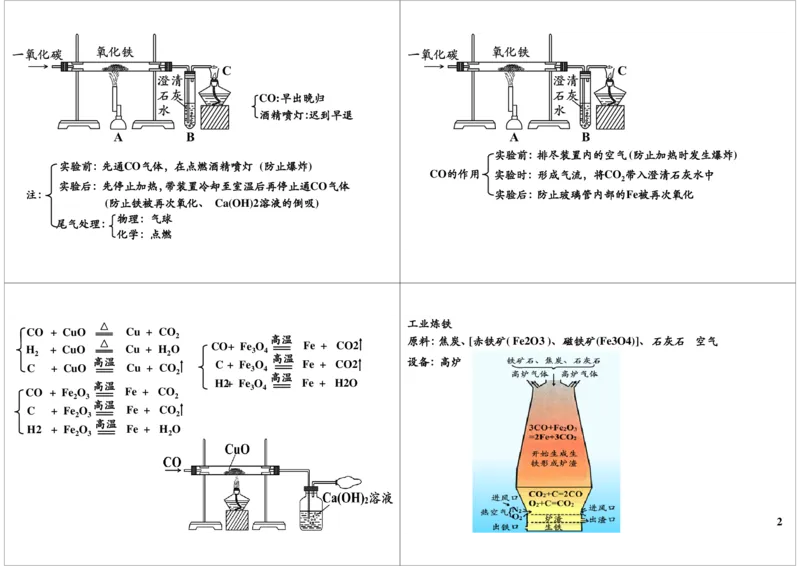
实验前:排尽装置内的空气(防止加热时发生爆炸)
实验前:先通CO气体,在点燃酒精喷灯 (防止爆炸)
CO的作用 实验时:形成气流,将CO 带入澄清石灰水中
2
实验后:先停止加热,带装置冷却至室温后再停止通CO气体
注: 实验后:防止玻璃管内部的Fe被再次氧化
(防止铁被再次氧化、 Ca(OH)2溶液的倒吸)
物理:气球
尾气处理:
化学:点燃
工业炼铁
CO + CuO Cu + CO
2
高温 原料:焦炭、[赤铁矿( Fe2O3 )、磁铁矿(Fe3O4)]、石灰石 空气
CO+ Fe O Fe + CO2
H + CuO Cu + H O 3 4
2 2
高温
高温 C + Fe O Fe + CO2 设备:高炉
C + CuO Cu + CO 3 4
2
高温
H2+ Fe O Fe + H2O
CO + Fe O 高温 Fe + CO 3 4
2 3 2
高温
C + Fe O Fe + CO
2 3 2
高温
H2 + Fe O Fe + H O
2 3 2
2高温 【例1】(2011清华附中月考) 在右图装置中通入X气体,并在管口P处点燃,实
原理:3CO+ Fe O 2Fe + 3CO
2 3 2 验结果澄清石灰水变浑浊,则X可以是( )
高温
3C+2Fe O 4Fe + 3CO A. H
2 3 2 2
点燃 B. CO
C + O CO
2 2 C. CO p
点燃 2
C + O CO D. O
2 2
点燃
CO +O CO
2
高温
CaCO CaO + CO
3 2
高温
CO + C CO
2
【例2】在密闭容器中盛有一氧化碳和氧气的混合气体共25g,点燃后将容器
中的全部气体通过足量的石灰水后,还能得到3g气体。对点燃前容器
中的一氧化碳和氧气的组成判断正确的是( )
A. 分别是20g和5g
B. 分别是17g和8g
C. 分别是14g和11g
D. 分别是12.5g
3