文档内容
北京市朝阳区 2019~2020 学年度第一学期期末质量检测高一年级化学
试卷
每小题只有一个选项符合题意。14个小题,每小题3分,共42分
1.下列物质中,属于酸的是
A. NaO B. NaOH C. MgCl D. HSO
2 2 2 4
2.下列物质中,属于电解质的是
A. Cu B. C. NaCl D. 氯水
3.当光束通过下列分散系时,能观察到丁达尔效应的是
A. KCl溶液 B. Fe(OH) 胶体
3
C. NaOH溶液 D. CuSO 溶液
4
4.下列含有共价键的物质是
A. NaCl B. HO C. MgCl D. KI
2 2
5.铟(In)是一种非常贴近我们生活的主族元素,手机、电脑、电视屏幕使用的都是含铟的导电玻璃。
的最外层电子数是3,下列说法不正确的是
A. In的原子核外有49个电子
B. 与 互 为同位素
C. In与Al处于同一主族
D. 的中子数为113
6.以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是
A. 反应③表明CO 具有酸性氧化物的性质
2
B. 反应④说明NaHCO 的稳定性强于NaCO
3 2 3C. 反应⑤、⑥可用于潜水艇中氧气的供给
D. 上述转化中发生的反应有分解反应、化合反应、置换反应
7.下列关系正确的是
A. 原子半径:Na<Cl B. 金属性:K>Na
C. 酸性:HPO >HSO D. 稳定性:HBr>HCl
3 4 2 4
8.CO与O 反应生成CO 的历程如下(部分微粒未画出):
2 2
下列分析不正确的是
A. CO 分子的空间结构是直线型
2
B. 在该过程中,CO断键形成C和O
C. CO和O生成了具有极性共价键的CO
2
D. CO和O生成CO 的过程涉及了电子转移
2
9.下列说法中不正确的是
A. 常温常压下,22.4 L N 中含有2 mol N
2
B. 0.5 mol Na SO 中含有的Na+ 的数目约为6.02×1023个
2 4
C. 配制500 mL 0.1 mol/L NaOH溶液,需要NaOH的质量为2 g
D. 在标准状况下,20 mL NH 和60 mL O 所含分子个数比为1∶3
3 2
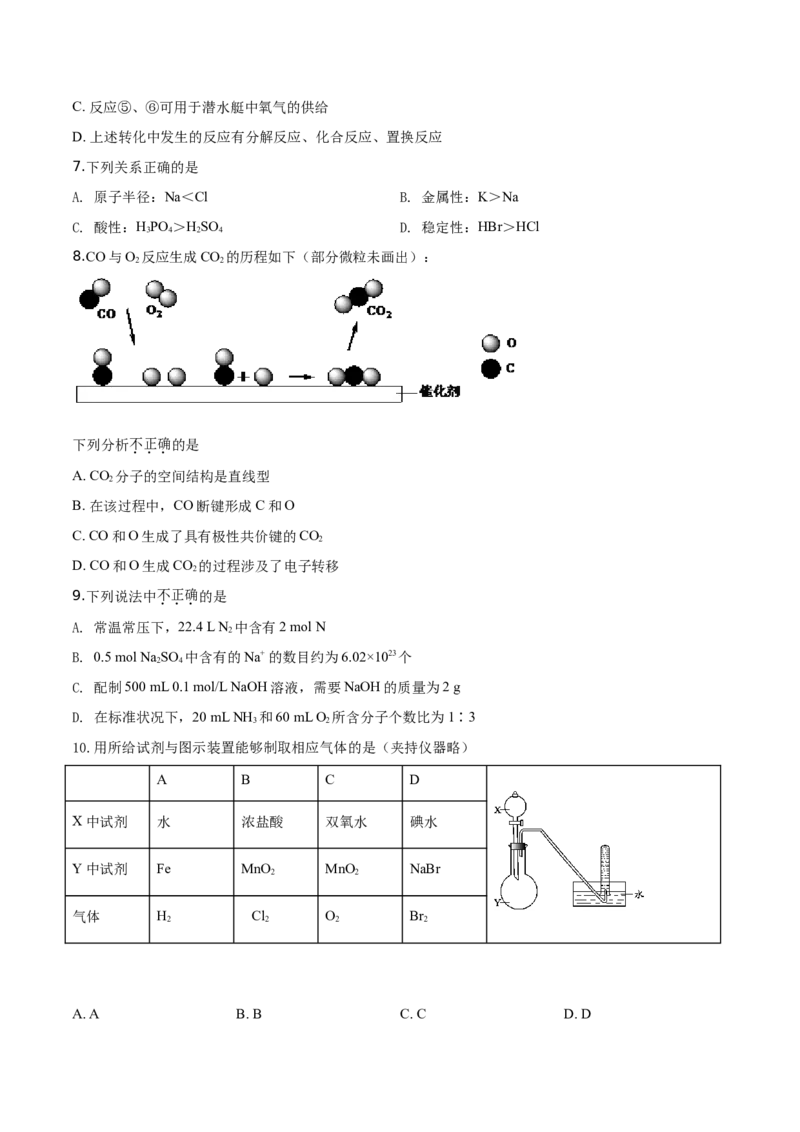
10.用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)
A B C D
X中试剂 水 浓盐酸 双氧水 碘水
Y中试剂 Fe MnO MnO NaBr
2 2
气体 H Cl O Br
2 2 2 2
A. A B. B C. C D. D11.下列解释事实的方程式不正确的是
A. 用稀NaOH溶液吸收氯气:Cl + 2OH- = Cl- + ClO- + H O
2 2
B. 用FeCl 溶液“腐蚀”覆铜板:Cu + 2Fe3+ = 2Fe2+ + Cu2+
3
C. 常温下,新切开的钠的光亮表面很快变暗:2Na + O = Na O
2 2 2
D. Cl 的氧化性强于Br :Cl + 2Br- = 2Cl- + Br
2 2 2 2
12.打印机使用的墨粉中含有Fe O。它的一种制备方法是:将FeSO 溶液、Fe (SO ) 溶液按一定比例混合,
3 4 4 2 4 3
再加入一定量的NaOH溶液,水浴加热。反应如下:
反应a:
下列分析不正确的是
A. Fe O 具有磁性
3 4
B. 反应a中,Fe2+ 是还原剂,Fe3+ 是氧化剂
C. 从左至右,反应a各物质的系数依次为1、2、8、1、4
D. Fe O 与盐酸反应,生成盐和水
3 4
13.根据有关操作与现象,所得结论不正确的是
选项 操作 现象 结论
A 向FeCl 溶液中滴加KI、淀粉溶液 溶液变蓝 I- 有还原性
3
B 向某溶液中滴加AgNO 溶液 产生白色沉淀 溶液一定含有Cl-
3
C 向Al(OH) 沉淀中滴加NaOH溶液 沉淀溶解 铝有一定的非金属性
3
D 向KMnO 滴加FeSO 溶液 紫色褪去 Fe2+有还原性
4 4
A. A B. B C. C D. D
14.x 一种用于食品加热的发热包,主要成分为CaO、铝粉、NaCO。使用时向发热包加适量水,就能持
2 3
续放热,温度可达100℃以上。可能发生的反应如下:
ⅰ.CaO + H O = Ca(OH)
2 2
ⅱ.Ca(OH) + Na CO = CaCO ↓+ 2NaOH
2 2 3 3
ⅲ.2Al + 2H O + 2NaOH = 2NaAlO + 3H ↑
2 2 2
(1)属于复分解反应 的是________(填序号)。
(2)反应ⅲ中,还原剂 是________。(3)使用时需要向发热包加水,水的作用是________(写出两点即可)。
15.全氮类物质因具有超高能量而成为超高含能材料的典型代表。我国科学家成功合成了全氮阴离子盐
——(N )(H O) (NH )Cl,是该领域的重大突破。
5 6 3 3 4 4
(1)氮的原子结构示意图为________。
(2)构成该全氮阴离子盐的离子是Cl-、HO+、NH +和________。
3 4
(3)氯与氢之间的作用对全氮阴离子盐的稳定性起着至关重要的作用。结合原子结构解释氯元素非金属
性强的原因:________。
16.2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸
亚铁锂(LiFePO )。LiFePO 的一种制备方法如下。
4 4
已知:HPO 能电离出PO 3-。
3 4 4
(1)Li在元素周期表中的位置是________。
(2)LiFePO 中,铁元素的化合价为________价。
4
(3)将反应Ⅰ补充完整:____Fe2+ + 2H+ + ____HO =____Fe3+ + 2H O 。____
2 2 2
(4)反应Ⅲ的化学方程式是_________。
17.钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为 ,钠在反应中容易___电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在________里,以隔绝空气。
(3)汽车安全气囊的气体发生剂NaN 可由金属钠生产。某汽车安全气囊内含NaN 、Fe O 和NaHCO 等
3 3 2 3 3
物质。
ⅰ.当汽车发生较严重的碰撞时,引发NaN 分解2NaN = 2Na + 3N,从而为气囊充气。N 的电子式为
3 3 2 2
_________。
ⅱ.产生的Na立即与Fe O 发生置换反应生成NaO,化学方程式是________。
2 3 2
ⅲ.NaHCO 是冷却剂,吸收产气过程释放的热量。NaHCO 起冷却作用时发生反应的化学方程式为
3 3
________。
ⅳ.一个安全气囊通常装有50 g NaN ,其完全分解所释放的N 为_______mol。
3 2(4)工业通过电解NaCl生产金属钠:2NaCl(熔融) 2Na+Cl ,过程如下:
2
已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入CaCl 从而把熔
2
点降至约580℃。
①把NaCl固体加热至熔融状态,目的是________。
②电解时,要避免产生的Na与Cl 接触而重新生成NaCl。用电子式表示NaCl的形成过程________。
2
③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是________。
④过程Ⅰ中,CaCl 能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中CaCl 却不断地被重新生成,
2 2
原因是________。
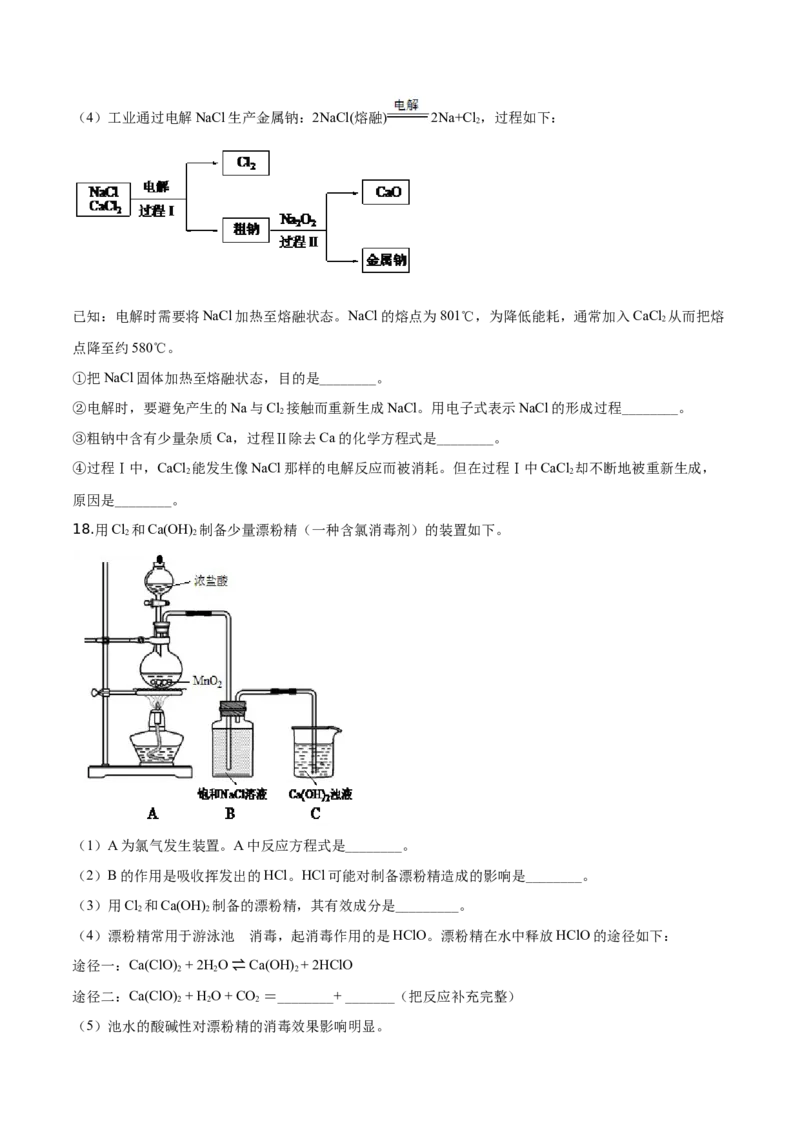
18.用Cl 和Ca(OH) 制备少量漂粉精(一种含氯消毒剂)的装置如下。
2 2
(1)A为氯气发生装置。A中反应方程式是________。
(2)B的作用是吸收挥发出的HCl。HCl可能对制备漂粉精造成的影响是________。
(3)用Cl 和Ca(OH) 制备的漂粉精,其有效成分是_________。
2 2
(4)漂粉精常用于游泳池 的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO) + 2H O ⇌ Ca(OH) + 2HClO
2 2 2
途径二:Ca(ClO) + H O + CO =________+ _______(把反应补充完整)
2 2 2
(5)池水的酸碱性对漂粉精的消毒效果影响明显。①池水碱性过强,杀毒作用会________(填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。通常加入NaCO、NaHCO 以降低酸性,起到降低酸性作用的离子
2 3 3
分别是________(填离子符号)。
(6)某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负
责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投
了过氧化氢(HO)消毒剂。消毒剂为什么不起作用了?_______。
2 2
19.某学习小组探究铁与氯气的反应途径及产物。
【问题提出】
(1)资料1:液氯能在钢瓶中储存。
资料2:铁与氯气在加热条件下能发生反应
资料3:铁与氯水能反应。实验:将铁粉放入氯水中,铁粉溶解,无气泡产生。
①经检验氯水呈酸性,原因 是________(用化学方程式表示)。
②依据实验现象,判断氯水中与Fe反应的微粒可能为_________。
据此,小组认为Fe与Cl 的反应与温度、湿度有关,探究如下。
2
【实验探究】 资料:高于300℃时FeCl 升华
3
(2)湿润的Cl 与Fe的反应:
2
实验 装置 操作及现象
Ⅰ 常温时将铁丝伸入A中,铁丝迅速变黑
将红热的铁丝伸入A中,铁丝剧烈燃
Ⅱ
烧,产生大量棕黄色烟。
①实验Ⅰ,向A中加水,经检验产物中有FeCl ,推测其形成的可能途径:
2
途径一: Fe + Cl = FeCl
2 2
途径二: 2Fe + 3Cl = 2FeCl ,_________。
2 3
②实验Ⅱ,_________(填操作和现象),A中产物含+3价铁。
(3)干燥的Cl 与Fe的反应:
2
实验 装置 操作及现象
常温时将铁丝伸入A中, 铁丝慢慢变
Ⅲ
黑,大量气体剩余。将红热的铁丝伸入A中,铁丝剧烈燃
Ⅳ
烧,产生大量棕黄色烟。
实验Ⅲ中有大量Cl 剩余,实验Ⅳ几乎无Cl 剩余,原因是________。
2 2