文档内容
北京市西城区 2019—2020 学年度第一学期期末试卷
高一化学 2020.1
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
第一部分(选择题)
每小题只有一个选项符合题意(每小题2分)
1.合金的应用促进了人类社会的发展。下列不属于合金的是( )
A.储氢合金 B.青花瓷 C.航母钢甲板 D.钛合金耐压球壳
A. A B. B C. C D. D
2.当光束通过下列分散系时,能观察到丁达尔效应的是( )
A. 盐酸 B. Fe(OH) 胶体 C. 蔗糖溶液 D. Na SO 溶液
3 2 4
3.下列物质不属于电解质的是( )
A. Na B. HSO C. NaOH D. NaSO
2 4 2 4
4.下列仪器不能用于加热的是( )
A. B. C. D.
5.下列元素中,属于第三周期的是( )
A. 氢 B. 碳 C. 氧 D. 氯
6.下列元素的原子半径最大的是
A. Na B. Al C. S D. Cl
7.下列物质中,含有共价键的是( )
A. HCl B. NaO C. MgCl D. NaCl
2 28.下列关于物质分类的叙述不正确的是( )
A. HNO 属于酸 B. Mg(OH) 属于碱
3 2
C. SO 属于氧化物 D. 液氯属于混合物
2
9.下列各组离子能在溶液中大量共存的是( )
A. Na+、H+、CO2- B. Fe2+、SO 2-、OH-
3 4
.
C Na+、Cl-、Ag+ D. K+、NO -、Cl-
3
10.下列反应的离子方程式书写正确的是( )
A. Fe与FeCl 溶液:Fe+Fe3+=2Fe2+
3
B. 稀HCl与KOH溶液:H++OH-=H O
2
C. CaCO 与稀HCl:CO2-+2H+=CO ↑+H O
3 3 2 2
D. FeO与稀HSO :FeO+2H+=Fe3++H O
2 4 2
11.有关NaO 的叙述不正确的是( )
2 2
A. 是淡黄色固体 B. 可以作供氧剂
C. 应密封保存 D. 氧元素的化合价为−2价
12. U常用于核裂变反应。下列关于 U的叙述正确的是( )
A. 质子数为235 B. 电子数为143
C. 核电荷数为235 D. 中子数为143
13.下列物质的电子式的书写,正确的是( )
A. B. C. D.
14.下列关于物质性质的比较,正确的是( )
A. 金属性:Al>Na B. 稳定性:HF>HCl
C. 酸性:HSiO>HSO D. 碱性:Al(OH) >Mg(OH)
2 3 2 4 3 2
15.在化学实验中,具有安全意识是重要的科学素养。下列实验操作不正确的是( )
A. 氢气点燃前,先检验氢气的纯度
B. 金属钠着火时,用干燥的沙土覆盖
C. 稀释浓硫酸时,将水沿烧杯内壁倒入浓硫酸中
D. 闻氯气时,用手在瓶口轻轻扇动,使极少量的氯气飘进鼻孔
16.下列物质间 的转化,不能一步实现的是( )
A. Na→Na O B. Fe O→Fe(OH)
2 2 2 3 3
C. Cl→FeCl D. FeCl →FeCl
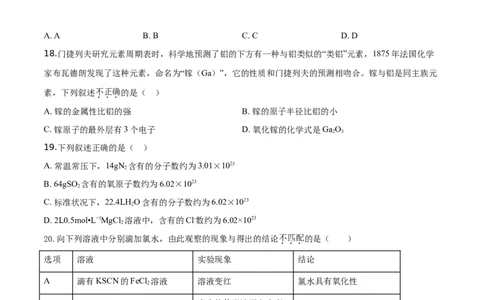
2 3 3 217.下列除杂试剂和分离方法都正确的是( )
选项 物质(括号内为杂质) 除杂试剂 分离方法
A Fe(Cu) 盐酸 过滤
B CO(HCl) NaOH溶液 洗气
2
C FeCl 溶液(FeCl ) 铁粉 过滤
2 3
D Fe O(Al O) 盐酸 过滤
2 3 2 3
A. A B. B C. C D. D
18.门捷列夫研究元素周期表时,科学地预测了铝的下方有一种与铝类似的“类铝”元素,1875年法国化学
家布瓦德朗发现了这种元素,命名为“镓(Ga)”,它的性质和门捷列夫的预测相吻合。镓与铝是同主族元
素,下列叙述不正确的是( )
A. 镓的金属性比铝的强 B. 镓的原子半径比铝的小
C. 镓原子的最外层有3个电子 D. 氧化镓的化学式是GaO
2 3
19.下列叙述正确的是( )
A. 常温常压下,14gN 含有的分子数约为3.01×1023
2
B. 64gSO 含有的氧原子数约为6.02×1023
2
C. 标准状况下,22.4LH O含有的分子数约为6.02×1023
2
D. 2L0.5mol•L−1MgCl 溶液中,含有的Cl-数约为6.02×1023
2
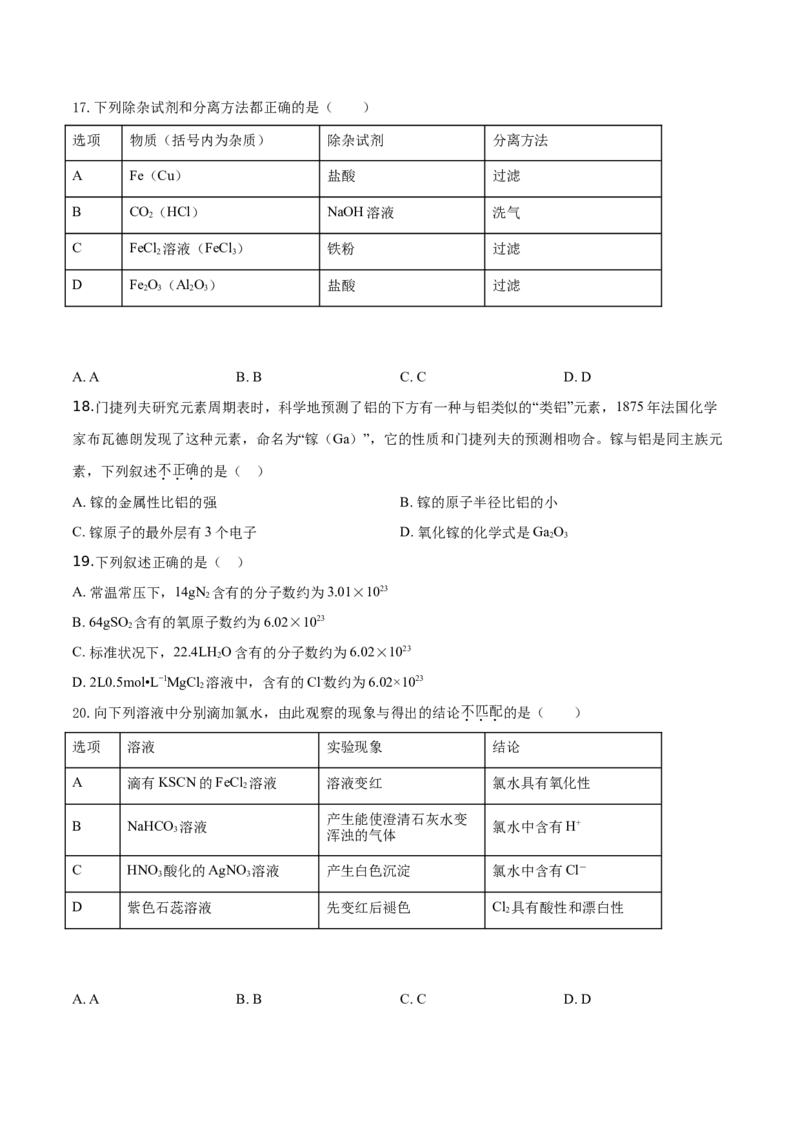
20.向下列溶液中分别滴加氯水,由此观察的现象与得出的结论不匹配的是( )
选项 溶液 实验现象 结论
A 滴有KSCN的FeCl 溶液 溶液变红 氯水具有氧化性
2
产生能使澄清石灰水变
B NaHCO 溶液 氯水中含有H+
3 浑浊的气体
C HNO 酸化的AgNO 溶液 产生白色沉淀 氯水中含有Cl-
3 3
D 紫色石蕊溶液 先变红后褪色 Cl 具有酸性和漂白性
2
A. A B. B C. C D. D第二部分(非选择题)
21.补齐物质与其用途的连线。___
22.运用分类的方法,可以发现物质及其变化的规律。NaO与CaO都属于__氧化物(填“酸性”或“碱性”)。
2
NaO可以分别与HO、CO、HCl反应,任选两个反应,写出其化学方程式___、__。
2 2 2
23.工业上冶炼铁的原理为:Fe O +3CO 2Fe+ 3CO。
2 3 2
(1)该反应中氧化剂是__(填化学式),碳元素被__(填“氧化”或“还原”)。
(2)若消耗了3molCO,则生成CO 的体积是__L(标准状况),转移电子的物质的量是___mol。
2
24.用NaCl固体配制100mL2.0mol·L−1NaCl溶液,请回答下列问题。
(1)用到的仪器有:托盘天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和__。
(2)用托盘天平称取NaCl固体的质量是__g。
(3)下列情况中,会使所配溶液浓度偏高的是__(填字母)。
A.定容时,俯视刻度线 B.转移液体时,有少量液体洒出
C.加蒸馏水超过了刻度线 D.没有洗涤烧杯和玻璃棒
25.实验室用如图装置制备并收集干燥纯净的Cl。
2
(1)装置A中反应的化学方程式是___。
(2)装置B的作用是__。
(3)装置C中盛放的物质是__。
(4)装置D用于收集Cl,请将图中装置D的导气管补充完整___。
2(5)装置E用于吸收尾气,E中反应的离子方程式是__。
26.阅读短文,回答问题。
世界卫生组织(WHO)和中国卫健委公认二氧化氯(ClO )为新时代绿色消毒剂,其特点是:无三致(致
2
癌、致畸、致突变),有三效(广谱、高效、快速)。国家疾病控制中心建议,为了避免传染病的传播,
餐饮用具可用200mg·L− 1的ClO 溶液浸泡,游泳池水可按5mg·L− 1用ClO 进行消毒。常温下,ClO 气体与
2 2 2
Cl 具有相似的颜色与气味,在水中的溶解度是Cl 的5~8倍。ClO 是强氧化剂,其有效氯是Cl 的2.6倍。
2 2 2 2
ClO 不与冷水反应,遇热水则分解成HClO、Cl 和O。
2 2 2
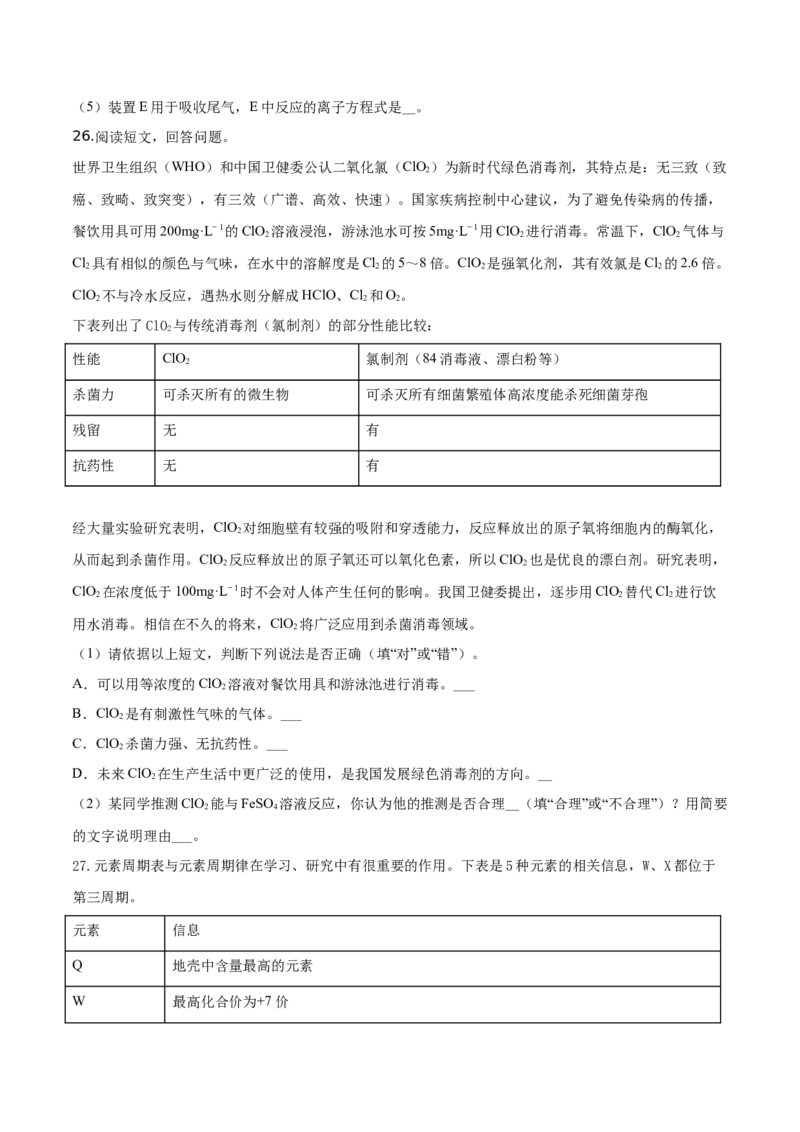
下表列出了ClO 与传统消毒剂(氯制剂)的部分性能比较:
2
性能 ClO 氯制剂(84消毒液、漂白粉等)
2
杀菌力 可杀灭所有的微生物 可杀灭所有细菌繁殖体高浓度能杀死细菌芽孢
残留 无 有
抗药性 无 有
经大量实验研究表明,ClO 对细胞壁有较强的吸附和穿透能力,反应释放出的原子氧将细胞内的酶氧化,
2
从而起到杀菌作用。ClO 反应释放出的原子氧还可以氧化色素,所以ClO 也是优良的漂白剂。研究表明,
2 2
ClO 在浓度低于100mg·L− 1时不会对人体产生任何的影响。我国卫健委提出,逐步用ClO 替代Cl 进行饮
2 2 2
用水消毒。相信在不久的将来,ClO 将广泛应用到杀菌消毒领域。
2
(1)请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
A.可以用等浓度的ClO 溶液对餐饮用具和游泳池进行消毒。___
2
B.ClO 是有刺激性气味的气体。___
2
C.ClO 杀菌力强、无抗药性。___
2
D.未来ClO 在生产生活中更广泛的使用,是我国发展绿色消毒剂的方向。__
2
(2)某同学推测ClO 能与FeSO 溶液反应,你认为他的推测是否合理__(填“合理”或“不合理”)?用简要
2 4
的文字说明理由___。
27.元素周期表与元素周期律在学习、研究中有很重要的作用。下表是5种元素的相关信息,W、X都位于
第三周期。
元素 信息
Q 地壳中含量最高的元素
W 最高化合价为+7价X 最高价氧化物对应 的水化物在本周期中碱性最强
Y 焰色试验(透过蓝色钴玻璃)火焰呈紫色
Z 原子结构示意图为:
(1)Q在周期表中的位置是__。
(2)W的最高价氧化物对应的水化物的化学式是___。
(3)X单质与水反应的离子方程式是__。
(4)金属性Y强于X,用原子结构解释原因:__,失电子能力Y大于X,金属性Y强于X。
(5)下列对于Z及其化合物的推断中,正确的是__(填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
28.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。如图为联合制碱法的主要过
程(部分物质已略去)。
资料:ⅰ.沉淀池中的反应为NaCl+CO +NH+H O=NaHCO ↓+NHCl
2 3 2 3 4
ⅱ.溶解度
物质 NaCl NH HCO NaHCO NH Cl
4 3 3 4
20°C溶解度/g 36.0 21.7 9.6 37.2
(1)煅烧炉中反应 的化学方程式是___,物质X是___(填化学式)。
(2)下列说法正确的是__(填字母)。
A.沉淀池中有NaHCO 析出,因为一定条件下NaHCO 的溶解度最小
3 3B.滤液中主要含有NaCl、NaCO 和NH Cl
2 3 4
C.设计循环 的目的是提高原料的利用率
(3)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与Cl 反应可制得一种在生产生活中常
2
用于漂白、消毒的物质,同时有NaHCO 生成,该反应的化学方程式是___。
3
(4)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼
烧,得到bg固体物质,则此样品中NaCO 的质量分数为__。
2 3
29.某小组为探究Cl、Br 、I 的氧化性强弱,设计实验如下:
2 2 2
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
实验Ⅰ
实验Ⅱ 取ⅰ中的黄色溶液少许,加入KI溶液,再加入淀粉溶液。
(1)ⅰ中反应的离子方程式是__。
(2)实验Ⅰ中ⅰ和ⅱ可以得出的结论是__。
(3)①甲同学认为:实验Ⅱ观察到__现象,得出氧化性Br >I。
2 2
②乙同学对上述实验进行反思,认为实验Ⅱ不能充分证明氧化性Br>I,他补做了实验Ⅲ。
2 2
另取ⅰ中的黄色溶液少许,先③步骤步骤,,,,,加入足量的NaBr固体,充分振
实验Ⅲ
荡,然后加入KI溶液和淀粉溶液。
补做实验Ⅲ的目的是__。
(4)综合实验Ⅰ和Ⅲ,得出氧化性Cl>Br >I。
2 2 2
30.某小组在探究Fe2+性质的实验中观察到异常现象。
实验Ⅰ 现象
溶液变红,片刻红色褪去,有气体生成(经检验为
O)。
2资料:ⅰ.Fe3++3SCN-=Fe(SCN) (红色),Fe(SCN) 中S元素的化合价为−2价
3 3
ⅱ.BaSO 是不溶于盐酸的白色沉淀
4
(1)实验Ⅰ体现了Fe2+的__性,补全HO 与FeCl 酸性溶液反应的离子方程式:__Fe2+ +__HO +__H+
2 2 2 2 2
=__Fe3++__HO
2
(2)探究“红色褪去”的原因,进行实验Ⅱ:将褪色后的溶液分三份分别进行实验。
实验Ⅱ得出的结论是:红色褪去的原因是__。
(3)为进一步探究“红色褪去”的原因,进行了实验Ⅲ。
实验Ⅲ 现象
溶液变红,一段时间后不褪色。
取上述反应后的溶液,滴加盐酸和BaCl 溶液 无白色沉淀产生。
2
分析上述三个实验,下列叙述正确的是__(填字母)。
A.实验Ⅲ中发生了氧化还原反应:4Fe2++O +4H+=4Fe3++2H O
2 2
B.通过实验Ⅲ推出实验Ⅰ中氧化FeCl 的只有O
2 2
C.O 在该实验条件下不能使红色溶液褪色
2
D.实验Ⅰ中红色褪去与HO 的氧化性有关
2 2
(4)上述实验探究过程用到的实验方法有__(写出一条)。