文档内容
南开中学 2019-2020 学年第一学期期末高一化学
一、选择题(共20小题,每小题只有一个正确答案,每小题3分,共60分)
1.在实验室中,通常将金属钠保存在( )
A. 水中 B. 煤油中 C. 四氯化碳中 D. 汽油中
2.下列物质中,不属于合金的是( )
A. 硬铝 B. 黄铜 C. 钢铁 D. 金
3.下列关于胶体和溶液的叙述正确的是( )
A. 溶液呈电中性,部分胶体带电荷,部分胶体不带电荷
B. 胶体与其他分散系的本质区别是能否产生丁达尔效应
C. 氢氧化铁胶体是一种红褐色的液体
D. 胶体是具有一定稳定性的分散剂
4.用光洁 的铂丝蘸取无色溶液在无色灯焰上灼烧时观察到黄色火焰,下列叙述正确的是( )
A. 只含有Na+ B. 一定含Na+,也可含K+
C. 既含Na+又含有K+ D. 可能含Na+或K+中一种
5.只用一种试剂可区别NaSO 、MgCl 、FeCl 、Al (SO )、(NH )SO 五种溶液,这种试剂是( )
2 4 2 2 2 4 3 4 2 4
A. Ba(OH) B. HSO C. NaOH D. AgNO
2 2 4 3
6.铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质
量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是( )
A. B.
.
C D.
7.为了除去硫酸铜溶液中的硫酸亚铁杂质,通常先加入合适的氧化剂使 转化为 下列物质中合适
的是( )
A. 溶液 B. 溶液 C. 氯水 D. 溶液
8.下列化学用语正确的是( )
A. 羟基 的电子式: B. 中子数为16的磷原子:C. 氟原子的结构示意 D. 的结构式:
9.下列反应的离子方程式正确的是( )
A. 向沸水中滴加 溶液制备 胶体:
B. 用 溶液腐蚀印刷铜电路板:
C. 用小苏打治疗胃酸过多:
D. 实验室用浓盐酸与 反应制 :
10.下列关于元素周期律叙述正确的是
A. 随着元素原子序数的递增,原子最外层电子数总是从1到8地重复出现
B. 元素的性质随着原子序数的递增而呈周期性的变化
C. 随着元素的原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1地重复出现
D. 元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化及元素主要化合
价的周期性变化
11.已知 、 、 和 均有还原性,它们在酸性溶液中还原性的强弱顺序为
,则下列反应不能发生的是( )
A. B.
C. D.
12.美、德两国成功合成具有化学特性的氢铝化合物 ,关于氢铝化合物的推测不正确的是( )
A. 氢铝化合物中铝显 价,氢显 价
B. 氢铝化合物与水反应生成氢氧化铝和氢气
C. 铝与水蒸气高温下反应生成氢铝化合物
D. 氢铝化合物具有强还原性
13.下列说法正确的是( )
① 、 、 属于碱性氧化物, 、 、 都能和碱溶液发生反应属于酸性氧化物
②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物
③混合物:漂白粉、水玻璃、 胶体、冰水混合物
④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
⑤硅导电,铝在浓硫酸中钝化均属于物理变化
⑥盐酸属于混合物,而液氯、冰醋酸均属于纯净物
A. ①③⑤ B. ④⑤⑥ C. ②④⑥ D. ②③④
14.下列物质中不能通过化合反应直接生成的是( )
A. B. C. D.
15.下列实验操作中正确的是( )
A. 配制一定物质的量浓度的 溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤
量筒2~3次,并将洗涤液一并倒入烧杯中稀释
B. 溶液的物质的量浓度为 ,用水稀释到物质的量浓度为 ,需要水
C. 配制一定物质的量浓度的氯化钾溶液:准确称取一定质量的氯化钾固体,放入 的容量瓶中,加
入 溶解,振荡摇匀
D. 将 溶解在 水中,配制溶质质量分数为10%的 溶液
16.X、Y、Z、Q、R均为短周期元素,且Y、Z、Q、R在周期表中的位置关系如下图所示。已知X与Y同
主族,X与Q能形成最简单的有机物。则下列有关说法正确的是( )
Q R
Y Z
A. 原子半径:r(Z)>r(Y)>(R)>r(Q)
B. 气态化合物的稳定性:QX >RX
4 3
C. X与Y形成的化合物中含有离子键D. 最高价含氧酸的酸性:XQO >XRO
2 3 3
17.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为 和 , 和 具有
相同的电子层结构。下列说法正确的是( )
A. 原子序数: B. 单质沸点:
C. 离子半径: D. 原子最外层电子数:
18.使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是( )
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤;
③转移溶液前容量瓶内有少量蒸馏水
④定容时,俯视容量瓶的刻度线;
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A. ①②⑤ B. ①③⑤ C. ③④⑤ D. ②③⑤
19.三聚氰胺又名蛋白精[分子式: ,相对分子质量:126]是一种低毒性化工产品.婴幼儿大量
摄入可引起泌尿系统疾患。有关三聚氰胺的下列说法正确的是( )
A. 三聚氰胺含氮原子数目为 B. 三聚氰胺含氮量约为10%
C. 标准状况下 的三聚氰胺的体积为 D. 三聚氰胺的摩尔质量为126
20.为了避免NO、NO 、NO 对大气的污染,常采用NaOH溶液进行吸收处理(反应方程式:2NO +
2 2 4 2
2NaOH=NaNO+NaNO +HO;NO +NO+2NaOH=2NaNO+HO)。现有由a mol NO、b mol NO 、c mol
3 2 2 2 2 2 2
NO 组成的混合气体恰好被V L NaOH溶液吸收(无气体剩余),则此NaOH溶液的物质的量浓度为( )
2 4
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
21.完成下列化学方程式
(1)过氧化钠与二氧化碳反应___________________________
(2)工业制漂白粉________________________
(3)氧化铝溶于氢氧化钠_____________________
(4)氢氧化亚铁 在空气中被氧化_____________________(5)铁与水蒸气高温下反应_____________________
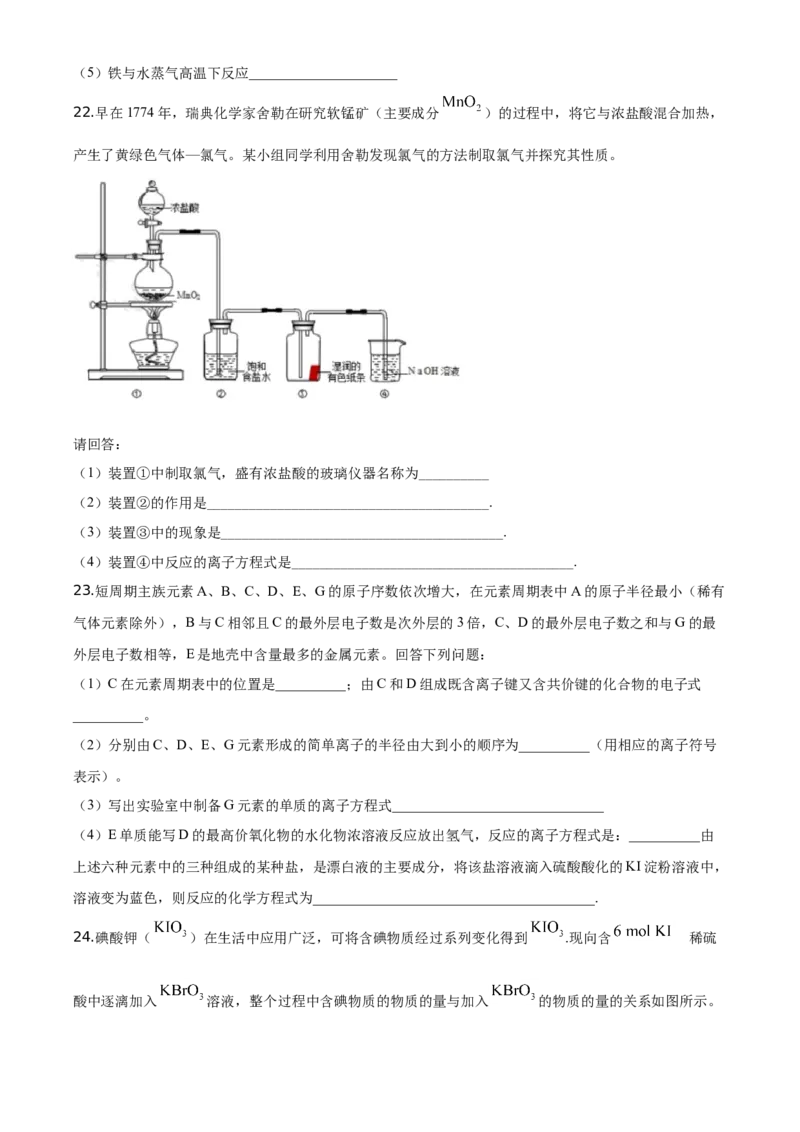
22.早在1774年,瑞典化学家舍勒在研究软锰矿(主要成分 )的过程中,将它与浓盐酸混合加热,
产生了黄绿色气体—氯气。某小组同学利用舍勒发现氯气的方法制取氯气并探究其性质。
请回答:
(1)装置①中制取氯气,盛有浓盐酸的玻璃仪器名称为__________
(2)装置②的作用是________________________________________.
(3)装置③中的现象是________________________________________.
(4)装置④中反应的离子方程式是________________________________________.
23.短周期主族元素A、B、C、D、E、G的原子序数依次增大,在元素周期表中A的原子半径最小(稀有
气体元素除外),B与C相邻且C的最外层电子数是次外层的3倍,C、D的最外层电子数之和与G的最
外层电子数相等,E是地壳中含量最多的金属元素。回答下列问题:
(1)C在元素周期表中的位置是__________;由C和D组成既含离子键又含共价键的化合物的电子式
__________。
(2)分别由C、D、E、G元素形成的简单离子的半径由大到小的顺序为__________(用相应的离子符号
表示)。
(3)写出实验室中制备G元素的单质的离子方程式______________________________
(4)E单质能写D的最高价氧化物的水化物浓溶液反应放出氢气,反应的离子方程式是:__________由
上述六种元素中的三种组成的某种盐,是漂白液的主要成分,将该盐溶液滴入硫酸酸化的KI淀粉溶液中,
溶液变为蓝色,则反应的化学方程式为________________________________________.
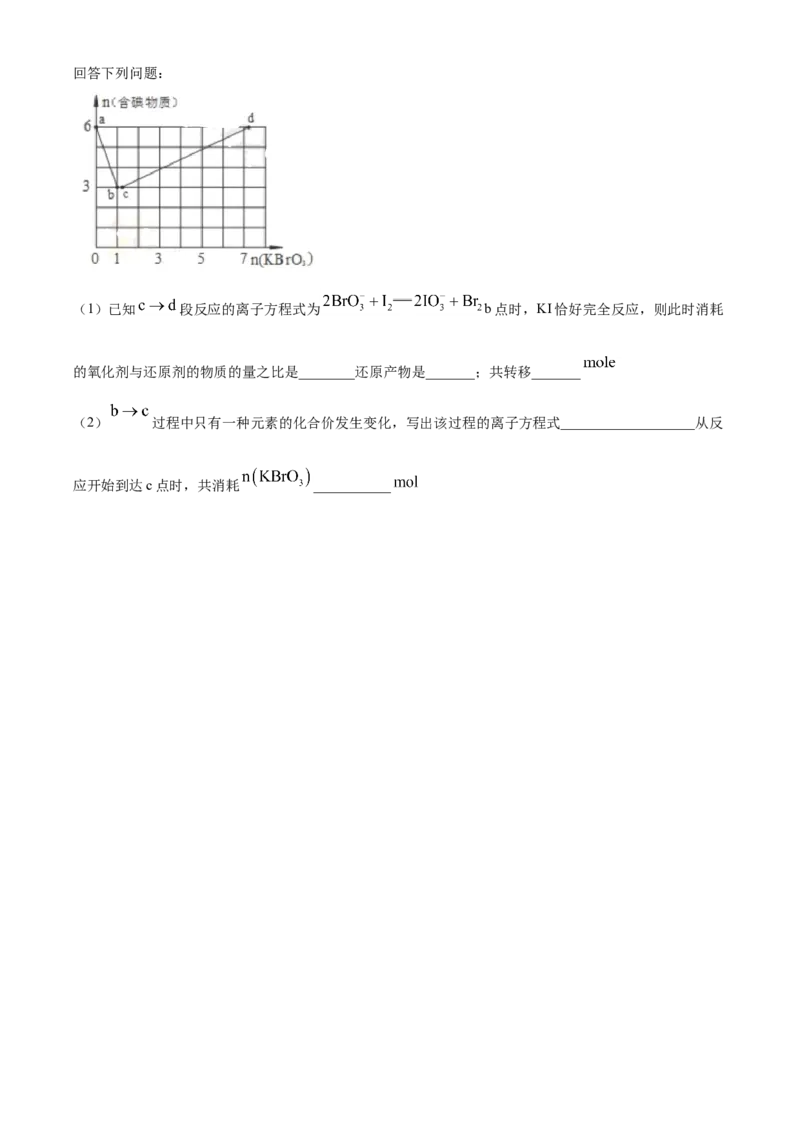
24.碘酸钾( )在生活中应用广泛,可将含碘物质经过系列变化得到 .现向含 的稀硫
酸中逐漓加入 溶液,整个过程中含碘物质的物质的量与加入 的物质的量的关系如图所示。回答下列问题:
(1)已知 段反应的离子方程式为 b点时,KI恰好完全反应,则此时消耗
的氧化剂与还原剂的物质的量之比是________还原产物是_______;共转移_______
(2) 过程中只有一种元素的化合价发生变化,写出该过程的离子方程式___________________从反
应开始到达c点时,共消耗 ___________