文档内容
第13讲 化学方程式及基本反应类型
命题点1 化学方程式的意义及书写
1.(2017·泰安)过氧化钠(Na O)因能与二氧化碳反应生成氧气,故可作为呼吸面具中氧气的来源,潜水艇遇到紧
2 2
急情况时,也使用过氧化钠来供氧,反应的化学方程式为2NaO+2CO===2Na CO+O,从该反应获取的以下信息,
2 2 2 2 3 2
正确的是()
①过氧化钠属于氧化物
②实验室可利用这一原理制取纯净的氧气
③该反应属于置换反应
④反应前后部分氧元素的化合价发生变化
A.①③④ B.①③ C.①④ D.①②③
2.(2017·临沂)下列化学方程式书写正确的是()
A.2NaOH+CuSO ===Cu(OH) ↓+NaSO
4 2 4
B.Ba(NO )+HSO ===BaSO ↓+HNO
3 2 2 4 4 3
C.C+2CuO=====2Cu+CO↑
2
D.Fe O+6HCl===2FeCl +3HO
2 3 2 2
3.(2017·怀化)如图中“ ”和“ ”分别表示两种元素的原子,能用该图表示的化学反应是()
A.2H+O=====2HO B.C+CO=====2CO
2 2 2 2
C.H+Cl=====2HCl D.2CO+O=====2CO
2 2 2 2
4.(2017·重庆A卷)在“欢迎来找茬”的趣味活动中,老师举出四个错误实例,在学生的错因分析中错误的是()
选项 错误实例 错因分析
A 铁与稀硫酸生成硫酸铁 反应产物不正确
B FeCl +3NaOH===Fe(OH) +NaCl 只缺少沉淀符号
3 3
C 2KMnO ===K MnO +MnO +O↑ 反应条件不正确
4 2 4 2 2
D 氢氧化钠俗名烧碱或纯碱 俗名的纯碱不正确
5.(2017·扬州)写出下列反应的化学方程式。
(1)磷与氧气反应________________________________________________________________________;
(2)硫酸铜溶液与氢氧化钙溶液反应___________________________________________________;
(3)碳酸钙分解________________________________________________________________________;
(4)铜与硝酸银溶液反应_______________________________________________。
命题点2 化学反应的基本类型
6.(2017·株洲)下列反应中属于化合反应的是()
A.2Na+2HO===2NaOH+H↑
2 2
B.Fe (SO )+Fe===3FeSO
2 4 3 4
C.CaCO =====CaO+CO↑
3 2
D.2NaCl+2HO=====2NaOH+Cl↑+H↑
2 2 2
7.(2017·邵阳)下列化学方程式及其反应类型都正确的是()
选项 化学方程式 反应类型
A Mg+O=====MgO 化合反应
2 2
B HO=====HO+O↑ 分解反应
2 2 2
C Fe+HSO ===FeSO+H↑ 置换反应
2 4 4 2
D 2KNO+Ba(OH) ===Ba(NO)+2KOH 复分解反应
3 2 3 2
命题点3 利用化学方程式的简单计算8.(2017·山西)在一次实验课上,同学们用加热氯酸钾和二氧化锰混合物的方法制取氧气。他们取了24.5 g 的混
合物,其中二氧化锰的质量分数为20%,加热到完全分解。通过计算,得出他们制得氧气的质量是多少?
重难点1 化学方程式的书写
(2017·雅安)下列反应的化学方程式正确的是()
A.铁在氧气中燃烧:2Fe+3O=====2Fe O
2 2 3
B.硫酸铵与烧碱混合:(NH )SO +2NaOH===Na SO +2HO+2NH ↑
4 2 4 2 4 2 3
C.铝片放入硝酸银溶液中:Al+AgNO===AlNO+Ag
3 3
D.向氯化镁溶液中滴入硫酸钾溶液:MgCl +KSO ===MgSO ↓+2KCl
2 2 4 4
(易错题)写出下列反应的化学方程式。
(1)碳在氧气中充分燃烧__________________________________________________;
(2)铁和稀硫酸反应_______________________________________________________;
(3)碳酸钠溶液与澄清石灰水混合_______________________________________________。
重难点2 利用化学方程式的简单计算
(2016·资阳)某食用纯碱中含有少量的氯化钠,为测定某纯碱中碳酸钠(Na CO)的含量,现取纯碱样品
2 3
12.5 g,加入150.0 g稀盐酸溶液恰好完全反应,测得反应后溶液总质量变为158.1 g。计算:
(1)反应中产生CO 的质量;
2
(2)纯碱样品中NaCO 的质量分数。
2 3
1.(2016·北京)下列关于S+O=====SO 的理解不正确的是()
2 2
A.表示硫与氧气在点燃条件下反应生成二氧化硫
B.参加反应的硫与氧气的质量比是2∶1
C.反应前后硫原子、氧原子的个数均不变
D.参加反应的氧气与生成的二氧化硫的分子个数比为1∶1
2.(2017·内江)下列化学方程式书写错误的是()
A.NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2
B.CO+Ca(OH) ===CaCO ↓+HO
2 2 3 2
C.CuSO +BaOH===CuOH↓+BaSO
4 4
D.3CO+Fe O=====2Fe+3CO
2 3 23.(2016·大庆)下列化学方程式与事实相符且正确的是()
A.碳在氧气中完全燃烧:2C+O=====2CO
2
B.用足量澄清石灰水检验二氧化碳:CO+Ca(OH) ===CaCO ↓+HO
2 2 3 2
C.用稀盐酸除铁锈:2HCl+FeO===FeCl +HO
2 2
D.用足量NaOH溶液在加热条件下检验NH HCO 中的NH:NaOH+NH HCO =====NH ↑+NaHCO
4 3 4 3 3 3
4.(易错题)(2017·嘉兴)以下四个化学反应都有气体产生,其反应类型和产生的气体性质均正确的是()
选项 化学反应方程式 反应类型 气体性质
A Fe+HSO ===FeSO+H↑ 置换反应 还原性
2 4 4 2
B 2HO=====2HO+O↑ 分解反应 可燃性
2 2 2 2
C 2KClO=====2KCl+3O↑ 化合反应 氧化性
3 2
复分解
D CaCO +2HCl===CaCl +HO+CO↑ 酸性
3 2 2 2 反应
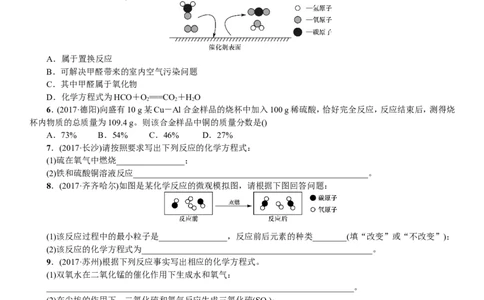
5.(2017·安徽)科学家发现,利用催化剂可有效消除室内装修材料释放的甲醛,其反应的微观示意图如下,下列有
关该反应的说法正确的是()
A.属于置换反应
B.可解决甲醛带来的室内空气污染问题
C.其中甲醛属于氧化物
D.化学方程式为HCO+O===CO +HO
2 2 2
6.(2017·德阳)向盛有10 g某Cu-Al合金样品的烧杯中加入100 g稀硫酸,恰好完全反应,反应结束后,测得烧
杯内物质的总质量为109.4 g。则该合金样品中铜的质量分数是()
A.73% B.54% C.46% D.27%
7.(2017·长沙)请按照要求写出下列反应的化学方程式:
(1)硫在氧气中燃烧________________;
(2)铁和硫酸铜溶液反应_______________________________________________________。
8.(2017·齐齐哈尔)如图是某化学反应的微观模拟图,请根据下图回答问题:
(1)该反应过程中的最小粒子是________________,反应前后元素的种类________(填“改变”或“不改变”);
(2)该反应的化学方程式为______________________________________________________。
9.(2017·苏州)根据下列反应事实写出相应的化学方程式。
(1)双氧水在二氧化锰的催化作用下生成水和氧气:
________________________________________________________________________。
(2)在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO ):_________________________________。
3
(3)Cu和AgNO 溶液反应,生成Cu(NO ) 溶液和Ag:___________________________________________。
3 3 2
(4)少量CuSO 溶液滴入NaOH稀溶液中生成Cu(OH) 沉淀和NaSO 溶液:
4 2 2 4
________________________________。
(5)一氧化碳和四氧化三铁(Fe O)在高温下反应,生成铁和二氧化碳:________________________________。
3 4
10.(2017·自贡)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱。现
有含1.6 kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素的质量分数。
(2)理论上与硫酸铜反应消耗铁粉的质量。11.(2016·绵阳)液化石油气的成分中含有丙烯(C H)和丁烯(C H),将二者的混合气体14 g在足量氧气中充分燃
3 6 4 8
烧,产生二氧化碳44 g,下列判断中不正确的是()
A.混合气体中碳与氢的质量之比一定是6∶1
B.消耗O 的质量一定为48 g
2
C.混合气体中丙烯(C H)的质量分数一定为50%
3 6
D.混合气体燃烧生成HO的质量一定为18 g
2
12.(2017·孝感)碳酸锌与碳酸钙有相似的化学性质。现将12.5 g碳酸锌固体高温煅烧一段时间,冷却后,向剩余
固体中加入足量稀硫酸。下列结论正确的个数是()
①共生成16.1 g硫酸锌
②煅烧越充分则消耗的硫酸越少
③煅烧后固体中氧元素的质量分数减小
④最终生成二氧化碳的总质量与煅烧时间的长短有关
A.1个 B.2个 C.3个 D.4个
13.(2017·山西)我们的胃液中含有盐酸,它有助于消化,但胃酸过多会引起胃部不适。有时可以用小苏打治疗,
反应的方程式为________________________________,化学反应前后一定没有变化的离子是____________(用离子
符号表示)。
14.(2017·泰安)化学是研究物质的组成、性质以及变化规律的科学。化学学习过程要关注物质的性质以及能发生
哪些变化和发生变化过程中的现象。现有A、B、C三种物质,它们可能是O、Fe、HO、HO、CaO、Fe O、HCl、NaOH、
2 2 2 2 2 3
Ca(OH) 、NaCO 中的—种。
2 2 3
(1)若 A、B 是由相同元素组成的化合物,且 B 分解能产生 A 和 C。请写出该化学反应方程式
________________________________。
(2)若A、B中含有相同的金属元素,并均可与C的溶液反应,生成金属元素化合价不同的两种盐溶液。则C的化
学式是________;请写出能产生黄色溶液的化学反应方程式________________________________。
(3)若A、B、C是三种不同类别的物质,分别属于酸、碱和盐,将它们依次加入同一个烧杯中:
①若均无明显现象,则A、B、C分别是________________(填化学式);
②若能产生白色沉淀,请写出酸、碱中和的化学反应方程式__________________________。参考答案
第13讲 化学方程式及基本反应类型
中考真题展
1 . C 2.C 3.D 4.B 5.(1)4P + 5O=====2PO (2)Ca(OH) + CuSO ===Cu(OH) ↓ + CaSO
2 2 5 2 4 2 4
(3)CaCO=====CaO+CO↑ (4)Cu+2AgNO===Cu(NO )+2Ag 6.B 7.C
3 2 3 3 2
8.设制得氧气的质量为x。
2KClO=====2KCl+3O↑
3 2
245 96
24.5 g×(1-20%) x
= x=7.68 g
答:制得氧气的质量是7.68 g。
导学提分训练
例 1 B 例 2 (1)C+O=====CO (2)Fe+HSO ===FeSO +H↑ (3)NaCO +Ca(OH) ===CaCO ↓+
2 2 2 4 4 2 2 3 2 3
2NaOH
例3 (1)反应中产生CO 的质量为12.5 g+150.0 g-158.1 g=4.4 g
2
(2)设纯碱样品中NaCO 的质量为x。
2 3
NaCO+2HCl===2NaCl+CO↑+HO
2 3 2 2
106 44
x 4.4 g
= x=10.6 g
纯碱样品中NaCO 的质量分数为×100%=84.8%
2 3
答:(1)反应中产生CO 的质量为4.4 g;(2)纯碱样品中NaCO 的质量分数为84.8%。
2 2 3
课后提分训练
1.B 2.C 3.B 4.A 5.B 6.C 7.(1)S+O=====SO (2)Fe+CuSO ===Cu+FeSO 8.(1)碳原子和氧原子
2 2 4 4
不 改 变 (2)2CO + O=====2CO 9.(1)2H O=====2HO + O↑ (2)2SO + O=====2SO (3)Cu +
2 2 2 2 2 2 2 2 32AgNO===Cu(NO )+2Ag (4)2NaOH+CuSO ===Cu(OH) ↓+NaSO (5)Fe O+4CO=====3Fe+4CO↑
3 3 2 4 2 2 4 3 4 2
10.(1)硫酸铜中铜元素的质量分数==40%
(2)设消耗铁粉的质量为x。
Fe+CuSO ===Cu+FeSO
4 4
56 160
x 1.6 kg
= x=0.56 kg
答:(1)硫酸铜中铜元素的质量分数为40%;(2)理论上与硫酸铜反应消耗铁粉的质量为0.56 kg。
11.C 12.B 13.NaHCO +HCl===NaCl+HO+CO↑ Na+、Cl- 14.(1)2H O=====2HO+O↑ (2)HCl
3 2 2 2 2 2 2
Fe O+6HCl===2FeCl +3HO (3)①HCl、NaOH、NaCO ②Ca(OH) +2HCl===CaCl +2HO
2 3 3 2 2 3 2 2 2