文档内容
第18讲 常见的酸和碱
(满分50分,限时40分钟)
一、选择题(每小题2分,共16分)
1.(2017,重庆B)小王同学往厨房的纯碱中滴加白醋,发现有气体生成。已知白醋里含
3%~5%的醋酸(CHCOOH),醋酸与盐酸的化学性质相似,下列说法不正确的是(D)(导学号
3
58504352)
A.白醋里含有氢离子
B.生成的气体是二氧化碳
C.白醋能使紫色石蕊试液变红
D.白醋与纯碱的反应属于中和反应
2.(2016,十堰)物质存放在烧杯中一段时间后,质量变大且变质的是(A)(导学号
58504353)
①浓盐酸 ②浓硫酸 ③烧碱 ④生石灰 ⑤澄清石灰水
A.③④⑤ B.②③④⑤
[来源:学.科.网]
C.①②③④⑤ D.④⑤
3.(2017,邵阳)下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的
是(D)
A.稀盐酸 B.二氧化碳
C.碳酸钙 D.石蕊溶液
4.(2017,连云港)下列有关实验现象的描述正确的是(A)(导学号 58504354)
A.小木棍蘸取浓硫酸一段时间后,小木棍变黑
B.硝酸铵固体溶于水后,溶液的温度几乎不变
C.氢氧化钠固体久置于表面皿上,无明显现象
D.尿素和熟石灰混合研磨,产生刺激性气味的气体
5.(2017,深圳)小明同学归纳总结了初中所学稀硫酸的化学性质,并用“HSO +X→盐
2 4
+Y”这种表达式进行整理。下列小明的观点错误的是(A)(导学号 58504355)
选项 X的物质类别 观点描述
A 金属 若X为Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为HO
2
C 碱 若X为NaOH,则盐为NaSO
2 4
D 盐 若X为BaCl ,则生成白色沉淀
2
6.(2017,潍坊)类比推理在化学学习和科学研究中具有重要意义。下列类比推理正确的
是(A)(导学号 58504356)
A.NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成蓝色沉淀
B.N 和O 都是非金属单质,两者的化学性质都非常活泼
2 2
C.盐酸和硫酸都是强酸,两者都易挥发
D.CaO和Fe O 都是金属氧化物,两者都能与水反应生成碱
2 3
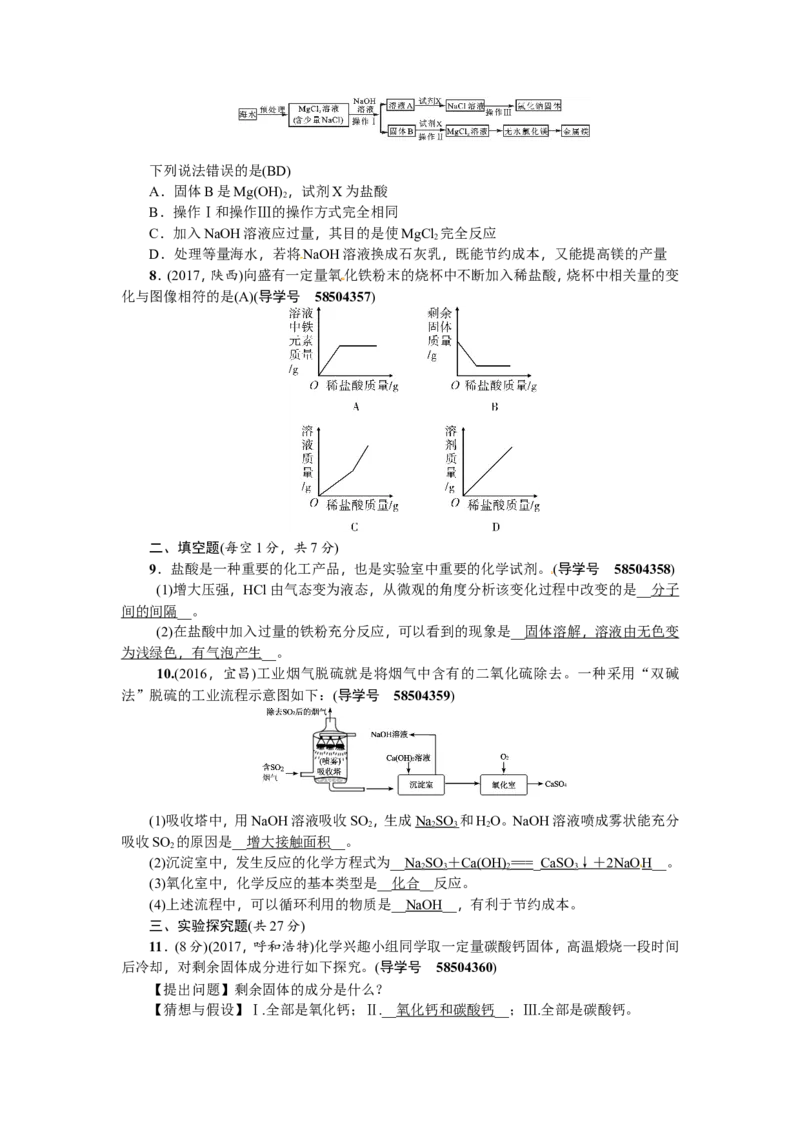
7.(多选)(2016,泰州)海水是一种重要的资源,利用海水可制取镁等物质。有人设计如下
实验流程:
[来源:学§科§网]下列说法错误的是(BD)
A.固体B是Mg(OH) ,试剂X为盐酸
2
B.操作Ⅰ和操作Ⅲ的操作方式完全相同
C.加入NaOH溶液应过量,其目的是使MgCl 完全反应
2
D.处理等量海水,若将NaOH溶液换成石灰乳,既能节约成本,又能提高镁的产量
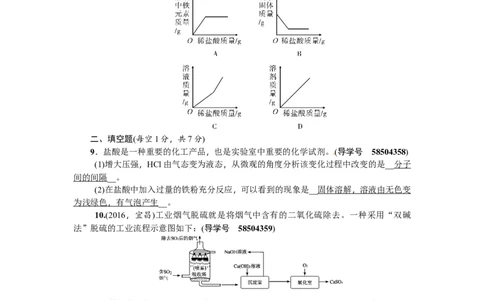
8.(2017,陕西)向盛有一定量氧化铁粉末的烧杯中不断加入稀盐酸,烧杯中相关量的变
化与图像相符的是(A)(导学号 58504357)
二、填空题(每空1分,共7分)
9.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。(导学号 58504358)
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是__分子
间的间隔__。
(2)在盐酸中加入过量的铁粉充分反应,可以看到的现象是__ 固体溶解 , 溶液由无色变
为浅绿色 , 有气泡产生 __。
10.(2016,宜昌)工业烟气脱硫就是将烟气中含有的二氧化硫除去。一种采用“双碱
法”脱硫的工业流程示意图如下:(导学号 58504359)
(1)吸收塔中,用NaOH溶液吸收SO ,生成NaSO 和HO。NaOH溶液喷成雾状能充分
2 2 3 2
吸收SO 的原因是__增大接触面积__。
2
(2)沉淀室中,发生反应的化学方程式为__NaSO + C a(OH ) == = _CaSO ↓ + 2NaO H__。
2 3 2 3
(3)氧化室中,化学反应的基本类型是__化合__反应。
(4)上述流程中,可以循环利用的物质是__NaOH__,有利于节约成本。
三、实验探究题(共27分)
11.(8分)(2017,呼和浩特)化学兴趣小组同学取一定量碳酸钙固体,高温煅烧一段时间
后冷却,对剩余固体成分进行如下探究。(导学号 58504360)
【提出问题】剩余固体的成分是什么?
【猜想与假设】Ⅰ.全部是氧化钙;Ⅱ.__氧化钙和碳酸钙__;Ⅲ.全部是碳酸钙。【实验探究】
(1)甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物。甲同学
据此认为试管中的固体有碳酸钙。乙同学认为上述实验不足以证明剩余固体中有碳酸钙,其
理由是__ 氧化钙与水反应生成的氢氧化钙微溶于水 , 也可能出现白色不溶物 __。
(2)乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,据
此得出猜想Ⅲ__不成立__(填“成立”或“不成立”)。乙同学继续向试管中加入几滴稀盐酸,
没有气泡产生,认为猜想Ⅰ成立。丙同学认为上述实验不足以证明猜想Ⅰ成立。其理由是__
氧化钙与水反应生成氢氧化钙 , 即使有碳酸钙 , 加入的少量稀盐酸也会先消耗氢氧化钙 , 不
会出现气泡__。
(3)丙同学设计实验证明了猜想Ⅱ成立。丙同学的实验方案是__取少量剩余固体于试管
中 , 加水振荡 , 过滤 , 取滤液滴加无色酚酞溶液 , 溶液变红;取滤渣滴加足量稀盐酸 ( 或稀硝
酸 ) , 有气泡产生 __(要求写出实验的操作和现象)。
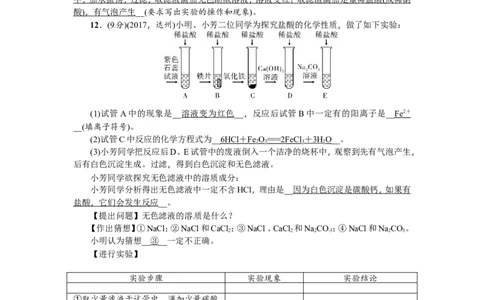
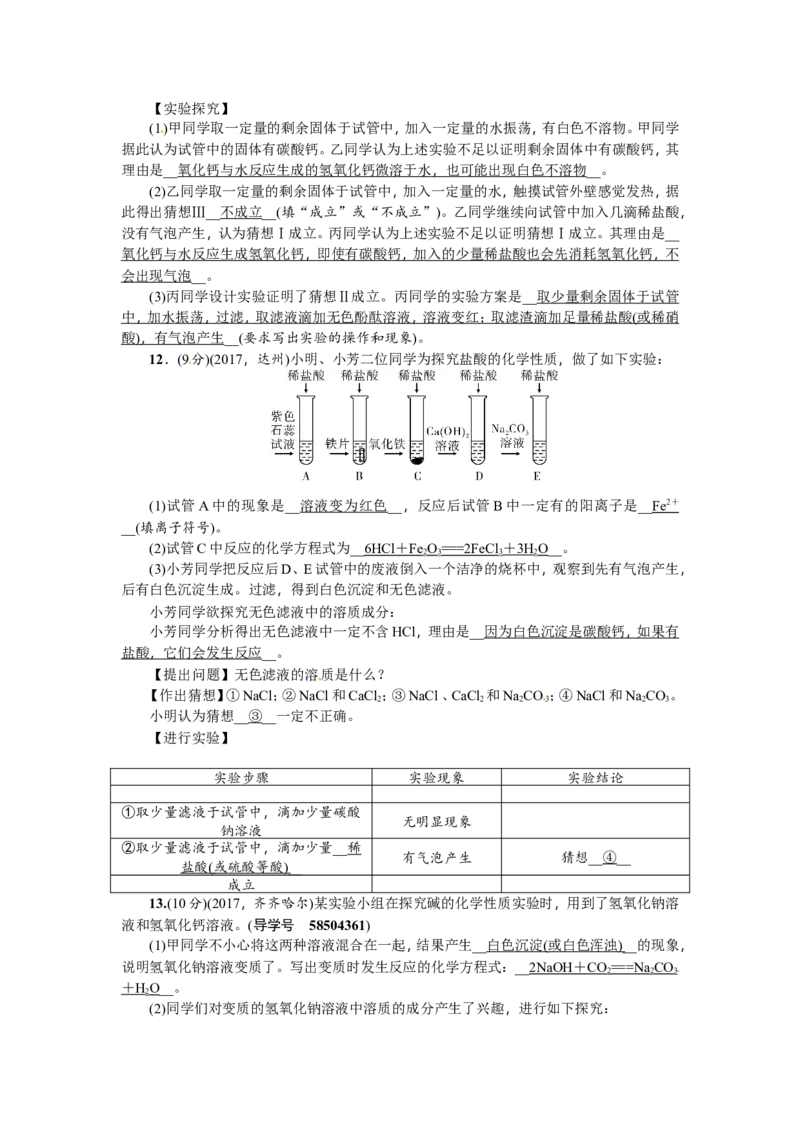
12.(9分)(2017,达州)小明、小芳二位同学为探究盐酸的化学性质,做了如下实验:
(1)试管A中的现象是__溶液变为红色__,反应后试管B中一定有的阳离子是__ Fe 2 +
__(填离子符号)。
(2)试管C中反应的化学方程式为__ 6HCl + Fe O == =2FeCl + 3H O__。
2 3 3 2
(3)小芳同学把反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到先有气泡产生,
后有白色沉淀生成。过滤,得到白色沉淀和无色滤液。
[来源:学科网ZXXK]
小芳同学欲探究无色滤液中的溶质成分:
小芳同学分析得出无色滤液中一定不含HCl,理由是__ 因为白色沉淀 是碳酸钙 , 如果有
盐酸 , 它们会发生反应 __。
【提出问题】无色滤液的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl ;③NaCl 、CaCl 和NaCO ;④NaCl和NaCO。
2 2 2 3 2 3
小明认为猜想__③__一定不正确。
【进行实验】
实验步骤 实验现象 实验结论
①取少量滤液于试管中,滴加少量碳酸
无明显现象
钠溶液
②取少量滤液于试管中,滴加少量__稀
有气泡产生 猜想__④__
盐酸 ( 或硫酸等酸 )__
成立
13.(10分)(2017,齐齐哈尔)某实验小组在探究碱的化学性质实验时,用到了氢氧化钠溶
液和氢氧化钙溶液。(导学号 58504361)
(1)甲同学不小心将这两种溶液混合在一起,结果产生__ 白色沉淀 ( 或白色浑浊 )__的现象,
说明氢氧化钠溶液变质了。写出变质时发生反应的化学方程式:__ 2NaOH + CO == =Na CO
2 2 3
+ H O__。
2 [来源:Z*xx*k.Com]
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
[来源:学.科.网]【提出问题】变质的氢氧化钠溶液中溶质的成分是什么?
【做出猜想】猜想一:NaCO;
2 3
猜想二:__NaCO 和 NaOH __(写化学式)。
2 3
【进行讨论】甲同学取少量待测液加入足量的稀盐酸,有气泡产生。认为猜想一成立。乙
同学不同意甲同学的观点,理由是__ 猜想二中也含有碳酸钠 , 加入足量的盐酸也能产生气泡
__。
【设计实验】请你验证猜想二成立,并完成实验报告。
实验操作 实验现象 实验
结论
①取一定量的待测液于试管中,加入
__ 产生白色沉淀 ( 或产生白色浑浊 )__
__过量的氯化钙__溶液
②充分反应后静置,取上层清液加入
溶液变红 猜想二
无色酚酞溶液
成立
【反思评价】在实验室中,氢氧化钠应__密封保存。