文档内容
2019 级高一下学期化学学科学业水平检测题
(等级考)
可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 S:32 Cl:35.5
Fe:56 Cu:64 Zn:65
一、选择题(每小题只有一个选项符合题意)
1. 化学知识无处不在,下列与古诗文或者记载对应的化学知识不正确的是
选项 古诗文或者记载 化学知识
A 《荀子·劝学》:冰,水为之,而寒于水。 冰的能量低于水,冰变为水需要吸收能量
《本草纲目》中“用浓酒和糟入甑,蒸令气
B 这种物质分离和提纯的方法是蒸馏
上,用器承滴露……”。
王安石诗句“爆竹声中一岁除,春风送暖
C 爆竹的燃放涉及氧化还原反应
入屠苏”。
《天工开物》中有如下描述:“世间丝、
D 文中的“裘”主要成分是纤维素
麻、裘、褐皆具素质……”。
A. A B. B C. C D. D
2. 截止到2020年5月18日全球新冠肺炎确诊人数超过482万,在阻击新冠肺炎的战役中最大程度的体现
了我国的政体优势。其中医用酒精(75%的乙醇)和“84” 消毒液(主要成分为次氯酸钠)、双氧水等均能起到杀
菌作用。设N 为阿伏伽德罗常数的值,下列说法不正确的是
A
A. 74.5g 次氯酸钠中含有的离子总数为2N
A
B. 46 g 75%的乙醇中含有的氧原子数为N
A
C. 34g H O 中含有的共用电子数为6N
2 2 A
D. 乙醇中的官能团为羟基,1mol 羟基中含有的电子数为9N
A
3. 下列示意图与化学用语表述内容不相符的是
A B C D
CH-CH=CH
3 2
正丁烷的球棍模型 丙烯的结构简式 原子核内有8个中子的碳原子 氮气的电子式
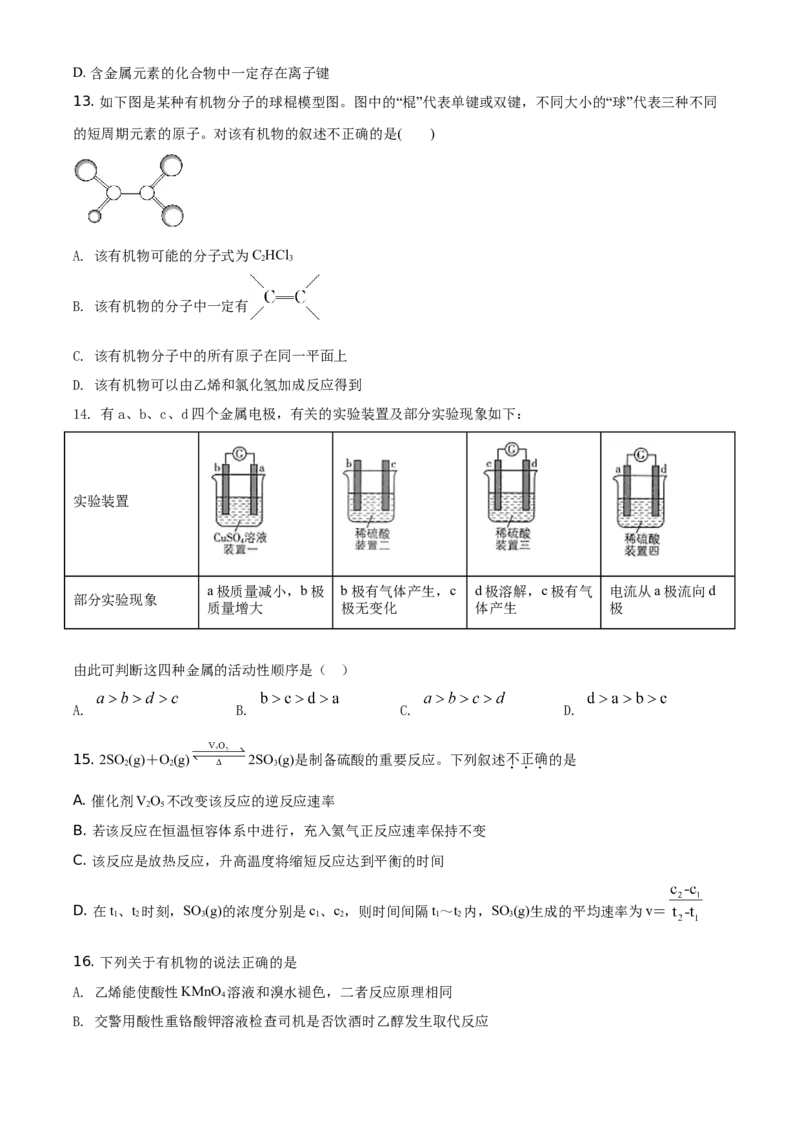
A. A B. B C. C D. D4. 下列有关“四同”概念的说法或者判断正确的是
A. 通式为C H ,且碳原子数不相等的物质一定互为同系物
n 2n+2
B. H、D、T 互为同素异形体
2 2 2
C. 和 互为同分异构体
D. 40K和40Ca互为同位素
5. 科学家预测,月球的土壤中吸附着数百万吨 e,100 吨 e 核聚变释放的能量相当于目前人类一年
消耗的能量。下列说法正确的是()
A. 的最外层电子数为 2,具有较强的金属性
B. e位于周期表第二周期第ⅡA 族
C. 其原子核中质子数为 2、中子数为 1
D. 核聚变是化学反应
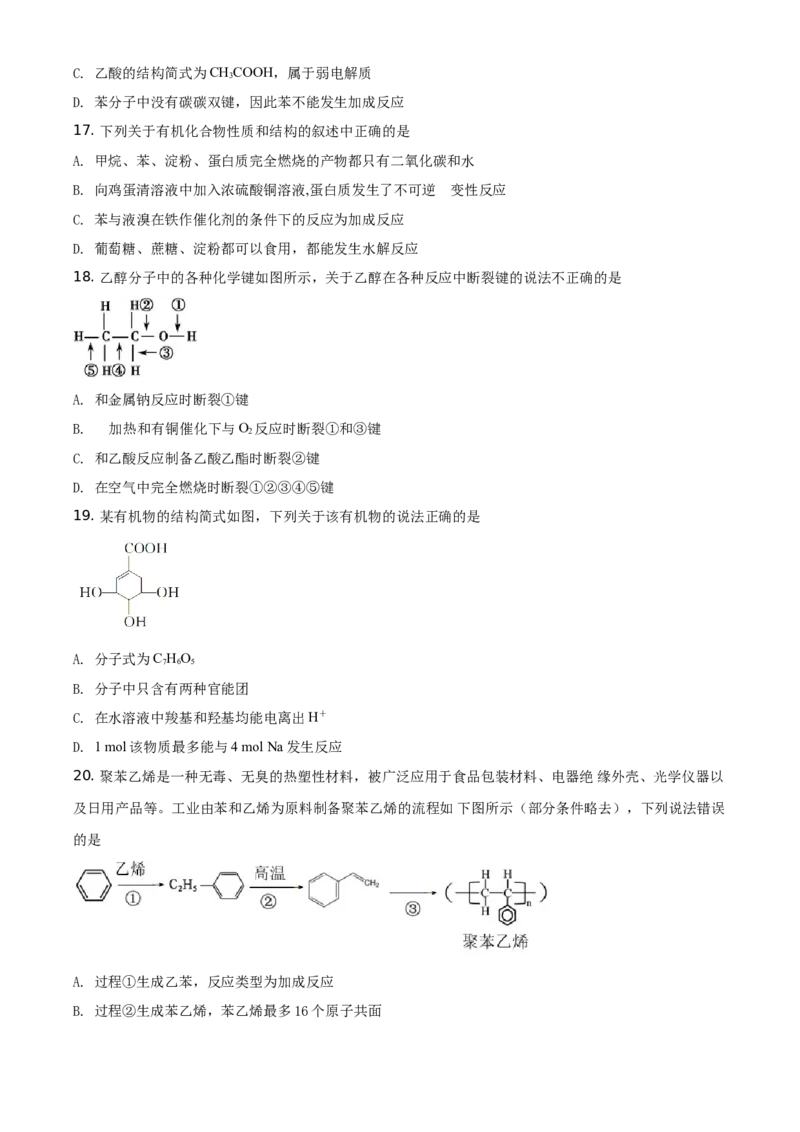
6. 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表一种元素,
其中O点代表氢元素。下列说法中不正确的是
A. 虚线相连的元素处于同一族
B. 离O点越远的元素原子半径越大
C. A、B、C最高价氧化物对应的水化物可相互反应
D. A、B组成的化合物中可能含有共价键
7. 下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
A. 2NaBr+Cl =2NaCl+Br B. 2NaOH+SiO =Na SiO +H O
2 2 2 2 3 2
C. 2NaO+2H O=4NaOH+O ↑ D. HS+Cl =S↓+2HCl
2 2 2 2 2 2
8. 根据元素周期表和元素周期律判断,下列叙述不正确的是
A. 氢元素与其他元素既可形成共价化合物也可形成离子化合物
B. 气态氢化物 的稳定性:HO > NH > SiH
2 3 4
C. 用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
D. 下图所示实验可证明元素的非金属性:Cl > C > Si9. X、Y是元素周期表第ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是
①X原子的电子层数比Y原子的电子层数多 ②X的气态氢化物比Y的气态氢化物稳定
③Y的单质能将X从NaX的溶液中置换出来 ④X在暗处可与H 反应,Y在加热条件下才能与H 反应
2 2
A. ①② B. ②③ C. ①③ D. ②④
10. 某化学兴趣小组按照如下流程进行“由镁铝合金制备硫酸铝晶体”的实验。
下列有关说法不正确的是
A. 金属X的原子结构示意图为
B. 固体A的化学式为Al(OH)
3
C. 硫酸铝在水中的电离方程式为:Al (SO ) = 2Al3++3
2 4 3
D. 操作②包含的步骤有蒸发浓缩、冷却结晶、分液、洗涤、干燥
11. 下列物质的制备过程中,涉及的反应原理及部分流程较为合理的是
A. 提纯硅:SiO CO+粗硅 SiCl 硅
2 2 4
B. 冶炼铝:铝土矿 NaAlO 无水AlCl Al
2 3
C. 制溴:浓缩海水 Br HBr(aq) Br
2 2
D. 制碘:海带 海带灰 I(aq) I
2 2
12. 关于化学键的叙述正确的是
A. 离子化合物中只存在离子键
B. 非金属元素组成的化合物中可能存在离子键
C. 由不同种元素组成的多原子分子里,一定只存在极性共价键D. 含金属元素的化合物中一定存在离子键
13. 如下图是某种有机物分子的球棍模型图。图中的“棍”代表单键或双键,不同大小的“球”代表三种不同
的短周期元素的原子。对该有机物的叙述不正确的是( )
A. 该有机物可能的分子式为C HCl
2 3
B. 该有机物的分子中一定有
C. 该有机物分子中的所有原子在同一平面上
D. 该有机物可以由乙烯和氯化氢加成反应得到
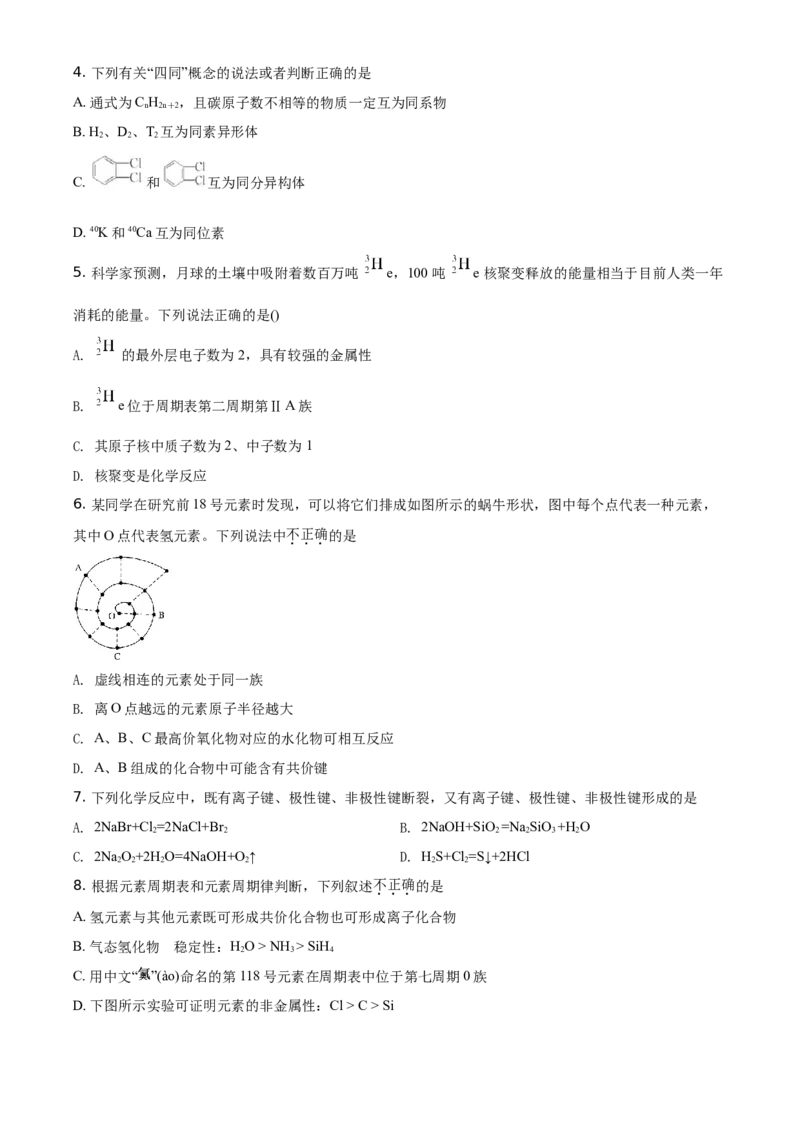
14. 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置
a极质量减小,b极 b极有气体产生,c d极溶解,c极有气 电流从a极流向d
部分实验现象
质量增大 极无变化 体产生 极
由此可判断这四种金属的活动性顺序是( )
A. B. C. D.
15. 2SO (g)+O(g) 2SO (g)是制备硫酸的重要反应。下列叙述不正确的是
2 2 3
A. 催化剂VO 不改变该反应的逆反应速率
2 5
B. 若该反应在恒温恒容体系中进行,充入氦气正反应速率保持不变
C. 该反应是放热反应,升高温度将缩短反应达到平衡的时间
D. 在t、t 时刻,SO (g)的浓度分别是c、c,则时间间隔t~t 内,SO (g)生成的平均速率为v=
1 2 3 1 2 1 2 3
16. 下列关于有机物的说法正确的是
A. 乙烯能使酸性KMnO 溶液和溴水褪色,二者反应原理相同
4
B. 交警用酸性重铬酸钾溶液检查司机是否饮酒时乙醇发生取代反应C. 乙酸的结构简式为CHCOOH,属于弱电解质
3
D. 苯分子中没有碳碳双键,因此苯不能发生加成反应
17. 下列关于有机化合物性质和结构的叙述中正确的是
A. 甲烷、苯、淀粉、蛋白质完全燃烧的产物都只有二氧化碳和水
B. 向鸡蛋清溶液中加入浓硫酸铜溶液,蛋白质发生了不可逆 的变性反应
C. 苯与液溴在铁作催化剂的条件下的反应为加成反应
D. 葡萄糖、蔗糖、淀粉都可以食用,都能发生水解反应
18. 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是
A. 和金属钠反应时断裂①键
B. 在加热和有铜催化下与O 反应时断裂①和③键
2
C. 和乙酸反应制备乙酸乙酯时断裂②键
D. 在空气中完全燃烧时断裂①②③④⑤键
19. 某有机物的结构简式如图,下列关于该有机物的说法正确的是
A. 分子式为C HO
7 6 5
B. 分子中只含有两种官能团
C. 在水溶液中羧基和羟基均能电离出H+
D. 1 mol该物质最多能与4 mol Na发生反应
20. 聚苯乙烯是一种无毒、无臭的热塑性材料,被广泛应用于食品包装材料、电器绝 缘外壳、光学仪器以
及日用产品等。工业由苯和乙烯为原料制备聚苯乙烯的流程如 下图所示(部分条件略去),下列说法错误
的是
A. 过程①生成乙苯,反应类型为加成反应
B. 过程②生成苯乙烯,苯乙烯最多16个原子共面C. 过程③原子利用率为100%,反应类型为加聚反应
D. 上述流程中涉及的五种有机物均可使溴水或高锰酸钾溶液褪色
二、非选择题
21. 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的离子半径由大到小的顺序为_________(用对应的离子符号表示)。
(2)②、③、⑦的最高价氧化物对应水化物的酸性由强到弱的顺序是______________。
(3)①、④、⑤中的某些元素可形成既含离子键又含极性共价键的化合物,写出符合要求的化合物的电子式:
______________。
(4)写出表中①~⑧元素中最高价氧化物对应水化物碱性最强的物质和自然界中含量最高的金属元素反应的
离子方程式:______________。
22. I.是关于化学反应2SO +O 2SO 的两个素材情景:
2 2 3
素材1:某温度和压强下,2升密闭容器中,不同时间点测得密闭体系中三种物质的物质的量
0 10 20 30 40 50 60 70
SO 1 0.7 0.5 0.35 0.2 0.1 0.1 0.1
2
O 0.5 0.35 0.25 0.18 0.1 0.05 0.05 0.05
2
SO 0 0.3 0.5 0.65 0.8 0.9 0.9 0.9
3
素材2:反应在不同条件下进行时SO 的转化率:(SO 的转化率是反应的SO 占起始SO 的物质的量分数,
2 2 2 2
SO 的转化率越大,化学反应的限度越大)
2
0.1 MPa 0.5 MPa 1 MPa 10 MPa
.
400 ℃ 992 99.6 99.7 99.9
500 ℃ 93.5 96.9 97.8 99.3
.
600 ℃ 73.7 85.8 900 96.4根据以上的两个素材回答问题:
(1)根据素材1中计算20~30s期间,用二氧化硫表示的化学反应平均速率为_______ mol·L-1·s-1。
(2)根据素材2中分析得到,提高该化学反应限度(即提高反应物SO 转化率)的途径有_______。
2
(3)根据素材1、素材2中分析得到,要实现素材1中SO 的平衡转化率需控制的反应条件是_____。
2
(4) 在恒温恒容的密闭容器中,发生反应2SO (g)+O(g) 2SO (g) 当下列物理量不再发生变化时:
2 2 3 ,
①混合气体的压强
②混合气体的密度;
③混合气体的总物质的量;
④混合气体的平均相对分子质量;
⑤各反应物或生成物的反应速率之比等于化学计量数之比。
一定能证明2SO (g)+O(g) 2SO (g)达到平衡状态的是_________(填序号)。
2 2 3
II.电池在通讯、交通及日常生活中有着广泛的应用。被称之为“软电池”的纸质电池,采用一个薄层纸片(在
其一边镀锌,而在其另一边镀二氧化锰)作为传导体。在纸内的离子“流过”水和氧化锌组成的碱性电解液。
电池总反应为Zn+2MnO +HO=ZnO+2MnO(OH),则当0.1 mol 负极完全溶解时,转移电子个数为
2 2
__________;该电池正极反应式为_____________。
23. 某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,
而且还能防止环境污染,生产流程如下:
已知石油裂解是生产H的主要方法,E的溶液和新制的氢氧化铜悬浊液反应可以生成砖红色沉淀,G是具
有香味的油状液体,试回答下列问题。
(1)A的名称为___________;G的官能团的名称为____________。
(2)H的结构简式_________。
(3)写出H发生加聚反应的化学方程式:_________________。
(4)D→E的化学方程式:______________。
(5)H→D的化学方程式:___________。
(6)写出G的同分异构体中与CHCOOH互为同系物的任意一种的结构简式:__________。
324. 已知数据:
物质 熔点/℃ 沸点/℃ 密度/g·cm-3
乙醇 -117.3 78.5 0.789
乙酸 16.6 117.9 1.05
乙酸乙酯 -83.6 77.5 0.90
浓硫酸(98%) — 338.0 1.84
实验室制取乙酸乙酯的主要步骤如下:
①在30 mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
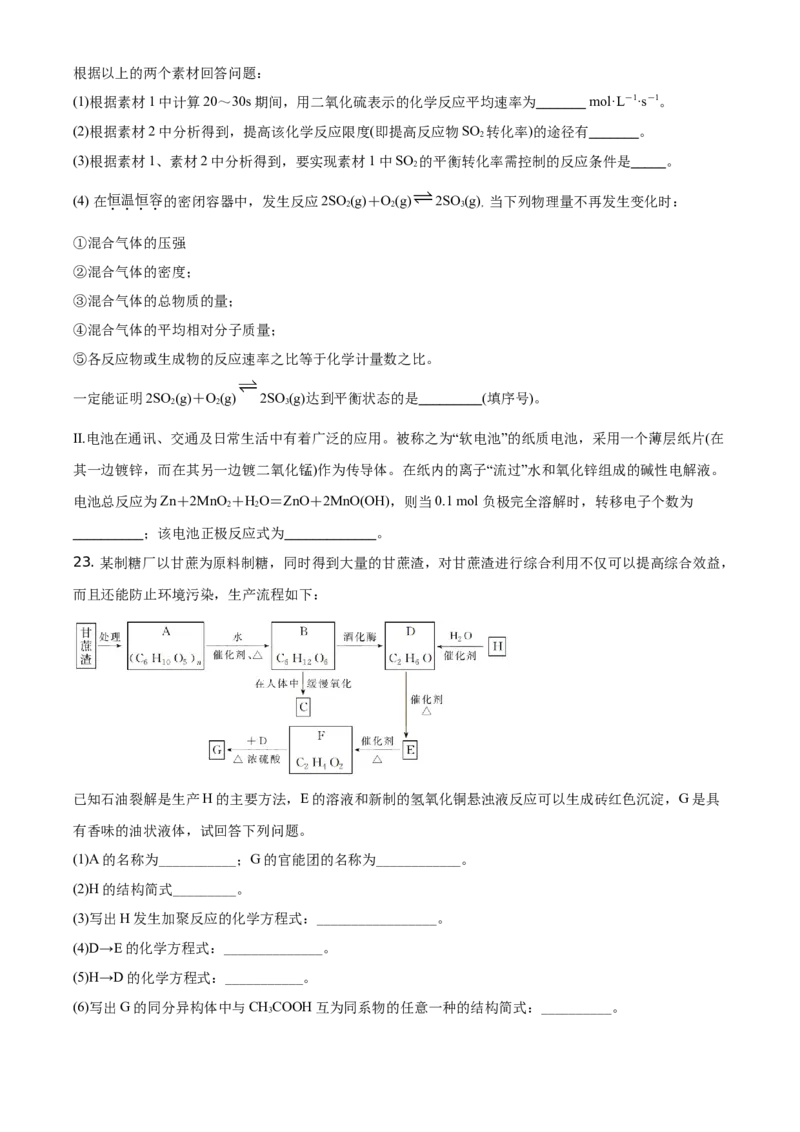
②按图1连接好装置(装置气密性良好),用小火均匀地加热装有混合液的大试管3~5 min;
③待试管B收集到一定量产物后停止加热,撤去试管B并用力振荡,然后静置分层;
④分离出乙酸乙酯层、洗涤和干燥。
请根据题目要求回答下列问题:
(1)写出制取乙酸乙酯的化学方程式:___________。
(2)上述实验中饱和碳酸钠溶液的作用不包括_________(填字母代号)。
A.反应乙酸 B.吸收部分乙醇C.降低乙酸乙酯的溶解度,有利于分层析出 D.吸收挥发出的硫酸,加
快反应速率
(3)步骤②中需要加热并且小火均匀加热的原因是___________。
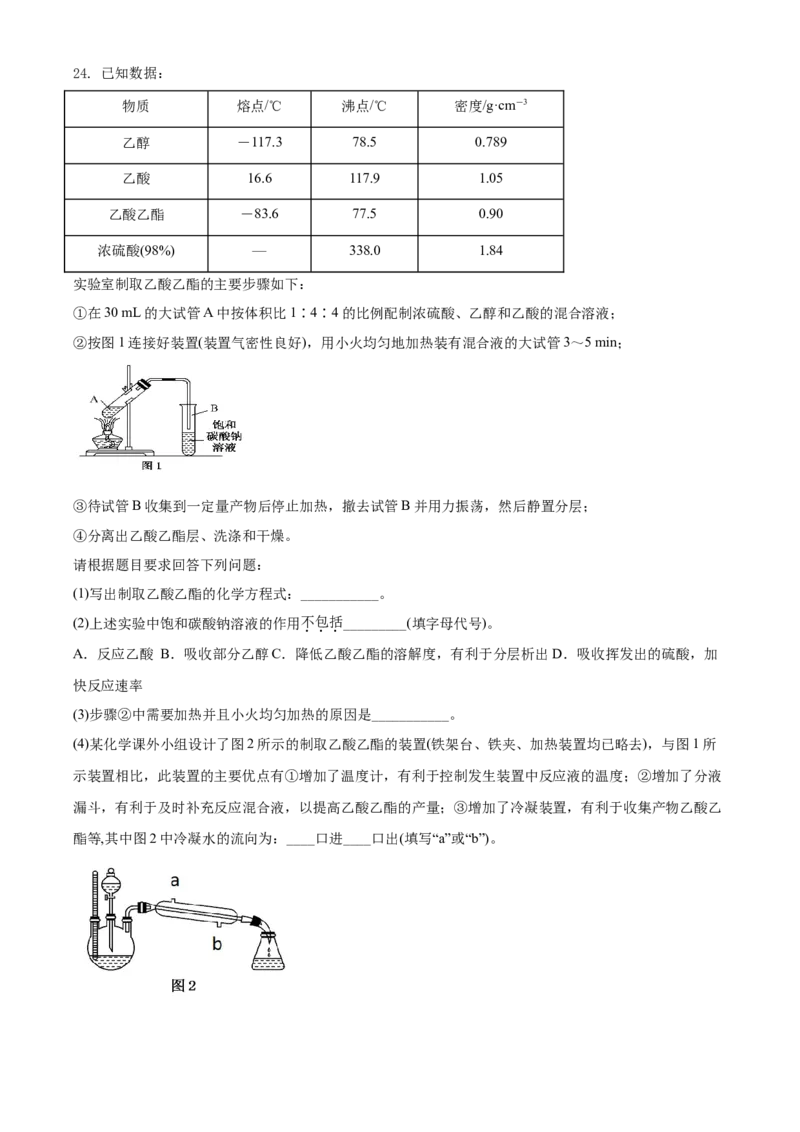
(4)某化学课外小组设计了图2所示的制取乙酸乙酯的装置(铁架台、铁夹、加热装置均已略去),与图1所
示装置相比,此装置的主要优点有①增加了温度计,有利于控制发生装置中反应液的温度;②增加了分液
漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙
酯等,其中图2中冷凝水的流向为:____口进____口出(填写“a”或“b”)。