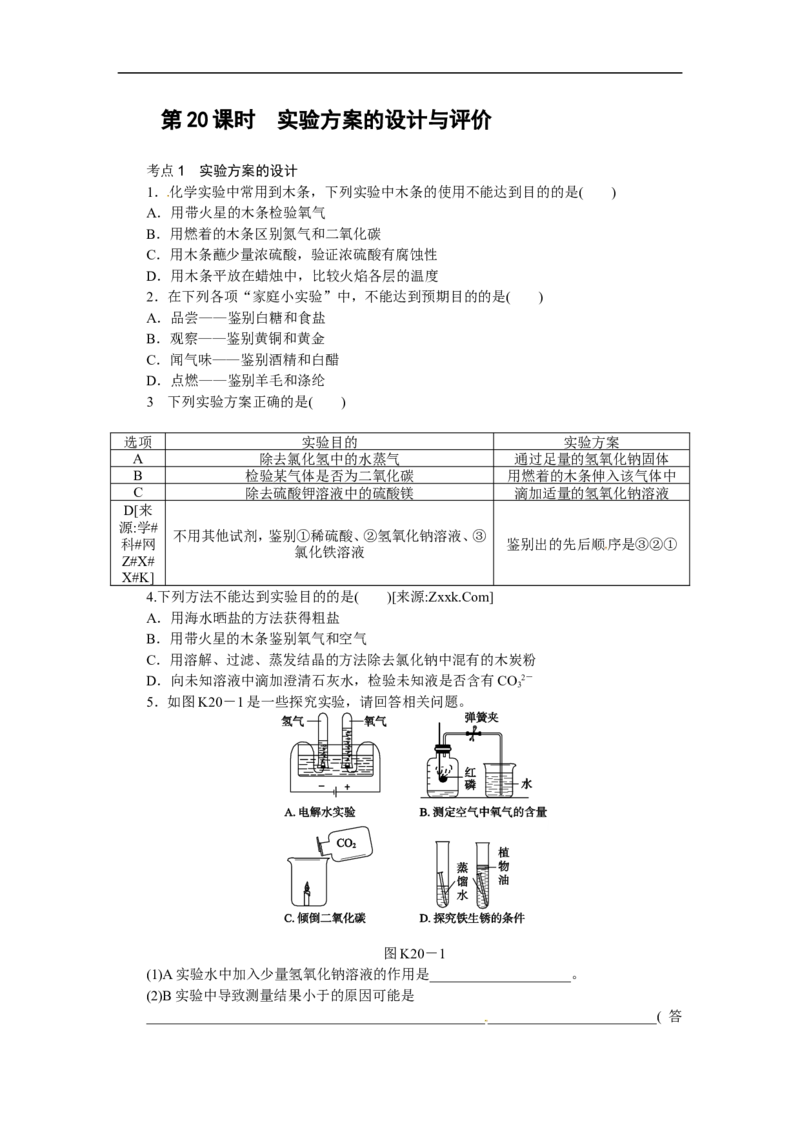文档内容
第 20 课时 实验方案的设计与评价
考点1 实验方案的设计
1.化学实验中常用到木条,下列实验中木条的使用不能达到目的的是( )
A.用带火星的木条检验氧气
B.用燃着的木条区别氮气和二氧化碳
C.用木条蘸少量浓硫酸,验证浓硫酸有腐蚀性
D.用木条平放在蜡烛中,比较火焰各层的温度
2.在下列各项“家庭小实验”中,不能达到预期目的的是( )
A.品尝——鉴别白糖和食盐
B.观察——鉴别黄铜和黄金
C.闻气味——鉴别酒精和白醋
D.点燃——鉴别羊毛和涤纶
3 下列实验方案正确的是( )
选项 实验目的 实验方案
A 除去氯化氢中的水蒸气 通过足量的氢氧化钠固体
B 检验某气体是否为二氧化碳 用燃着的木条伸入该气体中
C 除去硫酸钾溶液中的硫酸镁 滴加适量的氢氧化钠溶液
D[来
源:学#
不用其他试剂,鉴别①稀硫酸、②氢氧化钠溶液、③
科#网 鉴别出的先后顺序是③②①
氯化铁溶液
Z#X#
X#K]
4.下列方法不能达到实验目的的是( )[来源:Zxxk.Com]
A.用海水晒盐的方法获得粗盐
B.用带火星的木条鉴别氧气和空气
C.用溶解、过滤、蒸发结晶的方法除去氯化钠中混有的木炭粉
D.向未知溶液中滴加澄清石灰水,检验未知液是否含有CO2-
3
5.如图K20-1是一些探究实验,请回答相关问题。
图K20-1
(1)A实验水中加入少量氢氧化钠溶液的作用是____________________。
(2)B实验中导致测量结果小于的原因可能是
________________________________________________________________________( 答一点即可)。
(3)C实验可验证二氧化碳的主要物理性质是______________________。
(4)D实验验证铁生锈的条件之一是____________________。
考点2 实验方案的评价
6.某同学设计了以下四个实验方案,理论正确,操作可行,经济合理的是( )
A.Cu――→CuCl ――→Cu(OH)
2 2
B.HO――→O――→MgO
2 2
C.CaCO ――→CaO――→Ca(OH) ――→NaOH溶液
3 2
D.MgCl ――→Mg(OH) ――→Mg
2 2
7.下列四个实验方案设计中,合理可行的是( )
选项 实验目的 实验方案
A 鉴别氧气和二氧化碳 将两种气体分别通入滴有紫色石蕊溶液的水中
B 稀释浓硫酸 将水沿器壁慢慢注入浓硫酸里,并不断搅拌
C 除去氯化钠溶液中的氢氧化钠 加入适量的稀硫酸
D 除去氧化钙中的碳酸钙 加水充分溶解,过滤
8.B用下列方法鉴别物质不能达到实验目的的是( )
选项
[来源:
物质 鉴别方法
学科
网]
A 白酒与矿泉水 闻气味
B MnO 与炭粉[来源:Zxxk.Com] 分别加入过氧化氢溶液
2
NaSO 溶液
C 2 4 分别加入BaCl 溶液
与AgNO 溶液 2
3
NaOH溶液与
D 分别加入MgCl 溶液
Ca(NO ) 溶液 2
3 2
1.根据下列实验方案进行实验,能达到相应实验目的的是( )
图K20-2
A.图甲比较Zn和Fe的金属活动性强弱
B.图乙探究铁钉生锈时O 是否参与反应
2
C.图丙比较红磷和白磷的着火点
D.图丁测定空气中O 的含量
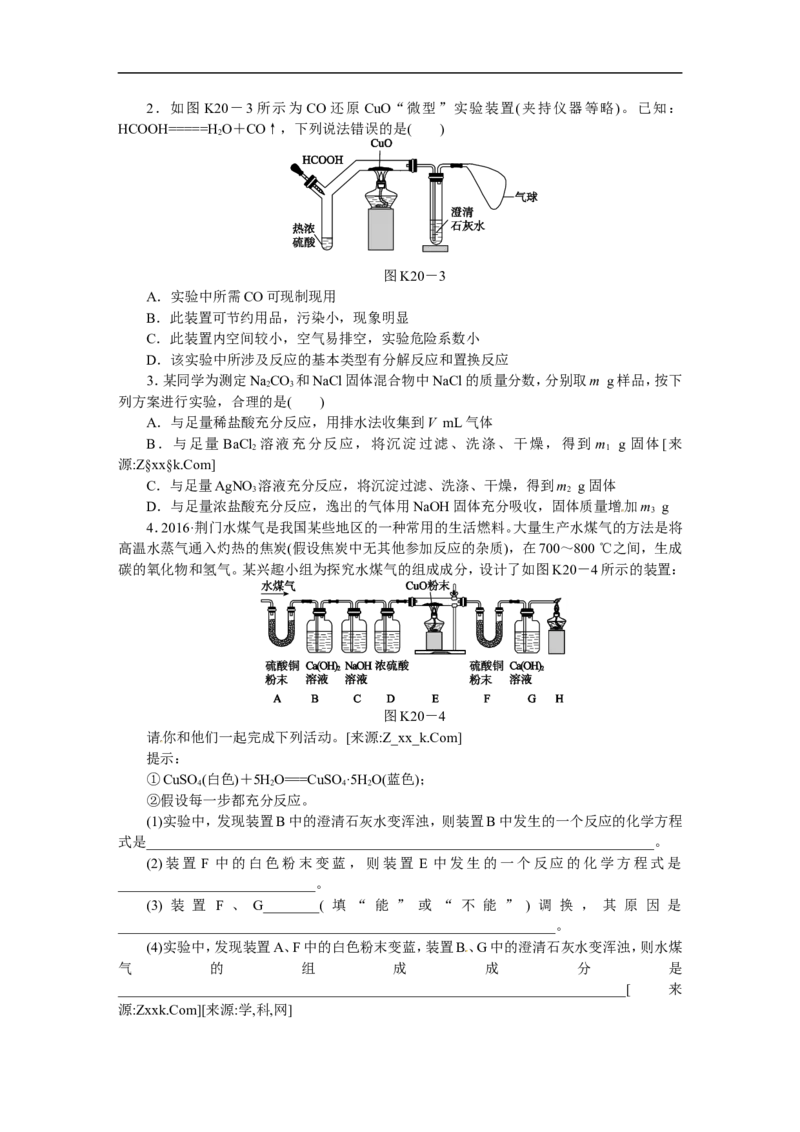
22.如图 K20-3 所示为 CO 还原 CuO“微型”实验装置(夹持仪器等略)。已知:
HCOOH=====HO+CO↑,下列说法错误的是( )
2
图K20-3
A.实验中所需CO可现制现用
B.此装置可节约用品,污染小,现象明显
C.此装置内空间较小,空气易排空,实验危险系数小
D.该实验中所涉及反应的基本类型有分解反应和置换反应
3.某同学为测定NaCO 和NaCl固体混合物中NaCl的质量分数,分别取m g样品,按下
2 3
列方案进行实验,合理的是( )
A.与足量稀盐酸充分反应,用排水法收集到V mL气体
B.与足量 BaCl 溶液充分反应,将沉淀过滤、洗涤、干燥,得到 m g 固体[来
2 1
源:Z§xx§k.Com]
C.与足量AgNO 溶液充分反应,将沉淀过滤、洗涤、干燥,得到m g固体
3 2
D.与足量浓盐酸充分反应,逸出的气体用NaOH固体充分吸收,固体质量增加m g
3
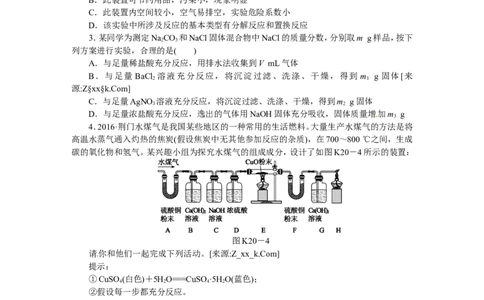
4.2016·荆门水煤气是我国某些地区的一种常用的生活燃料。大量生产水煤气的方法是将
高温水蒸气通入灼热的焦炭(假设焦炭中无其他参加反应的杂质),在700~800 ℃之间,生成
碳的氧化物和氢气。某兴趣小组为探究水煤气的组成成分,设计了如图K20-4所示的装置:
图K20-4
请你和他们一起完成下列活动。[来源:Z_xx_k.Com]
提示:
①CuSO (白色)+5HO===CuSO·5H O(蓝色);
4 2 4 2
②假设每一步都充分反应。
(1)实验中,发现装置B中的澄清石灰水变浑浊,则装置B中发生的一个反应的化学方程
式是________________________________________________________________________。
(2)装置 F 中的白色粉末变蓝,则装置 E 中发生的一个反应的化学方程式是
____________________________。
(3) 装 置 F 、 G________( 填 “ 能 ” 或 “ 不 能 ” ) 调 换 , 其 原 因 是
______________________________________________________________。
(4)实验中,发现装置A、F中的白色粉末变蓝,装置B、G中的澄清石灰水变浑浊,则水煤
气 的 组 成 成 分 是
________________________________________________________________________[ 来
源:Zxxk.Com][来源:学,科,网]__________。
[来源:Z_xx_k.Com]
参考答案
夯实基础
1.B [解析] 由于氧气有助燃性,能使带火星的木条复燃,故可用带火星的木条检验氧气;
氮气和二氧化碳都不燃烧,也不支持燃烧,能使燃着的木条熄灭,则用燃着的木条无法鉴别;
木条属于有机物,含有C、H、O元素,浓硫酸具有脱水性,能使木条中的H和O以水的形式脱
去而变黑,故能达到实验目的;蜡烛各层火焰的温度不同,小木条在各层的炭化程度就不同,
故能达到实验目的。
2.B 3.D 4.D
5.(1)增强水的导电性
(2)红磷的量不足(或装置漏气等)
(3)密度比空气大[来源:Z|xx|k.Com]
(4)与氧气接触
[解析] (1)A实验是电解水实验,水中加入少量氢氧化钠溶液的作用是增强水的导电性。
(2)B实验是测定空气中氧气的含量,导致测量结果小于的原因可能是红磷的量不足、装置漏
气等。(3)C实验中由蜡烛的熄灭可验证二氧化碳的主要物理性质是密度比空气大。(4)D实验
中与氧气接触的铁钉生锈,没有与氧气接触的铁钉不生锈,验证铁生锈的条件之一是与氧气
接触。
6.C [解析] 铜不与稀盐酸反应,该方案在理论上是错误的;水通电分解生成氢气和氧气,
镁与氧气反应生成氧化镁,该方案理论上正确,但水通电分解制取氧气成本较高,经济上不合
理;氯化镁与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,钠不与氢氧化镁反应,该方案在理论上是错误的。
7.A [解析] 二氧化碳能与水反应生成碳酸,碳酸能使紫色石蕊溶液变红,氧气不能,将
两种气体分别通过滴有紫色石蕊溶液的水中,能使紫色石蕊溶液变红的是二氧化碳,无明显
变化的是氧气,能一次鉴别出这两种气体;稀释浓硫酸时,要把浓硫酸缓缓沿器壁注入水中,
同时用玻璃棒不断搅拌,以使热量及时扩散,一定不能把水注入浓硫酸中;氢氧化钠能与稀硫
酸反应生成硫酸钠和水,能除去杂质但引入了新的杂质硫酸钠,不符合除杂的原则;CaO能与
水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂的原则。
8.C [解析] 白酒具有酒的芳香气味,矿泉水无气味,用闻气味的方法可以鉴别;分别加
入过氧化氢溶液,能使过氧化氢分解产生大量气泡的是二氧化锰,无明显变化的是炭粉,可以
鉴别;BaCl 溶液与AgNO 溶液和NaSO 溶液均能反应,分别生成氯化银白色沉淀、硫酸钡白
2 3 2 4
色沉淀,现象相同,不能鉴别;MgCl 溶液能与NaOH溶液反应生成氢氧化镁白色沉淀,与
2
Ca(NO ) 溶液不反应,可以鉴别。
3 2
能力提升
1.B [解析] 图甲没有控制变量,所加溶液中盐酸的溶质质量分数不同;图丙如果比较红
磷和白磷的着火点,白磷和红磷应该都放在薄铜片上;图丁木炭与氧气反应生成气体,影响空
气中氧气含量的测定。
2.D [解析] 甲酸在热的浓硫酸的作用下分解为水和一氧化碳,属于分解反应;一氧化碳
在加热的条件下与氧化铜反应生成铜和二氧化碳,反应物是两种化合物,不符合置换反应的
概念。
3.B [解析] 二氧化碳能溶于水,故用排水法收集的气体的体积会小于实际生成的气体
的体积;碳酸钠和氯化钠都能与硝酸银反应生成沉淀;浓盐酸具有挥发性,挥发出的氯化氢也
能与氢氧化钠反应。
4.(1)CO +Ca(OH) ===CaCO ↓+HO
2 2 3 2
(2)H +CuO=====Cu+HO
2 2
(3)不能 装置G中挥发出的水蒸气,会对装置F中是否有水生成的判断造成干扰
(4)一氧化碳、二氧化碳、水蒸气、氢气
[解析] (1)二氧化碳能使石灰水变浑浊,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水。(2)装
置F中的白色粉末变蓝,说明有水生成,装置E中氢气与氧化铜反应生成了铜和水。(3)装置F
是检验有无水蒸气生成的,G中能挥发出水蒸气,装置F、G不能调换,因为装置G中挥发出
的水蒸气,会对装置F中是否有水生成的判断造成干扰。(4)实验中发现装置A、F中的白色粉
末变蓝,分别说明水煤气中含有水蒸气、氢气(与氧化铜反应生成的水蒸气使F中的白色粉末
变蓝);装置B、G中的澄清石灰水变浑浊,分别说明水煤气中含有二氧化碳、一氧化碳(与氧化
铜反应生成的二氧化碳使G中的澄清石灰水变浑浊)。