文档内容
第5讲 金属和金属材料
命题点1 金属材料
1.(2017·广东)下列物品主要由合金制成的是()
A.塑料水杯 B.单车轮胎
C.羊毛衣服 D.青铜雕像
2.(2017·鄂州)下列关于金属材料的说法中正确的是()
A.铝制品表面应常用钢刷擦洗
B.可用铁桶盛装农药波尔多液
C.焊锡(锡铅合金)的熔点低,常用来焊接金属
D.钢因为比生铁的含碳量高,所以应用范围更广
3.(2017·苏州)下列关于金属的说法中,不正确的是()
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
命题点2 金属的化学性质
4.(2017·郴州)下列金属单质不能与稀盐酸反应放出氢气的是()
A.Cu B.Zn C.Mg D.Fe
5.(2017·东营)今年春季,在张献忠沉银考古现场,整齐堆放着金册、银册,金币、银币、铜币和银锭,还有铁刀、铁
矛等兵器。下列说法中错误的是()
A.“真金不怕火炼”说明了黄金的化学性质稳定
B.上述钱币用金、银、铜而不用铁,从化学角度看主要原因是铁的冶炼困难
C.自然界有天然的铜、银、金却没有天然的金属铁
D.常温下验证铁、铜、银三种金属的活动顺序时,至少需一种金属单质
6.(2017·泰安)现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质
量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是()
A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
命题点3 金属的活动性顺序及其应用
7.(2017·江西)我省明代科学家宋应星所著的《天工开物》中,详细记述了金、铜、铁、锌等金属的开采和冶炼方法,
记述的金属中金属活动性最强的是()
A.金 B.钢 C.铁 D.锌
8.(2017·临沂)有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和
Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属
的活动性由强到弱的顺序正确的是()
A.X Y Z B.X Z Y C.Y Z X D.Z Y X
9.(2017·随州)将一定量的金属M(M是Mg、Al、Zn、Fe中的一种)粉末放入AgNO 和Cu(NO ) 的混合溶液中,充
3 3 2
分反应后过滤,得到滤渣和无色滤液。向滤渣和滤液中分别滴加稀盐酸均无明显现象产生。
(1)金属M不可能是________(填名称)。
(2)滤渣中一定含有的金属是________;无色滤液中含有的阴离子是________(填符号)。命题点4 金属的冶炼
10.(2017·成都)工业上炼铁炼钢和轧制钢材的主要流程如下图:
已知生铁的含量含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)反应:①Fe O+3CO=====2Fe+3CO;②2Fe O+3C=====4Fe+3CO↑。属于置换反应的是________,用
2 3 2 2 3 2
于高炉炼铁的原理是________(填序号)。
(2)炼铁的固体原料需经过粉碎,其目的是____________________________。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是________。炉渣中含有硅酸钙(CaSiO ),其中
3
硅元素的化合价是________。
(4)炼钢炉中,通入纯氧的目的是__________________________________。将钢锭轧成钢板,体现了金属的
________性。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式________________________________________。
命题点5 金属的锈蚀和防护
11.(2017·青岛)下列防锈措施不合理的是()
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
12.(2017·宿迁)人类社会的发展离不开金属。
(1)钢铁的锈蚀主要是铁与空气中的____________等物质发生化学反应的结果;
(2)在空气中,铝的表面易生成致密的氧化膜,氧化膜的主要成分是________(写化学式);
(3)某同学取少量工厂废液[溶质是AgNO、Cu(NO )],向其中加入一定量的金属锌,反应结束后,发现溶液仍然
3 3 2
是蓝色。据此推断,反应后溶液中一定含有的溶质是___________________________________________。重难点1 金属的化学性质
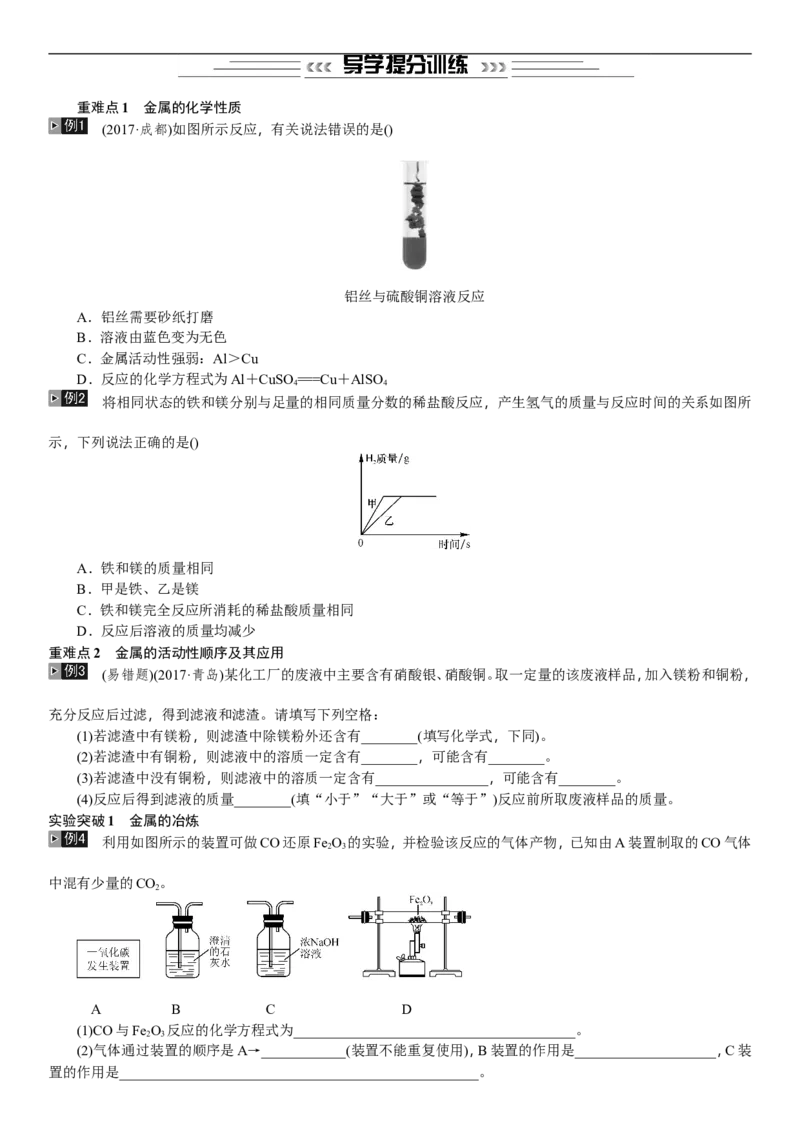
(2017·成都)如图所示反应,有关说法错误的是()
铝丝与硫酸铜溶液反应
A.铝丝需要砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性强弱:Al>Cu
D.反应的化学方程式为Al+CuSO ===Cu+AlSO
4 4
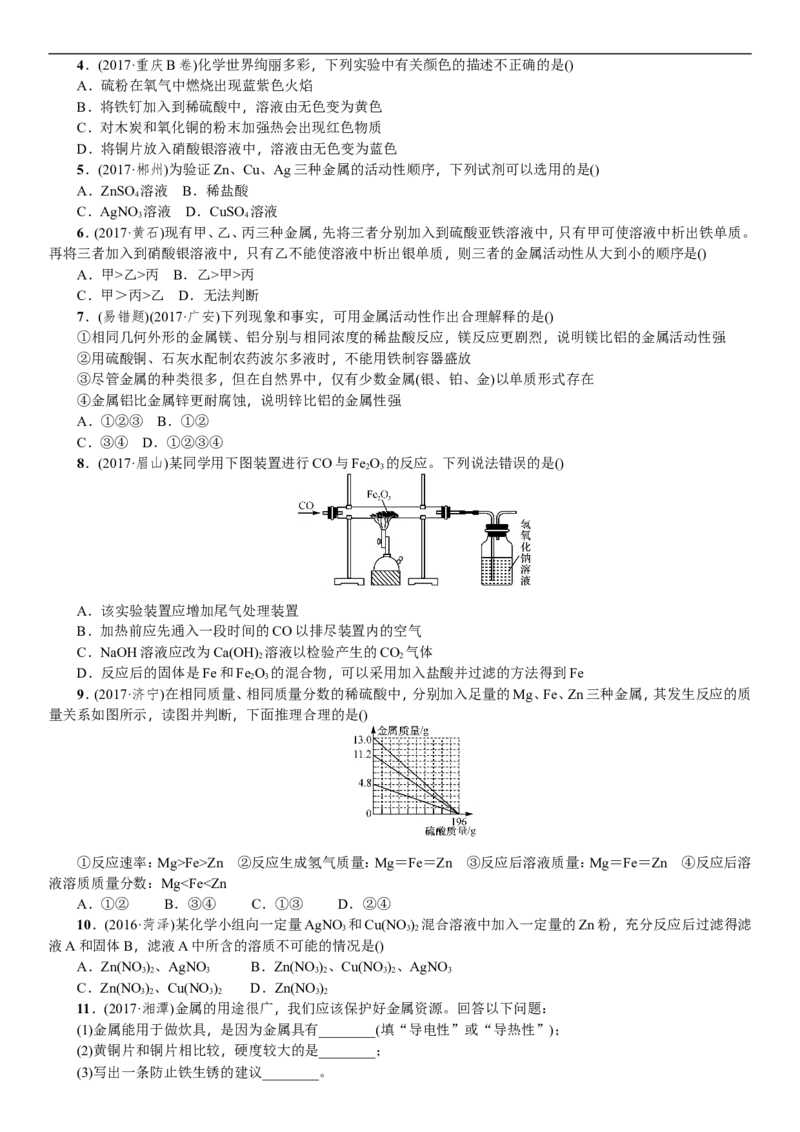
将相同状态的铁和镁分别与足量的相同质量分数的稀盐酸反应,产生氢气的质量与反应时间的关系如图所
示,下列说法正确的是()
A.铁和镁的质量相同
B.甲是铁、乙是镁
C.铁和镁完全反应所消耗的稀盐酸质量相同
D.反应后溶液的质量均减少
重难点2 金属的活动性顺序及其应用
(易错题)(2017·青岛)某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品,加入镁粉和铜粉,
充分反应后过滤,得到滤液和滤渣。请填写下列空格:
(1)若滤渣中有镁粉,则滤渣中除镁粉外还含有________(填写化学式,下同)。
(2)若滤渣中有铜粉,则滤液中的溶质一定含有________,可能含有________。
(3)若滤渣中没有铜粉,则滤液中的溶质一定含有________________,可能含有________。
(4)反应后得到滤液的质量________(填“小于”“大于”或“等于”)反应前所取废液样品的质量。
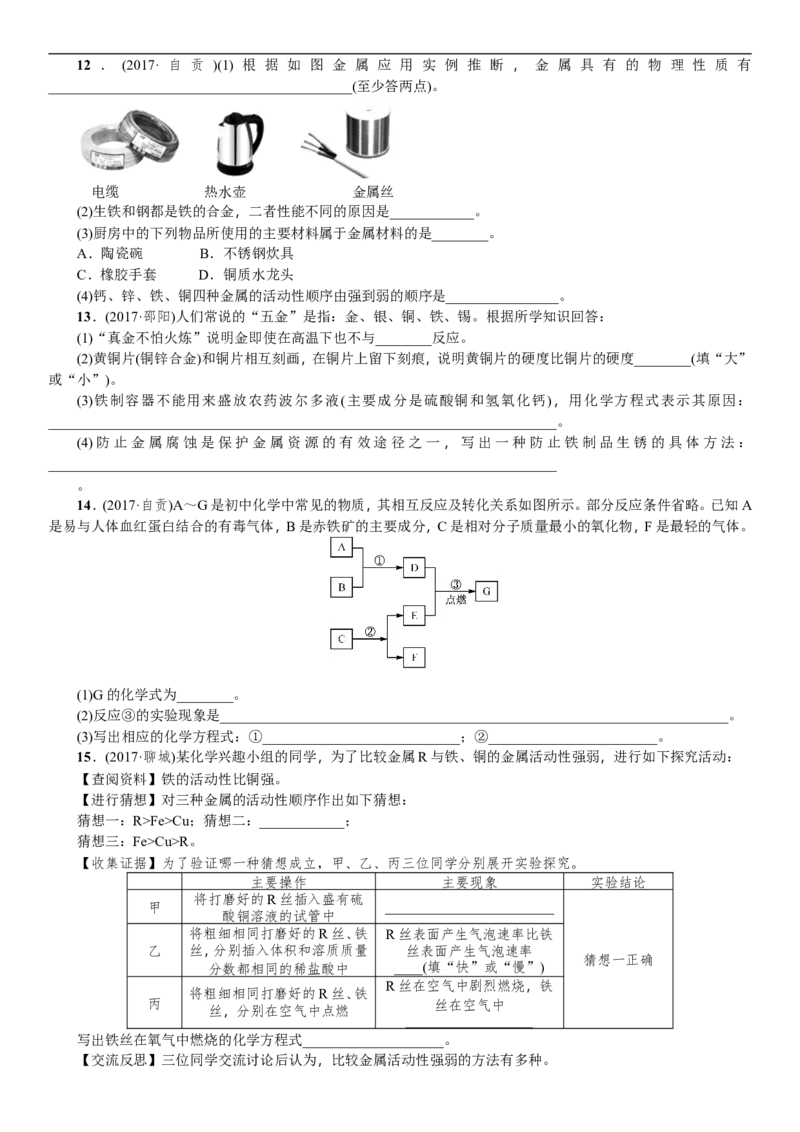
实验突破1 金属的冶炼
利用如图所示的装置可做CO还原Fe O 的实验,并检验该反应的气体产物,已知由A装置制取的CO气体
2 3
中混有少量的CO。
2
A B C D
(1)CO与Fe O 反应的化学方程式为________________________________________。
2 3
(2)气体通过装置的顺序是A→____________(装置不能重复使用),B装置的作用是____________________,C装
置的作用是___________________________________________________。(3)从环保角度考虑,对以上装置的改进措施是_________________________________________。
【拓展训练】
(4)实验中看到的实验现象为玻璃管中的粉末________________,澄清石灰水________。
(5)加热氧化铁之前,先通一会儿一氧化碳的作用是________________________。
(6)工业炼铁得到的铁与该实验中得到的铁有何不同____________________________________。
(7)CO还原Fe O 反应结束后要注意的操作是________________。
2 3
实验突破2 铁锈蚀条件的探究
(2017·安徽)某研究小组为探究“影响铁制品锈蚀快慢的影响因素”。取同浓度的稀氨水和稀醋酸用下图装
置完成表中实验,回答下列问题。
实验序号 ① ② ③ ④
实验温度/℃ 25 25 70 70
试剂 稀氨水 稀醋酸 稀氨水 稀醋酸
出现铁锈 1天 1天
5分钟 1分钟
所需时间 未见锈蚀 未见锈蚀
(1)铁锈的主要成分是________(填化学式)。
(2)实验②和④可探究________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应
选择的实验是____________(填实验序号)。
(3)根据表中实验现象得出的结论是_______________________________________________(写出1点即可)。
(4)影响铁制品锈蚀快慢除上述因素外,还有____________(写出 1 点即可),请设计实验方案
________________________________________________________________________。
【拓展训练】
(5)海水中含有氯化钠、氯化镁等物质,铁制品在海水中和在淡水中锈蚀的快慢是否一样,请你设计实验方案
________________________________________________________________________。
1.(2016·大连)下列有关金属的说法中,错误的是()
A.铜质插头是利用铜的导电性
B.钨制灯丝是利用钨的熔点低
C.铝制成铝箔是利用铝的延展性
D.用铁锅炒菜是利用铁的导热性
2.(2017·平凉)自2011年我省实施找矿战略行动以来,在铜、铅、锌、金、铁、铌、钽等金属方面取得找矿新成果。
下列关于铁、锌、铜三种金属及其合金的说法不正确的是()
A.铁在潮湿的空气中易生锈
B.可以用铁桶盛放硫酸铜溶液
C.可以用稀硫酸鉴别锌与铜的金属活动性强弱
D.黄铜(铜与锌的合金)的硬度大于纯铜
3.(2017·淮安)某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是()
A.定期用清水冲洗,除去灰尘
B.放于体验区,让观众触摸
C.用盐水除去铁剑上的锈斑
D.放在充满氮气的展览柜中4.(2017·重庆B卷)化学世界绚丽多彩,下列实验中有关颜色的描述不正确的是()
A.硫粉在氧气中燃烧出现蓝紫色火焰
B.将铁钉加入到稀硫酸中,溶液由无色变为黄色
C.对木炭和氧化铜的粉末加强热会出现红色物质
D.将铜片放入硝酸银溶液中,溶液由无色变为蓝色
5.(2017·郴州)为验证Zn、Cu、Ag三种金属的活动性顺序,下列试剂可以选用的是()
A.ZnSO 溶液 B.稀盐酸
4
C.AgNO 溶液 D.CuSO 溶液
3 4
6.(2017·黄石)现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。
再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从大到小的顺序是()
A.甲>乙>丙 B.乙>甲>丙
C.甲>丙>乙 D.无法判断
7.(易错题)(2017·广安)下列现象和事实,可用金属活动性作出合理解释的是()
①相同几何外形的金属镁、铝分别与相同浓度的稀盐酸反应,镁反应更剧烈,说明镁比铝的金属活动性强
②用硫酸铜、石灰水配制农药波尔多液时,不能用铁制容器盛放
③尽管金属的种类很多,但在自然界中,仅有少数金属(银、铂、金)以单质形式存在
④金属铝比金属锌更耐腐蚀,说明锌比铝的金属性强
A.①②③ B.①②
C.③④ D.①②③④
8.(2017·眉山)某同学用下图装置进行CO与Fe O 的反应。下列说法错误的是()
2 3
A.该实验装置应增加尾气处理装置
B.加热前应先通入一段时间的CO以排尽装置内的空气
C.NaOH溶液应改为Ca(OH) 溶液以检验产生的CO 气体
2 2
D.反应后的固体是Fe和Fe O 的混合物,可以采用加入盐酸并过滤的方法得到Fe
2 3
9.(2017·济宁)在相同质量、相同质量分数的稀硫酸中,分别加入足量的Mg、Fe、Zn三种金属,其发生反应的质
量关系如图所示,读图并判断,下面推理合理的是()
①反应速率:Mg>Fe>Zn ②反应生成氢气质量:Mg=Fe=Zn ③反应后溶液质量:Mg=Fe=Zn ④反应后溶
液溶质质量分数:MgFe>Cu;猜想二:____________;
猜想三:Fe>Cu>R。
【收集证据】为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究。
主要操作 主要现象 实验结论
将打磨好的R丝插入盛有硫
甲 ________________________
酸铜溶液的试管中
将粗细相同打磨好的R丝、铁 R丝表面产生气泡速率比铁
乙 丝,分别插入体积和溶质质量 丝表面产生气泡速率
猜想一正确
分数都相同的稀盐酸中 ____(填“快”或“慢”)
R丝在空气中剧烈燃烧,铁
将粗细相同打磨好的R丝、铁
丙 丝在空气中
丝,分别在空气中点燃
__________________
写出铁丝在氧气中燃烧的化学方程式____________________。
【交流反思】三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。【归纳总结】他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与________是否反应。
16.(2017·武汉)钢是铁的合金。为测定某钢样中铁的质量分数,取11.4 g钢样,向其中加入稀硫酸,产生氢气的质
量与加入稀硫酸的质量关系如图所示(不考虑钢样中其他成分与稀硫酸的反应)。
(1)钢________(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数(保留一位小数)。
17.(双选)(2017·龙东)将一定质量的Zn加入到Mg(NO )、Fe(NO )、AgNO 三种物质的混合溶液中,充分反应后
3 2 3 2 3
过滤,滤液仍为浅绿色,则下列判断正确的是()
A.滤渣一定为Ag、Fe
B.向滤液中滴加稀盐酸,可能产生白色沉淀
C.滤液中最多含有三种溶质
D.反应前后金属固体的质量可能不变
18.(2017·绍兴)往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的
质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是()
A.c点对应溶液中含有的金属离子为Zn2+和Cu2+
B.bc段(不含两端点)析出的金属是Fe
C.ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+
D.若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m 和m,则m>m
1 2 1 2
19.(2017·泸州)已知:铝在常温下能与O 反应,在铝表面形成一层氧化薄膜;Al O 能溶于NaOH溶液。某课外小
2 2 3
组对“铝与氯化铜溶液反应”进行如下探究。
①测得CuCl 溶液的pH<7;
2
②将铝片放入CuCl 溶液中,没有观察到现象;
2
③取出铝片用NaOH溶液浸泡一段时间,再取出铝片洗净后放入CuCl 溶液中,观察到铝表面产生无色气泡。
2
请回答下列问题:
(1)步骤①观察到CuCl 溶液呈________色,该溶液呈________(填“酸”“碱”或“中”)性。
2
(2)步骤③中还可能观察到的现象是__________,产生此现象的化学方程式是
____________________________________。
(3)步骤②中没有现象的原因是__________________________________________________。(4)小组对步骤③产生的气体提成以下猜想:
a.可能是Cl;
2
b.可能是O;
2
c.可能是________。
小组讨论得出c成立,理由是___________________________________________________。
20.(2017·杭州)小金利用图示装置进行甲、乙对比实验,探究温度对CO和Fe O 反应的影响(固定装置略)。
2 3
甲 乙
(1)从实验安全角度考虑,图示装置还应采取的改进措施是
________________________________________________________________________。
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤 操作 甲组现象 乙组现象
1 称量黑色粉末质量/g m m
1 2
2 取黑色粉末,用磁铁吸引 能被吸引 能被吸引
3 取黑色粉末,加入稀盐酸 全部溶解,有大量气泡 无明显现象
4 取黑色粉末,加入足量CuSO 溶液 有红色物质生成 无明显现象
4
① 甲 组 的 黑 色 粉 末 与 稀 盐 酸 反 应 的 化 学 方 程 式 是
________________________________________________________________________。
②小金查阅资料后发现Fe O 在常温下不与稀盐酸、CuSO 溶液反应,故猜想乙组的生成物为Fe O。他又发现
3 4 4 3 4
m 恰好为________g,这可成为支持上述猜想的新证据。
2
(3)甲、乙两组实验说明温度对CO和Fe O 反应有影响,且均体现出CO的________(填化学性质)。
2 3
参考答案
第5讲 金属和金属材料
中考真题展
1.D 2.C 3.B 4.A 5.B 6.B 7.D 8.B 9.(1)铁 (2)Cu、Ag NO 10.(1)② ①
(2)增大反应接触面积,加快反应速率 (3)N +4(4)使生铁中的碳转化为二氧化碳,降低生铁的碳含量 延展
2
(5)3H SO +Fe O===Fe (SO ) +3HO 11.B 12.(1)氧气和水蒸气(或O 和HO) Al O (3)硝酸铜和硝酸锌[或
2 4 2 3 2 4 3 2 2 2 2 3
Cu(NO ) 和Zn(NO )]
3 2 3 2
导学提分训练
例1 D 例2 C 例3 (1)Ag和Cu (2)Mg(NO) Cu(NO ) (3)Mg(NO) 、Cu(NO ) AgNO (4)小于
3 2 3 2 3 2 3 2 3例4 (1)Fe O+3CO=====2Fe+3CO (2)C→D→B 检验生成物中有二氧化碳 除去混合气体中的二氧化碳,防
2 3 2
止对一氧化碳的生成物检验造成干扰 (3)在B装置后增加尾气处理装置 (4)由红色逐渐变黑 变浑浊(5)排尽玻璃
管中的空气,防止发生爆炸 (6)工业炼铁得到的铁中含有碳等杂质,是生铁 (7)继续通入CO 例5 (1)Fe O (2)
2 3
温度 ①②或③④ (3)其他条件相同的情况下,温度越高,铁制品越容易生锈(或其他条件相同的情况下,酸性试剂
使铁制品容易生锈;其他答案合理均可) (4)酸的浓度 常温下,取两支试管,分别加入不同浓度的稀醋酸,并放入相
同的铁钉,观察出现铁锈所需的时间(其他合理答案均可) (5)常温下,取两支试管,分别加入等量的食盐水和蒸馏水,
观察出现铁锈所需的时间(其他合理答案均可)
课后提分训练
1.B 2.B 3.D 4.B 5.D 6.C 7.A 8.D 9.D 10.A 11.(1)导热性 (2)黄铜片 (3)涂油漆 12.(1)导电性、
导热性、延展性 (2)含碳量不同 (3)BD (4)钙、锌、铁、铜 13.(1)氧气 (2)大 (3)Fe+CuSO ===Cu+FeSO (4)
4 4
刷漆(或涂油或保持表面洁净、干燥或制成合金)(其他合理答案均可) 14.(1)Fe O (2)剧烈燃烧、火星四射、生成黑
3 4
色固体 (3)Fe O+3CO===2Fe+3CO 2HO=====2H↑+O↑ 15【. 进行猜想】Fe>R>Cu 【收集证据】R丝表面
2 3 2 2 2 2
有红色物质析出 快 不能燃烧 3Fe+2O=====Fe O 【归纳总结】盐溶液 16.(1)是
2 3 4
(2)设钢样中铁的质量为x。
Fe+HSO ===FeSO+H↑
2 4 4 2
56 2
x 0.4 g
= x=11.2 g
钢样中铁的质量分数为×100%=98.2%
答:此钢样中铁的质量分数为98.2%。
17.BD 18.C 19.(1)蓝 酸 (2)生成红色固体 2Al+3CuCl ===2AlCl +3Cu (3)铝在常温下与氧气反应,在
2 3
铝表面形成一层氧化薄膜 (4)H 铝能和显酸性的溶液反应生成铝盐和氢气 20.(1)在装置末端尖嘴导管处放置一
2
盏燃着的酒精灯(合理即可) (2)①Fe+2HCl===FeCl +H↑ ②4.64 ③还原性
2 2