文档内容
第6讲 酸和碱
第1课时 常见的酸和碱
一、选择题
1.(2014,聊城)氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是(B)
A.都能与指示剂作用
B.都能解离出氢氧根离子
C.都能解离出金属阳离子
D.都含有氢元素和氧元素
2.(2015,北京)下列物质常用于改良酸性土壤的是( A )
A.熟石灰 B.烧碱
C.食盐 D.大理石
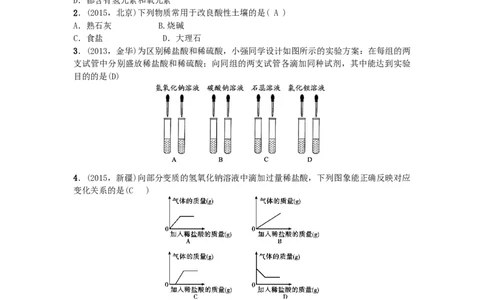
3.(2013,金华)为区别稀盐酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两
支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂,其中能达到实验
目的的是(D)
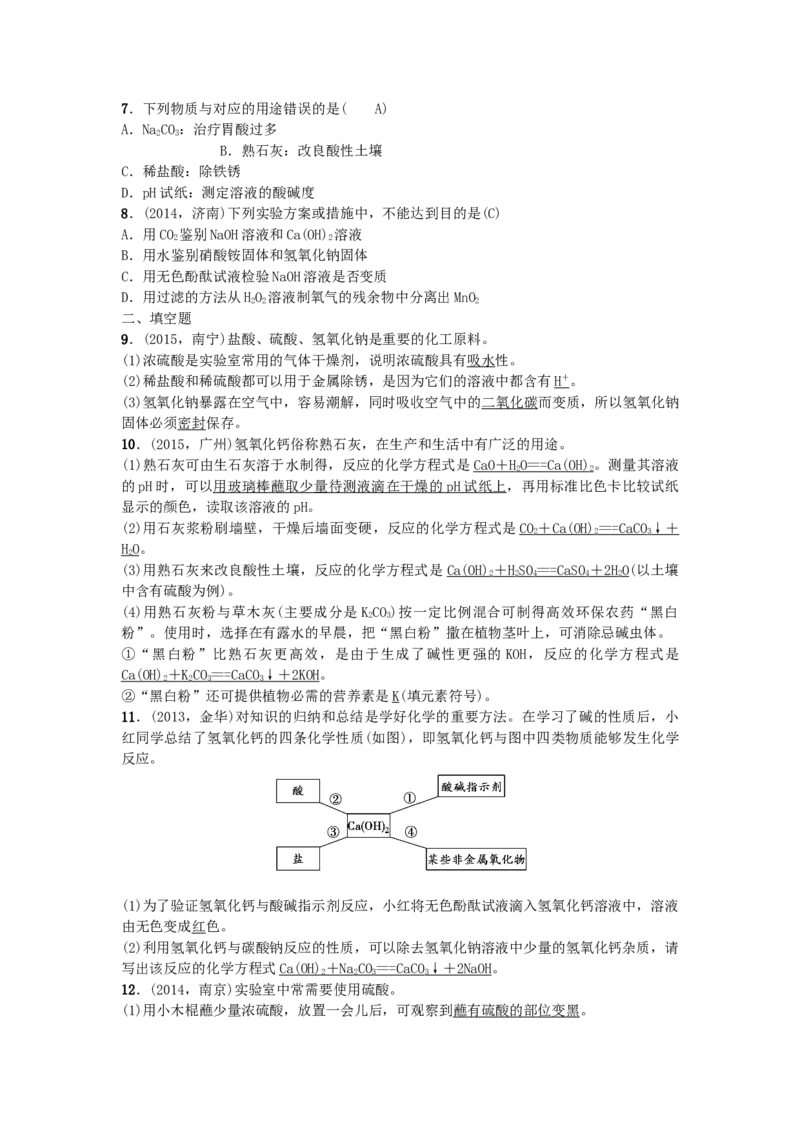
4.(2015,新疆)向部分变质的氢氧化钠溶液中滴加过量稀盐酸,下列图象能正确反映对应
变化关系的是(C )
5.(2015,福州)下列应用与中和反应原理无关的是(A)
A.用浓硫酸干燥湿润的氧气
B.用熟石灰改良酸性土壤
C.服用含氢氧化铝的药物治疗胃酸过多
D.用氢氧化钠溶液洗涤石油产品中的残留硫酸
6.(2015,眉山)下列物质暴露在空气中质量明显增加,溶于水温度明显降低的物质分别是
(B)
①氧化钙 ②硝酸铵 ③浓盐酸 ④氯化钠
A.②③ B.①② C.①④ D.④②7.下列物质与对应的用途错误的是( A)
A.NaCO:治疗胃酸过多
2 3
B.熟石灰:改良酸性土壤
C.稀盐酸:除铁锈
D.pH试纸:测定溶液的酸碱度
8.(2014,济南)下列实验方案或措施中,不能达到目的是(C)
A.用CO 鉴别NaOH溶液和Ca(OH) 溶液
2 2
B.用水鉴别硝酸铵固体和氢氧化钠固体
C.用无色酚酞试液检验NaOH溶液是否变质
D.用过滤的方法从HO 溶液制氧气的残余物中分离出MnO
2 2 2
二、填空题
9.(2015,南宁)盐酸、硫酸、氢氧化钠是重要的化工原料。
(1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具有吸水性。
(2)稀盐酸和稀硫酸都可以用于金属除锈,是因为它们的溶液中都含有 H + 。
(3)氢氧化钠暴露在空气中,容易潮解,同时吸收空气中的二氧化碳而变质,所以氢氧化钠
固体必须密封保存。
10.(2015,广州)氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途。
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是 Ca O + H O = = =Ca(OH ) 。测量其溶液
2 2
的pH时,可以 用玻璃棒蘸取少量待测液滴在干燥的 pH 试纸上 ,再用标准比色卡比较试纸
显示的颜色,读取该溶液的pH。
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是CO + Ca(OH ) = = =CaC O↓+
2 2 3
HO。
2
(3)用熟石灰来改良酸性土壤,反应的化学方程式是Ca(OH) + HSO = = =CaS O + 2 HO(以土壤
2 2 4 4 2
中含有硫酸为例)。
(4)用熟石灰粉与草木灰(主要成分是KCO)按一定比例混合可制得高效环保农药“黑白
2 3
粉”。使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体。
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的 KOH,反应的化学方程式是
Ca(OH) + KCO = = =CaC O ↓+ 2KO H。
2 2 3 3
②“黑白粉”还可提供植物必需的营养素是K(填元素符号)。
11.(2013,金华)对知识的归纳和总结是学好化学的重要方法。在学习了碱的性质后,小
红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学
反应。
(1)为了验证氢氧化钙与酸碱指示剂反应,小红将无色酚酞试液滴入氢氧化钙溶液中,溶液
由无色变成红色。
(2)利用氢氧化钙与碳酸钠反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请
写出该反应的化学方程式Ca(OH) + N aCO = = =CaC O ↓+ 2NaO H。
2 2 3 3
12.(2014,南京)实验室中常需要使用硫酸。
(1)用小木棍蘸少量浓硫酸,放置一会儿后,可观察到蘸有硫酸的部位变黑。(2)98%的浓硫酸稀释为稀硫酸时,一定要将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,
并用玻璃棒搅拌,此时若用手轻轻触碰烧杯外壁,有 热 ( 或烫 )的感觉。
(3)49 g质量分数为20%的稀硫酸与足量锌反应,最多生成氢气的质量是多少?(写出计算
过程)
解:49 g稀硫酸中HSO 的质量为49 g×20%=9.8 g
2 4
设最多生成氢气的质量为x。
Zn+HSO===ZnSO+H↑
2 4 4 2
98 2
9.8 g x
= x=0.2 g
三、实验探究题
13.(2013,重庆)硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料。它们既有相
似之处,又有不同之处。
(1)它们水溶液的pH都小于(填“大于”“小于”或“等于”)7。
(2)它们都能除铁锈,写出盐酸除铁锈的化学方程式FeO + 6HC l = = =2FeC l + 3 HO。
2 3 3 2
(3)它们都能与碱反应生成盐和水,该类反应叫做中和反应。
(4)打开两瓶盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是浓盐酸。
(5)写出把硫酸转变为盐酸的化学方程式 HSO + BaC l = = =BaS O ↓+ 2HC l。
2 4 2 4
14.(2015,乌鲁木齐) 盐酸、硫酸、氢氧化钠和氢氧化钙是初中化学中常见的物质,它们
有着较广泛的用途。
(1)酸与碱之间能发生 中和反应,写出一个上述四种物质之间能发生反应的化学方程式:
HSO + Ca(OH ) = = =CaS O + 2 H2O。
2 4 2 4 _
(2)氢氧化钙可以用来调节土壤的 酸碱 性,它的水溶液常用来检验 二氧化碳气体的
存在。
(3)将一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该
溶液的pH >(填“>”“<”或“=”)7。要准确测定该溶液的pH,需要用到的仪器是 p H 计 。
15.(2015,新疆)实验室常用碳酸钙和稀盐酸反应制取二氧化碳。化学兴趣小组的同学们
想探究反应后废液中溶质的成分,请你一同参与探究并回答问题。
【提出问题】废液中的溶质是什么物质?
【作出猜想】玉素甫同学认为:废液中溶质只有氯化钙;阿依古丽同学认为:废液中含有
的溶质是氯化钙和氯化氢。
【查阅资料】氯化钙溶液呈中性。
【实验与结论】
(1)请写出实验室制取二氧化碳反应的化学方程式CaCO + 2HC l = = =CaC l + H O + C O↑。
3 2 2 2
【玉素甫同学做对比实验】
实验步骤 实验现象 实验结论
取少量废液于试管中,滴入无色酚酞
溶液
溶液
无色
取少量氯化钙溶液于试管中,滴入无
溶液
色酚酞溶液
无色 废液中溶质只有氯化钙猜想正确
【实验评价】
(2)你认为玉素甫同学的实验不能(填“能”或“不能”)证明他的猜想,理由是酚酞试液遇酸性、中性溶液不显色,废液中可能含有氯化氢。
(3)如果你要证明阿依古丽同学的猜想是正确的,你选择 A(填字母)来代替酚酞试液,理由
是石蕊试液遇酸性、中性、碱性溶液显不同颜色。
A.紫色石蕊试液 B.氢氧化钠溶液
C.稀盐酸
(4)若实验证明了阿依古丽同学的猜想是正确的,向废液中加入过量的 碳酸钙,反应完
成后过滤就可得到只含氯化钙一种溶质的溶液。第2课时 中和反应、pH
一、选择题
1.(2015,广州)常温下,下列说法错误的是(C)
A.pH=2的溶液显酸性
B.pH=7的溶液显中性
C.溶液的pH由5变成2,其酸性减弱
D.pH>10的土壤不适于种植农作物,因为碱性太强
2.(2014,北京)下列数据是一些物质的pH,其中呈碱性的是(A)
A.液体肥皂 B.西瓜汁 C.酱油 D.柠檬汁
3.(2014,兰州)为了维持人体正常的生命活动,人体不同器官内的体液具有不同的酸碱性,
根据下表可知,在正常情况下(B)
体液 唾液 胆汁 胰液
pH 6.6~7.1 7.1~7.3 7.5~8.0
A.人体的唾液一定呈酸性
B.人体的胆汁一定呈碱性
C.人体的胰液能使紫色石蕊试液变红色
D.酚酞试液可精确测得以上体液的pH
4.(2015,宜宾)一些食物的近似pH如下,下列说法不正确的是(A)
食物 苹果汁 葡萄汁 牛奶 鸡蛋清
pH 2.9~3.3 3.5~4.5 6.3~6.6 7.6~8.0
A.葡萄汁比苹果汁的酸性强
B.苹果汁和葡萄汁都能使石蕊试液变红
C.牛奶和鸡蛋清都接近中性
D.胃酸过多的人应少饮苹果汁
5.(2015,重庆)某同学用pH试纸测得以下液体的pH,实验过程中pH试纸变成蓝色的是
(C)
A.雨水pH=6 B.食醋pH=3
C.肥皂水pH=10 D.食盐水pH=7
6.(2015,兰州)推理是化学学习中常用的思维方法。下列推理正确的是(A)
A.酸和碱能发生中和反应,则硝酸与氢氧化钠也能发生中和反应
B.铝表面的氧化铝薄膜能起到保护作用,则铁表面的氧化铁也能起到保护作用
C.碱溶液能使石蕊试液变蓝,则能使石蕊试液变蓝的溶液一定是碱
D.蔗糖的饱和溶液,不能再溶解蔗糖,也一定不能再溶解其他物质
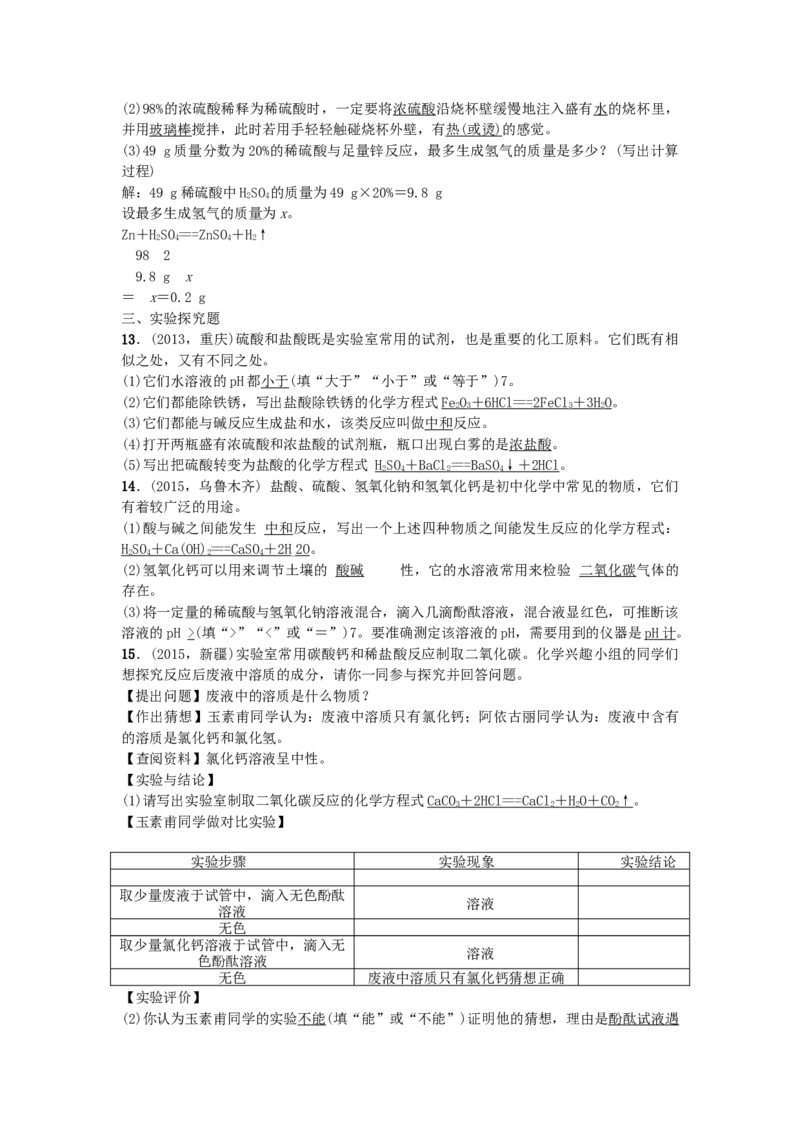
7.(2014,凉山)下列图象与对应选项关系合理的是(C)A.稀释一定溶质质量分数的氢氧化钠溶液
B.向一定溶质质量分数的盐酸中滴加氢氧化钠溶液至过量
C.等质量的锌、铁与足量的稀硫酸反应
D.熟石灰的溶解度与温度的关系
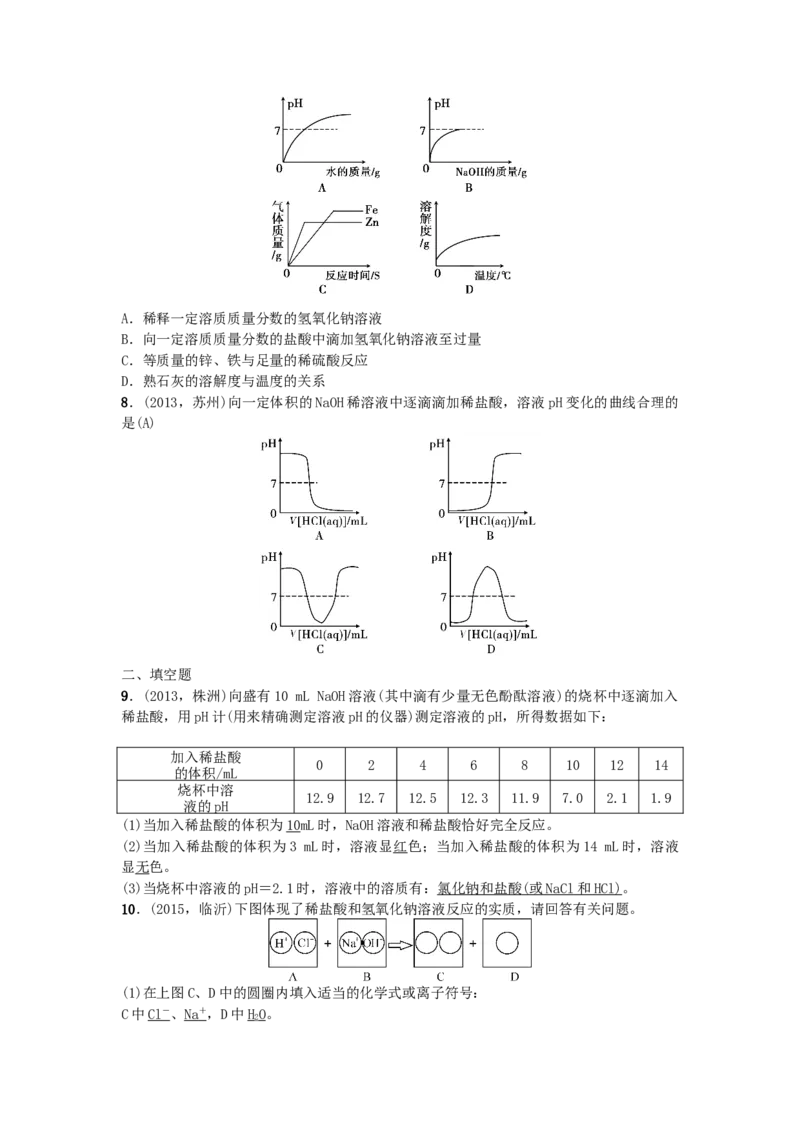
8.(2013,苏州)向一定体积的NaOH稀溶液中逐滴滴加稀盐酸,溶液pH变化的曲线合理的
是(A)
二、填空题
9.(2013,株洲)向盛有10 mL NaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入
稀盐酸,用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
加入稀盐酸
0 2 4 6 8 10 12 14
的体积/mL
烧杯中溶
12.9 12.7 12.5 12.3 11.9 7.0 2.1 1.9
液的pH
(1)当加入稀盐酸的体积为10mL时,NaOH溶液和稀盐酸恰好完全反应。
(2)当加入稀盐酸的体积为3 mL时,溶液显红色;当加入稀盐酸的体积为14 mL时,溶液
显无色。
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有: 氯化钠和盐酸 ( 或 NaC l 和 HCl )。
10.(2015,临沂)下图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题。
(1)在上图C、D中的圆圈内填入适当的化学式或离子符号:
C中 C l - 、 N a + ,D中HO。
2(2)用化学方程式表示图中所体现的化学反应 NaO H + _ HC l = = =NaC l + HO。
2
(3)以上变化的基本反应类型是复分解反应。
三、实验探究题
11.(2014,呼和浩特)某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,
向烧杯中的氢氧化钙溶液滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止
滴加稀盐酸,并对烧杯内溶液中溶质的成分进行探究。
(1)写出该中和反应的化学方程式Ca(OH) + 2HC l = = =CaC l + 2 HO。
2 2 2
(2)探究烧杯内溶液中溶质的成分。
【作出猜想】(A)溶质可能是CaCl 与Ca(OH);
2 2
(B)溶质可能是CaCl;
2
(C)溶质可能是CaCl 与HCl。
2
【查阅资料】CaCl 溶液呈中性。
2
【实验设计】①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡
观察到酚酞试液不变色。于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙能使
无色的酚酞试液变红。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
实验步骤 预计现象 预计结论
取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液
产生白色沉淀 猜想(B)正确
先产生气泡,后生成白色沉淀 猜想(C)正确
【交流反思】为确定猜想(C)正确,下列几种实验方案不合理的是D(填字母)。
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH<7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀
12.(2014,武威)某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导
下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀HSO 加入到盛有NaOH溶液的小烧杯中。
2 4
【学生板演】该反应的化学方程式_HSO + 2NaO H = = =N aSO_ + 2 HO_。
2 4 2 4 2
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么
呢?
【假设猜想】针对疑问,大家纷纷提出猜想。甲组同学的猜想如下:
猜想一:只有NaSO;
2 4
猜想二:有NaSO 和HSO;
2 4 2 4
猜想三:有NaSO 和NaOH;
2 4
猜想四:有NaSO、HSO 和NaOH。
2 4 2 4
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的猜想是 猜想四 。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO 溶液,无明显变
4
化,溶液中一定没有 NaOH ( 或氢氧化钠 ) 。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的 pH试纸、铜片、
BaCl 溶液、NaCO 溶液,进行如下三个方案的探究。
2 2 3
实验方案 测溶液pH 滴加NaCO 溶液 滴加BaCl 溶液
2 3 2实验操作
实验现象 试纸变色,
对比比色卡,
pH<7 有气泡产生 产生白色沉淀
实验结论 溶液中
有HSO 溶液中有HSO 溶液中有HSO
2 4 2 4 2 4
【得出结论】通过探究,全班同学一致确定猜想二是正确的。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指
出【实验探究】(2)中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
(1)实验操作中的错误是_ p H 试纸直接浸入溶液中 _。
(2)实验方案中也有一个是错误的,错误的原因是 BaCl 与 N aSO 反应也会生成白色沉淀,
2 2 4
不能证明一定有 HSO 存在_。
2 4