文档内容
高州市 2020~2021 学年度第二学期高一教学质量监测
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对
应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题
区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
3.本卷命题范围:必修第二册。
可能用到的相对原子质量:H-1 C-12 O-16 Cu-64
一、选择题:本题共16小题,共44分。第1~10题,每小题2分,第11~16题,每小题4分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 2021年5月15日,我国火星探测器“天问一号”成功着陆火星。天问一号探测器上使用了重量轻、强度高、
刚性好、宽温度范围下尺寸稳定的新型SiC增强铝基复合材料。下列说法错误的是
A. SiC是一种新型硅酸盐材料
B. SiC俗称金刚砂,具有类似金刚石的结构
C. SiC中的碳原子和硅原子通过共价键连接
D. SiC具有优异的高温抗氧化性能
【答案】A
【解析】
【分析】
【详解】A.SiC属于新型陶瓷,不属于硅酸盐材料,故A错误;
B.碳化硅俗称金刚砂,具有类似金刚石的结构,熔沸点高,硬度大,可用于制造耐高温、抗氧化的新型
陶瓷,B正确;
C.SiC属于共价化合物,碳原子和硅原子通过共价键连接,C正确;
D.SiC属于原子晶体,故SiC陶瓷具有耐高温、抗腐蚀等优异性能,D正确;
故选A。
2. 下列过程属于物理变化的是
A. 石油裂化 B. 煤的干馏 C. 海水晒盐 D. 海水提溴
【答案】C
【解析】
【分析】化学变化是指有新物质生成的变化,物理变化是指无新物质生成的变化,据此分析判断。【详解】A.石油裂化的目的是将长链的烷烃裂解后得到短链的轻质液体燃料烯烃,有新物质生成,是化
学变化,故A不选;
B.煤的干馏是将煤隔绝空气加强热,使之发生分解的过程,有新物质生成,是化学变化,故B不选;
C.海水晒盐是将海水中的水分蒸发,没有新物质生成,是物理变化,故C选;
D.海水提溴时,要用氯气把海水中 的溴离子置换成为单质溴,有新物质生成,是化学变化,故D不选;
故选C。
3. 下列过程的相应产物与酸雨无关的是
A. 含硫矿物冶炼时生成的二氧化硫
B. 化石燃料燃烧生成的二氧化碳
C. 机车发动机中氮气与氧气反应生成的氮氧化物
D. 工业制硝酸排放的含有氮氧化物的尾气
【答案】B
【解析】
【分析】酸雨包括硫酸型酸雨和硝酸型酸雨,据此分析判断。
【详解】A.含硫燃料的燃烧或含硫矿物的冶炼,会生成二氧化硫气体,直接排放会形成硫酸型酸雨,故
A不选;
B.化石燃料的燃烧产生大量的二氧化碳,二氧化碳的排放与酸雨无关,故B选;
C.机动车发动机的燃料燃烧时,在高温条件下使气缸中的氮气与氧气反应生成氮氧化物,直接排放会形
成硝酸型酸雨,故C不选;
D.工业制硝酸排放的含有氮氧化物的尾气,直接排放会形成硝酸型酸雨,故D不选;
故选B。
4. 氧化还原反应广泛应用于金属的冶炼,下列有关金属冶炼的说法错误的是
A. 电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B. 热分解法、热还原法、电解法冶炼金属中,金属元素都由化合态转变为游离态
C. 铝热反应中铝作为还原剂将铁从其氧化物中置换出来
D. 用磁铁矿炼铁的反应中,1molFe O 被CO还原成Fe,转移9mol电子
3 4
【答案】D
【解析】
【分析】
【详解】A.电解熔融氯化钠生成钠和氯气,故A正确;
B.冶炼金属是金属元素都由化合态转变为游离态,故B正确;
C.铝还原金属氧化物生成金属单质和氧化铝为铝热反应,故C正确;D.用磁铁矿炼铁的反应为 ,当有1 被 还原成 时,转移
8 电子,D项错误。
故选D。
5. 下列关于浓硫酸的说法正确的是( )
A. 不能用铁制容器盛装冷浓硫酸
B. 稀释浓硫酸是将水沿着容器壁慢慢倒入浓硫酸中
C. 浓硫酸能使蔗糖变黑,体现了浓硫酸的脱水性
D. 浓硫酸是一种常用的液体干燥剂,可用于干燥氨气
【答案】C
【解析】
【详解】A.铁单质与浓硫酸在常温下会钝化,可用铁制容器盛装冷浓硫酸,故A错误;
B.浓硫酸的稀释过程中需将浓硫酸加入水中,不能将水加热浓硫酸中,否则浓硫酸容易飞溅伤人,故B
错误;
C.浓硫酸能够将蔗糖中氢原子和氧原子按照2:1脱去,使蔗糖变黑,体现了浓硫酸的脱水性,故C正确;
D.浓硫酸具有强氧化性和酸性,不能用于干燥氨气,故D错误;
故答案为C。
【点睛】浓硫酸的吸水性:少量胆矾加入浓硫酸中→蓝色固体变白;
浓硫酸的脱水性:用玻璃棒蘸取浓硫酸滴在滤纸上→沾有浓HSO 的滤纸变黑;
2 4
浓硫酸强氧化性、酸性:将铜片加入盛有浓硫酸的试管中加热→铜片逐渐溶解,产生无色刺激性气味的气
体。
6. 下列说法正确的是
A. 异戊橡胶属于天然橡胶,经硫化后具有更好的弹性
B. 聚丙烯是由—CH—CH—CH—结构单元重复连接而成的
2 2 2
C. 维生素C具有还原性,可用作食品抗氧化剂
D. 淀粉、橡胶、腈纶都是天然高分子化合物
【答案】C
【解析】
【分析】
【详解】A.异戊橡胶是由异戊二烯合成的一种橡胶,最接近天然橡胶,其耐水性,电绝缘性超过天然橡
胶,属于合成橡胶,故A错误;B.聚丙烯是由 结构单元重复连接而成的,故B错误;
C.维生素C具有还原性,能够被氧气氧化,吸收氧气,可做食品抗氧化剂,故C正确;
D.淀粉、天然橡胶是天然高分子化合物,合成橡胶、腈纶都是合成高分子化合物,故D错误;
故选C。
7. 下列关于烃的叙述错误的是
A. 饱和烃的组成都满足通式C H
n 2n+2
B. 烯烃、炔烃、芳香烃都属于不饱和烃
C. 分子中碳碳键只有两种
D. 乙炔分子中4个原子在同一直线上
【答案】A
【解析】
【分析】
【详解】A.分子通式为C H 的烃,C处于饱和状态,属于饱和烃,也称烷烃,但饱和烃的组成不都满
n 2n+2
足通式C H ,如环丙烷,故A错误;
n 2n+2
B.烯烃(含碳碳双键)、炔烃(含碳碳三键)、芳香烃(含苯环)均含不饱和碳原子,都属于不饱和烃,故B正
确;
C. 分子中苯环上的碳碳键完全相同,是介于碳碳单键和双键之间的独特的键,苯环与甲基
间的为碳碳单键,故C正确;
D.乙炔是直线形分子,四个原子在同一直线上,故D正确;
故选A。
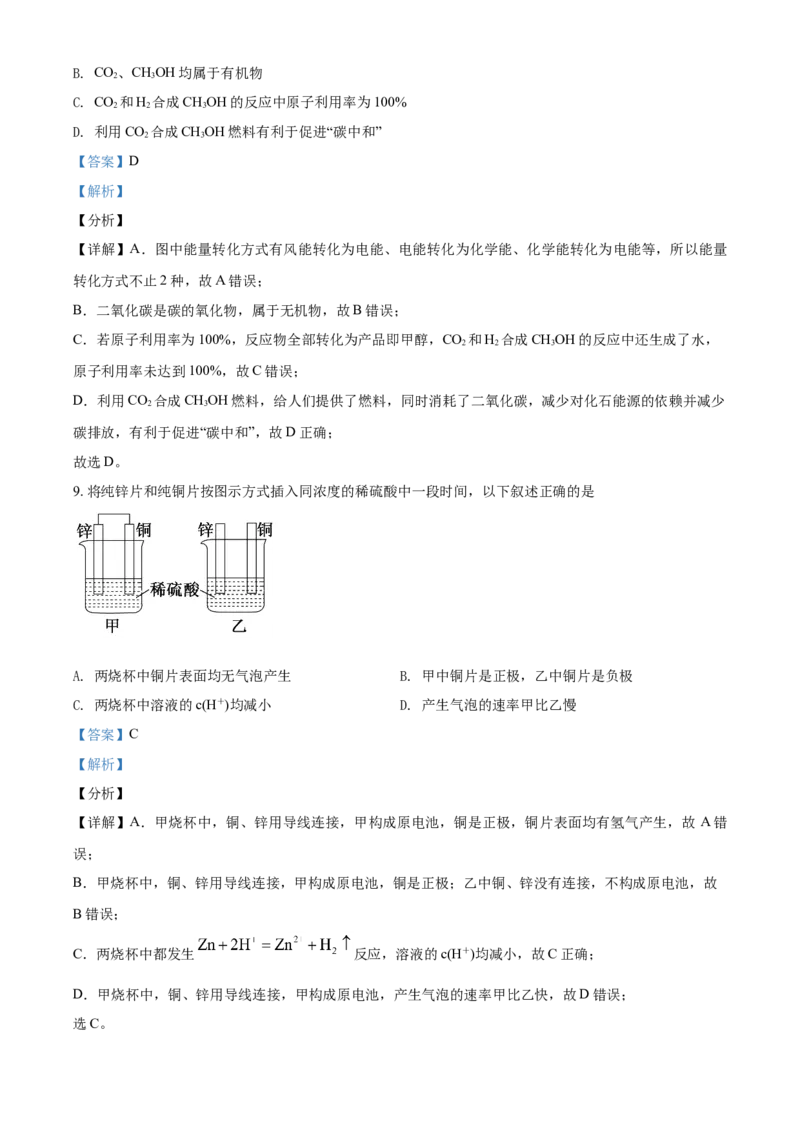
8. 科学家提出有关甲醇(CHOH)的碳循环如图所示。下列说法正确的是(“碳中和”是指CO 的排放总量和减
3 2
少总量相当)
A. 图中能量转化方式只有2种B. CO、CHOH均属于有机物
2 3
C. CO 和H 合成CHOH的反应中原子利用率为100%
2 2 3
D. 利用CO 合成CHOH燃料有利于促进“碳中和”
2 3
【答案】D
【解析】
【分析】
【详解】A.图中能量转化方式有风能转化为电能、电能转化为化学能、化学能转化为电能等,所以能量
转化方式不止2种,故A错误;
B.二氧化碳是碳的氧化物,属于无机物,故B错误;
C.若原子利用率为100%,反应物全部转化为产品即甲醇,CO 和H 合成CHOH的反应中还生成了水,
2 2 3
原子利用率未达到100%,故C错误;
D.利用CO 合成CHOH燃料,给人们提供了燃料,同时消耗了二氧化碳,减少对化石能源的依赖并减少
2 3
碳排放,有利于促进“碳中和”,故D正确;
故选D。
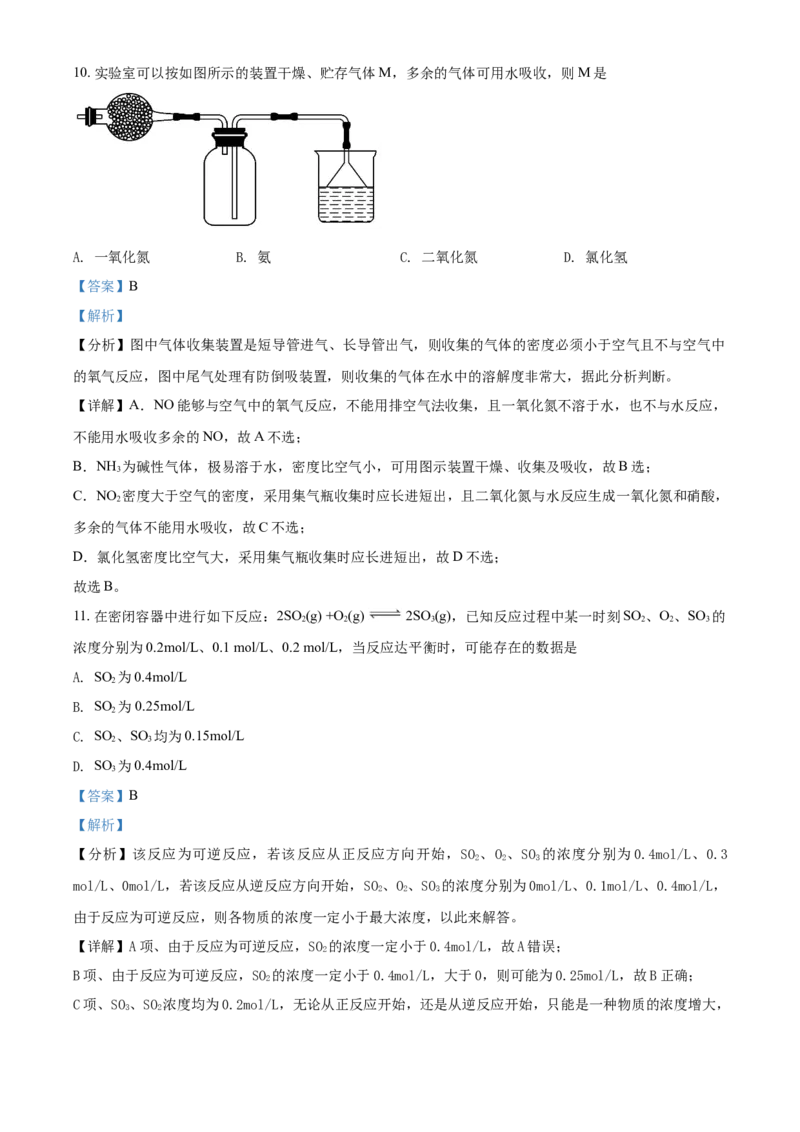
9. 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A. 两烧杯中铜片表面均无气泡产生 B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的c(H+)均减小 D. 产生气泡的速率甲比乙慢
【答案】C
【解析】
【分析】
【详解】A.甲烧杯中,铜、锌用导线连接,甲构成原电池,铜是正极,铜片表面均有氢气产生,故 A错
误;
B.甲烧杯中,铜、锌用导线连接,甲构成原电池,铜是正极;乙中铜、锌没有连接,不构成原电池,故
B错误;
C.两烧杯中都发生 反应,溶液的c(H+)均减小,故C正确;
D.甲烧杯中,铜、锌用导线连接,甲构成原电池,产生气泡的速率甲比乙快,故D错误;
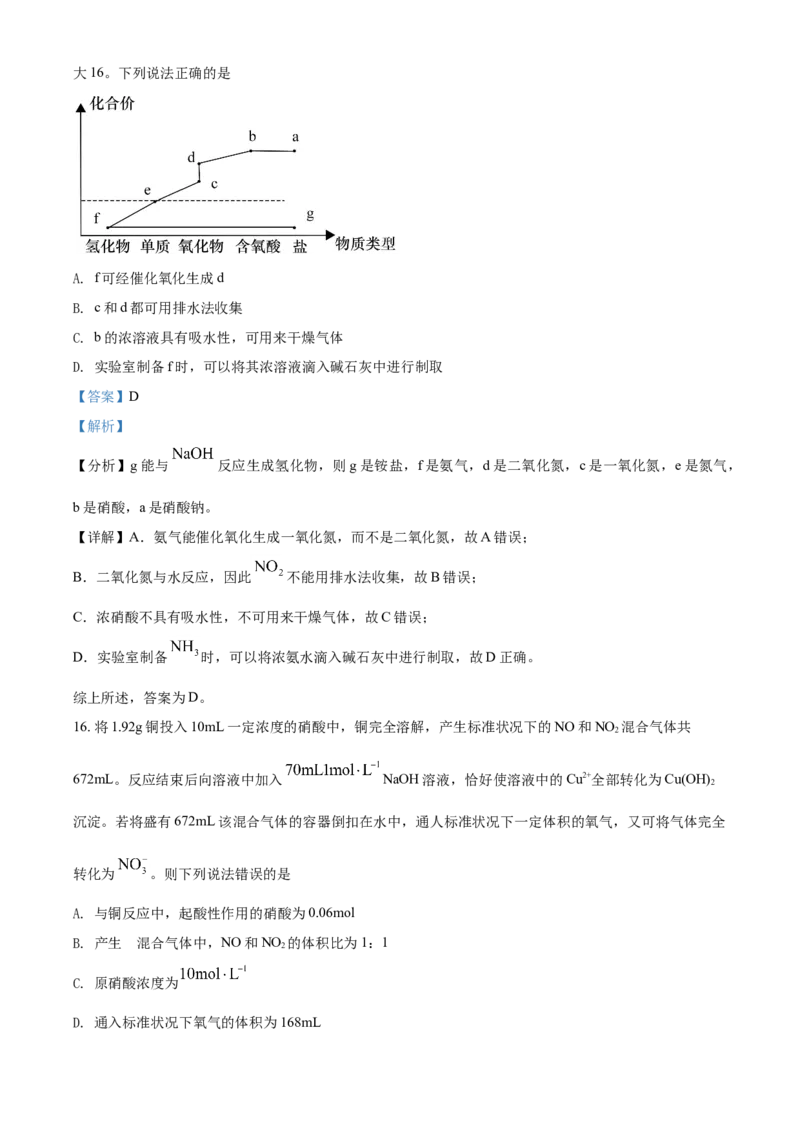
选C。10. 实验室可以按如图所示的装置干燥、贮存气体M,多余的气体可用水吸收,则M是
A. 一氧化氮 B. 氨 C. 二氧化氮 D. 氯化氢
【答案】B
【解析】
【分析】图中气体收集装置是短导管进气、长导管出气,则收集的气体的密度必须小于空气且不与空气中
的氧气反应,图中尾气处理有防倒吸装置,则收集的气体在水中的溶解度非常大,据此分析判断。
【详解】A.NO能够与空气中的氧气反应,不能用排空气法收集,且一氧化氮不溶于水,也不与水反应,
不能用水吸收多余的NO,故A不选;
B.NH 为碱性气体,极易溶于水,密度比空气小,可用图示装置干燥、收集及吸收,故B选;
3
C.NO 密度大于空气的密度,采用集气瓶收集时应长进短出,且二氧化氮与水反应生成一氧化氮和硝酸,
2
多余的气体不能用水吸收,故C不选;
D.氯化氢密度比空气大,采用集气瓶收集时应长进短出,故D不选;
故选B。
11. 在密闭容器中进行如下反应:2SO (g) +O (g) 2SO(g),已知反应过程中某一时刻SO 、O、SO 的
2 2 3 2 2 3
浓度分别为0.2mol/L、0.1 mol/L、0.2 mol/L,当反应达平衡时,可能存在的数据是
A. SO 为0.4mol/L
2
B. SO 为 0.25mol/L
2
C. SO 、SO 均为0.15mol/L
2 3
D. SO 为0.4mol/L
3
【答案】B
【解析】
【分析】该反应为可逆反应,若该反应从正反应方向开始,SO 、O 、SO 的浓度分别为0.4mol/L、0.3
2 2 3
mol/L、0mol/L,若该反应从逆反应方向开始,SO 、O 、SO 的浓度分别为0mol/L、0.1mol/L、0.4mol/L,
2 2 3
由于反应为可逆反应,则各物质的浓度一定小于最大浓度,以此来解答。
【详解】A项、由于反应为可逆反应,SO 的浓度一定小于0.4mol/L,故A错误;
2
B项、由于反应为可逆反应,SO 的浓度一定小于0.4mol/L,大于0,则可能为0.25mol/L,故B正确;
2
C项、SO、SO 浓度均为0.2mol/L,无论从正反应开始,还是从逆反应开始,只能是一种物质的浓度增大,
3 2另一种物质的浓度减小,SO、SO 浓度不会均为0.15mol/L,故C错误;
3 2
D项、由于反应为可逆反应,SO 的浓度一定小于0.4mol/L,故D错误。
3
故选B。
【点睛】本题考查可逆反应,注意可逆反应的特点为不完全转化性,学会利用极限转化的思想来分析物质
的最大浓度,但实际浓度一定小于最大浓度是解答关键。
12. 微型纽扣电池在现代生活中有广泛应用。一种银锌纽扣电池的电极分别为Ag O和Zn,电解质溶液为
2
KOH,电极反应为Zn+2OH—2e-=ZnO+H O和Ag O+HO+2e-=2Ag+2OH-。下列说法错误的是
2 2 2
A. 在使用过程中,电池负极区溶液的碱性减弱
B. 使用过程中,电子由Zn极经外电路流向Ag O极
2
C. 电池总反应为Ag O+Zn=2Ag+ZnO
2
D. Zn是负极发生还原反应,Ag O是正极发生氧化反应
2
【答案】D
【解析】
【分析】
【详解】A.根据电极反应式知,锌作负极,氧化银作正极,负极上氢氧根离子参与反应导致氢氧根离子
浓度减小,负极的碱性减弱,故A正确;
B.锌是负极,氧化银是正极,电子从锌沿导线流向氧化银,故B正确;
C.负极反应为:Zn+2OH—2e-=ZnO+H O,正极反应为:Ag O+HO+2e-=2Ag+2OH-,根据得失电子守恒可
2 2 2
得总反应:Ag O+Zn=2Ag+ZnO,故C正确;
2
D.负极锌失电子发生氧化反应,正极氧化银得电子发生还原反应,故D错误;
故选D。
13. 对于下列实验,描述其反应的离子方程式正确的是
A. 向澄清石灰水中通入少量SO 气体:Ca2++SO+H O=CaSO↓+2H+
2 2 2 3
B. 向氢氧化钠溶液中通入过量SO 气体:SO +OH-=HSO
2 2
C. 向溴水中通入适量SO 气体:SO +Br +H O=2H++2Br-+SO
2 2 2 2
D. 向氢硫酸溶液中通入少量氯气:S2-+Cl=S↓+2Cl-
2
【答案】B
【解析】
【分析】
【详解】A.向澄清石灰水中通入少量SO 气体反应生成亚硫酸钙沉淀和水,离子方程式为:Ca2++2OH-
2
+SO═CaSO ↓+H O,故A错误;
2 3 2B.过量SO 气体通入氢氧化钠溶液中反应生成亚硫酸氢钠,离子方程式为:SO +OH-═HSO ,故B正确;
2 2
C.SO 气体通入溴水中反应生成氢溴酸和硫酸,离子方程式 为:SO +Br +2H O═4H++2Br-+SO ,故C错
2 2 2 2
误;
D.向氢硫酸中通入少量氯气反应生成硫沉淀和盐酸,氢硫酸为弱酸,离子方程式为:HS+Cl ═2H+
2 2
+S↓+2Cl-,故D错误;
故选B。
14. 晶体硅(熔点1410℃)是良好的半导体材料。由石英砂(SiO)制纯硅过程如下:SiO Si(粗)
2 2
SiCl SiCl (纯) Si(纯)。下列叙述错误的是
4 4
A. 生成粗硅的化学方程式为:SiO+C Si +CO↑
2 2
B. 上述流程中的化学反应均为氧化还原反应
C. 气态SiCl 中混有杂质元素的氯化物,提纯的方法是冷凝成液态后蒸馏
4
D. H 还原SiCl 时,生成的两种产物分别为固态和气态,容易分离
2 4
【答案】A
【解析】
【详解】A.SiO 和焦炭在高温下反应生成Si和CO,化学方程式为:SiO+C Si+2CO↑,故A符合题
2 2
意;
B.SiO 转化为粗Si,硅元素的化合价从+4价降低到0价,Si(粗)转化为SiCl ,硅元素的化合价从0价升
2 4
高到+4价,SiCl (纯)转化为Si(纯),硅元素的化合价从+4价降低到0价,上述流程中化合价均有变化,化
4
学反应均为氧化还原反应,故B不符合题意;
C.四氯化硅沸点低,通过冰水装置冷却能使四氯化硅冷却为液体,气态SiCl 中混有杂质元素的氯化物,
4
提纯的方法是冷凝成液态后蒸馏,故C不符合题意;
D.H 还原SiCl 时,生成的两种产物分别为硅和氯化氢,硅为固态,氯化氢为气态,容易分离,故D不符
2 4
合题意;
答案选A。
15. 如图是某元素的化合价——物质类型二维图。其中正盐g与NaOH反应可生成f,d的相对分子质量比c大16。下列说法正确的是
A. f可经催化氧化生成d
B. c和d都可用排水法收集
C. b的浓溶液具有吸水性,可用来干燥气体
D. 实验室制备f时,可以将其浓溶液滴入碱石灰中进行制取
【答案】D
【解析】
【分析】g能与 反应生成氢化物,则g是铵盐,f是氨气,d是二氧化氮,c是一氧化氮,e是氮气,
b是硝酸,a是硝酸钠。
【详解】A.氨气能催化氧化生成一氧化氮,而不是二氧化氮,故A错误;
B.二氧化氮与水反应,因此 不能用排水法收集,故B错误;
C.浓硝酸不具有吸水性,不可用来干燥气体,故C错误;
D.实验室制备 时,可以将浓氨水滴入碱石灰中进行制取,故D正确。
综上所述,答案为D。
16. 将1.92g铜投入10mL一定浓度的硝酸中,铜完全溶解,产生标准状况下的NO和NO 混合气体共
2
672mL。反应结束后向溶液中加入 NaOH溶液,恰好使溶液中的Cu2+全部转化为Cu(OH)
2
沉淀。若将盛有672mL该混合气体的容器倒扣在水中,通人标准状况下一定体积的氧气,又可将气体完全
转化为 。则下列说法错误的是
A. 与铜反应中,起酸性作用的硝酸为0.06mol
B. 产生 的混合气体中,NO和NO 的体积比为1:1
2
C. 原硝酸浓度为
D. 通入标准状况下氧气的体积为168mL【答案】D
【解析】
【分析】
【 详 解 】 A . , 生 成 的 Cu(NO ) 的 物 质 的 量 为 0.03mol 。 将
3 2
0.03molCu(NO ) 全部转化为Cu(OH) 沉淀,只需消耗0.06molNaOH,而实际消耗了0.07molNaOH,这说明
3 2 2
硝酸与铜反应后,过量的 HNO 为 0.01mol。与铜反应中,起酸性作用的硝酸的物质的量
3
,故A正确;
B.根据得失电子守恒可列出方程 ,根据产生标准状况下0.672L的混合
气体的体积可列出方程 ,解得
,故产生的混合气体中,NO和NO 的体积比为1:1,故B正确;
2
C.与铜反应中,起氧化作用的硝酸的物质的量 ,原硝酸溶液中溶质HNO
3
的物质的量
,原硝酸浓
度 ,故C正确;
D.NO和NO 的体积比为1:1的混合气体与氧气和水发生反应的化学方程式为
2
,故通入标准状况下氧气的物质的量为0.015mol,体积为336mL(标
准状况),故D错误;
故答案选D。
二、非选择题:本题共4小题,共56分。
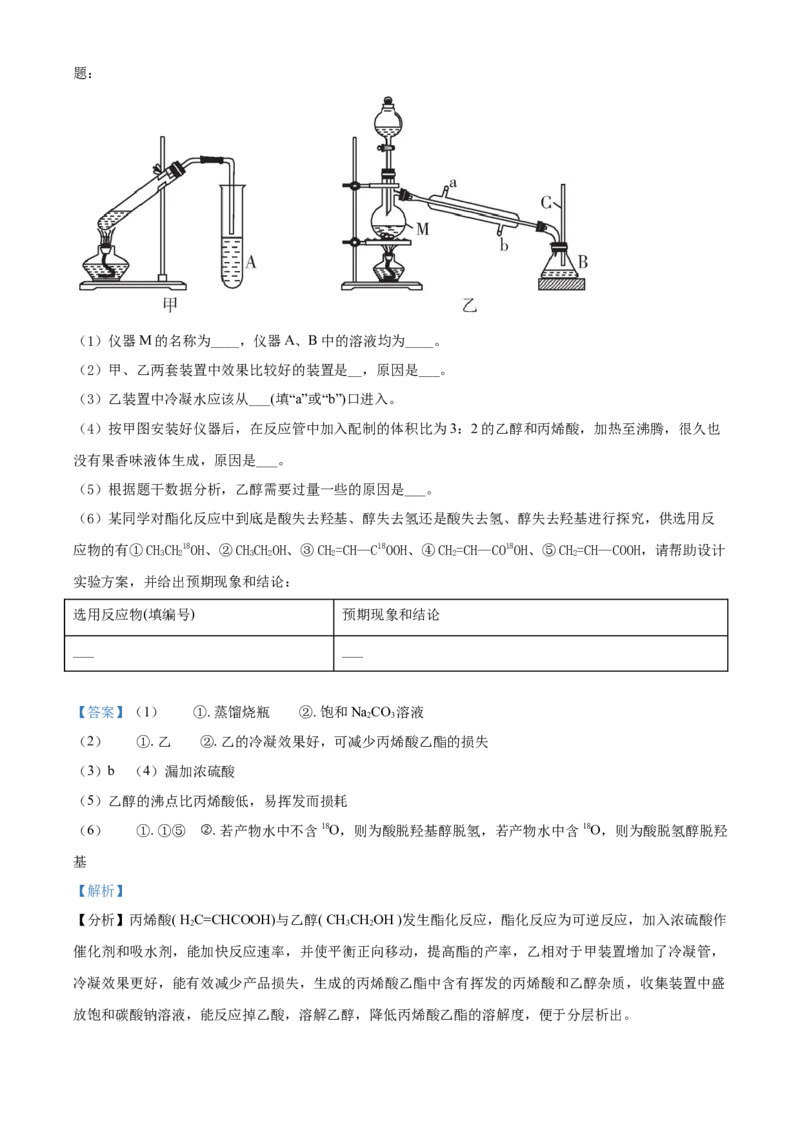
17. 某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸(H C=CHCOOH)与乙醇(CHCHOH)酯化反应
2 3 2
的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃。回答下列问题:
(1)仪器M的名称为____,仪器A、B中的溶液均为____。
(2)甲、乙两套装置中效果比较好的装置是__,原因是___。
(3)乙装置中冷凝水应该从___(填“a”或“b”)口进入。
(4)按甲图安装好仪器后,在反应管中加入配制的体积比为3:2的乙醇和丙烯酸,加热至沸腾,很久也
没有果香味液体生成,原因是___。
(5)根据题干数据分析,乙醇需要过量一些的原因是___。
(6)某同学对酯化反应中到底是酸失去羟基、醇失去氢还是酸失去氢、醇失去羟基进行探究,供选用反
应物的有①CHCH18OH、②CHCHOH、③CH=CH—C18OOH、④CH=CH—CO18OH、⑤CH=CH—COOH,请帮助设计
3 2 3 2 2 2 2
实验方案,并给出预期现象和结论:
选用反应物(填编号) 预期现象和结论
___ ___
【答案】(1) ①. 蒸馏烧瓶 ②. 饱和NaCO 溶液
2 3
(2) ①. 乙 ②. 乙的冷凝效果好,可减少丙烯酸乙酯的损失
(3)b (4)漏加浓硫酸
(5)乙醇的沸点比丙烯酸低,易挥发而损耗
(6) ①. ①⑤ ②. 若产物水中不含18O,则为酸脱羟基醇脱氢,若产物水中含18O,则为酸脱氢醇脱羟
基
【解析】
【分析】丙烯酸( H C=CHCOOH)与乙醇( CH CHOH )发生酯化反应,酯化反应为可逆反应,加入浓硫酸作
2 3 2
催化剂和吸水剂,能加快反应速率,并使平衡正向移动,提高酯的产率,乙相对于甲装置增加了冷凝管,
冷凝效果更好,能有效减少产品损失,生成的丙烯酸乙酯中含有挥发的丙烯酸和乙醇杂质,收集装置中盛
放饱和碳酸钠溶液,能反应掉乙酸,溶解乙醇,降低丙烯酸乙酯的溶解度,便于分层析出。【小问1详解】
由图可知,仪器M蒸馏烧瓶,仪器A、B均为收集装置,盛放饱和碳酸钠溶液,能反应掉乙酸,溶解乙醇,
降低丙烯酸乙酯的溶解度,便于分层析出;
【小问2详解】
乙相对于甲装置增加了冷凝管,冷凝效果更好,能有效减少产品损失;
【小问3详解】
冷凝管中冷凝水应该从下口进上口出,保证冷凝管内始终充满水;
【小问4详解】
酯化反应中需添加浓硫酸作催化剂和吸水剂,加快反应速率并提高酯的产率;
【小问5详解】
已知乙醇的沸点为78.5°C,丙烯酸的沸点为141°C,乙醇的沸点比丙烯酸低,易挥发而损失;
【小问6详解】
根据题意醇酸反应生成酯和水,利用18O示踪原子法来判断出到底是:酸失去羟基、醇失去氢还是酸失去
氢、醇失去羟基,最好18O在一种产物中出现易判断,故选择①CHCH18OH和⑤CH=CH—COOH,若产
3 2 2
物水中不含18O,则为酸脱羟基醇脱氢,若产物水中含18O,则为酸脱氢醇脱羟基。
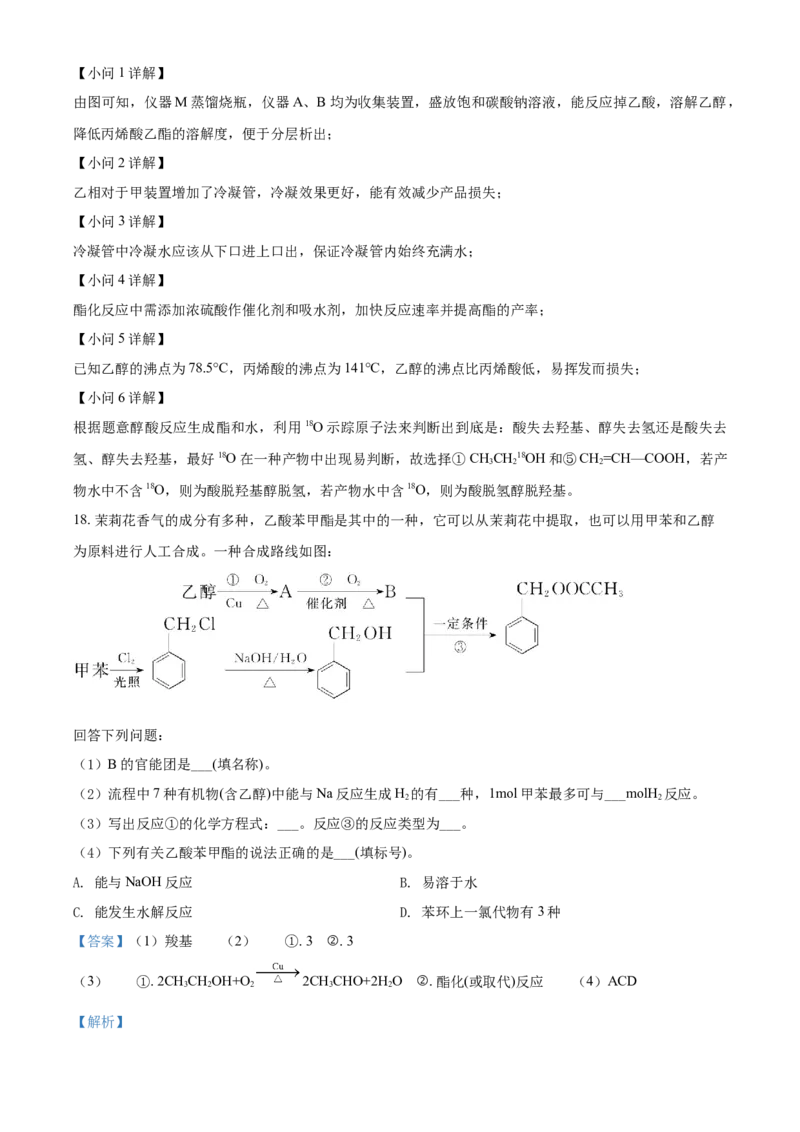
18. 茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇
为原料进行人工合成。一种合成路线如图:
回答下列问题:
(1)B的官能团是___(填名称)。
(2)流程中7种有机物(含乙醇)中能与Na反应生成H 的有___种,1mol甲苯最多可与___molH 反应。
2 2
(3)写出反应①的化学方程式:___。反应③的反应类型为___。
(4)下列有关乙酸苯甲酯的说法正确的是___(填标号)。
A. 能与NaOH反应 B. 易溶于水
C. 能发生水解反应 D. 苯环上一氯代物有3种
【答案】(1)羧基 (2) ①. 3 ②. 3
(3) ①. 2CHCHOH+O 2CHCHO+2H O ②. 酯化(或取代)反应 (4)ACD
3 2 2 3 2
【解析】【分析】乙醇在Cu催化作用下加热反应生成CHCHO(A),CHCHO继续被氧化为CHCOOH(B),甲苯和
3 3 3
氯气在光照条件下发出侧链取代生成 , 在碱性条件下水解生成 ;在一定条件下
与CHCOOH发生酯化反应生成 ,据此分析解答。
3
【小问1详解】
由以上分析可知,B为乙酸,乙酸中的官能团为羧基,故答案为:羧基;
【小问2详解】
流程中的7种有机物(含乙醇)中能与Na反应生成H 的有乙醇、乙酸、苯甲醇,共3种;甲苯分子中只有苯
2
环能够与氢气发生加成反应,因此1mol甲苯最多可与3molH 反应,故答案为:3;3;
2
【小问3详解】
反应①为乙醇在铜催化作用下发生氧化反应生成乙醛,反应的化学方程式为 2CHCHOH+O
3 2 2
2CHCHO+2H O;根据上面的分析可知,反应③为酯化(取代)反应,故答案为:2CHCHOH+O
3 2 3 2 2
2CHCHO+2H O;取代反应(或酯化反应);
3 2
【小问4详解】
A.乙酸苯甲酯中含有酯基,能与NaOH发生取代反应,故A正确;
B.乙酸苯甲酯属于酯类,难溶于水,故B错误;
C.乙酸苯甲酯中含有酯基,能与NaOH溶液中发生水解反应,故C正确;
D.乙酸苯甲酯 的苯环上有3种H原子,一氯代物有3种,故D正确;
故答案为ACD。
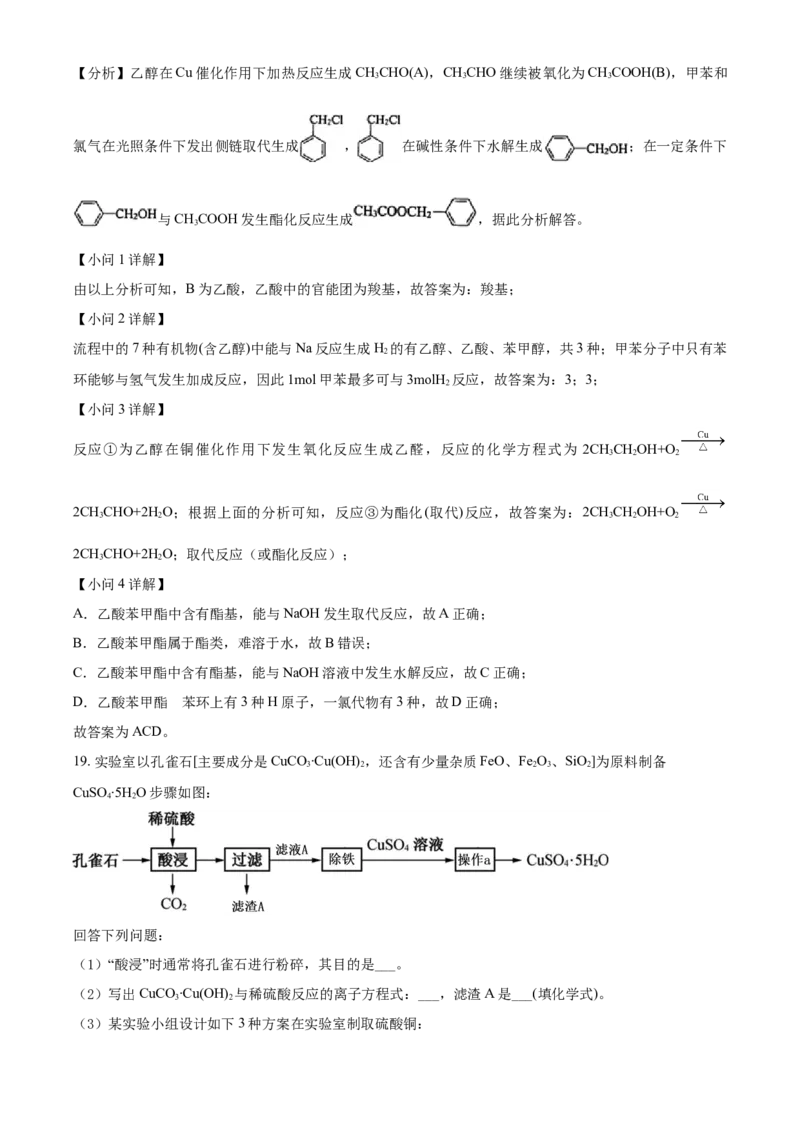
19. 实验室以孔雀石[主要成分是CuCO∙Cu(OH) ,还含有少量杂质FeO、Fe O、SiO]为原料制备
3 2 2 3 2
CuSO ∙5H O步骤如图:
4 2
回答下列问题:
(1)“酸浸”时通常将孔雀石进行粉碎,其目的是___。
(2)写出CuCO∙Cu(OH) 与稀硫酸反应的离子方程式:___,滤渣A是___(填化学式)。
3 2
(3)某实验小组设计如下3种方案在实验室制取硫酸铜:方案一:浓硫酸与铜加热反应
方案二:铜加入稀硝酸和稀硫酸的混合酸中
方案三:铜粉与稀硫酸的混合物中通入热空气反应
其中,最佳方案是___(填编号),理由是___。
(4)由CuSO 溶液获得CuSO ∙5H O的操作a包括___、___、过滤、洗涤、干燥等步骤。
4 4 2
【答案】(1)加快溶解速率
(2) ①. CuCO∙Cu(OH) +4H+=2Cu2++3H O+CO↑ ②. SiO
3 2 2 2 2
(3) ①. 方案三 ②. 方案一和方案二均产生有害气体,酸的利用率也不高
(4) ①. 蒸发浓缩 ②. 冷却结晶
【解析】
【分析】孔雀石主要成份是CuCO∙Cu(OH) ,还含有少量杂质FeO、Fe O 、SiO],向孔雀石中加稀硫酸反
3 2 2 3 2
应生成二氧化碳、硫酸铜、硫酸亚铁、硫酸铁,二氧化硅不反应,过滤得到滤渣二氧化硅、将滤液中铁除
掉后,将硫酸铜溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,最终得到CuSO ∙5H O;
4 2
【小问1详解】
“酸浸”时通常将孔雀石进行粉碎,其目的是增加接触面积,使反应更充分,加快溶解速率;故答案为:加
快溶解速率;
【小问2详解】
CuCO∙Cu(OH) 与稀硫酸反应生成硫酸铜、二氧化碳和水,其离子方程式:CuCO∙Cu(OH) +4H+=2Cu2++
3 2 3 2
3HO+CO↑,滤渣A是SiO;故答案为:CuCO∙Cu(OH) +4H+=2Cu2++3HO+CO↑;SiO;
2 2 2 3 2 2 2 2
【小问3详解】
方案一:浓硫酸与铜加热反应,会生成污染性的气体且消耗的原料多;
方案二:铜加入稀硝酸和稀硫酸的混合酸中,会生成污染性气体氮氧化物;
方案三:铜粉与稀硫酸的混合物中通入热空气反应,不产生污染性气体,且消耗的硫酸量较少,因此,最
佳方案是方案三,理由是方案一和方案二均产生有害气体,酸的利用率也不高;
故答案为:方案三;方案一和方案二均产生有害气体,酸的利用率也不高。
【小问4详解】
由CuSO 溶液获得CuSO ∙5H O的操作a包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤;故答案为:
4 4 2
蒸发浓缩、冷却结晶。
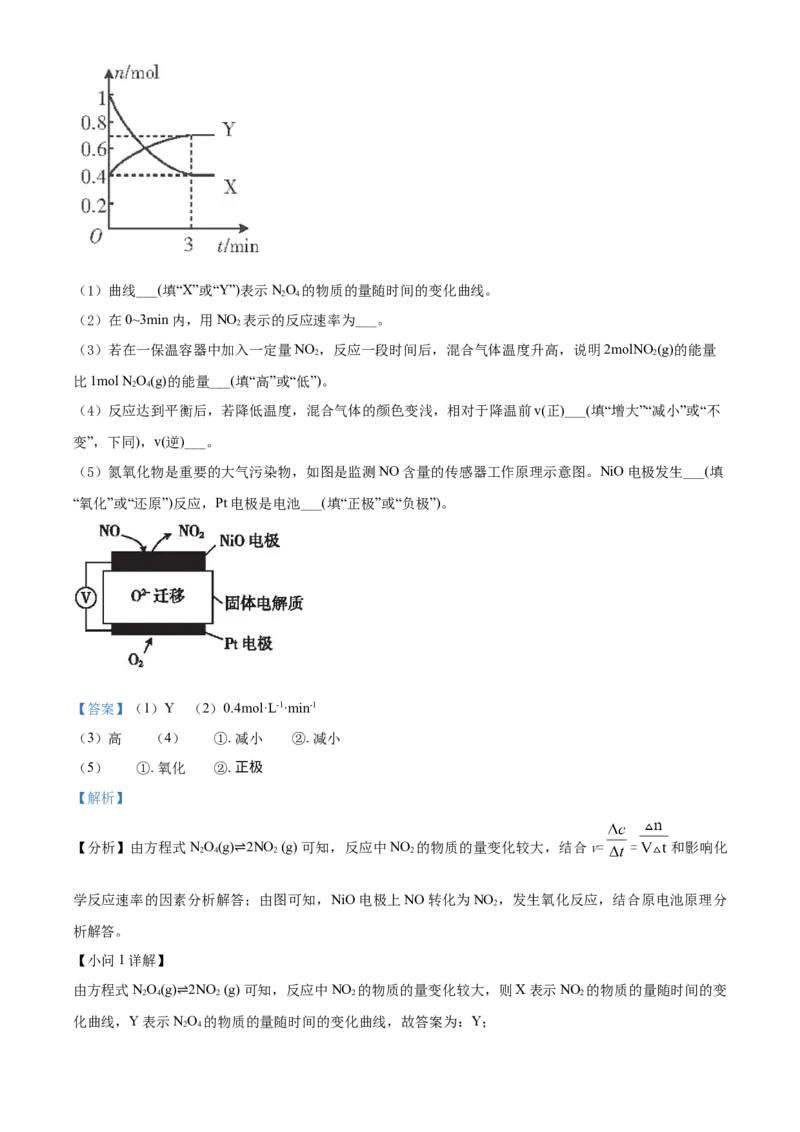
20. 一定温度下,在体积为0.5L的恒容密闭容器中,NO 和NO 之间发生反应:2NO (g)(红棕色)
2 2 4 2
NO(g)(无色),反应过程中各物质的物质的量与时间的关系如图所示。回答下列问题:
2 4(1)曲线___(填“X”或“Y”)表示NO 的物质的量随时间的变化曲线。
2 4
(2)在0~3min内,用NO 表示的反应速率为___。
2
(3)若在一保温容器中加入一定量NO ,反应一段时间后,混合气体温度升高,说明2molNO (g)的能量
2 2
比1mol NO(g)的能量___(填“高”或“低”)。
2 4
(4)反应达到平衡后,若降低温度,混合气体的颜色变浅,相对于降温前v(正)___(填“增大”“减小”或“不
变”,下同),v(逆)___。
(5)氮氧化物是重要的大气污染物,如图是监测NO含量的传感器工作原理示意图。NiO电极发生___(填
“氧化”或“还原”)反应,Pt电极是电池___(填“正极”或“负极”)。
【答案】(1)Y (2)0.4mol·L-1·min-1
(3)高 (4) ①. 减小 ②. 减小
(5) ①. 氧化 ②. 正极
【解析】
【分析】由方程式NO(g) 2NO (g) 可知,反应中NO 的物质的量变化较大,结合v= = 和影响化
2 4 2 2
⇌
学反应速率的因素分析解答;由图可知,NiO电极上NO转化为NO ,发生氧化反应,结合原电池原理分
2
析解答。
【小问1详解】
由方程式NO(g) 2NO (g) 可知,反应中NO 的物质的量变化较大,则X表示NO 的物质的量随时间的变
2 4 2 2 2
化曲线,Y表示N⇌O 的物质的量随时间的变化曲线,故答案为:Y;
2 4【小问2详解】
X为NO 的变化曲线,在 0~3min内变化0.6mol,则v= =0.4 mol/(L•min),故答案为:0.4 mol/
2
(L•min);
【小问3详解】
若在一保温容器中加入一定量NO ,反应一段时间后,混合气体温度升高,说明该反应为放热反应,说明
2
2molNO (g)的能量比1mol NO(g)的能量高,故答案为:高;
2 2 4
【小问4详解】
反应达到平衡后,若降低温度,混合气体的颜色变浅,说明平衡正向移动,降低温度,反应速率减慢,相
对于降温前v(正)、v(逆)均减小,故答案为:减小;减小;
【小问5详解】
根据图示,NiO电极上NO转化为NO ,发生氧化反应,为负极,Pt电极为正极,故答案为:氧化;正极。
2