文档内容
南阳一中 2021 年秋期高一年级第二次月考
化学试题
需要用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Fe-56 Ba-137
第I卷(选择题)
一、选择题(本题16小题,每题3分,共48分,每小题只有一个选项符合题意)
1. N 为阿伏加德罗常数的数值,下列说法中正确的是:
A
①0.5molO 与11.2LO 所含的分子数一定相等
3 2
②24g金属镁变为镁离子时失去的电子数为N
A
③通常状况下,N 个CO 分子占有的体积为22.4L
A 2
④常温常压下,92g的NO 和NO 混合气体含有的原子数为6N
2 2 4 A
⑤常温下,4.4gCO 和NO(不反应)混合物中所含有的原子数为0.3N
2 2 A
⑥1.8gH O所含的质子数目为N
2 A
⑦标准状况下,22.4LSO 含有的分子数为N
3 A
⑧在常温常压下,1molO 含有的原子数为2N
2 A
为
⑨0.5molMgCl 溶液中,含有Cl-个数 0.5N
2 A
⑩将含有0.1molFeCl 的氯化铁溶液滴入沸水中可制得Fe(OH) 胶粒数目为0.01N
3 3 A
A. ①②④⑧ B. ④⑤⑥⑧ C. ③⑥⑨⑩ D. ④⑤⑧⑨
2. 一定温度下,某物质在水中的溶解度为S,计算该温度下这种饱和溶液中溶质的物质的量浓度,必不可
少的物理量是( )
①溶液中溶质的摩尔质量 ②溶液中溶质和溶剂的质量比 ③溶液的密度 ④溶液的体积
A. ①② B. ②③ C. ①③ D. ②④
3. 下表中对离子方程式的评价不合理的是
选
化学反应及其离子方程式 评价
项
HSO 溶液与Ba(OH) 溶液反应:2H++SO +2OH-
A 2 4 2 正确
+Ba2+=BaSO ↓+2H O
4 2
错误,碳酸镁不应写成离子
B 向碳酸镁浊液中加入足量稀盐酸:CO +2H+=CO ↑+H O
2 2 形式
向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3+
C 正确
+3H O=Fe(OH) ↓
2 3D 向NaOH溶液中加入CuCl 溶液:2OH-+Cu2+=Cu(OH) ↓ 正确
2 2
A. A B. B C. C D. D
4. VLFe (SO ) 溶液中含有ag ,取此溶液0.5VL,用水稀释至2VL,则稀释后的溶液中Fe3+的物质的
2 4 3
量浓度为
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
5. 在同温同压下,ag气体A与bg气体B的分子数相同,下列说法中不正确的是
A. A与B两种气体的相对分子质量之比为a:b
B. 在同温同压下,等质量的A与B两种气体的体积之比为a:b
的
C. 同质量 A、B两种气体的分子个数之比为b:a
D. 在同温同压下,A气体与B气体的密度之比为a:b
的
6. 下列说法正确 是
①胶体产生丁达尔效应是由胶粒直径大小决定的
②胶体与溶液的分离可用渗析的方法
③胶体都是均匀、透明的液体
④江河入海口处形成沙洲与胶体的性质有关
⑤胶体不稳定,静置后容易产生沉淀
⑥水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
A. ①②③④ B. ①②④⑥ C. ①③④⑥ D. ②③④⑥
7. 标准状况下,现有①6.72 L CH ②3.01×1023个HCl分子 ③13.6 g H S ④0.2 molNH ,对这四种气体的关
4 2 3
系有以下四种表述,其中不正确的是
A. 体积:②>③>①>④ B. 物质的量:②>③>④>①
C. 质量:②>③>①>④ D. 氢原子个数:①>③>④>②
8. 把V L含有Fe (SO ) 和KSO 的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使铁离子
2 4 3 2 4
完全沉淀为氢氧化铁;另一份加入含b mol BaCl 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合
2
溶液中钾离子的浓度为A. (b-a)/V mol·L-1 B. (2b-a)/V mol·L-1
C. 2(2b-a)/V mol·L-1 D. 2(b-a)/V mol·L-1
9. 在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中共存的是( )
A. 含有大量SO 的溶液:加入Mg2+、Cu2+、Cl-、NO
B. 滴加酚酞变红的溶液:加入SO 、Cu2+、K+、
C. 所含溶质为NaHSO 的溶液:加入K+、CO 、NO 、Na+
4
D. 常温下,加入铁粉能生成H 的溶液:加入Na+、Ca2+、Cl-、HCO
2
10. 下列指定反应的离子方程式正确的是
A. 向硫酸铁溶液中加入铜粉:Fe3++Cu=Fe2++Cu2+
B. CHCOOH溶液除去水垢中的CaCO ∶CaCO +2H+=Ca2++H O+CO↑
3 3 3 2 2
C. Fe(OH) 溶于过量稀盐酸:Fe(OH) +3H+=Fe3++3H O
3 3 2
D. 将NaHSO 与Ba(OH) 溶液混合至中性:H++SO +Ba2++OH-=BaSO ↓+H O
4 2 4 2
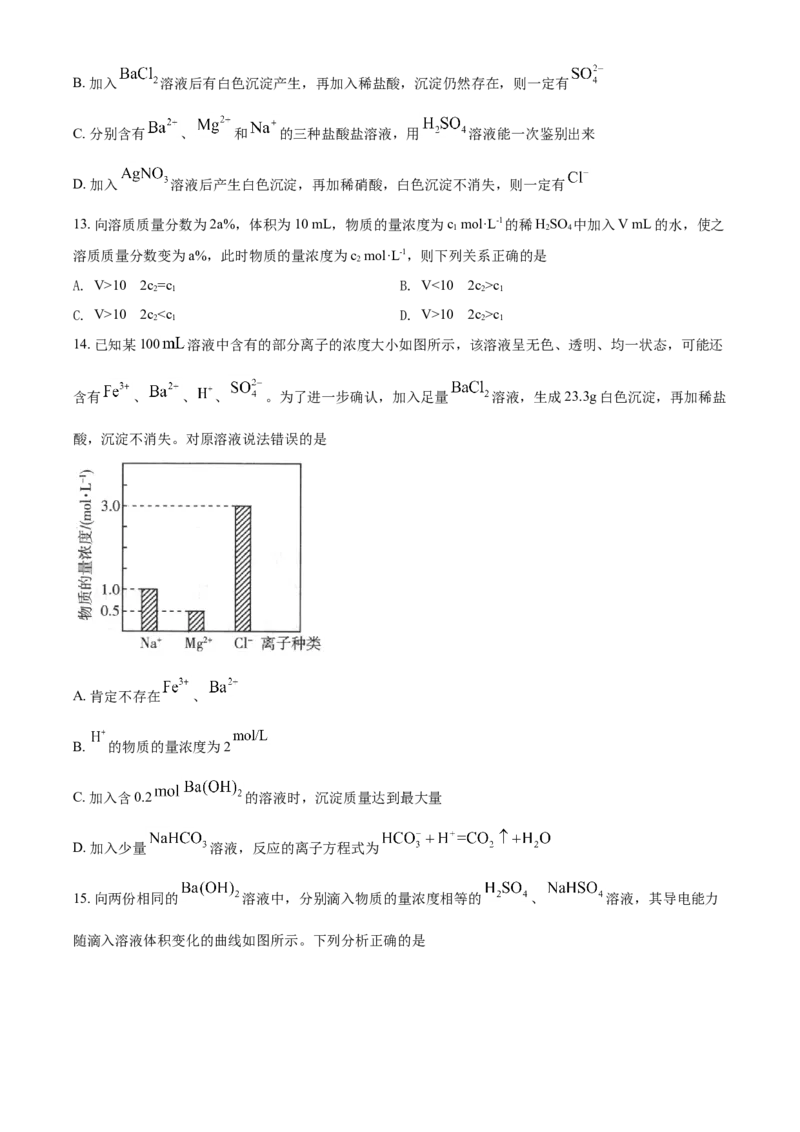
11. 海水晒盐可以得到粗盐,粗盐中含有泥沙等不溶性杂质。可能含MgCl 、CaCl 和NaSO 等可溶性杂质,
2 2 2 4
某同学设计如图实验方案提纯粗盐,同时验证可溶性杂质是否存在。对该过程 的认识中,正确的是
A. 操作I中需要进行搅拌,目的是提高氯化钠的溶解度
B. 操作Ⅱ和操作Ⅲ顺序可以互换
C. 沉淀b中共有三种物质
D. 操作IV中加入盐酸的目的是除去过量的OH-和CO
12. 下列对于某些离子的检验及结论正确的是
A. 加入稀盐酸产生气体,将该气体通入澄清石灰水中,溶液变浑浊,则一定有B. 加入 溶液后有白色沉淀产生,再加入稀盐酸,沉淀仍然存在,则一定有
C. 分别含有 、 和 的三种盐酸盐溶液,用 溶液能一次鉴别出来
D. 加入 溶液后产生白色沉淀,再加稀硝酸,白色沉淀不消失,则一定有
13. 向溶质质量分数为2a%,体积为10 mL,物质的量浓度为c mol·L-1的稀HSO 中加入V mL的水,使之
1 2 4
溶质质量分数变为a%,此时物质的量浓度为c mol·L-1,则下列关系正确的是
2
A. V>10 2c=c B. V<10 2c>c
2 1 2 1
C. V>10 2c10 2c>c
2 1 2 1
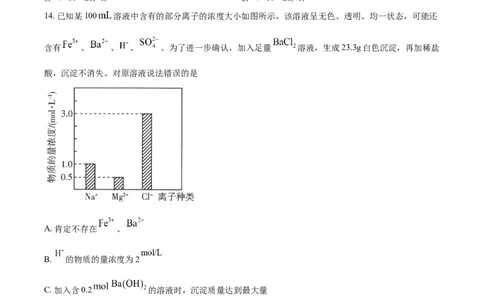
14. 已知某100 溶液中含有的部分离子的浓度大小如图所示,该溶液呈无色、透明、均一状态,可能还
含有 、 、 、 。为了进一步确认,加入足量 溶液,生成23.3g白色沉淀,再加稀盐
酸,沉淀不消失。对原溶液说法错误的是
A. 肯定不存在 、
B. 的物质的量浓度为2
C. 加入含0.2 的溶液时,沉淀质量达到最大量
D. 加入少量 溶液,反应的离子方程式为
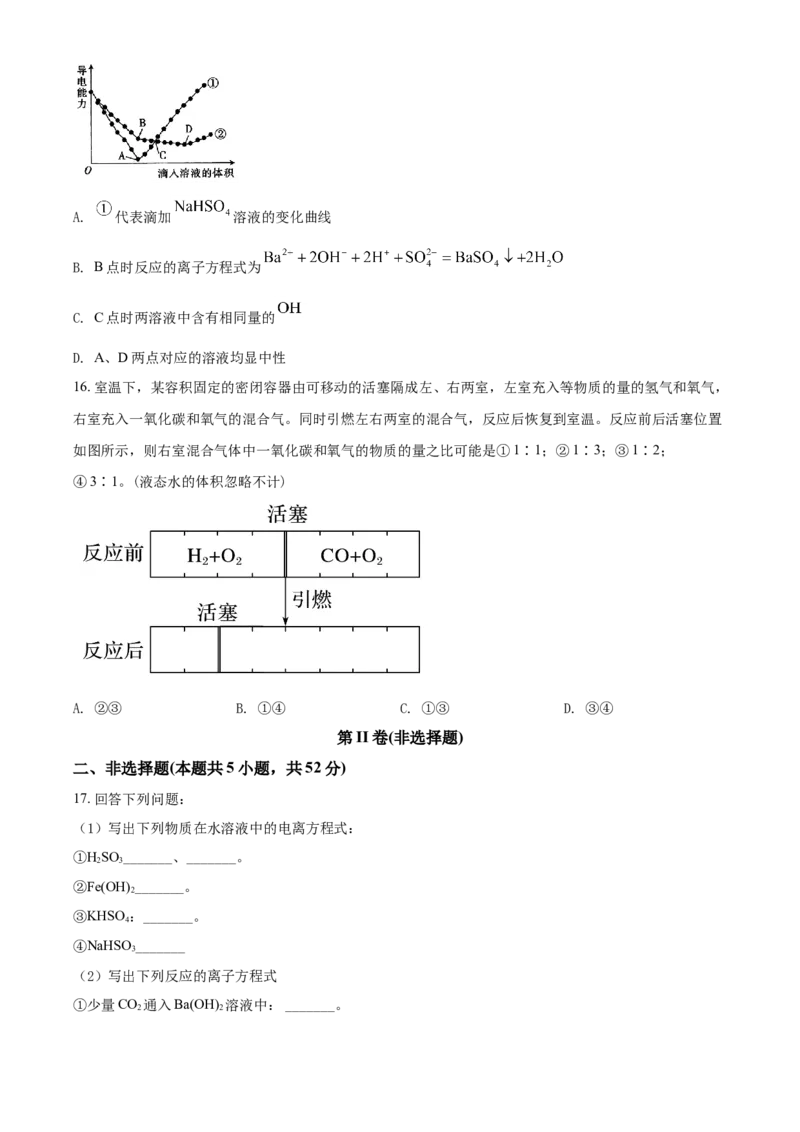
15. 向两份相同的 溶液中,分别滴入物质的量浓度相等的 、 溶液,其导电能力
随滴入溶液体积变化的曲线如图所示。下列分析正确的是A. 代表滴加 溶液的变化曲线
B. B点时反应的离子方程式为
C. C点时两溶液中含有相同量的
D. A、D两点对应的溶液均显中性
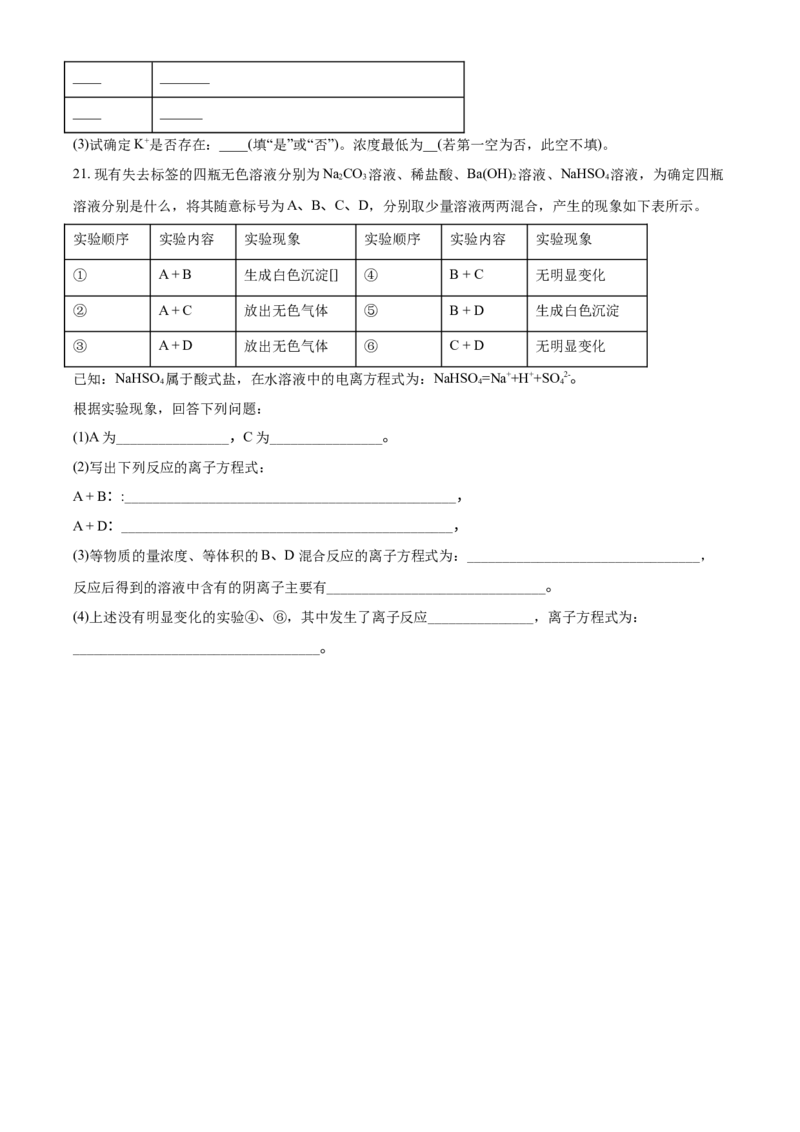
16. 室温下,某容积固定的密闭容器由可移动的活塞隔成左、右两室,左室充入等物质的量的氢气和氧气,
右室充入一氧化碳和氧气的混合气。同时引燃左右两室的混合气,反应后恢复到室温。反应前后活塞位置
如图所示,则右室混合气体中一氧化碳和氧气的物质的量之比可能是①1∶1;②1∶3;③1∶2;
④3∶1。(液态水的体积忽略不计)
A. ②③ B. ①④ C. ①③ D. ③④
第II卷(非选择题)
二、非选择题(本题共5小题,共52分)
17. 回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
①HSO _______、_______。
2 3
②Fe(OH) _______。
2
③KHSO:_______。
4
④NaHSO_______
3
(2)写出下列反应的离子方程式
①少量CO 通入Ba(OH) 溶液中: _______。
2 2②NH HCO 溶液与少量NaOH溶液反应:_______。
4 3
③醋酸溶液与碳酸钙反应:_______。
④NaHCO 溶液与少量氢氧化钙溶液反应:_______
3
(3)用一种试剂除去下列各物质中的杂质(括号内的物质),写出所用的试剂及反应的离子方程式或除杂方
法。
①BaCl (HCl):试剂_______,离子方程式_______。
2
②CO(HCl):试剂_______,除杂方法_______。
2
18. 现有12种物质:①Al ②稀硝酸 ③HNO ④液氨⑤CO ⑥空气 ⑦NaCl ⑧CaCO
3 2 3
⑨NaHCO
3
⑩乙醇 ⑪Al
2
O
3
⑫石墨
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 混合物 ___________
(2) 电解质,但熔融状态下并不导电 ___________
(3) 电解质,熔融状态能导电 ___________
(4) 电解质,但难溶于水 ___________
(5) 非电解质 ___________
(6) 既不是电解质,也不是非电解质,但本身能导电 ___________
19. 如下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)该浓盐酸的物质的量浓度为___________mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生现需450 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取___________ mL上述浓盐酸进行配制。
②配制时正确的操作顺序是(用字母表示)________;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中, 用玻璃棒
慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
的
③在配制过程中,下列实验操作对所配制 稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影
响”)。
I、用量筒量取浓盐酸时俯视观察凹液面____________;
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶_________;
III、溶液注入容量瓶前没有恢复到室温就进行定容____________。
(4)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度
为________mol/L。(填字母)(2分)
(5)现将100mL 0.5mol/L的盐酸与200mL 0.1mol/LCuCl 溶液混合,体积变化忽略不计,所得溶液中Cl-
2
的物质的量浓度是_________________。
20. 由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、 、Mg2+、Ba2+、 、
。将该混合物溶于水后得澄清溶液,现取3份各100mL的该溶液分别进行如下实验:
序号 实验内容 实验结果
① 加AgNO 溶液 有白色沉淀生成
3
② 加足量NaOH溶液并加热 收集到气体1.12L(标准状况)
第一次称量读数为6.27g;
加足量BaCl 溶液后,对所得沉淀进行洗涤、干燥、
③ 2
称量;再向沉淀中加足量稀盐酸,然后干燥、称量
第二次称量读数为2.33g
试回答下列问题:
(1)根据实验①对Cl-是否存在的判断是____(填“一定存在”“一定不存在”或“不能确定”),根据实验①②③判
断混合物中一定不存在的离子是____。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
阴离子符号 物质的量浓度/(mol·L-1)____ _______
____ ______
(3)试确定K+是否存在:____(填“是”或“否”)。浓度最低为__(若第一空为否,此空不填)。
21. 现有失去标签的四瓶无色溶液分别为NaCO 溶液、稀盐酸、Ba(OH) 溶液、NaHSO 溶液,为确定四瓶
2 3 2 4
溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
实验顺序 实验内容 实验现象 实验顺序 实验内容 实验现象
① A + B 生成白色沉淀[] ④ B + C 无明显变化
② A + C 放出无色气体 ⑤ B + D 生成白色沉淀
③ A + D 放出无色气体 ⑥ C + D 无明显变化
已知:NaHSO 属于酸式盐,在水溶液中的电离方程式为:NaHSO=Na++H++SO2-。
4 4 4
根据实验现象,回答下列问题:
(1)A为________________,C为________________。
(2)写出下列反应的离子方程式:
A + B::_______________________________________________,
A + D:_______________________________________________,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为:_________________________________,
反应后得到的溶液中含有的阴离子主要有_______________________________。
(4)上述没有明显变化的实验④、⑥,其中发生了离子反应_______________,离子方程式为:
___________________________________。