文档内容
电子式的书写及分子间作用力
【学习目标】
1、掌握离子化合物、共价分子电子式的书写
2、掌握范德华力及氢键对物质性质的影响
【主干知识梳理】
一、电子式的概念及书写技巧
1、电子式的概念:在元素符号周围用“·”或“×”来表示原子的最外层电子(价电子)的式子
【微点拨】元素符号周围标明元素原子的最外层电子,每个方向不能超过2个电子。当最外层电子数小于或等
于4时以单电子分布,多于4时多出部分以电子对分布
2、电子式的书写
(1)原子的电子式:书写主族元素原子的电子式,直接用“·”或“×”把最外层电子一一表示出来即可
氢原子 氯原子 氮原子 钠原子 氧原子 钙原子
(2)简单阳离子(单核)的电子式:简单阳离子的电子式就是离子符号本身,不需标示最外层电子
钠离子 锂离子 镁离子 铝离子
Na+ Li+ Mg2+ Al3+
(3)简单阴离子(单核)的电子式:在书写电子式时,不但要表达出最外层所有电子数(包括得到的电子),而且还应
用“[ ]”括起来,并在“[ ]”右上角标出“n-”以表示其所带的电荷
Cl— O2— S2— N3—
(4)原子团的电子式:作为离子的原子团,无论是阴离子,还是阳离子,不仅要画出各原子最外层的电子,而且
都应用“[ ]”括起来,并在“[ ]”右上角标明电性和电量
NH + HO+ OH— O2— S2— C 2—
4 3 2 2 2
(5)离子化合物的电子式:离子化合物的电子式由阳离子的电子式和阴离子的电子式组成的,对于化合物是由多
种离子组成的物质,相同离子间要隔开排列,注意相同的离子不能合并
CaO KS CaF NaOH NaH
2 2
CaC NaO FeS NH Cl NH
2 2 2 2 4 5
MgN NaN Al S
3 2 3 2 3
(6)离子键的形成(离子化合物的形成过程):离子键的形成用电子式表示式时,前面写出成键原子的电子式,后
面写出离子化合物的电子式,中间用一箭头“→”连起来即可,如:
(7)共价化合物的电子式(共价分子):共价化合物分子是由原子通过共用电子对结合而形成的,书写电子式时,
应把共用电子对写在两成键原子之间,然后不要忘记写上未成键电子结构式:用一根短线表示一对共用电子对的式子叫做结构式。(未成键的电子不用标明)
分子 Cl O N HO
2 2 2 2
电子式
结构式
分子 CH CO HO HClO
4 2 2 2
电子式
结构式
分子 CCl BF PCl PCl
4 3 3 5
电子式
结构式
(8)共价键的形成 (共价分子的形成过程):共价键的形成用电子式表示时,同样是前面写出成键原子的电子式,
后面写出共价分子的电子式,中间用一箭头“→”连起来即可,如:
【即学即练1】
1、判断正误(正确打“√”,错误的打“×”,并改正)
(1)Na S ( ) (2)Na O ( ) (3)MgBr ( )
2 2 2
(4)H O ( ) (5)OH- ( ) (6)HClO ( )
2
(7)Cl ( ) (8)O ( ) (9)H S ( )
2 2
(10)Na+ ( ) (11) ( )
2、含有极性键且分子中各原子都满足8电子稳定结构的化合物是( )
A.CH B.CH===CH C.CO D.N
4 2 2 2 2
3、下列物质中所有原子均满足最外层8电子稳定结构的化合物是( )
A.PCl B.P C.CCl D.NH
5 4 4 3
4、下列分子中所有原子都满足最外层为8电子结构的是( )
A.BF B.HO C.SiCl D.PCl
3 2 4 5
5、下列分子中所有原子都满足最外层8电子结构的是( )
①光气(COCl ) ②六氟化硫 ③二氟化氙 ④三氟化硼 ⑤BeCl ⑥PCl ⑦PCl ⑧OF
2 2 3 5 2
A.①③⑥⑧ B.③④⑤⑦ C.①⑥⑧ D.②④⑤
二、分子间作用力与氢键
1、分子间作用力(范德华力)及其对物质性质的影响
(1)定义:把分子聚集在一起的作用力,叫做分子间作用力,又称范德华力(2)证明分子间作用力的存在:降低气体的温度时,气体分子的平均动能逐渐减小。随着温度降低,分子间的距
离逐渐减小,最后凝聚在一起,形成液态或固体。在这个过程中,分子由不规则运动的混乱状态转变为有规
则排列,这个事实证明分子间存在着相互作用
(3)主要特征
①广泛存在于分子之间
②只有分子间充分接近时才有分子间的相互作用力,如固体和液体物质中
③分子间作用力的能量远远小于化学键
④由分子构成的物质,其熔点、沸点、溶解度等物理性质主要由分子间作用力的大小决定
(4)范德华力对物质性质的影响:范德华力影响物质的物理性质,主要包括熔点、沸点。一般来说,对于组成和
结构相似的物质,相对分子量越大,范德华力越大,克服范德华力所需消耗的能量越大,物质的熔、沸点就
越高
2、氢键及其对物质性质的影响
(1)氢键的形成:当氢原子与非金属性很大的F、O、N原子形成H—F、H—O、H—N共价键时,由于F、O、N
的非金属性比氢大得多,致使这些共价键的电子对会强烈的偏向 F、O、N原子的一边,会使F、O、N原子
带有“少量的负电荷”,而氢原子带有“少量的正电荷”
(2)氢键的定义:由已经与非金属性很强的原子(N、O、F)形成共价键的氢原子(如:水分子中的氢)与另一个分子
中非金属性很强的原子(如:水中的氧)之间的作用力。氢键是比分子间作用力强的分子间作用,但它不是化
学键,仍属于分子间作用力的范畴
(3)氢键表示方法:X—H…Y(X、Y可相同或不同,一般为F、O、N)“—”表示共价键,“…”表示氢键
如:HF 分子间的氢键可表示为:F—H…F—H
(4)氢键对物质性质的影响
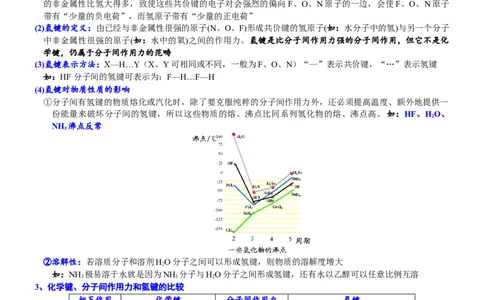
①分子间有氢键的物质熔化或汽化时,除了要克服纯粹的分子间作用力外,还必须提高温度、额外地提供一
份能量来破坏分子间的氢键,所以这些物质的熔、沸点比同系列氢化物的熔、沸点高。如:HF、HO、
2
NH 沸点反常
3
②溶解性:若溶质分子和溶剂HO分子之间可以形成氢键,则物质的溶解度增大
2
如:NH 极易溶于水就是因为NH 分子与HO分子之间形成氢键,还有水以乙醇可以任意比例互溶
3 3 2
3、化学键、分子间作用力和氢键的比较
相互作用 化学键 分子间作用力 氢键
某些含强极性键氢化物分子之
存在范围 相邻原子 ( 离子 ) 之间 分子之间
间 ( 如 HF 、 H O 、 NH 等 )
2 3
比化学键弱,比分子间作用力
作用力比较 强 很弱
强
物质的物理性质及化学
影响范围 物质的物理性质 物质的物理性质
性质
【即学即练2】
1、判断正误,正确的划“√”,错误的划“×”
(1)共价化合物分子间均存在分子间作用力( )
(2)F 、Cl、Br 、I 的熔沸点逐渐升高,是因为分子间作用力越来越大( )
2 2 2 2
(3)H O的稳定性大于HS,是因为水分子间存在氢键( )
2 2(4)HF、HCl、HBr、HI的稳定性逐渐减弱,其熔沸点逐渐升高( )
2、关于氢键,下列说法不正确的是( )
A.HF的沸点比HCl的沸点高是由于HF分子间存在氢键
B.水在结冰时体积膨胀,是由于水分子之间存在氢键
C.NH 的稳定性很强,是因为其分子间能形成氢键
3
D.在氨水中水分子和氨分子之间也存在着氢键
3、下列事实与氢键有关的是( )
A.HF、HCl、HBr、HI的热稳定性依次减弱
B.水加热到很高的温度都难以分解
C.CH、SiH、GeH 、SnH 的熔点随相对分子质量的增大而升高
4 4 4 4
D.氨气在水中溶解度很大
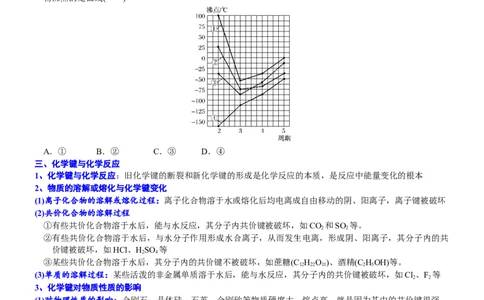
4、图中四条曲线分别表示ⅣA、ⅤA、ⅥA、ⅦA族元素的气态氢化物的沸点,其中表示ⅥA族元素气态氢化
物沸点的是曲线( )
A.① B.② C.③ D.④
三、化学键与化学反应
1、化学键与化学反应:旧化学键的断裂和新化学键的形成是化学反应的本质,是反应中能量变化的根本
2、物质的溶解或熔化与化学键变化
(1)离子化合物的溶解或熔化过程:离子化合物溶于水或熔化后均电离成自由移动的阴、阳离子,离子键被破坏
(2)共价化合物的溶解过程
①有些共价化合物溶于水后,能与水反应,其分子内共价键被破坏,如CO 和SO 等。
2 2
②有些共价化合物溶于水后,与水分子作用形成水合离子,从而发生电离,形成阴、阳离子,其分子内的共
价键被破坏,如HCl、HSO 等
2 4
③某些共价化合物溶于水后,其分子内的共价键不被破坏,如蔗糖(C H O )、酒精(C HOH)等。
12 22 11 2 5
(3)单质的溶解过程:某些活泼的非金属单质溶于水后,能与水反应,其分子内的共价键被破坏,如Cl、F 等
2 2
3、化学键对物质性质的影响
(1)对物理性质的影响:金刚石、晶体硅、石英、金刚砂等物质硬度大、熔点高,就是因为其中的共价键很强,
破坏时需消耗很多的能NaCl等部分离子化合物,也有很强的离子键,故熔点也较高
(2)对化学性质的影响:N 分子中有很强的共价键,故在通常状况下,N 很稳定,HS、HI等分子中的共价键较
2 2 2
弱,故它们受热时易分解
4、化学键的存在
5、键的强弱与成键粒子的关系(1)离子键的强弱与阴、阳离子半径大小以及电荷数的多少有关。离子半径越小,电荷数越多,其离子键的作用
就越强
(2)共价键的强弱与成键双方原子核间距有关。原子半径越小,原子间核间距就越小,共价键就越牢固,作用就
越强
(3)离子键的强弱影响该离子化合物的熔、沸点、溶解性等;共价键的强弱往往会影响分子的稳定性或一些物质
熔、沸点的高低
【即学即练3】
1、判断正误,正确的划“√”,错误的划“×”
(1)1molKHSO 加热熔化可电离出2N 阳离子( )
4 A
(2)共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏( )
(3)共价化合物熔点都低于离子化合物( )
(4)分子内共价键越强,分子越稳定,其熔、沸点也越高( )
(5)含有阳离子的化合物一定含有阴离子( )
(6)含有离子键的物质不可能是单质( )
2、从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学变化的
是( )
A.金刚石变成石墨 B.NaCl熔化
C.HCl溶于水电离出H+和Cl- D.电解熔融的Al O 制取Al
2 3
3、在下列变化过程中,既有离子键被破坏又有共价键被破坏的是 ( )
A.将SO 通入水中 B.烧碱溶于水
2
C.将HCl通入水中 D.硫酸氢钠溶于水
4、短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相
同。下列化合物中同时存在极性和非极性共价键的是 ( )
A.ZY B.XY C.ZY D.ZYX
2 2 2 2 2
5、有以下9种物质:①Ne ②HCl ③P ④HO ⑤NaS ⑥NaOH ⑦NaO ⑧NH Cl ⑨AlCl 。请
4 2 2 2 2 2 4 3
用上述物质的序号填空:
(1)不存在化学键的是__________________________________
(2)只存在极性共价键的是_________________________________
(3)只存在非极性共价键的是____________________________
(4)既存在非极性共价键又存在极性共价键的是___________________
(5)只存在离子键的是__________________________________
(6)既存在离子键又存在共价键的是___________________________
【课后作业】
1、下列离子化合物的电子式书写正确的是( )
A.Ca2+[Cl] B.Na+[S]-2Na+ C.[Mg2+][O]2- D.K+[F]-
2、下列关于电子式的说法不正确的是( )
A.每种元素的原子都可以写出电子式 B.简单阳离子的电子式与它的离子符号相同
C.阴离子的电子式要加方括号表示 D.电子式就是核外电子排布的式子
3、下列物质的电子式正确的是( )
A.NaOH B.Na+[Cl]- C.[NH ]+[Cl]- D.K+[Br]-
4
4、下列各式为用电子式表示的物质的形成过程,其中正确的是( )5、下列电子式中正确的是( )
A.[Ca2+][O]2- B.Na+Cl- C.[Br]-Mg2+[Br]- D.Na[O]2-
6、下列有关电子式的叙述正确的是( )
A.H、He、Li的电子式分别为H·、·He·、·Li
B.氯原子的电子式为·Cl,Cl-的电子式为Cl
C.钠离子、镁离子、铝离子的电子式分别为Na+、Mg2+、Al3+
D.NaO的电子式为Na+[O]2-Na+,HO的电子式为H+[O]2-H+
2 2
7、下列用电子式表示的化合物的形成过程正确的是( )
8、下列表示物质结构的化学用语正确的是( )
A.H、D、T表示同一种核素
B.MgCl 的形成过程:Cl Mg Cl―→[Cl]-Mg2+[Cl] -
2
C.Cl-的结构示意图:
D.NH Cl的电子式:
4
9、下列说法中不正确的是( )
①水分子的电子式为H-[ClH]- ②离子半径由小到大的顺序是Mg2+M
③F、Cl、Br 、I 熔沸点随相对分子质量增大而升高
2 2 2 2
④由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
⑤干冰升华会破坏共价键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦NaO 中既含离子键又含非极性键
2 2
A.②⑤⑥ B.③⑤⑦ C.②④⑤ D.①③⑦
16、下列有关叙述正确的是( )
A.O和O中子数相同,质子数不同,互为同位素
B.HO比HS稳定,H—S键比H—O键更难断裂
2 2
C.NaO 晶体中阳离子与阴离子个数比为1∶1
2 2
D.NaO晶体中存在离子键,是离子化合物
2
17、(1)有下列物质:He、N、CaO、HSO 、NaS、KOH、NaHCO 。
2 2 4 2 3
①其中只含共价键的是________,②只含离子键的是________,③既含有共价键又含有离子键的是________
④属于共价化合物的是________,⑤属于离子化合物的是________
(2)下列变化中,不需要破坏化学键的是________
A.硫酸与氢氧化钠反应 B.加热氯酸钾使其分解
C.冰熔化 D.氯化钠溶于水
18、下列分子中所有原子都满足最外层8电子结构的是________
A.光气(COCl ) B.六氟化硫 C.二氟化氙 D.三氟化硼
2
E.BeCl F.PCl G.PCl H.N
2 3 5 2
19、设X、Y、Z代表三种元素。已知:
①X+和Y-两种离子具有相同的电子层结构
②Z元素原子核内质子数比Y元素原子核内质子数少 9个
③Y和Z两种元素可以形成四核42个电子的-1价阴离子
据此,请填空:
(1)写出X、Y、Z三种元素的名称:X______,Y______,Z________
(2)X、Y两种元素最高价氧化物对应水化物相互反应的离子方程式为________________________________
(3)用电子式表示X、Z形成化合物的过程:___________________________________
20、为保持街道整洁、湿润,在路面或广场上喷洒化学式为 XY 的溶液作保湿剂。X原子的结构示意图为
2
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外
层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ 型分子。
2
(1)m=________,该保湿剂的化学式为________
(2)Z、W元素的名称分别为________、________
(3)下列说法正确的是________
A.XY 和WZ 都为离子化合物 B.XY 中仅含离子键,WZ 中仅含极性共价键
2 2 2 2
C.HZ比HY的稳定性强 D.X的阳离子比Y的阴离子半径大
2(4)下列化学用语表达正确的是________
A.XY 的电子式:X2+[YY]2-
2
B.WZ 的结构式:Z===W===Z
2
C.Y元素的单质与HZ水溶液反应的离子方程式:Y+Z2-===2Y-+Z↓
2 2
D.用电子式表示XY 的形成过程:Y X Y―→[Y]-X2+[Y]-
2
21、A、B、C、D、E是相邻的三个周期中的五种元素,它们的原子序数依次增大,A与E位于同主族,B、
C、D位于同周期。已知:①除A外其他各元素的原子都有内层电子,其中 B最外层电子数是次外层电子数
的2倍,②A与B,B与C能生成气态分子X和Y,③D和E能生成离子化合物,且离子的电子层结构相同,
试回答:
(1)元素或物质的名称:A________,B________,C______,D________,E________,X________,Y________
(2)写出D与E形成化合物的电子式:______________。画出E的原子结构示意图________
(3)写出X分子的电子式________,结构式_________。写出Y分子的电子式________,结构式_____________
(4)用电子式表示A与C原子形成分子的过程________________ __,写出只含A、C元素的阳离子和阴离子的电
子式____________
22、A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大,D、G同主族,A与B、C、D能形成
电子数相同的三种常见分子,E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电
子层结构。
(1)三种元素的名称:B__________,D__________,F__________
(2)A 与 D、A 与 G 均可形成 18e-的化合物。两 种化合物在 水溶液中 反应的化学方程式为
______________________
(3)A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为________________;
只含离子键的化合物的电子式为______________
(4)E离子的半径__________(填“大于”、“小于”或“等于”)F离子的半径 ;E和F元素最高价氧化物对应
的水化物之间反应的离子方程式为________________________________________。
(5)写出由上述各种元素形成的粒子中与BC-电子数相等的两种分子的化学式:______________、__________
【电子式的书写及分子间作用力】答案
【即学即练1】
1、 (1)× (2)×
(10)× Na+ (11)×
2、C。解析:CH、CH===CH 中氢不满足8电子稳定结构,A、B项错;N 中只含有非极性键且为单质,D项
4 2 2 2
错。
3、C。解析:判断原子满足最外层8电子结构的方法为最外层电子数+所成价键数=8,故A、D项错;P 为单
4
质,而非化合物,故B项错;C项中5原子最外层均为8电子稳定结构,C项正确。
4、C。解析 A项,BF 中形成三个共用电子对,硼原子最外层只有6个电子,未达到8电子结构,错误;B项,
3
HO中氢原子最外层只有2个电子,错误;C项,SiCl 中Si与Cl形成4个共用电子对,两种原子的最外层电子
2 4
均达到8电子结构,正确;D项,PCl 中P不符合8电子结构,错误。
55、C。解析:根据碳原子的成键特征可推断光气(COCl )的结构式是COClCl,电子式是 ,PCl 分子
2 3
中原子的成键数与最外层电子数之和为8,OF 的结构式为 ,这3种分子符合题意;SF 、XeF 、PCl 中
2 6 2 5
的S、Xe、P原子的最外层电子数超过8个;BF 和BeCl 中的B、Be原子的最外层电子数少于8个(分别为6个
3 2
和4个)。
【即学即练2】
1、(1)√ (2)√ (3)× (4)×
2、C。解析:氢键是某些氢化物(NH 、HO、HF)分子间存在的比分子间作用力稍强的作用力。它的存在使氢
3 2
化物的熔点、沸点相对较高,因此HF的沸点高是由氢键所致;水在结冰时体积膨胀是由于水分子大范围的以
氢键相互联结,形成相对疏松的晶体,从而在结构上有许多空隙,造成体积膨胀;氨分子和水分子之间主要是
以氢键结合的,故A、B、D选项正确;NH 的稳定性取决于N—H键,而不是氢键,故C不正确。
3
3、D。解析:NH 在水中的溶解度很大,其主要原因是NH 与HO之间形成氢键。
3 3 2
4、A
【即学即练3】
1、(1)× (2)× (3)× (4)× (5)√ (6)√
2、AD
3、D
4、B。解析:由Y2-与Z+核外电子层的结构相同,可知Y在Z的上一周期,所以Y为O、Z为Na,则X为
H。A选项NaO只有离子键;B选项HO 既有非极性共价键,也
2 2 2
5、(1)① (2)②⑨ (3)③ (4)④ (5)⑤ (6)⑥⑦⑧
【课后作业】
1、D。解析:书写离子化合物的电子式时,每个离子要单独写,不能将角码合并写在一起表示,A项错误,应
改为[Cl]-Ca2+[Cl]-;离子电荷表示法(如R2-)与化合价(如R)不同,“2-”表示带两个单位负电荷,而“-
2”则表示化合价为-2价,另外,化合价应写在元素符号的正上方,B项错误,应改为Na+[S]2-Na+;在简单阳
离子符号周围不用方括号,只用简单离子符号表示即可,C项错误,应改为Mg2+[O]2-。
2、D。解析:任何原子均可以利用电子式表示,A正确;简单阳离子由于在形成过程中已失去最外层电子,所
以其电子式书写方式就是其离子符号本身,B正确;无论是简单阴离子,还是复杂的阴离子,都应标出电子对
等,还应加中括号,并在括号的右上方标出离子所带的电荷,C正确,电子式表示的是最外层电子的排布,不
是核外全部电子的排布,D错误。
3、D。解析:NaOH的电子式应为Na+[OH]-,A项错误;NaCl的电子式应为Na+[Cl]-,B项错误;
NH Cl的电子式应为 ,C项错误。
4
4、D。解析:A中KBr的电子式为K+[Br]-,B中弯箭头方向错误,应为Na S
Na―→Na+[S]2-Na+,C中CaCl 的电子式错误,应为[Cl]-Ca2+[Cl]-。
2
5、C。解析:氧化钙的电子式为Ca2+[O]2-,故A错误;氯化钠的电子式为Na+[Cl]-,故B错误;溴化
镁的电子式为[Br]-Mg2+[Br]-,故C正确;氧化钠的电子式为:Na+[O]2-Na+,故D错误。
6、C。解析:A 中锂原子的电子式应为 Li·;B 中 Cl-的电子式应为[Cl]-;D 中 HO 的电子式应为
2
HOH;金属阳离子的电子式与离子符号相同,C正确。
7、C。解析:NaBr的电子式应写成Na+[Br]-,A项错误;用电子式表示CaF 的形成过程应写成
2
F Ca F―→[F]-Ca2+[F]-,B项错误;用电子式表示化合物的形成过程,
应将“===”写成“―→”,D项错误。8、B。解析:H、D、T是同一种元素的三种核素,故A错误;氯离子是由氯原子得一个电子形成,核电荷数仍
为17,故氯离子的结构示意图为 ,故C错误;氯化铵为离子化合物,氯离子的最外层电子数必须标出,
氯化铵正确的电子式为 ,故D错误。
9、C。解析:HO为共价化合物,电子式应为HOH,①错误;HCl为共价化合物,形成过程应为H×+
2
·Cl―→HCl,④错误。
10、C
11、A。解析:A项,N最外层5个电子,形成三个共用电子对,故正确;B项,NaCl是离子化合物,电子式为
Na+[Cl]-,故错误;C 项,HCl 是共价化合物,电子式为 HCl,故错误;D 项,CO 的电子式为
2
OCO,故错误。
12、B。解析:A项,加热NH Cl破坏了NH Cl内的离子键和共价键;C项,水通电分解破坏了水分子内的共价
4 4
键;D项,HCl溶于水,破坏了HCl分子内的共价键;B项,干冰升华没有化学键的破坏。
13、B。解析:氢键不是化学键,A项错误;离子化合物中可能含有共价键,例如NaOH中O与H之间含有共
价键,B项正确;I 的挥发是物理变化,破坏了分子间作用力,共价键不变,C项错误;非极性键不一定只存在
2
双原子单质中,例如CHCHOH分子中C与C之间含有非极性键,D项错误。
3 2
14、D。解析:化学反应的实质是旧键的断裂,新键的生成,特征是产生新物质,A项正确;CH 、CF 、
4 4
CCl 、CBr 熔、沸点逐渐升高,原因是分子间作用力逐渐增大,B项正确;NH 和HO间可以形成氢键,这也
4 4 3 2
是氨极易溶于水的原因之一,C项正确;NH H中含有离子键、极性键,不存在非极性键,D项错误。
4
15、D。解析:NH 分子中N原子与N原子之间形成非极性共价键,N原子与H原子之间形成极性共价键,故
2 4
①正确;R2-和M+的电子层结构相同,则离子的核外电子数相等,且M处于R相邻的下一周期,所以原子序数:
M>R,故②错误;F 、Cl 、Br 、I 是组成和结构相似的分子,熔沸点随相对分子质量增大而升高,故③正确;
2 2 2 2
氢化物的酸性与元素的非金属性无关,并且酸性:HCl<HBr<HI,故④错误;干冰升华会破坏分子间作用力,
没有破坏共价键,故⑤错误;HF分子很稳定,是因为H-F键的键能大,稳定性与氢键无关,故⑥错误;在
NaO 中Na+与O之间存在离子键,在O内部含有非极性键,故⑦正确。所以正确的是①③⑦。故选D。
2 2
16、D。解析:O和O质子数都为8,中子数分别为8和10,故A错误;HO比HS稳定,H—O键比H—S键
2 2
更难断裂,故B错误;NaO 晶体中阳离子为钠离子,阴离子为过氧根离子,个数比为1∶2,故C错误;NaO晶
2 2 2
体中钠离子与氧离子之间的作用力为离子键,含有离子键的化合物是离子化合物,故D正确;故选D。
17、(1)①N、HSO ②CaO、Na S ③KOH、NaHCO ④HSO ⑤CaO、Na S、KOH、NaHCO (2)C
2 2 4 2 3 2 4 2 3
解析:(1)N 、HSO 分子中只含共价键;CaO、NaS中只含离子键;KOH、NaHCO 中既含有离子键又含有共
2 2 4 2 3
价键,He分子中不含化学键。(2)A项反应中有化学键的断裂和形成,化学键被破坏;NaCl溶于水离子键被破
坏;KClO 受热分解破坏离子键和共价键;冰熔化后变为液态水,共价键未被破坏。
3
18、A、F、H
解析:根据碳原子形成4个键,氧原子形成2个键,氯原子形成1个键的成键特征可写出光气(COCl )的电子式
2
是 ,PCl 分子中原子的成键数与最外层
3
电子数之和为8,N 的电子式为N⋮⋮N,这3种分子符合题意;SF 、XeF 、PCl 中的S、Xe、P的最外层电
2 6 2 5
子数超过8个;BF 和BeCl 中的B、Be原子分别形成3个、2个共价键,所以其最外层电子数为6个、4个,均
3 2
少于8个。
19、(1)钾 氯 氧
(2)H++OH-===H O
2
(3)解析:根据X+和Y-两种离子具有相同的电子层结构,可确定X为第ⅠA族元素,Y为第ⅦA族元素,Z元素
原子核内质子数比Y元素原子核内质子数少9个,Z为Y的前一周期的氧族元素;不难判断出,Y和Z两种元
素,形成的4核42个电子的-1价阴离子为ClO,X+为K+。
20、(1)20 CaCl (2)硫 碳 (3)B (4)BD
2
解析:X原子的结构示意图为 ,由于K层最多容纳2个电子,L层最多容纳8个电子,可
知a=2,b=8,故X为Ca元素;由化学XY 可知Y的化合价为-1价,而X的阳离子与Y的阴离子的电子层
2
结构相同,离子核外电子数均为18,则Y原子核外电子数为17,故Y为Cl,则该融雪剂为CaCl ;元素Z、W
2
均为短周期元素,它们原子的最外层电子数均是其电子层数的 2倍,符合条件的元素有He、C、S,由于Z与Y
相邻且Z、W能形成一种WZ 型分子,则Z为S元素,W为C元素,二者形成的分子为CS 。(1)由上述分析可
2 2
知,m=2+8+8+2=20,该融雪剂的化学式为CaCl ;(2)由上述分析可知,Z为硫元素、W为碳元素;
2
(3)CaCl 属于离子化合物,而CS 是共价化合物,故A错误;CaCl 中仅含离子键,CS 中只含共价键,且是极
2 2 2 2
性共价键,故B正确;因氯的非金属性强于硫,所以稳定性HCl>H S,故C错误;核外电子排布相同的离子,
2
核电荷数越大,离子的半径越小,所以半径Ca2+