文档内容
硫和硫的氧化物
【学习目标】
1、掌握硫在周期表中的位置,硫元素的存在形式,熟悉单质硫的物理性质和化学性质
2、掌握SO 的物理性质和化学性质及实验室制法,理解SO 的酸性、漂白性及强还原性
2 2
【主干知识梳理】
一、硫
1、硫元素在自然界中的存在形式
(1)游离态:存在于火山喷口附近或地壳的岩层里
(2)化合态:主要以硫化物和硫酸盐的形式存在。在岩层深处和海底的无氧环境下,硫元素与铁、铜等金属元素
形成的化合物通常以硫化物的形式存在,如硫铁矿(FeS)、黄铜矿(CuFeS)等。在地表附近,硫化物转化为硫
2 2
酸盐,如石膏(CaSO·2H O)、芒硝(NaSO ·10H O)等
4 2 2 4 2
2、硫单质的物理性质:硫(俗称硫黄)是一种黄色晶体,质脆,易研成粉末。硫难溶于水,微溶于酒精,易溶于
二硫化碳。因此可以用CS 洗涤内壁附着硫的试管
2
3、硫单质的化学性质
硫的原子结构示意图为 ,位于元素周期表的第三周期、第 Ⅵ A 族,硫原子的最外电子层有 6 个 电
子,在化学反应中容易得到2个电子,形成 - 2 价硫的化合物,表现较强的氧化性:S――→――→SO
2
(1)与金属反应 (与变价金属反应,均是金属被氧化成最低价态)——体现硫的氧化性
①硫粉与钠研磨爆炸:2Na+S===Na S
2
②硫与铝共热:2Al+3S Al S (制取Al S 的唯一途径)
2 3 2 3
③铁与硫粉共热:Fe+S FeS (黑色固体,不溶于水)
④铜与硫粉共热:2Cu+S Cu S (黑色固体,不溶于水)
2
⑤硫与银反应:2Ag+S===Ag S (银器变黑)
2
⑥硫与汞反应:Hg+S===HgS (汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理)
(2)与非金属反应
①硫在氧气中燃烧:S+O=====SO (硫在空气中燃烧发出淡蓝色火焰;在纯氧中燃烧发出蓝紫色火焰)
2 2
【微点拨】①该反应体现了单质硫具有还原性
②硫在过量、纯净的O 中燃烧的产物是SO 而不是SO
2 2 3
②硫与氢气共热:S+H HS (该反应体现了单质硫具有氧化性)
2 2
(3)与强氧化性酸(如:浓硫酸、硝酸)反应——体现硫的还原性
①硫与浓HSO 反应:S+2HSO (浓) 3SO ↑+2HO
2 4 2 4 2 2
②硫与浓HNO 反应:S+6HNO (浓) HSO +6NO ↑+2HO
3 3 2 4 2 2
(4)与强碱的反应——既体现氧化性,又体现还原性
3S+6NaOH 2Na S+Na SO +3HO (用热碱溶液清洗硫)
2 2 3 2
①NaS与稀HSO 反应:Na S+HSO ===HS↑+Na SO
2 2 4 2 2 4 2 2 4
②NaSO 与稀HSO 反应:Na SO +HSO ===Na SO +SO ↑+HO (实验室制SO 的方法)
2 3 2 4 2 3 2 4 2 4 2 2 2
③向NaS和NaSO 的混合溶液中加入稀HSO :2Na S+Na SO +3HSO ===3S↓+3Na SO +3HO
2 2 3 2 4 2 2 3 2 4 2 4 2
4、用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药(S+2KNO+3C=====KS+3CO↑+N↑)
3 2 2 2
【微点拨】实验室除去试管内壁附着硫的两种方法:
①物理法:加二硫化碳(CS)溶解;②化学法:加氢氧化钠溶液溶解
2
【对点训练1】
1、下列关于硫的说法不正确的是( )
A.试管内壁附着的硫可用二硫化碳溶解除去
B.游离态的硫存在于火山喷口附近或地壳的岩层里C.单质硫既有氧化性,又有还原性
D.硫在过量纯氧中的燃烧产物是三氧化硫
2、下列说法中正确的是( )
A.硫与金属或非金属反应均作氧化剂
B.分离黑火药中的硝酸钾、木炭、硫黄要用到二硫化碳、水及过滤操作
C.过量的硫与铁反应生成Fe S,表现了硫单质的氧化性
2 3
D.硫只以化合态形式存在于自然界中
3、下列化合物能由两种单质直接化合生成的是( )
A.Fe S B.CuS C.SO D.SO
2 3 3 2
二、二氧化硫
1、物理性质
二氧化硫是一种无色、有刺激性气味的有毒气体,密度比空气的大,易液化,易溶于水。在通常情况下,1
体积的水可以溶解约40 体积的SO
2
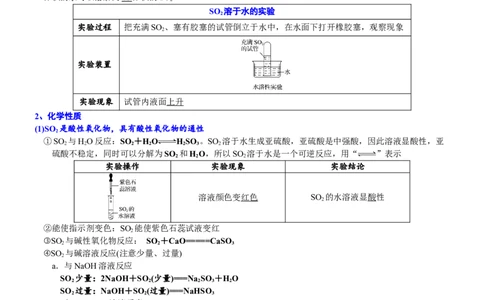
SO 溶于水的实验
2
实验过程 把充满SO 、塞有胶塞的试管倒立于水中,在水面下打开橡胶塞,观察现象
2
实验装置
实验现象 试管内液面上升
2、化学性质
(1)SO 是酸性氧化物,具有酸性氧化物的通性
2
①SO 与HO反应:SO +HO HSO 。SO 溶于水生成亚硫酸,亚硫酸是中强酸,因此溶液显酸性,亚
2 2 2 2 2 3 2
硫酸不稳定,同时可以分解为SO 和HO,所以SO 溶于水是一个可逆反应,用“ ”表示
2 2 2
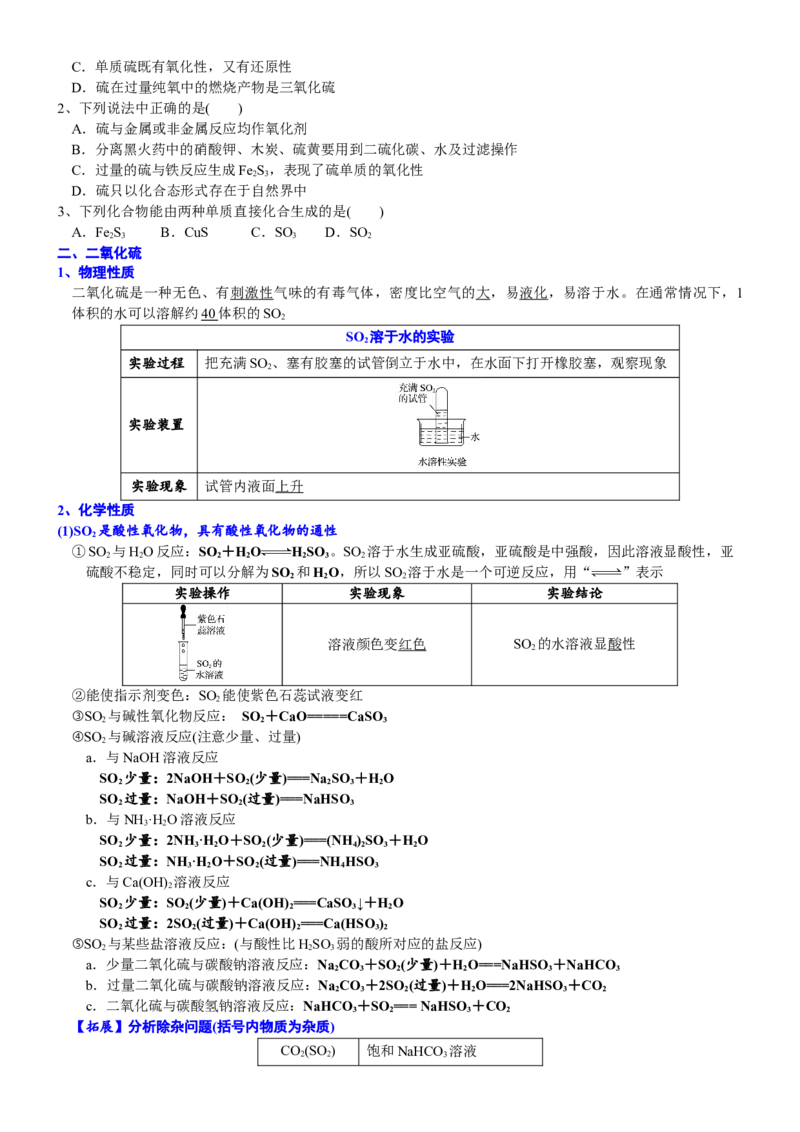
实验操作 实验现象 实验结论
溶液颜色变红色 SO 的水溶液显酸性
2
②能使指示剂变色:SO 能使紫色石蕊试液变红
2
③SO 与碱性氧化物反应: SO +CaO=====CaSO
2 2 3
④SO 与碱溶液反应(注意少量、过量)
2
a.与NaOH溶液反应
SO 少量:2NaOH+SO (少量)===Na SO +HO
2 2 2 3 2
SO 过量:NaOH+SO (过量)===NaHSO
2 2 3
b.与NH ·H O溶液反应
3 2
SO 少量:2NH ·HO+SO (少量)===(NH)SO +HO
2 3 2 2 4 2 3 2
SO 过量:NH ·HO+SO (过量)===NHHSO
2 3 2 2 4 3
c.与Ca(OH) 溶液反应
2
SO 少量:SO (少量)+Ca(OH) ===CaSO ↓+HO
2 2 2 3 2
SO 过量:2SO (过量)+Ca(OH) ===Ca(HSO )
2 2 2 3 2
⑤SO 与某些盐溶液反应:(与酸性比HSO 弱的酸所对应的盐反应)
2 2 3
a.少量二氧化硫与碳酸钠溶液反应:Na CO +SO (少量)+HO===NaHSO +NaHCO
2 3 2 2 3 3
b.过量二氧化硫与碳酸钠溶液反应:Na CO +2SO (过量)+HO===2NaHSO +CO
2 3 2 2 3 2
c.二氧化硫与碳酸氢钠溶液反应:NaHCO +SO === NaHSO +CO
3 2 3 2
【拓展】分析除杂问题(括号内物质为杂质)
CO(SO ) 饱和NaHCO 溶液
2 2 3CO(HCl) 饱和NaHCO 溶液
2 3
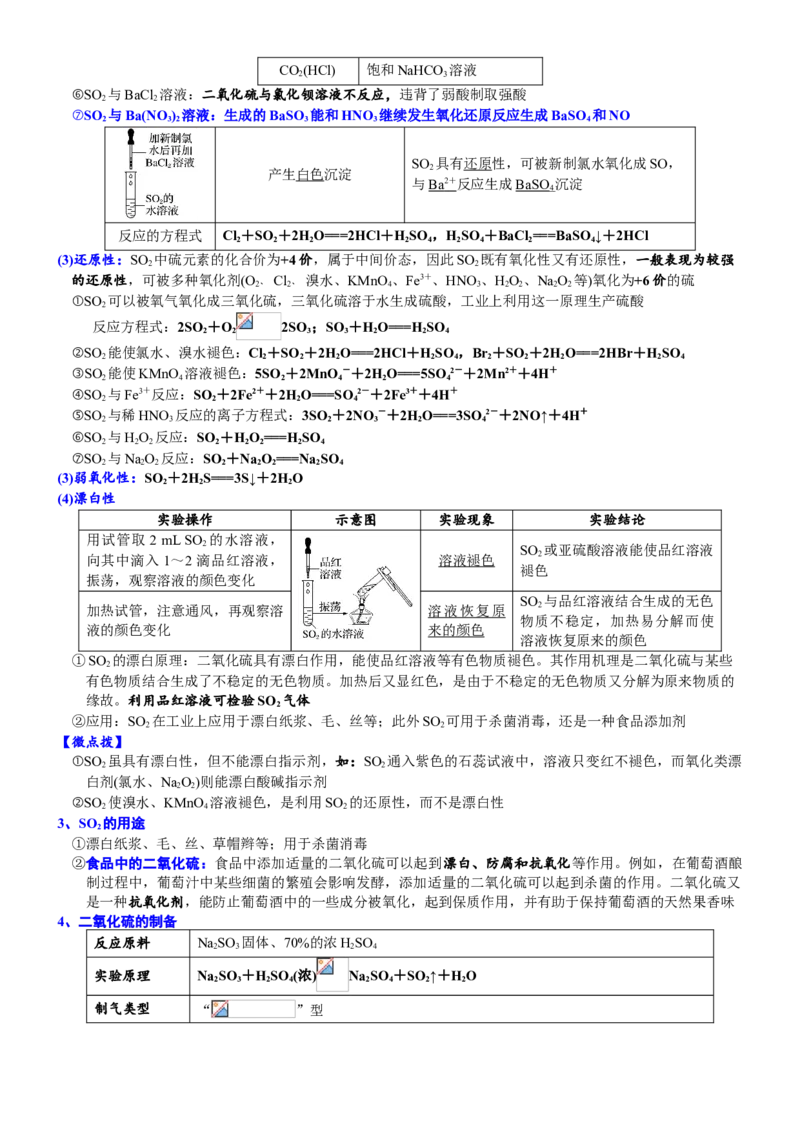
⑥SO 与BaCl 溶液:二氧化硫与氯化钡溶液不反应,违背了弱酸制取强酸
2 2
⑦SO 与Ba(NO ) 溶液:生成的BaSO 能和HNO 继续发生氧化还原反应生成BaSO 和NO
2 3 2 3 3 4
SO 具有还原性,可被新制氯水氧化成SO,
产生白色沉淀 2
与 Ba 2 + 反应生成BaSO 沉淀
4
反应的方程式 Cl +SO +2HO===2HCl+HSO ,HSO +BaCl ===BaSO ↓+2HCl
2 2 2 2 4 2 4 2 4
(3)还原性:SO 中硫元素的化合价为+4价,属于中间价态,因此SO 既有氧化性又有还原性,一般表现为较强
2 2
的还原性,可被多种氧化剂(O ﹑Cl﹑溴水、KMnO 、Fe3+、HNO、HO、NaO 等)氧化为+6价的硫
2 2 4 3 2 2 2 2
①SO 可以被氧气氧化成三氧化硫,三氧化硫溶于水生成硫酸,工业上利用这一原理生产硫酸
2
反应方程式:2SO +O 2SO ;SO +HO===H SO
2 2 3 3 2 2 4
②SO 能使氯水、溴水褪色:Cl +SO +2HO===2HCl+HSO ,Br +SO +2HO===2HBr+HSO
2 2 2 2 2 4 2 2 2 2 4
③SO 能使KMnO 溶液褪色:5SO +2MnO -+2HO===5SO 2-+2Mn2++4H+
2 4 2 4 2 4
④SO 与Fe3+反应:SO +2Fe2++2HO===SO2-+2Fe3++4H+
2 2 2 4
⑤SO 与稀HNO 反应的离子方程式:3SO +2NO -+2HO===3SO 2-+2NO↑+4H+
2 3 2 3 2 4
⑥SO 与HO 反应:SO +HO===H SO
2 2 2 2 2 2 2 4
⑦SO 与NaO 反应:SO +Na O===Na SO
2 2 2 2 2 2 2 4
(3)弱氧化性:SO +2HS===3S↓+2HO
2 2 2
(4)漂白性
实验操作 示意图 实验现象 实验结论
用试管取2 mL SO 的水溶液,
2 SO 或亚硫酸溶液能使品红溶液
向其中滴入1~2滴品红溶液, 溶液褪色 2
褪色
振荡,观察溶液的颜色变化
SO 与品红溶液结合生成的无色
加热试管,注意通风,再观察溶 溶液恢复原 2
物质不稳定,加热易分解而使
液的颜色变化 来的颜色
溶液恢复原来的颜色
①SO 的漂白原理:二氧化硫具有漂白作用,能使品红溶液等有色物质褪色。其作用机理是二氧化硫与某些
2
有色物质结合生成了不稳定的无色物质。加热后又显红色,是由于不稳定的无色物质又分解为原来物质的
缘故。利用品红溶液可检验SO 气体
2
②应用:SO 在工业上应用于漂白纸浆、毛、丝等;此外SO 可用于杀菌消毒,还是一种食品添加剂
2 2
【微点拨】
①SO 虽具有漂白性,但不能漂白指示剂,如:SO 通入紫色的石蕊试液中,溶液只变红不褪色,而氧化类漂
2 2
白剂(氯水、NaO)则能漂白酸碱指示剂
2 2
②SO 使溴水、KMnO 溶液褪色,是利用SO 的还原性,而不是漂白性
2 4 2
3、SO 的用途
2
①漂白纸浆、毛、丝、草帽辫等;用于杀菌消毒
②食品中的二氧化硫:食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用。例如,在葡萄酒酿
制过程中,葡萄汁中某些细菌的繁殖会影响发酵,添加适量的二氧化硫可以起到杀菌的作用。二氧化硫又
是一种抗氧化剂,能防止葡萄酒中的一些成分被氧化,起到保质作用,并有助于保持葡萄酒的天然果香味
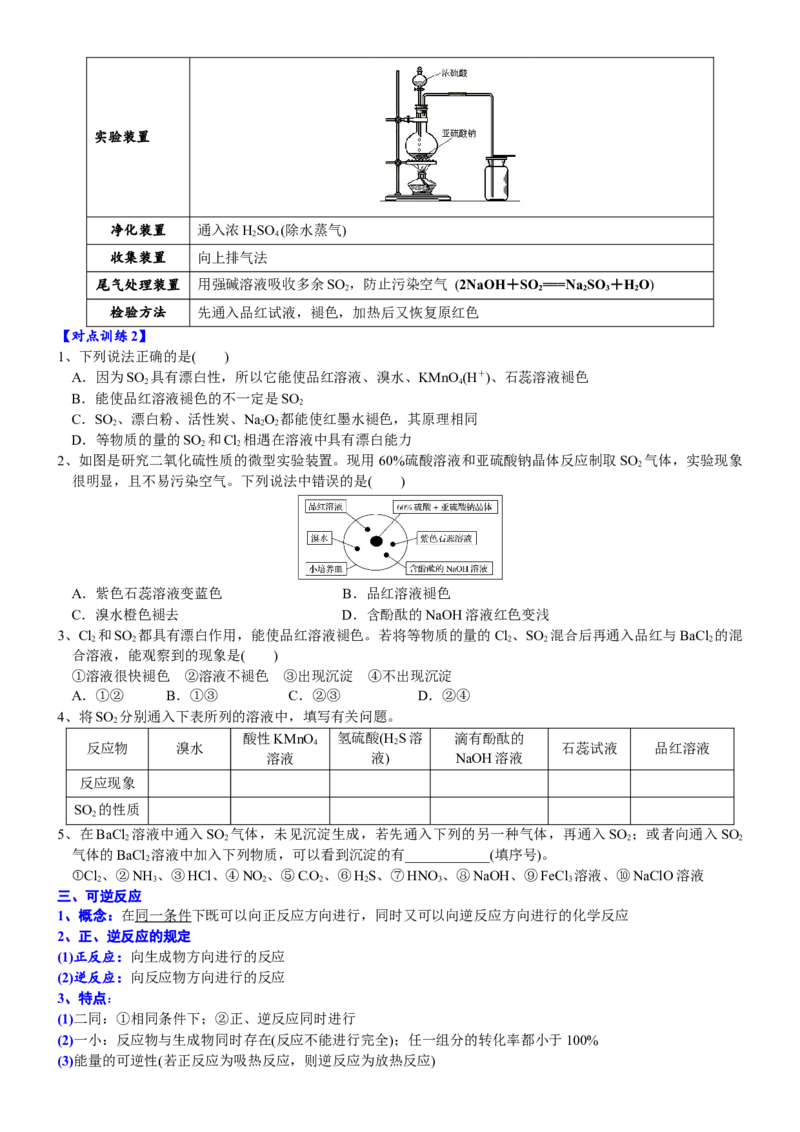
4、二氧化硫的制备
反应原料 NaSO 固体、70%的浓HSO
2 3 2 4
实验原理 Na SO +HSO (浓) Na SO +SO ↑+HO
2 3 2 4 2 4 2 2
制气类型 “ ”型实验装置
净化装置 通入浓HSO (除水蒸气)
2 4
收集装置 向上排气法
尾气处理装置 用强碱溶液吸收多余SO ,防止污染空气 (2NaOH+SO ===Na SO +HO)
2 2 2 3 2
检验方法 先通入品红试液,褪色,加热后又恢复原红色
【对点训练2】
1、下列说法正确的是( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、KMnO (H+)、石蕊溶液褪色
2 4
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同
2 2 2
D.等物质的量的SO 和Cl 相遇在溶液中具有漂白能力
2 2
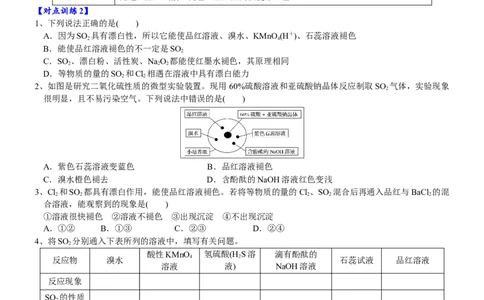
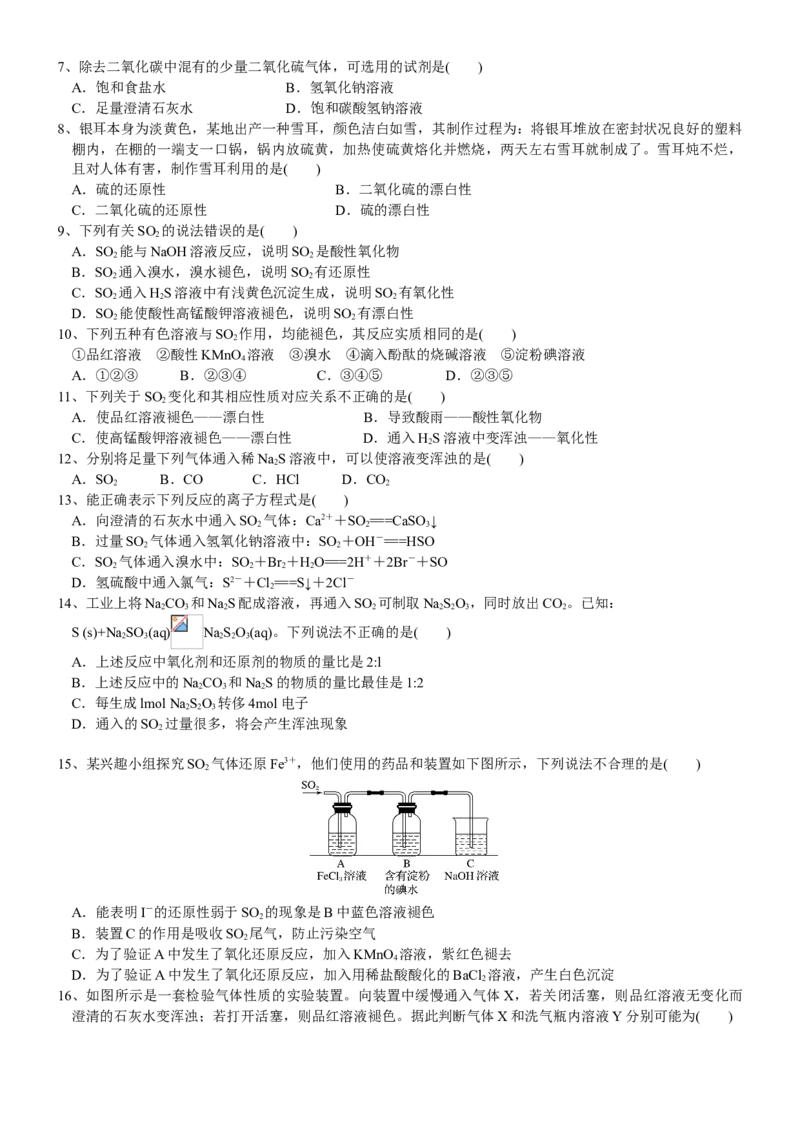
2、如图是研究二氧化硫性质的微型实验装置。现用 60%硫酸溶液和亚硫酸钠晶体反应制取SO 气体,实验现象
2
很明显,且不易污染空气。下列说法中错误的是( )
A.紫色石蕊溶液变蓝色 B.品红溶液褪色
C.溴水橙色褪去 D.含酚酞的NaOH溶液红色变浅
3、Cl 和SO 都具有漂白作用,能使品红溶液褪色。若将等物质的量的Cl、SO 混合后再通入品红与BaCl 的混
2 2 2 2 2
合溶液,能观察到的现象是( )
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
A.①② B.①③ C.②③ D.②④
4、将SO 分别通入下表所列的溶液中,填写有关问题。
2
酸性KMnO 氢硫酸(H S溶 滴有酚酞的
反应物 溴水 4 2 石蕊试液 品红溶液
溶液 液) NaOH溶液
反应现象
SO 的性质
2
5、在BaCl 溶液中通入SO 气体,未见沉淀生成,若先通入下列的另一种气体,再通入SO ;或者向通入SO
2 2 2 2
气体的BaCl 溶液中加入下列物质,可以看到沉淀的有____________(填序号)。
2
①Cl、②NH 、③HCl、④NO 、⑤CO、⑥HS、⑦HNO、⑧NaOH、⑨FeCl 溶液、⑩NaClO溶液
2 3 2 2 2 3 3
三、可逆反应
1、概念:在同一条件下既可以向正反应方向进行,同时又可以向逆反应方向进行的化学反应
2、正、逆反应的规定
(1)正反应:向生成物方向进行的反应
(2)逆反应:向反应物方向进行的反应
3、特点:
(1)二同:①相同条件下;②正、逆反应同时进行
(2)一小:反应物与生成物同时存在(反应不能进行完全);任一组分的转化率都小于100%
(3)能量的可逆性(若正反应为吸热反应,则逆反应为放热反应)4、表示方法:在方程式中用“ ”表示
5、可逆反应的普遍性:大多数化学反应都为可逆反应:
【对点训练3】
1、判断正误,正确的划“√”,错误的划“×”
(1)2H O2H↑+O↑为可逆反应( )
2 2 2
(2)可逆反应不等同于可逆过程。可逆过程包括物理变化和化学变化,而可逆反应属于化学变化( )
2、下列反应属于可逆反应的是( )
A.氢气在氧气中燃烧生成水,电解水生成氢气和氧气
B.二氧化硫通入品红溶液褪色,加热后又恢复红色
C.久置在空气中的氯水与氢氧化钠溶液的反应
D.常温下二氧化硫通入水中,与水反应生成亚硫酸
3、向含有 2mol 的 SO 的容器中通入过量氧气发生 2SO +O 2SO ,充分反应后生成 SO 的物质的量
2 2 2 3 3
__2mol(填“<”、“>”或“=”,下同),SO 的物质的量__0mol
2
四、三氧化硫(SO )
3
1、物理性质:通常情况下,SO 是一种无色易挥发的晶体,熔点为16.8℃,沸点为44.8℃,常温下为液态,在
3
标准状况下为固态
2、化学性质:SO 是硫酸的酸酐,具有酸性氧化物的通性
3
(1)能溶于水形成硫酸:SO+HO===H SO
3 2 2 4
SO 能强烈的吸水,在空气中发“烟”,与水剧烈反应生成HSO ,同时放出大量热,形成酸雾
3 2 4
(2)能与碱(石灰乳)反应:SO +Ca(OH) ===CaSO +HO
3 2 4 2
(3)与碱性氧化物反应:SO +CaO===CaSO
3 4
(4)与某些盐溶液反应:Na CO +SO ===Na SO +CO ↑
2 3 3 2 4 2
【对点训练4】
1、下列有关三氧化硫的说法中正确的是( )
A.SO 极易溶于水,且与水反应生成HSO B.SO 、SO 均具有漂白性,均能使石蕊溶液变红色
3 2 4 2 3
C.SO 可与碱反应,但不与碱性氧化物反应 D.SO 在空气中易被氧化为SO
3 2 3
2、下列说法中正确的是( )
A.三氧化硫极易溶于水,能与水反应生成硫酸 B.标准状况下,1 mol三氧化硫的体积为22.4 L
C.二氧化硫在空气中易被氧化为三氧化硫 D.三氧化硫具有漂白性,能使品红溶液褪色
【课后作业】
1、下列物质在一定条件下能够与硫黄发生反应,且硫作还原剂的是( )
A.O B.Fe C.H D.Zn
2 2
2、常温下单质硫主要以S 形式存在。加热时,S 会转化为S、S、S 等。当温度达到750 ℃时,硫蒸气主要以
8 8 6 4 2
S 形式存在(占92%)。下列说法中正确的是( )
2
A.S 转化为S、S、S 属于物理变化 B.不论哪种硫分子,完全燃烧时都生成二氧化硫
8 6 4 2
C.S、S、S、S 都是硫元素形成的单质,为同种物质 D.把硫单质在空气中加热到750 ℃即得S
2 4 6 8 2
3、下列硫化物中不能直接用金属单质和硫单质反应制得的是( )
A.CuS B.FeS C.ZnS D.MgS
4、除去试管壁上附着的硫,可采用的方法是( )
A.通入氢气后加热 B.伸入灼热的铁丝 C.用水洗涤 D.用二硫化碳洗涤后再用水洗
5、下列说法正确的是( )
A.硫的非金属性较强,只以化合态存在于自然界中
B.硫与非金属单质反应时均作氧化剂
C.硫粉在空气中燃烧生成SO ,在过量的纯氧中燃烧可以生成SO
2 3
D.在反应3S+6KOH KS+KSO +3HO中,S既是氧化剂又是还原剂
2 2 3 2
6、关于二氧化硫的下列叙述中,不正确的是( )
A.能使含有酚酞的氢氧化钠溶液褪色 B.能使石蕊溶液先变红色再褪色
C.能使品红溶液褪色 D.能使溴水褪色7、除去二氧化碳中混有的少量二氧化硫气体,可选用的试剂是( )
A.饱和食盐水 B.氢氧化钠溶液
C.足量澄清石灰水 D.饱和碳酸氢钠溶液
8、银耳本身为淡黄色,某地出产一种雪耳,颜色洁白如雪,其制作过程为:将银耳堆放在密封状况良好的塑料
棚内,在棚的一端支一口锅,锅内放硫黄,加热使硫黄熔化并燃烧,两天左右雪耳就制成了。雪耳炖不烂,
且对人体有害,制作雪耳利用的是( )
A.硫的还原性 B.二氧化硫的漂白性
C.二氧化硫的还原性 D.硫的漂白性
9、下列有关SO 的说法错误的是( )
2
A.SO 能与NaOH溶液反应,说明SO 是酸性氧化物
2 2
B.SO 通入溴水,溴水褪色,说明SO 有还原性
2 2
C.SO 通入HS溶液中有浅黄色沉淀生成,说明SO 有氧化性
2 2 2
D.SO 能使酸性高锰酸钾溶液褪色,说明SO 有漂白性
2 2
10、下列五种有色溶液与SO 作用,均能褪色,其反应实质相同的是( )
2
①品红溶液 ②酸性KMnO 溶液 ③溴水 ④滴入酚酞的烧碱溶液 ⑤淀粉碘溶液
4
A.①②③ B.②③④ C.③④⑤ D.②③⑤
11、下列关于SO 变化和其相应性质对应关系不正确的是( )
2
A.使品红溶液褪色——漂白性 B.导致酸雨——酸性氧化物
C.使高锰酸钾溶液褪色——漂白性 D.通入HS溶液中变浑浊——氧化性
2
12、分别将足量下列气体通入稀NaS溶液中,可以使溶液变浑浊的是( )
2
A.SO B.CO C.HCl D.CO
2 2
13、能正确表示下列反应的离子方程式是( )
A.向澄清的石灰水中通入SO 气体:Ca2++SO ===CaSO ↓
2 2 3
B.过量SO 气体通入氢氧化钠溶液中:SO +OH-===HSO
2 2
C.SO 气体通入溴水中:SO +Br +HO===2H++2Br-+SO
2 2 2 2
D.氢硫酸中通入氯气:S2-+Cl===S↓+2Cl-
2
14、工业上将NaCO 和NaS配成溶液,再通入SO 可制取NaSO,同时放出CO。已知:
2 3 2 2 2 2 3 2
S (s)+Na SO (aq) NaSO(aq)。下列说法不正确的是( )
2 3 2 2 3
A.上述反应中氧化剂和还原剂的物质的量比是2:l
B.上述反应中的NaCO 和NaS的物质的量比最佳是1:2
2 3 2
C.每生成lmol Na SO 转侈4mol电子
2 2 3
D.通入的SO 过量很多,将会产生浑浊现象
2
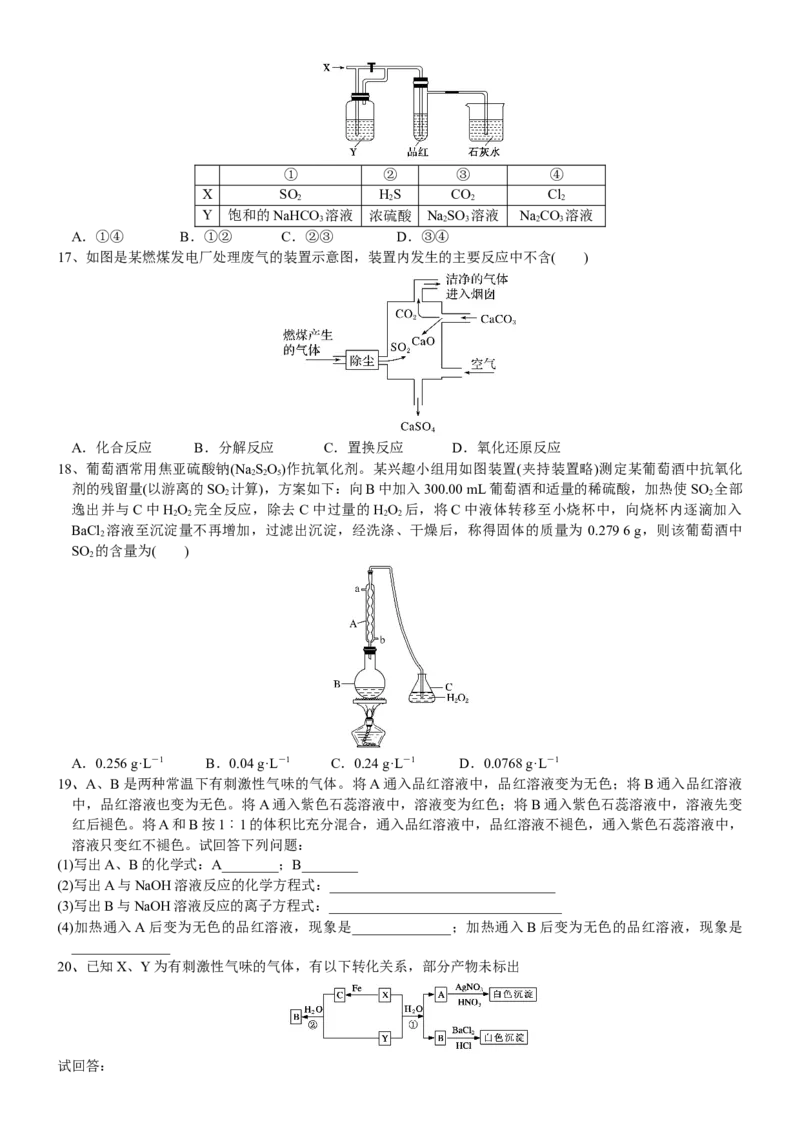
15、某兴趣小组探究SO 气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是( )
2
A.能表明I-的还原性弱于SO 的现象是B中蓝色溶液褪色
2
B.装置C的作用是吸收SO 尾气,防止污染空气
2
C.为了验证A中发生了氧化还原反应,加入KMnO 溶液,紫红色褪去
4
D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl 溶液,产生白色沉淀
2
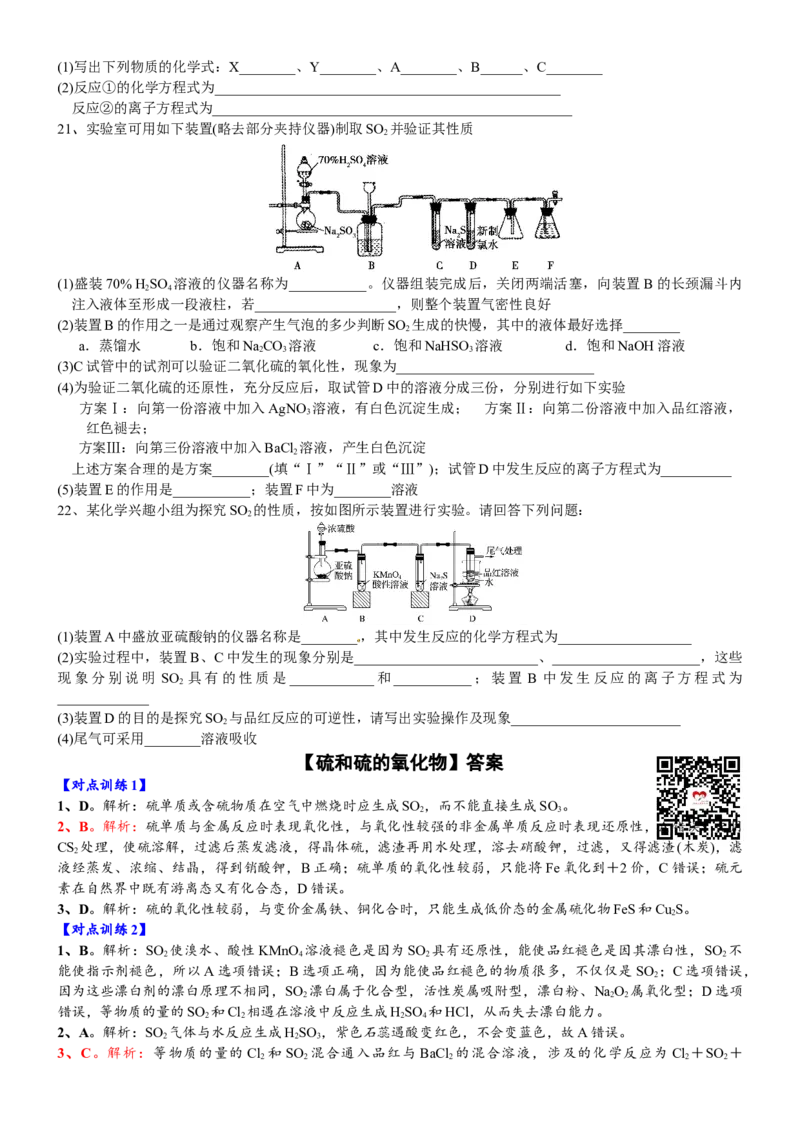
16、如图所示是一套检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而
澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色。据此判断气体X和洗气瓶内溶液Y分别可能为( )① ② ③ ④
X SO HS CO Cl
2 2 2 2
Y 饱和的NaHCO 溶液 浓硫酸 NaSO 溶液 NaCO 溶液
3 2 3 2 3
A.①④ B.①② C.②③ D.③④
17、如图是某燃煤发电厂处理废气的装置示意图,装置内发生的主要反应中不含( )
A.化合反应 B.分解反应 C.置换反应 D.氧化还原反应
18、葡萄酒常用焦亚硫酸钠(Na SO)作抗氧化剂。某兴趣小组用如图装置(夹持装置略)测定某葡萄酒中抗氧化
2 2 5
剂的残留量(以游离的SO 计算),方案如下:向B中加入300.00 mL葡萄酒和适量的稀硫酸,加热使SO 全部
2 2
逸出并与C中HO 完全反应,除去C中过量的HO 后,将C中液体转移至小烧杯中,向烧杯内逐滴加入
2 2 2 2
BaCl 溶液至沉淀量不再增加,过滤出沉淀,经洗涤、干燥后,称得固体的质量为 0.279 6 g,则该葡萄酒中
2
SO 的含量为( )
2
A.0.256 g·L-1 B.0.04 g·L-1 C.0.24 g·L-1 D.0.0768 g·L-1
19、A、B是两种常温下有刺激性气味的气体。将A通入品红溶液中,品红溶液变为无色;将B通入品红溶液
中,品红溶液也变为无色。将A通入紫色石蕊溶液中,溶液变为红色;将B通入紫色石蕊溶液中,溶液先变
红后褪色。将A和B按1︰1的体积比充分混合,通入品红溶液中,品红溶液不褪色,通入紫色石蕊溶液中,
溶液只变红不褪色。试回答下列问题:
(1)写出A、B的化学式:A________;B________
(2)写出A与NaOH溶液反应的化学方程式:________________________________
(3)写出B与NaOH溶液反应的离子方程式:_________________________________
(4)加热通入A后变为无色的品红溶液,现象是______________;加热通入B后变为无色的品红溶液,现象是
______________
20、已知X、Y为有刺激性气味的气体,有以下转化关系,部分产物未标出
试回答:(1)写出下列物质的化学式:X________、Y________、A________、B______、C________
(2)反应①的化学方程式为_________________________________________________
反应②的离子方程式为___________________________________________________
21、实验室可用如下装置(略去部分夹持仪器)制取SO 并验证其性质
2
(1)盛装70% H SO 溶液的仪器名称为___________。仪器组装完成后,关闭两端活塞,向装置 B的长颈漏斗内
2 4
注入液体至形成一段液柱,若____________________,则整个装置气密性良好
(2)装置B的作用之一是通过观察产生气泡的多少判断SO 生成的快慢,其中的液体最好选择________
2
a.蒸馏水 b.饱和NaCO 溶液 c.饱和NaHSO 溶液 d.饱和NaOH溶液
2 3 3
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为____________________________
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验
方案Ⅰ:向第一份溶液中加入AgNO 溶液,有白色沉淀生成; 方案Ⅱ:向第二份溶液中加入品红溶液,
3
红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl 溶液,产生白色沉淀
2
上述方案合理的是方案________(填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为__________
(5)装置E的作用是___________;装置F中为________溶液
22、某化学兴趣小组为探究SO 的性质,按如图所示装置进行实验。请回答下列问题:
2
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为___________________
(2)实验过程中,装置B、C中发生的现象分别是__________________________、_____________________,这些
现象分别说明 SO 具有的性质是____________和___________;装置 B 中发生反应的离子方程式为
2
_____________
(3)装置D的目的是探究SO 与品红反应的可逆性,请写出实验操作及现象________________________
2
(4)尾气可采用________溶液吸收
【硫和硫的氧化物】答案
【对点训练1】
1、D。解析:硫单质或含硫物质在空气中燃烧时应生成SO ,而不能直接生成SO 。
2 3
2、B。解析:硫单质与金属反应时表现氧化性,与氧化性较强的非金属单质反应时表现还原性,A错误;先用
CS 处理,使硫溶解,过滤后蒸发滤液,得晶体硫,滤渣再用水处理,溶去硝酸钾,过滤,又得滤渣(木炭),滤
2
液经蒸发、浓缩、结晶,得到销酸钾,B正确;硫单质的氧化性较弱,只能将Fe氧化到+2价,C错误;硫元
素在自然界中既有游离态又有化合态,D错误。
3、D。解析:硫的氧化性较弱,与变价金属铁、铜化合时,只能生成低价态的金属硫化物FeS和Cu S。
2
【对点训练2】
1、B。解析:SO 使溴水、酸性KMnO 溶液褪色是因为SO 具有还原性,能使品红褪色是因其漂白性,SO 不
2 4 2 2
能使指示剂褪色,所以A选项错误;B选项正确,因为能使品红褪色的物质很多,不仅仅是SO ;C选项错误,
2
因为这些漂白剂的漂白原理不相同,SO 漂白属于化合型,活性炭属吸附型,漂白粉、NaO 属氧化型;D选项
2 2 2
错误,等物质的量的SO 和Cl 相遇在溶液中反应生成HSO 和HCl,从而失去漂白能力。
2 2 2 4
2、A。解析:SO 气体与水反应生成HSO ,紫色石蕊遇酸变红色,不会变蓝色,故A错误。
2 2 3
3、C。解析:等物质的量的Cl 和SO 混合通入品红与 BaCl 的混合溶液,涉及的化学反应为 Cl +SO +
2 2 2 2 22HO===H SO +2HCl、BaCl +HSO ===BaSO ↓+2HCl,相应的现象是溶液不会褪色,出现白色沉淀。
2 2 4 2 2 4 4
4、
酸性KMnO 氢硫酸(H S溶 滴有酚酞的
反应物 溴水 4 2 石蕊试液 品红溶液
溶液 液) NaOH溶液
褪色 褪色 有浅黄色沉淀
反应现象 褪色 变红 褪色
生成
SO 的性质 还原性 还原性 氧化性 酸性 酸性 漂白性
2
5、①②④⑥⑦⑧⑨⑩
【对点训练3】
1、(1)× (2)×
2、D。解析:可逆反应判断的关键是“两同”:同一条件,同时发生。选项 A、B中的反应为不在同一条件进
行的反应,选项C中的反应为盐酸与氢氧化钠的中和反应,它们都不是可逆反应。
3、< >
【对点训练4】
1、A。解析:SO 不具有漂白性,SO 不能漂白指示剂,两者均可使石蕊溶液变红色,故B错误;SO 不易被空
3 2 2
气中的氧气氧化,只有在催化剂存在下加热才能被氧化为SO ,故D错误;SO 既可与碱反应,也可与碱性氧化
3 3
物反应,故C错误。
2、A。解析:标准状况下,三氧化硫为固态, 1 mol三氧化硫的体积不等于22.4 L;三氧化硫不具有漂白性,
不能使品红溶液褪色;在催化剂、加热的条件下,二氧化硫才能在空气中被氧化为三氧化硫。
【课后作业】
1、A。解析:硫是较活泼的非金属元素,能与许多金属、非金属发生反应。硫与活泼非金属单质氧气反应时,
表现出还原性;硫与金属单质、氢气等反应时,表现出氧化性;硫与变价金属反应时,一般生成低价金属的硫
化物。
2、B。解析:硫单质之间的转化为化学变化,A不正确;不论哪种硫分子,完全燃烧的产物均为二氧化硫,B
正确;S 、S 、S 、S 都是硫元素形成的单质,但是,构成分子的原子数不同,不是同种物质,C不正确;硫单
2 4 6 8
质在空气中加热会燃烧生成二氧化硫,不可能与S 相互转化,D不正确。
2
3、A
4、D。解析:硫与氢气反应需要加热,实验操作复杂,且产物硫化氢有毒;硫与铁反应需要加热,其产物硫化
亚铁固体会附着在试管壁上;硫不溶于水,微溶于酒精,易溶于二硫化碳,试管壁上的硫可用二硫化碳溶解而
除去。
5、D
6、B。解析:二氧化硫是一种酸性氧化物,能与氢氧化钠溶液反应,使含有酚酞的氢氧化钠溶液红色褪去;能
与水反应生成亚硫酸,而使石蕊溶液变为红色,红色不再褪去;二氧化硫具有漂白性,能使品红溶液褪色;二
氧化硫具有还原性,能与溴水反应,使溴水褪色。
7、D。解析:二氧化碳和二氧化硫都能与氢氧化钠溶液、石灰水反应,都不能与饱和食盐水反应。因为亚硫酸
的酸性强于碳酸,可用饱和碳酸氢钠溶液除去二氧化碳中的二氧化硫气体。
8、B。解析:硫黄燃烧生成的二氧化硫具有漂白性,使淡黄色银耳变成洁白如雪的雪耳。
9、D。解析:SO 能与NaOH溶液发生反应生成NaSO 和HO,说明SO 是酸性氧化物,故A正确;SO 与溴
2 2 3 2 2 2
水发生反应的化学方程式为SO +Br +2HO===H SO +2HBr,说明SO 有还原性,故B正确;SO 与HS发生
2 2 2 2 4 2 2 2
反应的化学方程式为SO +2HS===3S+2HO,说明SO 有氧化性,故C正确;SO 能使酸性高锰酸钾溶液褪色,
2 2 2 2 2
是因为发生了氧化还原反应,说明SO 有还原性,故D错误。
2
10、D。解析:SO 使品红溶液褪色,SO 表现了漂白性;SO 使酸性KMnO 溶液、溴水、淀粉碘溶液褪色,
2 2 2 4
SO 表现了还原性;SO 使滴入酚酞的烧碱溶液褪色,SO 表现的是酸性氧化物的性质。所以,反应实质相同的
2 2 2
是②③⑤。
11、C。解析:SO 具有漂白性,能使品红溶液褪色,但是不能漂白酸碱指示剂;SO 具有酸性氧化物的通性,
2 2
能够与水反应生成亚硫酸,在空气中氧化为硫酸,随雨水落下形成酸雨;SO 具有还原性,能使高锰酸钾溶液
2
褪色;SO 中的硫元素化合价处于+4价,具有弱氧化性,能氧化HS:2HS+SO ===3S↓+2HO。故选C。
2 2 2 2 2
12、A。解析:二氧化硫具有氧化性,与NaS反应生成S沉淀;CO与稀NaS溶液不反应,无浑浊;足量HCl
2 2
气体通入稀NaS溶液中发生反应生成氯化钠和硫化氢,但无浑浊;足量CO 气体通入稀NaS溶液中发生反应
2 2 2生成碳酸氢钠和硫化氢,但无浑浊。
13、B。解析:向澄清的石灰水中通入SO 气体,反应的化学方程式是SO (少量)+Ca(OH) ===CaSO ↓+HO,
2 2 2 3 2
对应的离子方程式是Ca2++2OH-+SO ===CaSO ↓+HO,A不正确;过量SO 气体通入氢氧化钠溶液中,反应
2 3 2 2
的化学方程式是SO +NaOH===NaHSO ,对应的离子方程式是SO +OH-===HSO,B正确;SO 气体通入溴水
2 3 2 2
中,反应的化学方程式是SO +Br+2HO===2HBr+HSO ,对应的离子方程式是SO +Br+2HO===4H++2Br
2 2 2 2 4 2 2 2
-+SO,C不正确;氢硫酸中通入氯气,反应的化学方程式是HS+Cl===S↓+2HCl,对应的离子方程式是HS
2 2 2
+Cl===S↓+2H++2Cl-,D不正确。
2
14、C。解析:将NaCO 和NaS配成溶液,再通入SO 可制取NaSO,同时放出CO,并结合S (s)
2 3 2 2 2 2 3 2
+Na SO (aq) NaSO(aq),根据电子守恒,恰好完全反应时发生反应的化学方程式为
2 3 2 2 3
2NaS+Na CO+4SO═3Na SO+CO ;A.在2NaS+Na CO+4SO═3Na SO+CO 中,NaS为还原剂,SO 为氧
2 2 3 2 2 2 3 2 2 2 3 2 2 2 3 2 2 2
化剂,则氧化剂与还原剂的物质的量之比为2︰1,故A正确;B.恰好完全反应时,在
2NaS+Na CO+4SO═3Na SO+CO 中,NaCO 和NaS的物质的量比最佳是1:2,故B正确;C.反应
2 2 3 2 2 2 3 2 2 3 2
2NaS+Na CO+4SO═3Na SO+CO 中2NaS转化为3NaSO,转移8个电子,则生成1molNa SO,转移
2 2 3 2 2 2 3 2 2 2 2 3 2 2 3
mol电子,故C错误;D.如果SO 过量很多,溶液显酸性,而NaSO 在酸性条件下不稳定,生成硫和SO ,
2 2 2 3 2
故D正确;答案为C。
15、C
16、A。解析:SO 、Cl 均具有漂白性,且均与NaHCO 溶液、NaCO 溶液反应生成CO,A项正确。
2 2 3 2 3 2
17、C。解析:根据图示可知,装置中发生的反应有:碳酸钙分解生成氧化钙和二氧化碳;二氧化硫与氧化钙
化合生成亚硫酸钙;亚硫酸钙与氧气反应,既是化合反应,又是氧化还原反应。
18、A。解析:逸出的SO 与C中HO 完全反应:SO +HO===H SO ,加入BaCl 溶液发生反应的方程式为:
2 2 2 2 2 2 2 4 2
HSO +BaCl ===BaSO ↓+2HCl,过滤出BaSO 质量为0.279 6 g。
2 4 2 4 4
SO ~HSO ~BaSO
2 2 4 4
64 233
m(SO ) 0.279 6 g
2
m(SO )=0.076 8 g,则该葡萄酒中SO 的含量为
2 2
=0.256 g·L-1。
19、(1)SO Cl
2 2
(2)2NaOH+SO ===Na SO +HO
2 2 3 2
NaOH+SO ===NaHSO
2 3
(3)2OH-+Cl ===Cl-+ClO-+HO
2 2
(4)溶液变为红色 无明显变化
:解析:具有漂白作用,能使品红溶液褪色的气体有Cl 、SO 、O 等。A气体不能使紫色石蕊溶液褪色,但能使
2 2 3
紫色石蕊溶液变红色,所以A为SO :HO+SO HSO ;B气体使紫色石蕊溶液先变红后褪色,为Cl :HO
2 2 2 2 3 2 2
+Cl===HCl+HClO,HCl使紫色石蕊溶液变红,HClO能使紫色石蕊溶液变为无色。如果将Cl 与SO 等体积
2 2 2
混合,通入溶液中,则发生下列反应:Cl +SO +2HO===H SO +2HCl,生成的盐酸和硫酸都没有漂白作用,
2 2 2 2 4
它们只能使紫色石蕊溶液变红。
20、(1)Cl SO HCl HSO FeCl
2 2 2 4 3
(2)Cl+SO +2HO===2HCl+HSO
2 2 2 2 4
2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
解析:A与HNO 酸化的AgNO 反应产生白色沉淀。A中含Cl-,B与盐酸酸化的BaCl 反应,产生白色沉淀,
3 3 2
B中含SO,又根据X、Y均为有刺激性气味的气体,且X能与Fe反应,则X为Cl,Y为SO ,A为HCl,B为
2 2
HSO ,C为FeCl 。
2 4 3
21、(1)分液漏斗;液柱高度保持不变
(2)c
(3)有浅黄色沉淀生成
(4)Ⅲ;SO +Cl +2HO===4H++SO+2Cl-
2 2 2(5)防止倒吸;NaOH
解析:(1)根据仪器特点,该仪器名称为分液漏斗,液注高度保持不变,说明气密性良好;(2)SO 易溶于水,能
2
与NaSO 溶液、NaHCO 溶液反应,但在NaHSO 溶液中溶解度较小,c项正确;(3)SO 能将S2-氧化,生成硫
2 3 3 3 2
单质,所以现象为有浅黄色沉淀生成;(4)方案Ⅰ,氯水中加入AgNO 溶液也可得到白色沉淀;方案Ⅱ中二氧化
3
硫和氯水均可使品红褪色;方案Ⅲ中产生沉淀可证明 SO 与Cl 发生了氧化还原反应(因溶液显酸性,不会产生
2 2
BaSO 沉淀,而是BaSO 沉淀),选方案Ⅲ;(5)E为安全瓶,防止倒吸;装置F起到吸收尾气中SO 、HS的作用,
3 4 2 2
可选用NaOH溶液。
22、(1)蒸馏烧瓶 Na SO +HSO (浓)===Na SO +SO ↑+HO
2 3 2 4 2 4 2 2
(2)溶液由紫红色变为无色 无色溶液中出现黄色浑浊
还原性 氧化性 5SO +2MnO+2HO===2Mn2++5SO+4H+
2 2
(3)品红溶液褪色后,关闭分液漏斗的活塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH(答案合理即可)