文档内容
氮气与氮的氧化物
【学习目标】
1、掌握氮气的结构、氮气的性质及氮的固定
2、熟悉氮的氧化物,重点理解NO和NO 性质,会进行氮的氧化物溶于水的计算
2
3、熟悉氮的氧化物对环境及人类健康的影响
【主干知识梳理】
一、氮气与氮的固定
1、氮元素的位置、结构
氮的原子结构示意图为 ,位于元素周期表的第二周期、第 Ⅴ A 族。氮原子的最外电子层有 5 个 电
子,既不容易得到3个电子,也不容易失去5个电子。因此,氮原子一般通过共用电子对与其他原子相互结
合构成物质
2、氮元素的存在
既有游离态,又有化合态。氮元素在自然界中主要以氮分子的形式存在于空气中(N 约占空气总体积的78%、
2
总质量的75%),部分氮元素存在于动植物体内的蛋白质中,还有部分氮元素存在于土壤、海洋里的硝酸盐和
铵盐中
3、氮气的物理性质
N 是一种无色、无味的气体,ρ(N )<ρ ,难溶于水
2 2 (空气)
4、氮气的分子结构
电子式: ,结构式:N≡N;氮氮键很难断裂,通常情况下,氮气的化学性很质稳定、不活泼,不
易与其他物质反应
5、氮气的化学性质
常温下氮气很稳定,N 的化学性质很不活泼,很难与其它物质发生反应,但这种稳定是相对的,在一定
2
条件下(如:高温、放电、点燃),也能跟某些物质(如:H、O、Mg等)发生反应
2 2
(1)与氢气反应生成NH :N+3H 2NH
3 2 2 3
(2)与氧气在放电或高温条件下生成NO:N+O 2NO (在闪电时会发生反应)
2 2
N+O=====2NO (在汽车引擎中会发生反应)
2 2
(3)与活泼金属(Mg、Li)反应:3Mg+N=====MgN 6Li+N=====2LiN
2 3 2 2 3
氮化镁与水的反应:MgN+6HO===3Mg(OH) ↓+2NH ↑ (金属氮化物易水解,生成氨气和相应的碱)
3 2 2 2 3
6、氮气的用途
(1)工业上合成氨,制硝酸
(2)代替稀有气体作焊接金属时的保护气,以防止金属被空气氧化
(3)在灯泡中填充氮气以防止钨丝被氧化或挥发
(4)保存粮食、水果等食品,以防止腐烂
(5)医学上用液氮作冷冻剂,以便在冷冻麻醉下进行手术
(6)高科技利用液氮制造低温环境,使某些超导材料获得超导性能
7、氮气的制法
(1)实验室制法:加热NH Cl饱和溶液和NaNO 晶体的混合物:NaNO +NH Cl NaCl+N↑+2HO
4 2 2 4 2 2
(2)工业制法:工业上从液态空气中,利用液态氮的沸点比液态氧的沸点低加以分离而制得氮气
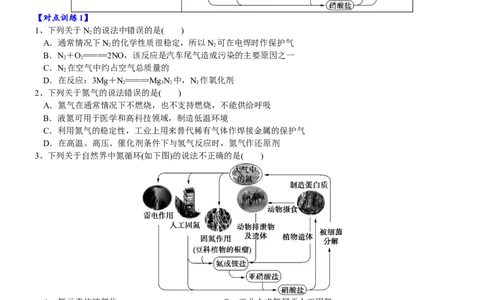
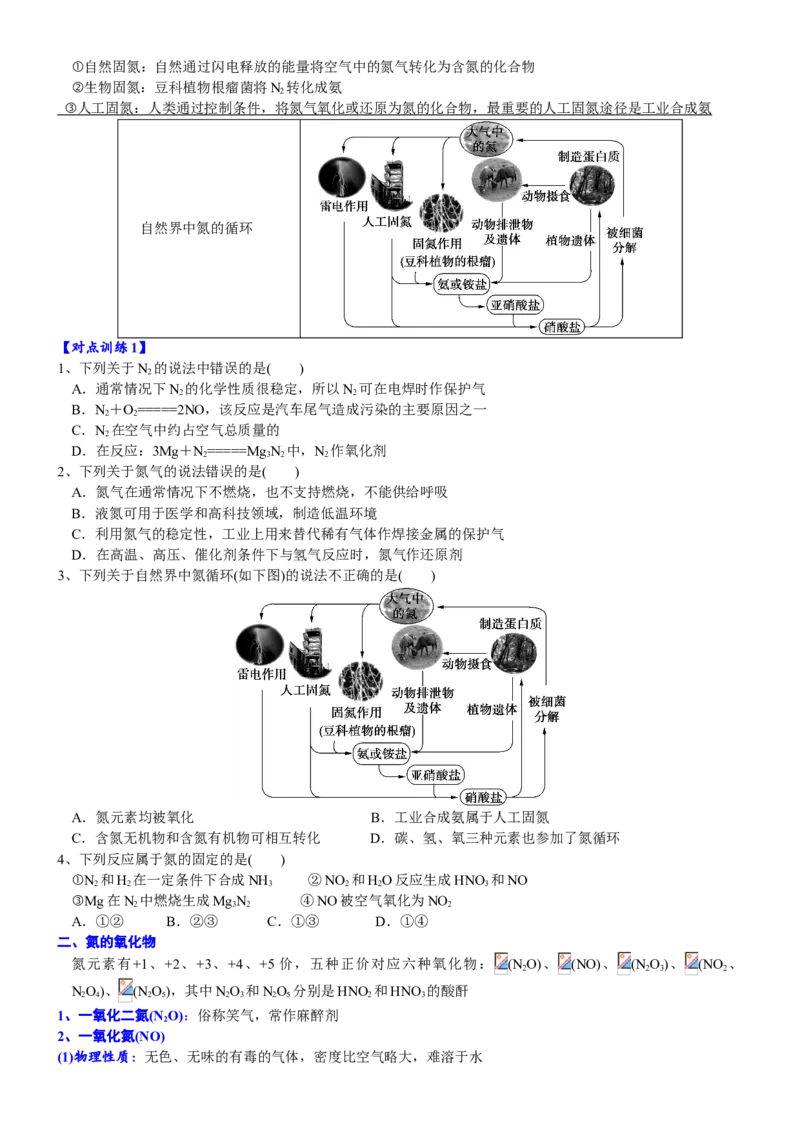
8、氮的固定
(1)概念:将大气中游离态的氮转化为氮的化合物的过程,叫做氮的固定
(2)氮的固定有三种途径①自然固氮:自然通过闪电释放的能量将空气中的氮气转化为含氮的化合物
②生物固氮:豆科植物根瘤菌将N 转化成氨
2
③ 人工固氮:人类通过控制条件,将氮气氧化或还原为氮的化合物,最重要的人工固氮途径是工业合成氨
自然界中氮的循环
【对点训练1】
1、下列关于N 的说法中错误的是( )
2
A.通常情况下N 的化学性质很稳定,所以N 可在电焊时作保护气
2 2
B.N+O=====2NO,该反应是汽车尾气造成污染的主要原因之一
2 2
C.N 在空气中约占空气总质量的
2
D.在反应:3Mg+N=====MgN 中,N 作氧化剂
2 3 2 2
2、下列关于氮气的说法错误的是( )
A.氮气在通常情况下不燃烧,也不支持燃烧,不能供给呼吸
B.液氮可用于医学和高科技领域,制造低温环境
C.利用氮气的稳定性,工业上用来替代稀有气体作焊接金属的保护气
D.在高温、高压、催化剂条件下与氢气反应时,氮气作还原剂
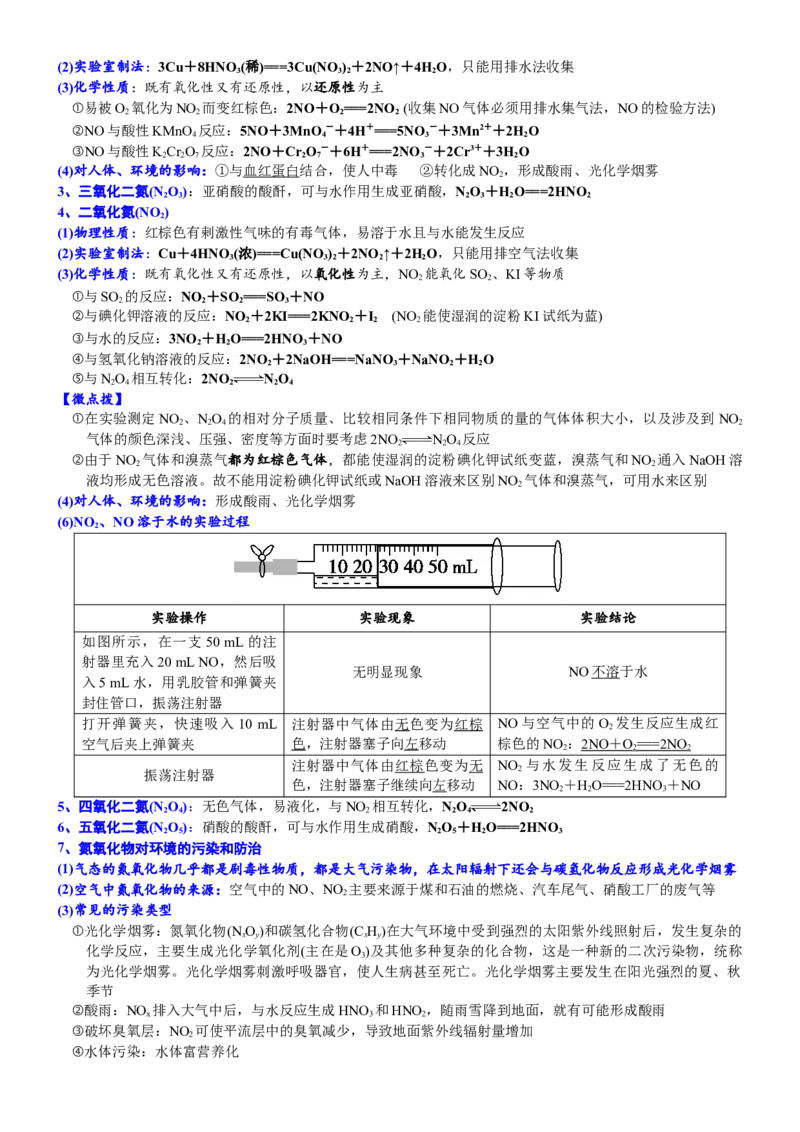
3、下列关于自然界中氮循环(如下图)的说法不正确的是( )
A.氮元素均被氧化 B.工业合成氨属于人工固氮
C.含氮无机物和含氮有机物可相互转化 D.碳、氢、氧三种元素也参加了氮循环
4、下列反应属于氮的固定的是( )
①N 和H 在一定条件下合成NH ②NO 和HO反应生成HNO 和NO
2 2 3 2 2 3
③Mg在N 中燃烧生成MgN ④NO被空气氧化为NO
2 3 2 2
A.①② B.②③ C.①③ D.①④
二、氮的氧化物
氮元素有+1、+2、+3、+4、+5 价,五种正价对应六种氧化物: (N O)、 (NO)、 (NO)、 (NO 、
2 2 3 2
NO)、 (N O),其中NO 和NO 分别是HNO 和HNO 的酸酐
2 4 2 5 2 3 2 5 2 3
1、一氧化二氮(N O):俗称笑气,常作麻醉剂
2
2、一氧化氮(NO)
(1)物理性质:无色、无味的有毒的气体,密度比空气略大,难溶于水(2)实验室制法:3Cu+8HNO (稀)===3Cu(NO )+2NO↑+4HO,只能用排水法收集
3 3 2 2
(3)化学性质:既有氧化性又有还原性,以还原性为主
①易被O 氧化为NO 而变红棕色:2NO+O===2NO (收集NO气体必须用排水集气法,NO的检验方法)
2 2 2 2
②NO与酸性KMnO 反应:5NO+3MnO -+4H+===5NO -+3Mn2++2HO
4 4 3 2
③NO与酸性KCr O 反应:2NO+CrO-+6H+===2NO -+2Cr3++3HO
2 2 7 2 7 3 2
(4)对人体、环境的影响:①与血红蛋白结合,使人中毒 ②转化成NO ,形成酸雨、光化学烟雾
2
3、三氧化二氮(N O):亚硝酸的酸酐,可与水作用生成亚硝酸,NO+HO===2HNO
2 3 2 3 2 2
4、二氧化氮(NO)
2
(1)物理性质:红棕色有剌激性气味的有毒气体,易溶于水且与水能发生反应
(2)实验室制法:Cu+4HNO (浓)===Cu(NO )+2NO ↑+2HO,只能用排空气法收集
3 3 2 2 2
(3)化学性质:既有氧化性又有还原性,以氧化性为主,NO 能氧化SO 、KI等物质
2 2
①与SO 的反应:NO +SO ===SO +NO
2 2 2 3
②与碘化钾溶液的反应:NO
2
+2KI===2KNO
2
+I
2
(NO
2
能使湿润的淀粉KI试纸为蓝)
③与水的反应:3NO +HO===2HNO +NO
2 2 3
④与氢氧化钠溶液的反应:2NO +2NaOH===NaNO +NaNO +HO
2 3 2 2
⑤与NO 相互转化:2NO NO
2 4 2 2 4
【微点拨】
①在实验测定NO 、NO 的相对分子质量、比较相同条件下相同物质的量的气体体积大小,以及涉及到 NO
2 2 4 2
气体的颜色深浅、压强、密度等方面时要考虑2NO NO 反应
2 2 4
②由于NO 气体和溴蒸气都为红棕色气体,都能使湿润的淀粉碘化钾试纸变蓝,溴蒸气和NO 通入NaOH溶
2 2
液均形成无色溶液。故不能用淀粉碘化钾试纸或NaOH溶液来区别NO 气体和溴蒸气,可用水来区别
2
(4)对人体、环境的影响:形成酸雨、光化学烟雾
(6)NO、NO溶于水的实验过程
2
实验操作 实验现象 实验结论
如图所示,在一支50 mL的注
射器里充入20 mL NO,然后吸
无明显现象 NO不溶于水
入5 mL水,用乳胶管和弹簧夹
封住管口,振荡注射器
打开弹簧夹,快速吸入 10 mL 注射器中气体由无色变为红棕 NO与空气中的O 发生反应生成红
2
空气后夹上弹簧夹 色,注射器塞子向左移动 棕色的NO : 2NO + O == =2NO
2 2 2
注射器中气体由红棕色变为无 NO 与水发生反应生成了无色的
振荡注射器 2
色,注射器塞子继续向左移动 NO:3NO +HO===2HNO +NO
2 2 3
5、四氧化二氮(N O):无色气体,易液化,与NO 相互转化,NO 2NO
2 4 2 2 4 2
6、五氧化二氮(N O):硝酸的酸酐,可与水作用生成硝酸,NO+HO===2HNO
2 5 2 5 2 3
7、氮氧化物对环境的污染和防治
(1)气态的氮氧化物几乎都是剧毒性物质,都是大气污染物,在太阳辐射下还会与碳氢化物反应形成光化学烟雾
(2)空气中氮氧化物的来源:空气中的NO、NO 主要来源于煤和石油的燃烧、汽车尾气、硝酸工厂的废气等
2
(3)常见的污染类型
①光化学烟雾:氮氧化物(NO)和碳氢化合物(CH)在大气环境中受到强烈的太阳紫外线照射后,发生复杂的
x y x y
化学反应,主要生成光化学氧化剂(主在是O)及其他多种复杂的化合物,这是一种新的二次污染物,统称
3
为光化学烟雾。光化学烟雾刺激呼吸器官,使人生病甚至死亡。光化学烟雾主要发生在阳光强烈的夏、秋
季节
②酸雨:NO 排入大气中后,与水反应生成HNO 和HNO,随雨雪降到地面,就有可能形成酸雨
x 3 2
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加
2
④水体污染:水体富营养化(4)常见的NO 尾气处理方法
x
①碱液吸收法:2NO +2NaOH===NaNO +NaNO +HO NO +NO+2NaOH===2NaNO +HO
2 3 2 2 2 2 2
NO 、NO的混合气能被足量烧碱溶液完全吸收的条件是:n(NO )≥n(NO)。一般适合工业尾气中NO 的处理
2 2 x
②催化转化:在催化剂、加热条件下,氨可将氮氧化物转化为无毒气体(N )或NO 与CO在一定温度下催化转
2 x
化为无毒气体(N 和CO)。一般适用于汽车尾气的处理
2 2
【对点训练2】
1、最新的病毒学研究证实,一氧化氮对SARS病毒有直接抑制作用。下列关于一氧化氮的叙述正确的是( )
A.一氧化氮是一种红棕色气体
B.常温常压下,一氧化氮不能与空气中的氧气直接化合
C.一氧化氮可由氮气和氧气在放电条件下直接化合得到
D.一氧化氮易溶于水,不能用排水法收集
2、已知某厂排放的尾气中NO、NO 的体积比为1∶1,该厂采用NaOH溶液来处理该尾气,处理后所得溶液中只
2
有一种含氮的钠盐。则该含氮的钠盐中,氮元素的化合价为( )
A.-3 B.+1 C.+3 D.+5
3、发射卫星的运载火箭,其推进剂引燃后发生剧烈反应,产生的大量高温气体从火箭尾部喷出。引燃后产生的
高温气体主要是CO 、HO、N 、NO,这些气体均为无色,但在卫星发射现场看到火箭喷出大量红烟。产生
2 2 2
红烟的原因是( )
A.高温下N 遇空气生成NO B.NO遇空气生成NO
2 2 2
C.CO 与NO反应生成CO和NO D.NO和HO反应生成H 和NO
2 2 2 2 2
4、如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但
不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被
水充满。原来试管中盛装的( )
A.可能是N 与NO 的混合气体 B.可能是O 与NO 的混合气体
2 2 2 2
C.不可能是NO与NO 的混合气体 D.只能是NO 一种气体
2 2
5、下列关于NO和NO 的说法正确的是( )
2
A.NO 是红棕色气体,易溶于水,属于酸性氧化物
2
B.NO 可由N 和O 直接化合得到
2 2 2
C.NO和NO 均既可以用排空气法收集又可以用排水法收集
2
D.NO和NO 在一定条件下可以相互转化
2
6、诺贝尔化学奖曾授予德国化学家Gerhard Ertl,以表彰他对固体表面化学研究过程中的重大发现。使CO、
NO 等在铂表面发生化学反应转变成无毒气体,以减少汽车尾气中有毒气体的排放,正是此项研究的重要应
x
用之一。下列有关说法不正确的是( )
A.CO在铂表面被氧化生成CO,铂起催化作用 B.汽车尾气中的NO 在铂表面发生反应的产物是N
2 x 2
C.CO在铂表面可能和O、NO 反应 D.NO、CO、CO 均能与人体中的血红蛋白结合
2 x x 2
三、氮的氧化物和氧气、水的反应与计算
类型1、NO (或NO 与N 的混合气体)溶于水
2 2 2
1、计算依据:①3NO +HO===2HNO +NO
2 2 3
例1、将20ml充满NO和NO 的混合气体的试管倒立于盛水的水槽中,充分反应后,剩余气体的体积变为
2
10ml,求原混合气体中NO和NO 各占多少毫升?
2类型2、NO 和O 的混合气体溶于水
2 2
1、计算依据: 3NO +HO===2HNO +NO ①
2 2 3
2NO+O===2NO ②
2 2
由方程式①×2+②得:4NO +O+2HO===4HNO ③
2 2 2 3
2、讨论法:由总反应③可知
V(NO )∶V(O )
2 2
例2、将充满NO 和O 的混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的
2 2
一半处停止了,则原混合气体中NO 和O 的体积比是多少?
2 2
类型3、NO和O 的混合气体溶于水
2
1、计算依据: 2NO+O===2NO ①
2 2
3NO +HO===2HNO +NO ②
2 2 3
由方程式①×3+②×2得:4NO+3O+2HO===4HNO ③
2 2 3
2、讨论法:由总反应③可知
V(NO)∶V(O )
2
例3、一定条件下,将等体积的NO和O 混合于一试管中,然后将试管倒立于盛有水的水槽中,充分反应后剩
2
余气体的体积与原混合气体的体积之比是多少?
类型4、NO、NO 和O 三种混合气体同时通入水中
2 2
1、计算依据: 3NO +HO===2HNO +NO
2 2 3
4NO+3O+2HO===4HNO
2 2 3
2、假设法:假设NO 与水先反应,按反应3NO +HO===2HNO +NO,求出生成NO的体积,再加上原混合气
2 2 2 3
体中NO的体积,得NO的总体积,最后按反应4NO+3O+2HO===4HNO 进行计算
2 2 3
例4、常温下盛有10mlNO 和10mlNO组成的混合气体的大试管倒立于水中,当缓缓通入O 一段时间后,试管
2 2
内残留2ml气体,则通入O 体积可能为多少毫升?
2
四、酸雨及防治
1、SO 、NO 的主要来源、危害和防治
2 x(1)来源
①SO :主要来源于煤、石油和某些含硫的金属矿物的燃烧或冶炼
2
②NO:主要来源于机动车产生的尾气
x
(2)SO 、NO 对人体的危害
2 x
①SO 与NO 会引起呼吸道疾病,危害人体健康,严重时会使人死亡
2 x
②溶于水形成酸雨
(3)防治
①调整能源结构,发展清洁能源
②研究煤的脱硫技术,改进燃烧技术,减少二氧化硫和氮氧化物的排放
③加强工厂废气的回收处理
④改进汽车尾气的处理技术,控制尾气排放
2、酸雨
(1)概念:pH小于5.6的雨水
(2)成因:主要是大气中SO 和NO 的溶于雨水形成的
2 2
(3)类型
①硫酸型:SO ―→ HSO ―→ HSO ,化学方程式:SO +HO HSO ,2HSO +O===2HSO
2 2 3 2 4 2 2 2 3 2 3 2 2 4
②硝酸型:NO ―→HNO,化学方程式: 3NO +HO===2HNO +NO
2 3 2 2 3
(4)危害
①直接损伤农作物,破坏森林、草原,使土壤、湖泊酸化
②会加速建筑物、桥梁、工业设备、运输工具及通信电缆的腐蚀
(5)酸雨防治
①工业废气排放到大气中之前,必须进行适当处理,防止有害物质污染大气
②减少化石燃料的直接燃烧,如脱硫处理
【对点训练4】
1、酸雨形成的最主要原因是( )
A.森林遭乱砍滥伐,破坏了生态平衡 B.工业上大量燃烧含硫燃料
C.大气中二氧化碳的含量增多 D.汽车排出大量尾气
2、下列污染现象主要与二氧化硫有关的是( )
A.酸雨 B.光化学烟雾 C.臭氧层空洞 D.温室效应
【课后作业】
1、将空气中的氮气转化成氮的化合物的过程称为固氮。能实现人工固氮的是( )
A.雷雨天闪电 B.NH 催化氧化制NO C.豆科植物根瘤菌 D.工业合成氨
3
2、关于氮气的性质说法中错误的是( )
A.氮在自然界中既以游离态存在又以化合态存在
B.通常情况下,氮气性质很不活泼
C.可在氧气中燃烧生成一氧化氮
D.大气、陆地和水体中的氮元素在不停地进行着氮的循环
3、在二氧化氮被水吸收的反应中,发生还原反应和氧化反应的物质的量之比是( )
A.3∶1 B.1∶3 C.1∶2 D.2∶1
4、下列关于NO的叙述正确的是( )
A.NO易溶于水,所以可用排空气法收集 B.NO是一种有刺激性气味的红棕色气体
C.常温常压下,含等质量氧元素的NO和CO的体积相等 D.NO不能通过化合反应获得
5、下列关于氮的氧化物的说法中,正确的是( )
A.氮的氧化物都是酸性氧化物
B.氮的氧化物都既有氧化性,又有还原性
C.NO 与 HO 反应生成 HNO,所以 NO 是酸性氧化物
2 2 3 2
D.NO 和 NO 均有毒
2
6、下列物质的转化必须加入氧化剂且通过一步反应就能完成的是( )
①N→NO ②NO →NO ③NO →HNO ④N→NO ⑤N→NH
2 2 2 2 3 2 2 3A.① B.②⑤ C.④ D.③④
7、湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体可能是下列气体中的( )
①Cl ②NO ③HS ④SO ⑤溴蒸气 ⑥HCl
2 2 2 2
A.①③④ B.①②⑤ C.①②⑥ D.②④⑥
8、常温下,将充满等体积混合气体的试管倒立在水槽中,试管内气体体积不会明显减少的是( )
① ② ③ ④ ⑤ ⑥
NO、O NO 、O CO、O NH 、O Cl、SO N、NO
2 2 2 2 3 2 2 2 2
A.③⑥ B.④⑤ C.②③ D.①④
9、标准状况下,使NO 和O 按4︰1的体积比充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧
2 2
瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为( )
A. mol·L-1 B. mol·L-1 C. mol·L-1 D. mol·L-1
10、按图进行实验。试管中装有12 mL NO,然后间歇而又缓慢地通入8 mL O ,下列是有关最终状态的描述:
2
①试管内气体呈红棕色 ②试管内气体呈无色 ③试管内液面不变 ④试管内液面上升 ⑤试管内气体是 O
2
⑥试管内气体是NO。其中正确的是( )
A.①③ B.②④⑤ C.②④⑥ D.②③⑤
11、将盛有30 mL NO和NO 混合气体的试管倒置于放满水的水槽中,最后试管中气体的体积是20 mL,则原混
2
合气体中NO的体积是( )
A.24 mL B.15 mL C.18 mL D.12 mL
12、将盛有N 和NO 混合气体的试管倒立于水中,经过足够长的时间后,试管内气体的体积缩小为原来的一半,
2 2
则原混合气体中N 和NO 的体积比是( )
2 2
A.1∶1 B.1∶2 C.1∶3 D.3∶1
13、在一定温度和压强下,将一容积为15 mL的试管充满NO 后,倒置于一个盛有水的水槽中。当试管内液面
2
上升至一定高度不再变化时,在相同条件下再通入O,若要使试管内液面仍保持在原高度,则通入O 的体积
2 2
为( )
A.3.75 mL B.7.5 mL C.8.75 mL D.10.5 mL
14、在一定条件下,将m体积NO和n体积O 同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残
2
留体积的气体,该气体与空气接触后变为红棕色,则m与n的比值为( )
A.3∶2 B.2∶3 C.8∶3 D.3∶8
15、将盛有1 mol NO和NO 混合气体的试管倒立于盛满水的水槽中,再通入0.4 mol O ,充分反应后,整个试
2 2
管充满水。则原混合气体中NO与NO 体积比为( )
2
A.1∶2 B.3∶7 C.2∶5 D.无法确定
16、在一定条件下,将NO 和O 的混合气体12mL通入足量水中,充分反应后剩余2mL气体(同温同压下),则
2 2
原混合气体中氧气的体积为( )
A.1.2mL B.2.4mL C.3mL D.4mL
17、空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施
不利于“蓝天工程”建设的是( )
A.推广使用燃煤脱硫技术,防治SO 污染 B.实施绿化工程,防止扬尘污染
2
C.研制开发燃料电池汽车,消除机动车尾气污染 D.加大石油、煤炭的开采速度,增加化石燃料的供应量
18、我国城市环境中的大气污染主要是( )
A.二氧化碳、氯化氢、酸雨 B.二氧化硫、一氧化碳、二氧化氮、烟尘
C.二氧化氮、一氧化碳、氯气 D.二氧化硫、二氧化碳、氮气、粉尘
19、以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
选项 氧化物 环境问题 主要来源
A CO 酸雨 化石燃料的燃烧
2
B SO 光化学烟雾 汽车尾气的排放
2C NO 温室效应 工厂废气的排放
2
D CO CO中毒 燃料的不完全燃烧
20、将一支盛有a mL NO和b mL NO 气体的试管倒立于水槽中,然后通入a mL O ,问:
2 2
(1)若a=b,则充分反应后试管内气体体积为________ mL
(2)若a<b,则充分反应后试管内气体体积为________ mL
(3)若a>b,则充分反应后试管内气体体积为________ mL
21、氮氧化合物(用NO 表示)是大气污染的重要因素,根据NO 的性质特点,开发出多种化学治理氮氧化合物
x x
污染的方法。
(1)用氨可将氮氧化物转化为无毒气体。已知:4NH +6NO=====5N +6HO,8NH +6NO =====7N +12HO。
3 2 2 3 2 2 2
同温同压下,3.5LNH 恰好将3.0LNO和NO 的混合气体完全转化为N,则原混合气体中NO和NO 的体积之
3 2 2 2
比是________
(2)工业尾气中氮的氧化物常采用碱液吸收法处理。
① NO 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比 1∶1,写出该反应的化学方程式:
2
________________
②NO与NO 按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,该钠盐的化学式是______
2
(3)纯碱溶液也能用于处理氮氧化合物废气,反应原理与上述(2)类似,同时产生CO。
2
①请写出纯碱溶液吸收NO 的化学方程式:____________________________
2
②现有一定量的某工业废气,其中含有 3.36LNO 、1.12LNO(已换算为标准状况,假设不含 NO),恰好被
2 2 4
200mL碳酸钠溶液吸收,所得盐的物质的量分别为________、________,该碳酸钠溶液的物质的量浓度为
_____mol/L
【氮气与氮的氧化物】答案
【对点训练1】
1、C。解析:N 在空气中约占空气总体积的,C错误
2
2、D。解析:氮气的化学性质很稳定,在通常情况下不燃烧,也不支持燃烧,不能供给呼吸,A项正确;液氮
汽化吸热,可用于制造低温环境,B项正确;氮气的化学性质很稳定,可用作焊接金属的保护气,C项正确;
氮气与氢气生成氨气的反应中,N的化合价从0降低到-3,作氧化剂,D项错误。]
3、A。解析:A.N→NH 过程中氮元素由0价变为-3价,被还原。B.工业合成氨的过程属于人工固氮。C.1828
2 3
年,德国化学家维勒首次利用无机物氰酸铵合成了尿素;而含氮的有机物也可以直接分解为无机物。D.雷电发
生时涉及的反应有N +O=====2NO,2NO+O===2NO,3NO +HO===2HNO +NO,HNO3进入土壤,与矿物
2 2 2 2 2 2 3
质结合成硝酸盐;豆科植物也可以将N2合成氮肥,生物体内含有C元素,所以碳、氢、氧三种元素都参加了
氮循环。
4、C。解析:氮的固定是将游离态的氮转化为化合态的氮。
【对点训练2】
1、C。解析:NO是一种无色难溶于水的气体,可以用排水法收集;常温常压下,NO容易与氧气直接化合生成
NO 。
2
2、C。解析:体积比为1∶1的NO、NO 通入NaOH溶液中只生成一种产物,反应后的化合价应介于+2价和+4
2
价之间,应为+3价,发生反应的化学方程式为NO+NO +2NaOH===2NaNO +HO。
2 2 2
3、B。解析:高温下N 遇空气不会直接生成NO ,A错误;NO遇氧气发生反应2NO+O===2NO ,生成红棕
2 2 2 2
色的NO ,B正确;高温条件下一氧化碳在空气中不可能为反应产物,CO 与NO高温条件下不反应,C错误;
2 2
一氧化氮和水之间不会发生反应,D错误。]
4、B。解析:若是N 与NO 的混合气体,无论鼓入多少氧气,最后都有N 剩余,试管内不可能完全被水充满;
2 2 2
若是O 与NO 的混合气体,由4NO +O+2HO===4HNO ,水可以充满试管;若是NO与NO 的混合气体通入
2 2 2 2 2 3 2
适量O,水可以充满试管。]
2
5、D。解析:NO 不是酸性氧化物,A项错误;在高温或放电条件下,N 和O 直接化合生成NO,NO与O 反
2 2 2 2
应生成NO ,B项错误;NO易与空气中的氧气反应生成NO ,只能用排水法收集,NO 能与水反应,只能用排
2 2 2
空气法收集,C项错误;NO和O 反应生成NO ,NO 与HO反应生成HNO 和NO,D项正确。
2 2 2 2 3
6、D。解析:CO、NO 在铂表面发生的反应为CO+NOCO +N(未配平),也可能是CO与O 反应,此过程中
x x 2 2 2铂作催化剂;CO 不能与人体中的血红蛋白结合。
2
三、氮的氧化物和氧气、水的反应与计算
例1、NO:5ml ,NO :15ml
2
例2、2:3
例3、1:8
例4、12ml或8.5ml
【对点训练4】
1、B。解析:空气中硫的氧化物和氮的氧化物随雨水降下就形成酸雨。酸雨的形成主要是由于空气中SO 和
2
NO 的增多。在我国主要是SO 的增多。空气中SO 的主要来源是①化石燃料(煤和石油产品)的燃烧;②含硫矿
x 2 2
石的冶炼;③硫酸、磷肥、纸浆厂的工业废气。目前,由于汽车用的燃料汽油、柴油等都经过了脱硫处理,所
以形成酸雨的最主要原因是工业上大量燃烧含硫燃料
2、A。解析:光化学烟雾主要是由汽车排出的氮氧化物、碳氢化合物等造成的;臭氧层空洞是由氟氯代烃等的
排放引起的;温室效应主要是由大气中CO 含量的不断增加造成的。
2
【课后作业】
1、D
2、C。解析:通常情况下氮气的性质很不活泼,在放电或高温条件下,能跟氧气反应。
3、C。解析:二氧化氮与水反应生成硝酸和一氧化氮,氧化剂和还原剂都是二氧化氮,发生还原反应和氧化反
应的物质的量之比为1∶2。
4、C。解析:NO易于被氧气氧化,不能使用排空气法收集;NO是一种无色无味的气体;常温常压下,NO能
与空气中的氧气直接化合生成二氧化氮。故选C。
5、D。解析:NO、NO 等不是酸性氧化物;NO 中氮元素为最高价,只有氧化性;NO 与HO反应生成HNO
2 2 5 2 2 3
时N的价态发生了变化,故NO 不是酸性氧化物。
2
6、C。解析 该题有两个要求:(1)必须加入氧化剂;(2)通过一步反应就能完成。反应①、③、④从化合价角度
来看都是升高,但反应①N→NO 不能通过一步反应完成;而反应③NO →HNO 虽然氮的化合价升高,但不加
2 2 2 3
氧化剂也能完成,如3NO +HO===2HNO +NO,在该反应中,NO 既是氧化剂又是还原剂;只有反应
2 2 3 2
④N→NO必须加入氧化剂且通过一步反应就能完成。
2
7、B。解析:显蓝色表明接触过程中发生氧化还原反应生成了单质I。其反应如下:①Cl+2KI===I +2KCl,
2 2 2
②3NO +HO===2HNO +NO,HNO 将KI氧化成I,⑤Br +2KI===I +2KBr。
2 2 3 3 2 2 2
8、A。解析:NO、O 倒扣在水槽中发生反应4NO+3O +2HO===4HNO ,HNO 易溶于水会导致试管内气体
2 2 2 3 3
体积会明显减少水面明显上升;NO 、O 倒扣在水槽中发生反应4NO +O +2HO===4HNO ,会导致试管内气
2 2 2 2 2 3
体体积会明显减少水面明显上升;CO、O 倒扣在水槽中不发生反应,故试管内气体体积不会明显减少;NH 、
2 3
O 倒扣在水槽中,氨气极易溶于水会导致试管内气体体积会明显减少水面明显上升;Cl 、SO 倒扣在水槽中发
2 2 2
生反应Cl +SO +2HO===2HCl+HSO ,会导致试管内气体体积会明显减少水面明显上升;N 、NO倒扣在水
2 2 2 2 4 2
槽中均不溶于水且不与水反应,故试管内气体体积不会明显减少,则本题选A。
9、C。解析:根据4NO +O +2HO===4HNO 可知,当NO 和O 体积比为4︰1时,二者恰好完全与水反应,
2 2 2 3 2 2
此时水能充满整个烧瓶。设烧瓶容积为V,则混合气体的物质的量n(混)= mol,n(NO )=× mol。据上述方程式
2
可知:生成硝酸的物质的量n(HNO)=× mol,则c(HNO)== mol·L-1。
3 3
10、C。解析:根据4NO+3O+2HO===4HNO 可得,剩余气体应为NO,体积为 mL,试管内液面上升。
2 2 3
11、B。解析:NO 与水反应3NO +HO===2HNO +NO,设原混合气体中NO与NO 的体积分别为x、y,则据
2 2 2 3 2
题意,剩余气体体积20 mL是原NO气体与上述反应生成的NO气体的总体积,列方程即可得NO和NO 体积
2
都是15 mL。
12、C。解析:将试管倒立于水中,只有NO 和HO反应,生成的NO与不反应的N 为剩余气体。设原混合气
2 2 2
体的体积为V,NO 的体积为x,根据差量法求解:
2
3NO +HO===2HNO +NO ΔV
2 2 3 减
3 1 2
x
解得:x=,V(N )=V-=,故=。
2
13、C。解析:15 mL NO 与水反应后生成5 mL NO,根据反应4NO+3O+2HO===4HNO ,使5 mL NO完全
2 2 2 3
被氧化需O 体积为5 mL×=3.75 mL。据题意,通入的O 应过量5 mL,则共需通入O 8.75 mL。
2 2 214、C。解析:气体与空气接触后变为红棕色,说明反应后 NO是过量的。NO和氧气同时通入水中的化学方程
式是4NO+3O +2HO===4HNO ,所以参加该反应的NO是,所以氧气的体积是×=n,所以m与n的比值为
2 2 3
8∶3。
15、B。解析:设 1 mol NO 和 NO 的混合气体中有 a mol NO 和(1-a) mol NO ,根据 4NO+3O +
2 2 2
2HO===4HNO 和4NO +O +2HO===4HNO 可得:a+=0.4,解得a=0.3,因此V(NO)∶V(NO )=3∶7,故选
2 3 2 2 2 3 2
B。
16、AD。解析:首先分析剩余的2mL气体有两种可能。如果剩余2mLO ,则V(NO)=×(12-2) mL=8mL,则
2 2
混合气中:V(O )=12mL-8mL=4mL。若剩余的2mL气体是NO,则混合气中的V(O )=(12mL-2mL×3)×=
2 2
1.2mL。
17、D。解析:A、B、C都是可采取的措施,在D中,若加大不可再生资源石油、煤的开采,会造成资源缺乏,
同时会使空气中SO 、NO 的含量增加。
2 x
18、B。解析:常见的大气污染物是氮的氧化物、硫的氧化物、一氧化碳及烟尘。
19、D。解析:A项,二氧化碳是造成温室效应的气体,造成酸雨的气体是二氧化硫及氮氧化物,错误;B项,
氮的氧化物是造成光化学烟雾的气体,错误;C项,二氧化碳是造成温室效应的气体,错误;D项,CO有毒,
主要来自燃料的不完全燃烧,正确。
20、(1)0 (2) (3)
解析:(1)根据反应:4NO +O +2HO===4HNO 4NO+3O +2HO===4HNO ,a mL NO和b mL NO 气体的试
2 2 2 3, 2 2 3 2
管倒立于水槽中,然后通入a mL O ,若a=b,对于两个反应中的气体均会转化为硝酸,所以试管中气体的体
2
积是0;(2)若a<b,则二氧化氮会有剩余,a mL NO消耗氧气是 mL,所以剩余二氧化氮是(b-a) mL,根据
3NO +HO===2HNO +NO,则生成NO的体积是;(3)若a>b,则此时一氧化氮和二氧化氮均参加了的反应,
2 2 3
氧气会剩余,根据反应4NO +O +2HO===4HNO 、4NO+3O +2HO===4HNO ,a mL NO和b mL NO 气体
2 2 2 3 2 2 3 2
消耗氧气的体积是:,所以剩余氧气的体积是:。
21、(1)1∶3
(2)①2NO +2NaOH===NaNO +NaNO +HO ②NaNO
2 3 2 2 2
(3)①Na CO +2NO ===NaNO +NaNO +CO ②NaNO :0.05mol NaNO :0.15mol 0.5mol·L-1
2 3 2 3 2 2 3 2
解析:(1)设NO的体积为V(NO),NO 的体积为V(NO),依据方程式知,处理NO需NH :V(NO),处理NO
2 2 3 2
需NH :V(NO),则
3 2
解得V(NO)=0.75L
V(NO)=2.25L
2
V(NO)∶V(NO )=1∶3。
2
(2)①生成两种钠盐,必然是NO 的歧化反应,依据量的关系可知两种盐分别为NaNO 和NaNO 。
2 3 2
②NO中氮的化合价为+2价,NO 中氮的化合物为+4价,二者1∶1混合时与NaOH反应生成一种钠盐,依据电
2
子守恒可知,钠盐中氮的化合价为+3,即为NaNO 。
2
(3)②n(NO)=0.15mol,n(NO)=0.05mol
2
Na2CO3+NO2+NO===2NaNO2+CO
2
则单独与NaCO 反应的NO 为0.15mol-0.05mol=0.1mol
2 3 2
Na2CO3+2NO2===NaNO3+NaNO2+CO
2
所以共生成NaNO :0.05mol,NaNO :0.15mol
3 2
c(Na CO)==0.5mol·L-1。
2 3