文档内容
绝密★启用前
江西省 2025—2026学年度第一学期期中考试
高 一 化 学 试 卷
试卷共6页,18小题,满分100分。考试用时75分钟。
注意事项:
1.考查范围:必修第一册第一章和第二章第一、二节氯气的性质。
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
可能用到的相对原子质量:H—1 O—16 Na—23 S—32 Cl—35.5
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.历史承载过去,也启迪未来。下列技艺中涉及氧化还原反应的是
A.古代织布机织布 B.古法炼铁 C.磨黄豆浆 D.雕刻窗花
2.常温下,下列离子在水溶液中能大量共存的是
A.Na+、HCO-、OH- B.H+、CO2-、SO2- C.Ca2+、Cl-、NO- D.Ba2+、OH-、SO2-
3 3 4 3 4
3.江西古代科技奇才宋应星所著的《天工开物》是古代中国技术的百科全书,其中涉及了硝石
(KNO)、铁、胡粉[2PbCO·Pb(OH)]、绿矾(FeSO·7HO)等多种物质。下列说法错误的是
3 3 2 4 2
A.铁粉在潮湿的空气中易被氧化
B.2PbCO·Pb(OH)能与稀盐酸反应
3 2
C.FeSO·7HO属于混合物
4 2
D.利用交叉分类法分类,KNO 可分类为钾盐和硝酸盐
3
4.下列检验 NaCl固体中是否含有 KCl的操作错误的是
盐酸清洗铂丝 灼烧
A.溶解固体 B.将铂丝处理干净 C.蘸取待测液 D.观察焰色
高一化学 第 1页(共6页)
书书书5.劳动创造是人类最基本和最重要的社会实践。下列所述化学知识正确且与劳动项目有关联
的是
选项 劳动项目 化学知识
A 用生石灰制作简易干燥剂 生石灰与水反应放出大量的热
B 用“洁厕灵”(主要成分是稀盐酸)除碳酸钙型水垢 CaCO+2HClCaCl+CO↑+HO
3 2 2 2
C 制作烟花时添加碳酸锂作着色剂 碳酸锂受热易分解
D 用钢瓶储存液氯 Fe与氯水在常温下不反应
6.化学是一门以实验为基础的科学。下列说法正确的是
A.实验室中,少量金属 Na保存在装有煤油的细口瓶中
B.金属 Na着火常用湿润的砂子灭火
C.在实验室中进行 Na与 Cl的实验,该实验的安全提示图标中无
2
D.可以将 Na置于坩埚中加热进行 Na在空气中燃烧的实验
7.下列物质之间的转化关系能够实现的是
HO Na NaCl溶液 稀硝酸
A.NaO 2 →O →NaO B.AgNO →AgCl→HCl
2 2 2 2 3
Cl NaOH溶液 O HO
C.Fe→ 2 FeCl→Fe(OH) D.Cu→ 2 CuO 2 →Cu(OH)
△ 2 2 △ 2
电解
8.工业上采用电解饱和食盐水的方法制备 Cl:2NaCl+2HO2NaOH+Cl↑+H↑。下列说
2 2 2 2
法正确的是
A.HO发生了氧化反应
2
B.若消耗36gHO,则会生成2g还原产物
2
C.纯净的 H 能在 Cl中安静地燃烧,产生大量白烟
2 2
2e-
↓
电解
D.该反应的电子转移情况可表示为2NaCl+2HO2NaOH+Cl↑+H↑
2 2 2
9.下列反应的离子方程式书写正确的是
A.向少量铜粉中滴加稀硫酸:Cu+2H+Cu2++H↑
2
B.过量 CO 与稀 NaOH溶液反应:2OH-+CO CO2-
2 2 3
C.少量Ca(HCO)溶液与过量NaOH溶液反应:2HCO-+2OH-+Ca2+CaCO↓+CO2-+2HO
3 2 3 3 3 2
D.Mg与 AgNO 溶液反应:Mg+Ag+Mg2++Ag
3
10.“价—类”二维图是一种在高中化学中广泛应用的工具。Cl元素的部分化合价与物质类别
的关系如图所示。下列说法正确的是
( )
!"
%
#
& ’
$"
单质 氢化物 钠盐 含氧酸
高一化学 第 2页(共6页)A.常温下能通过一步反应实现 e→b→c的转化
B.e的酸性比 b强
C.d溶液和 c溶液均属于电解质
D.氯原子的最外电子层上有7个电子,极易得到电子,所以 a不具有还原性
11.侯德榜发明联合制碱法,为我国化学工业发展和技术创新作出了重要贡献。联合制碱法简
易流程如图所示,沉淀池中发生反应:NaCl+NH+HO+CO NaHCO↓+NHCl。下列
3 2 2 3 4
说法错误的是
饱和食盐水
$% ’
&
!" !’"$%
合成氨厂 # 沉淀池 ( 煅烧炉 !’$%
& )
A.物质 a为 CO 和 HO,其中 CO 为酸性氧化物
2 2 2
B.沉淀池中发生反应的离子方程式为 NH+HO+CO HCO-+NH+
3 2 2 3 4
C.与 NaHCO 相比较,NaCO 的溶解度更大,热稳定性更强
3 2 3
D.沉淀池中分离出 NaHCO 采取的方法为过滤
3
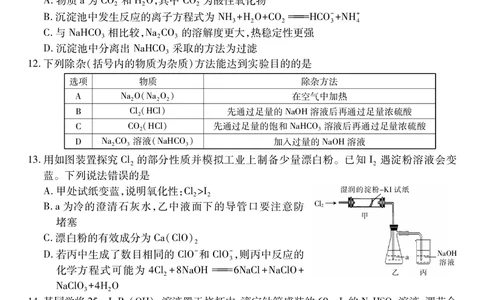
12.下列除杂(括号内的物质为杂质)方法能达到实验目的的是
选项 物质 除杂方法
A NaO(NaO) 在空气中加热
2 2 2
B Cl(HCl) 先通过足量的NaOH溶液后再通过足量浓硫酸
2
C CO(HCl) 先通过足量的饱和NaHCO 溶液后再通过足量浓硫酸
2 3
D NaCO 溶液(NaHCO) 加入过量的NaOH溶液
2 3 3
13.用如图装置探究 Cl的部分性质并模拟工业上制备少量漂白粉。已知 I遇淀粉溶液会变
2 2
蓝。下列说法错误的是
A.甲处试纸变蓝,说明氧化性:Cl>I 湿润的淀粉$%&试纸
2 2
B.a为冷的澄清石灰水,乙中液面下的导管口要注意防 !" #
甲
堵塞
C.漂白粉的有效成分为 Ca(ClO)
2
D.若丙中生成了数目相同的 ClO-和 ClO-,则丙中反应的 (’)*
3 ’
溶液
化学方程式可能为 4Cl+8NaOH6NaCl+NaClO+
2 乙 丙
NaClO+4HO
3 2
14.某同学将25mLBa(OH)溶液置于烧杯中,滴定针筒盛装约60mL的 NaHSO 溶液,调节合
2 4
适的滴速,将NaHSO 溶液滴入 Ba(OH) 溶液中。实验过程中测得溶液电导率(电导率越
4 2
大,溶液导电能力越强)随滴加NaHSO 溶液的体积变化关系如图所示。下列说法正确的是
4
!"""
#"""
$%""
&%%%
’"""
(%%%
)"""
*+""
,%%%
高一化学 第 3页(共6页)
#,10/".!!-率导电
!"#
A.NaHSO 溶液中含有带正电荷的水合钠离子:
4
B.a点时,反应后溶液中含有的主要离子为 Na+和 OH-
C.a→b过程中,反应的离子方程式为 Ba2++SO2-
4
BaSO↓ ! 4
"
D.NaHSO在水中的电离方程式为 NaHSO Na++HSO-
4 4 4
+ ,+ *+ 2% (% 3% &%
#-04二、非选择题:本题共4小题,共58分。
15.(14分)钠及其化合物在生产生活中具有重要的应用价值。
(1)食盐中含有 NaCl和 KIO,KIO 属于 (填“酸”“碱”“盐”或“氧化物”);将1滴
3 3
20%氯化钠溶液滴入50mL99.7%乙醇溶液中能形成胶体,胶体粒子的直径为
(填字母);利用 效应可区分溶液和胶体。
A.<1nm B.1~100nm C.>100nm
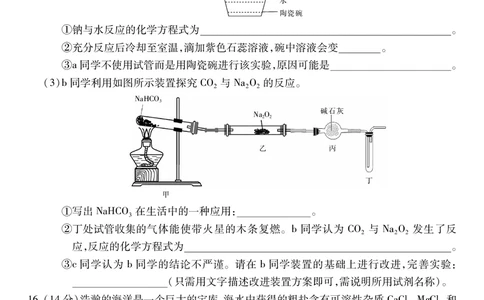
(2)a同学用如图所示装置探究钠与水的反应。
钠
水
陶瓷碗
①钠与水反应的化学方程式为 。
②充分反应后冷却至室温,滴加紫色石蕊溶液,碗中溶液会变 。
③a同学不使用试管而是用陶瓷碗进行该实验,原因可能是 。
(3)b同学利用如图所示装置探究 CO 与 NaO 的反应。
2 2 2
!"#$%
&
碱石灰
!"%
’ ’
乙 丙
丁
甲
①写出 NaHCO 在生活中的一种应用: 。
3
②丁处试管收集的气体能使带火星的木条复燃。b同学认为 CO 与 NaO 发生了反
2 2 2
应,反应的化学方程式为 。
③c同学认为 b同学的结论不严谨。请在 b同学装置的基础上进行改进,完善实验:
(只需用文字描述改进装置方案即可,需说明所用试剂名称)。
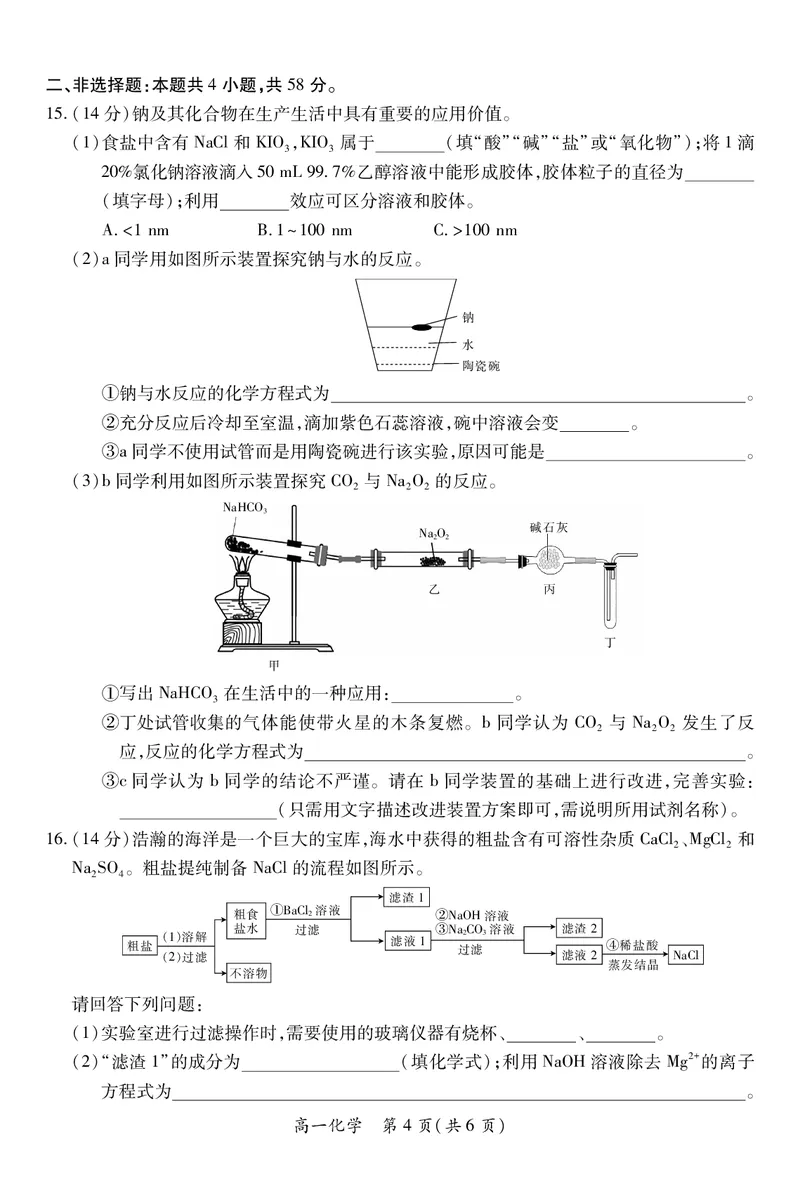
16.(14分)浩瀚的海洋是一个巨大的宝库,海水中获得的粗盐含有可溶性杂质 CaCl、MgCl和
2 2
NaSO。粗盐提纯制备 NaCl的流程如图所示。
2 4
滤渣!
粗食 !#$%& " 溶液 #’$()溶液
盐水 过滤 $’$%( 溶液 滤渣"
粗盐 !!"溶解 滤液! 过 " 滤 * "稀盐酸
!""过滤 滤液" ’$%&
蒸发结晶
不溶物
请回答下列问题:
(1)实验室进行过滤操作时,需要使用的玻璃仪器有烧杯、 、 。
(2)“滤渣1”的成分为 (填化学式);利用 NaOH溶液除去 Mg2+的离子
方程式为 。
高一化学 第 4页(共6页)(3)试剂①和试剂③的添加顺序不能互换,否则会造成的后果是 。
(4)添加的稀盐酸需要过量,若稀盐酸少量,则会有杂质产生。写出少量稀盐酸与足量
NaCO 溶液反应的化学方程式: 。
2 3
(5)该工艺使用的粗盐中,NaCl的质量分数为 90%,100g粗盐经过上述流程,实际制得的
NaCl质量大于90g,原因是 。
电解
(6)电解熔融的 NaCl会发生反应:2NaCl(熔融)2Na+Cl↑,请用双线桥表示该反应电
2
子转移的情况: (只需注明电子转移方向和数目即可)。
17.(15分)ClO 常温下为黄绿色气体,极易溶于水,受热易分解,常用作消毒剂;NaClO(亚氯
2 2
酸钠)是一种较稳定的含氯消毒剂,可用于制备 ClO。
2
请回答下列问题:
(1)NaClO中Cl元素的化合价为 价;将NaClO置于火焰上灼烧,焰色为 色。
2 2
(2)NaClO 的一种制备原理如下:
2
i.3NaClO+3HSO HClO+2ClO↑+3NaHSO+HO;
3 2 4 4 2 4 2
ii.ClO+NaOH+HO →NaClO+HO+O(未配平)。
2 2 2 2 2 2
①反应 i中氧化产物为 ;反应 i中 HSO 体现了 (填化学性质)性。
2 4
②补全并配平反应 ii的化学方程式: 。
③在发生反应 ii的条件下,ClO、HO、NaClO、O 四种物质中,氧化性最强的为 。
2 2 2 2 2
(3)一种二氧化氯泡腾片主要成分为NaClO 和NaHSO,将该泡腾片投入水中,会发生反应生
2 4
成ClO、NaCl、NaSO 和HO,该反应过程中,氧化剂和还原剂的质量之比为 。
2 2 4 2
(4)NaClO 与 NaOH的混合溶液可用于脱除有毒气体 NO,反应生成 NaNO、NaCl和 HO。
2 3 2
该反应的离子方程式为 。
18.(15分)某化学兴趣小组利用如图所示装置制备 Cl并探究其与水的反应。
2
浓盐酸
气球 酸化后的!"#$ 溶液
%
浸润饱和食盐水
的脱脂棉
&’($ ) 溶液 分散有无水*+*, -
干燥的紫色 的珍珠棉块
石蕊试纸 湿润的
紫色石蕊试纸
蒸馏水
已知:常温下,浓盐酸能与 KMnO 溶液反应产生 Cl。
4 2
(1)Cl与 HO反应的离子方程式为 ;新制氯水呈黄绿
2 2
色的原因是含有 (填微粒符号)。
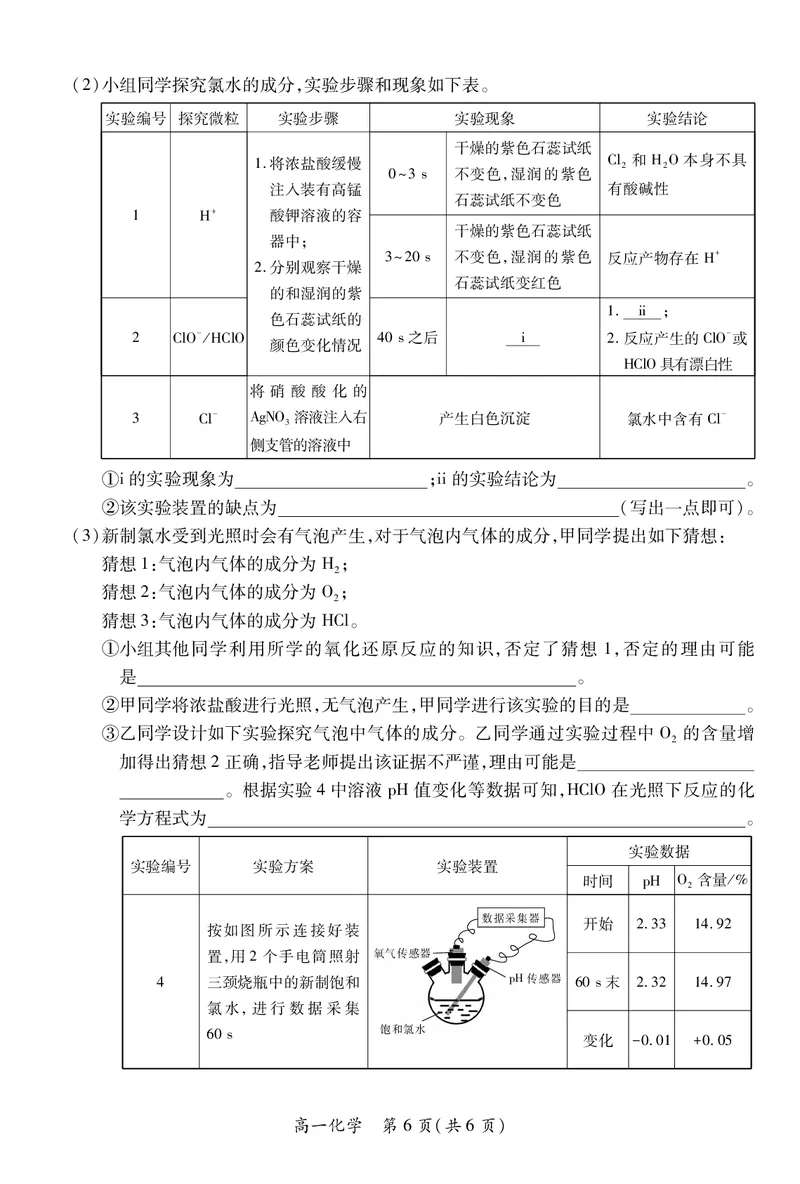
高一化学 第 5页(共6页)(2)小组同学探究氯水的成分,实验步骤和现象如下表。
实验编号 探究微粒 实验步骤 实验现象 实验结论
干燥的紫色石蕊试纸
1.将浓盐酸缓慢 Cl和 HO本身不具
2 2
0~3s 不变色,湿润的紫色
注入装有高锰 有酸碱性
石蕊试纸不变色
1 H+ 酸钾溶液的容
干燥的紫色石蕊试纸
器中;
3~20s 不变色,湿润的紫色 反应产物存在H+
2.分别观察干燥
石蕊试纸变红色
的和湿润的紫
1. ii ;
色石蕊试纸的
2 ClO-/HClO 40s之后 i 2.反应产生的ClO-或
颜色变化情况
HClO具有漂白性
将 硝 酸 酸 化 的
3 Cl- AgNO溶液注入右 产生白色沉淀 氯水中含有Cl-
3
侧支管的溶液中
①i的实验现象为 ;ii的实验结论为 。
②该实验装置的缺点为 (写出一点即可)。
(3)新制氯水受到光照时会有气泡产生,对于气泡内气体的成分,甲同学提出如下猜想:
猜想1:气泡内气体的成分为 H;
2
猜想2:气泡内气体的成分为 O;
2
猜想3:气泡内气体的成分为 HCl。
①小组其他同学利用所学的氧化还原反应的知识,否定了猜想 1,否定的理由可能
是 。
②甲同学将浓盐酸进行光照,无气泡产生,甲同学进行该实验的目的是 。
③乙同学设计如下实验探究气泡中气体的成分。乙同学通过实验过程中 O 的含量增
2
加得出猜想2正确,指导老师提出该证据不严谨,理由可能是
。根据实验4中溶液 pH值变化等数据可知,HClO在光照下反应的化
学方程式为 。
实验数据
实验编号 实验方案 实验装置
时间 pH O 含量/%
2
数据采集器 开始 2.33 14.92
按如图所示连接好装
置,用 2个手电筒照射 氧气传感器
4 三颈烧瓶中的新制饱和 !"传感器 60s末 2.32 14.97
氯水,进行数据采集
60s 饱和氯水
变化 -0.01 +0.05
高一化学 第 6页(共6页)