文档内容
氨和铵盐
【学习目标】
1、掌握氨的物理性质和化学性质,熟悉喷泉实验及发生的原理
2、掌握氨气的实验室制法及操作要点
3、掌握铵盐的性质
【主干知识梳理】
一、氨
1、氨分子的结构
氨的电子式为 ,结构式为 ,氨的结构为三角锥形,N原子位于锥顶,三个H原子位于锥底
2、物理性质
氨是无色、有刺激性气味的气体,密度比空气小,很容易液化;氨极易溶于水,在常温常压下,1体积水大
约可溶解700 体积氨。氨气溶于水时,需防止倒吸现象的发生
3、氨的化学性质
(1)与水的反应
氨溶于水的水溶液称为氨水,其中大部分NH 与水结合成一水合氨(NH ·H O),NH ·H O为弱电解质,只能部
3 3 2 3 2
分电离成NH +和OH-:NH +HO NH ·HO NH ++OH―
4 3 2 3 2 4
①NH 是唯一能使湿润的红色石蕊试纸变蓝的气体,常用此性质检验NH
3 3
②液氨与氨水的比较
液氨 氨水
物质成分 纯净物(非电解质) 混合物(NH ·H O为弱电解质)
3 2
粒子种类 NH 分子 NH 、NH ·H O、HO、NH、OH-、H+
3 3 3 2 2
主要性质 不具有碱性 具有碱的通性
存在条件 常温常压下不能存在 在常温常压下可存在
③氨水的性质:氨水具有弱碱性,能使无色酚酞试液变为浅红色,使红色石蕊试液变为蓝色。氨水的浓度越
大,密度反而越小(是一种特殊情况)。NH ·H O不稳定,故加热氨水时有氨气逸出:NH ·HO NH ↑+
3 2 3 2 3
HO
2
④氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水。通常把氨水盛装在玻璃容
器、橡皮袋、陶瓷坛或内涂沥青的铁桶里
⑤有关氨水浓度的计算:氨水虽然大部分以NH ·H O形式存在,但计算时仍以NH 作溶质
3 2 3
(2)氨气与酸(盐酸、硝酸、硫酸等)反应,生成铵盐
①蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,其现象是有大量白烟产生,其原因是:浓氨水和浓盐酸
均有挥发性,挥发出来的NH 和HCl在空气中相遇,化合生成NH Cl固体小颗粒,即为白烟
3 4
反应的化学方程式:HCl+NH ===NHCl (产生白烟,可用于检验NH )
3 4 3
②将浓盐酸改为浓硝酸,也会出现相同的现象
反应的化学方程式:NH +HNO ===NHNO (产生白烟,可用于检验NH )
3 3 4 3 3
③与硫酸反应:2NH +HSO ===(NH)SO (浓硫酸没有挥发性,不能形成白烟,不能用浓硫酸干燥氨气)
3 2 4 4 2 4
④与CO、SO 等酸性氧化物反应:NH +CO +HO===NHHCO 或2NH +CO +HO===(NH)CO
2 2 3 2 2 4 3 3 2 2 4 2 3
(3)NH 的还原性:NH 分子中氮元素的化合价为 - 3 价,在化学反应中氮元素化合价可能的变化是只能升高,
3 3
不能降低,因此氨具有还原性。NH 能与与O、CuO、Cl 等的反应
3 2 2
①氨的催化氧化:氨气在催化剂(如铂等)、加热条件下,被氧气氧化生成 NO和HO。此反应是放热反应,
2
叫做氨的催化氧化(或叫接触氧化),是工业制硝酸的反应原理之一
4NH +5O=====4NO+6HO (工业制硝酸的基础,也是工业上制NO的方法)
3 2 2
②与纯氧反应:4NH + 3O (纯氧)===== 2N + 6H O (黄绿色火焰)
3 2 2 2
③与CuO反应:2NH +3CuO N+3Cu+3HO (氨气还原CuO是实验室制氮气的方法之一)
3 2 2
④氨气与氯气反应:
氨气与少量氯气反应的化学方程式为:8NH +3Cl ===N+6NH Cl
3 2 2 4
氨气与足量氯气反应的化学方程式为:2NH + 3Cl ===N + 6HCl
3 2 2【微点拨】工业制HNO 的反应原理及流程
3
流程示意图
将氨和空气的混合气(氧∶氮≈2∶1)通入灼热(760~840 ℃)的铂铑合金网,在合
主要流程 金网的催化作用下,氨被氧化成一氧化氮(NO),生成的一氧化氮结合反应后残
余的氧气继续被氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸
4NH +5O=====4NO+6HO
3 2 2
各步反应的化
2NO+O===2NO
学方程式 2 2
3NO +HO===2HNO +NO
2 2 3
(4)与盐溶液反应
被滴试剂 现象 离子方程式
FeCl 溶液 生成红褐色沉淀 Fe3++3NH ·H O===Fe(OH) ↓+3NH
3 3 2 3
AlCl 溶液 生成白色沉淀 Al3++3NH ·H O===Al(OH) ↓+3NH
3 3 2 3
4、氨的用途
①氨是氮肥工业及制造硝酸、碳铵、纯碱等的重要原料
②氨也是有机合成工业中的常用原料 (如:尿素、合成纤维、染料等)
③氨还以用作制冷剂。液氨作制冷剂的原因是氨易液化,液氨汽化时要吸收大量的热,使周围温度急剧降低
【对点训练1】
1、关于氨的下列叙述中,错误的是( )
A.氨易液化,因此液氨常用来作制冷剂 B.氨易溶解于水,可用来做喷泉实验
C.实验室常用向下排空气法收集氨 D.氨溶于水能导电,氨是电解质
2、下列有关氨的叙述不正确的是( )
A.氨分子中氮元素的化合价只能升高,氨具有还原性
B.氨的催化氧化反应的化学方程式是4NH +5O=====4NO+6HO
3 2 2
C.氨的催化氧化反应中,若氧气过量,则有红棕色气体生成
D.NH 与酸的反应为中和反应
3
3、如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下
表中对实验现象所做的解释正确的是( )
选项 实验现象 解释
A 浓盐酸附近产生白烟 NH 与浓盐酸反应产生了NH Cl固体
3 4
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是AlCl 溶液
3
干燥红色石蕊试纸不变色,湿润红色
D NH 是一种可溶性碱
石蕊试纸变蓝 3
二、氨气的实验室制法
1、实验过程及实验装置
原理 2NH Cl+Ca(OH) CaCl +2NH ↑+2HO
4 2 2 3 2
反应原料 实验室一般用氯化铵或硫酸铵与Ca(OH) 固体
2实验装置
发生装置 “ ”型,与实验室利用氯酸钾和二氧化锰加热制取氧气的装置相同
通常用碱石灰干燥氨气,不能用五氧化二磷、浓硫酸和无水氯化钙干燥
净化装置
NH 极易溶于水 密度比空气小,只能用向下排空气法收集,试管口塞一团疏松的棉花团,目
收集装置 3
的是防止氨气与空气形成对流,以收集到较纯净的氨气
多余的氨气要吸收掉(可在导管口放一团用水或稀硫酸浸润的棉花球)以避免污染空气。在吸收
时要防止倒吸,常采用的装置如图所示:
尾气处理
①方法一:用镊子夹住一片湿润的红色石蕊试纸放在试管口,若试纸变蓝,说明已经收集满
验满方法
②方法二:用蘸取浓盐酸的玻璃棒靠近试管口,若有白烟生成,说明已经收集满
2、实验室制取氨气时注意事项
①NH Cl可用(NH )SO 等代替,但不能用NH HCO 或NH NO 代替。因为加热过程中NH NO 可能发生爆炸
4 4 2 4 4 3 4 3 4 3
性的分解反应,发生危险;而NH HCO 极易分解产生CO,使生成的中混有较多CO 杂质
4 3 2 2
②消石灰不能用KOH或NaOH代替,原因是:NaOH、KOH易吸水、易结块,不利于生成的NH 逸出,而且
3
高温下NaOH、KOH会腐蚀试管
③氨气干燥时:不能用CaCl 、PO 、浓硫酸作干燥剂,因为NH 能与CaCl 反应生成CaCl ·8NH 。PO 与浓
2 2 5 3 2 2 3 2 5
硫酸均能与NH 反应,生成相应的盐。所以NH 通常用碱石灰干燥
3 3
④收集NH 时所用的仪器必须干燥,导气管要插入管底;试管口要塞一团用水或稀硫酸浸湿的棉花球,可减小
3
NH 与空气的对流速度,使收集的气体纯净,同时也可避免污染空气
3
3、快速制备氨的方法
方法 化学方程式(或原理) 气体发生装置
加热浓氨水 NH ·HO HO+NH ↑
3 2 2 3
NaOH溶于水放热,促使氨水分解,且OH-浓度的增大有利
浓氨水+固体NaOH
于NH 的放出
3
NH ·H O+CaO===NH↑+Ca(OH)
3 2 3 2
浓氨水+固体CaO CaO的作用:①吸水后放热促进NH 的放出;
3
②增加溶液中的OH-浓度,减小NH 的溶解度
3
4、氨的工业制法:N+3H 2NH
2 2 3
【对点训练2】
1、下列方法适合实验室制取氨气的是( )
A.N 和H 催化加热制取氨气 B.加热NH Cl制取氨气
2 2 4
C.向碱石灰固体上滴加浓氨水 D.将NH Cl溶液和NaOH溶液混合
4
2、实验室制取少量干燥的氨涉及下列装置,其中正确的是( )A.①是NH 发生装置 B.②是NH 吸收装置
3 3
C.③是NH 发生装置 D.④是NH 收集、检验装置
3 3
3、在标准状况下,将多余的氨用水吸收,下图中哪个装置最好( )
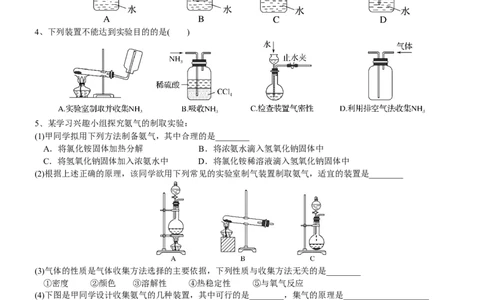
4、下列装置不能达到实验目的的是( )
5、某学习兴趣小组探究氨气的制取实验:
(1)甲同学拟用下列方法制备氨气,其中合理的是________
A.将氯化铵固体加热分解 B.将浓氨水滴入氢氧化钠固体中
C.将氢氧化钠固体加入浓氨水中 D.将氯化铵稀溶液滴入氢氧化钠固体中
(2)根据上述正确的原理,该同学欲用下列常见的实验室制气装置制取氨气,适宜的装置是________
(3)气体的性质是气体收集方法选择的主要依据,下列性质与收集方法无关的是________
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(4)下图是甲同学设计收集氨气的几种装置,其中可行的是________,集气的原理是____________________
三、铵盐及NH的检验
1、铵盐:由铵离子和酸根离子构成的盐,铵盐属于铵态氮肥
如:硫酸铵[(NH )SO ,俗称硫铵,又称肥田粉],氯化铵[NH Cl,俗称氯铵],硝酸铵[NH NO ,俗称硝铵],
4 2 4 4 4 3
碳酸氢铵[NH HCO ,俗称碳铵]
4 3
2、结构:离子晶体,具有离子键、共价键,是由非金属元素组成的离子化合物
3、铵盐的物理性质:铵盐都是白色固体,均易溶于水4、铵盐的化学性质
(1)不稳定性:铵盐受热易分解,但不一定都有NH 生成
3
①在试管中加热氯化铵固体,观察到的现象是氯化铵白色固体消失,在试管上方重新凝成白色固体
反应的化学方程式:NH Cl NH ↑+HCl↑,NH +HCl===NHCl
4 3 3 4
【微点拨】该过程不是升华,利用NH Cl的这种性质常用来分离提纯NH Cl固体
4 4
②NH HCO 固体受热分解:NH HCO NH ↑+CO ↑+HO
4 3 4 3 3 2 2
③(NH )CO 固体受热分解:(NH )CO 2NH ↑+CO ↑+HO
4 2 3 4 2 3 3 2 2
④NH NO 受热分解较为复杂:NH NO NO↑+2HO,2NH NO 2N↑+O↑+4HO
4 3 4 3 2 2 4 3 2 2 2
(2)与碱反应
①固体反应(NH Cl固体与NaOH固体共热):NH Cl+NaOH NH ↑+NaCl+HO
4 4 3 2
②溶液中的反应
a.若是铵盐溶液与碱溶液共热,写成NH ↑+HO
3 2
(NH )SO 与NaOH两溶液混合加热:NH+OH- NH ↑+HO
4 2 4 3 2
b.若是铵盐溶液与浓碱溶液,写成NH ↑+HO
3 2
浓NaOH溶液中加入硫酸铵固体:OH-+NH===NH↑+HO
3 2
c.若是反应物为稀溶液且不加热时或无特殊说明写NH ·H O
3 2
NH Cl与NaOH两稀溶液混合:NH+OH-===NH·HO
4 3 2
5、用途:可用作氮肥,炸药,焊药
6、NH +的检验和铵盐的检验方法
4
(1)NH +的检验:取少量待测溶液于试管中,再加入浓的NaOH溶液,加热产生能使湿润红色石蕊试纸变蓝的
4
气体(或将蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生),则该溶液中存在NH
(2)铵盐的检验方法
①取少许样品与碱混合于试管中共热,将湿润的红色石蕊试纸靠近管口,若试纸变蓝,则证明样品中含有NH
②取少许样品于试管中,放入碱后加热,用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明样品中
含有NH
【对点训练3】
1、下列说法中正确的是( )
A.所有铵盐受热均可以分解,产物均有NH
3
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH+OH- NH ↑+HO
4 3 2
D.NH Cl和NaCl的固体混合物可用升华法分离
4
2、现欲分离氯化钠和氯化铵的混合物,可采用的方法是 ( )
A.加入NaOH溶液 B.加入AgNO 溶液
3
C.加热并冷却 D.加入水
3、检验铵盐的一般方法是将待测物取少许置于试管中,然后( )
A.加水溶解后,再滴入酚酞溶液 B.加强碱溶液加热后,用湿润的红色石蕊试纸在试管口检验
C.加入强酸溶液加热后,再滴入酚酞溶液 D.加入强碱溶液加热后,再滴入酚酞溶液
四、喷泉实验——氨极易溶于水
在干燥的圆底烧瓶里充满,用带有玻璃管和胶头滴管(预先吸入水)的橡胶塞塞紧瓶口。
实验过程 倒置烧瓶,使玻璃管插入盛有水的烧杯中(预先在水里滴入少量酚酞溶液)。打开弹簧
夹,挤压胶头滴管,使水进入烧瓶。观察并描述现象,分析出现这些现象的可能原因实验装置
实验现象 烧杯中的溶液由玻璃管进入烧瓶,形成喷泉,瓶内液体呈红色
实验结论
氨易溶于水,水溶液呈碱性
方程式 NH +HO NH ·H O
3 2 3 2
1、喷泉实验的原理:因为烧瓶内气体易溶于水或易与水反应,使瓶内压强减小,形成压强差,大气压将烧杯中
的水压入烧瓶而形成喷泉
2、能形成喷泉的条件:从原理上讲,气体要易溶于水或易与水反应,以形成足够大的压强差;从实验条件上讲,
烧瓶内气体要充满,气体和仪器均要干燥,装置的气密性要好
3、使容器内外产生较大压强差的两种方法
(1)减小内压法:使烧瓶外气压不变,烧瓶内气压减小
实验装置
烧瓶内气体与液体接触→气体溶解或发生化学反应→烧瓶内压强减小→外部液体迅速进入形
原理
成喷泉
引发喷泉 打开橡皮管上的弹簧夹,挤压滴管的胶头,则烧杯中的水由玻璃管进入烧瓶,形成喷泉
常见气体与吸收剂的组合
气体 HCl NH CO、Cl、HS、SO NO +O
3 2 2 2 2 2 2
吸收剂 水或NaOH溶液 水或盐酸 NaOH溶液 水
气体在溶液中的溶解度很大或通过反应,使气体的物质的量迅速减小,产生足
组合时的条件
够的压强差(负压)
(2)增大外压法:使烧瓶外气压增大,烧瓶内气压不变
实验装置
锥形瓶内液体挥发或发生化学反应产生气体→容器内压强增大→锥形瓶内液体迅速流入烧瓶
原理
形成喷泉
实例 喷雾器、人造喷泉、火山喷发等
【对点训练4】
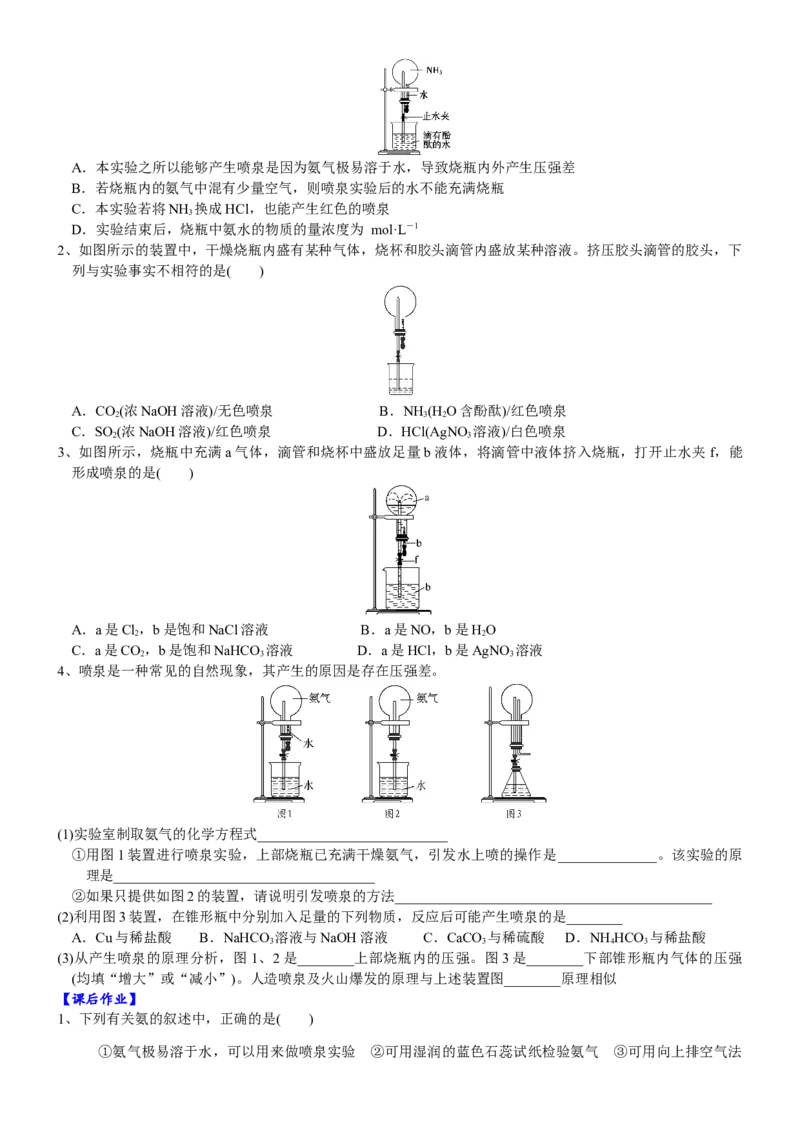
1、标准状况下,在干燥的烧瓶中充满纯净的NH ,进行如图所示的喷泉实验,下列说法错误的是( )
3A.本实验之所以能够产生喷泉是因为氨气极易溶于水,导致烧瓶内外产生压强差
B.若烧瓶内的氨气中混有少量空气,则喷泉实验后的水不能充满烧瓶
C.本实验若将NH 换成HCl,也能产生红色的喷泉
3
D.实验结束后,烧瓶中氨水的物质的量浓度为 mol·L-1
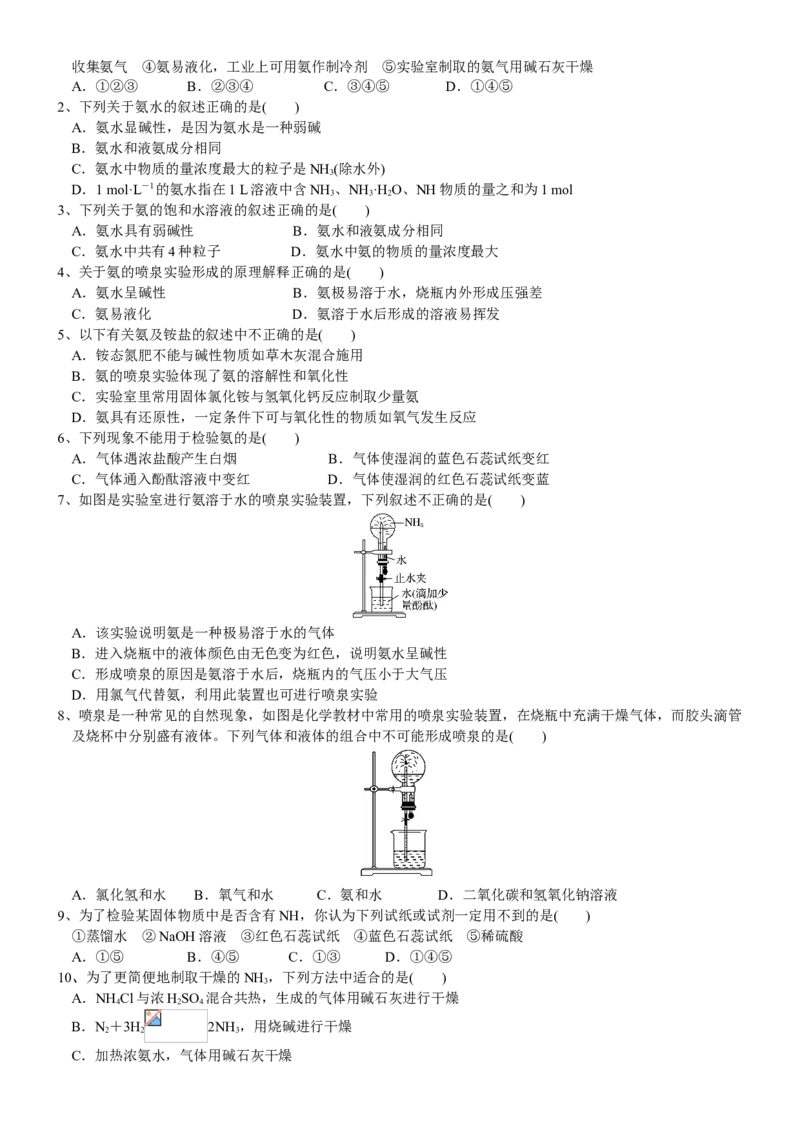
2、如图所示的装置中,干燥烧瓶内盛有某种气体,烧杯和胶头滴管内盛放某种溶液。挤压胶头滴管的胶头,下
列与实验事实不相符的是( )
A.CO(浓NaOH溶液)/无色喷泉 B.NH (H O含酚酞)/红色喷泉
2 3 2
C.SO (浓NaOH溶液)/红色喷泉 D.HCl(AgNO 溶液)/白色喷泉
2 3
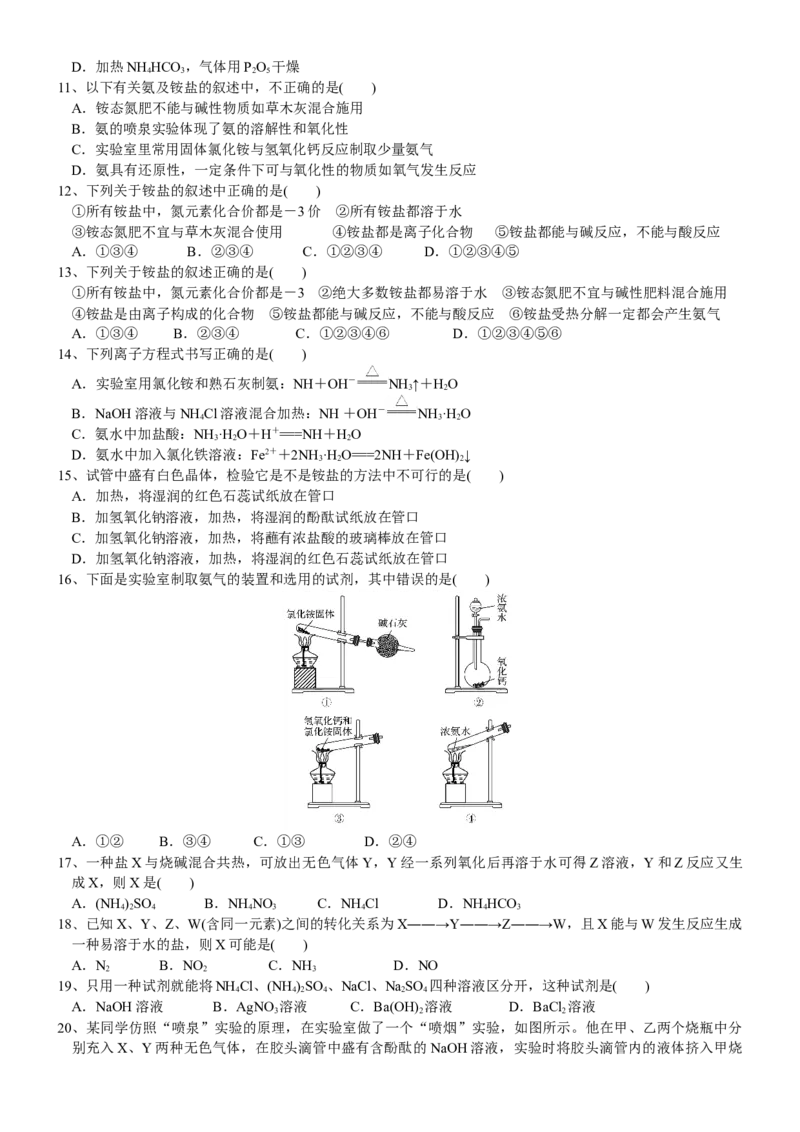
3、如图所示,烧瓶中充满a气体,滴管和烧杯中盛放足量b液体,将滴管中液体挤入烧瓶,打开止水夹f,能
形成喷泉的是( )
A.a是Cl,b是饱和NaCl溶液 B.a是NO,b是HO
2 2
C.a是CO,b是饱和NaHCO 溶液 D.a是HCl,b是AgNO 溶液
2 3 3
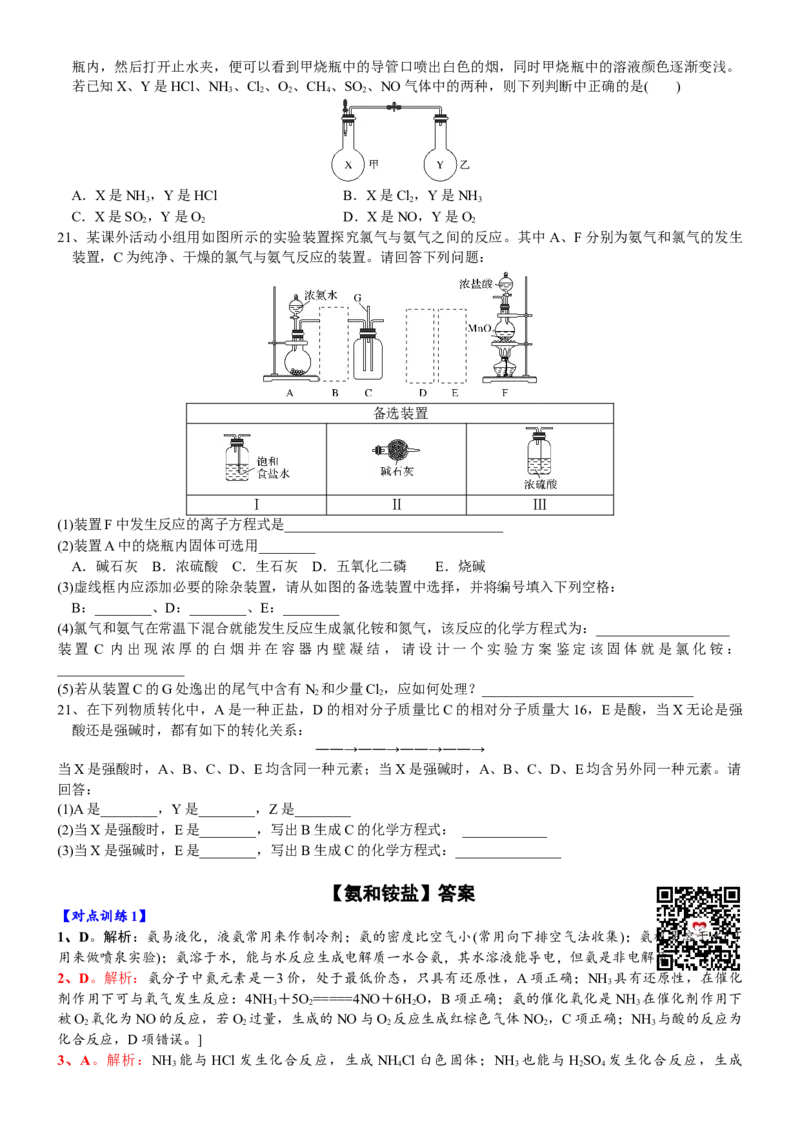
4、喷泉是一种常见的自然现象,其产生的原因是存在压强差。
(1)实验室制取氨气的化学方程式___________________________
①用图1装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是______________。该实验的原
理是_____________________________________
②如果只提供如图2的装置,请说明引发喷泉的方法_____________________________________________
(2)利用图3装置,在锥形瓶中分别加入足量的下列物质,反应后可能产生喷泉的是________
A.Cu与稀盐酸 B.NaHCO 溶液与NaOH溶液 C.CaCO 与稀硫酸 D.NH HCO 与稀盐酸
3 3 4 3
(3)从产生喷泉的原理分析,图1、2是________上部烧瓶内的压强。图3是________下部锥形瓶内气体的压强
(均填“增大”或“减小”)。人造喷泉及火山爆发的原理与上述装置图________原理相似
【课后作业】
1、下列有关氨的叙述中,正确的是( )
①氨气极易溶于水,可以用来做喷泉实验 ②可用湿润的蓝色石蕊试纸检验氨气 ③可用向上排空气法收集氨气 ④氨易液化,工业上可用氨作制冷剂 ⑤实验室制取的氨气用碱石灰干燥
A.①②③ B.②③④ C.③④⑤ D.①④⑤
2、下列关于氨水的叙述正确的是( )
A.氨水显碱性,是因为氨水是一种弱碱
B.氨水和液氨成分相同
C.氨水中物质的量浓度最大的粒子是NH (除水外)
3
D.1 mol·L-1的氨水指在1 L溶液中含NH 、NH ·H O、NH物质的量之和为1 mol
3 3 2
3、下列关于氨的饱和水溶液的叙述正确的是( )
A.氨水具有弱碱性 B.氨水和液氨成分相同
C.氨水中共有4种粒子 D.氨水中氨的物质的量浓度最大
4、关于氨的喷泉实验形成的原理解释正确的是( )
A.氨水呈碱性 B.氨极易溶于水,烧瓶内外形成压强差
C.氨易液化 D.氨溶于水后形成的溶液易挥发
5、以下有关氨及铵盐的叙述中不正确的是( )
A.铵态氮肥不能与碱性物质如草木灰混合施用
B.氨的喷泉实验体现了氨的溶解性和氧化性
C.实验室里常用固体氯化铵与氢氧化钙反应制取少量氨
D.氨具有还原性,一定条件下可与氧化性的物质如氧气发生反应
6、下列现象不能用于检验氨的是( )
A.气体遇浓盐酸产生白烟 B.气体使湿润的蓝色石蕊试纸变红
C.气体通入酚酞溶液中变红 D.气体使湿润的红色石蕊试纸变蓝
7、如图是实验室进行氨溶于水的喷泉实验装置,下列叙述不正确的是( )
A.该实验说明氨是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C.形成喷泉的原因是氨溶于水后,烧瓶内的气压小于大气压
D.用氯气代替氨,利用此装置也可进行喷泉实验
8、喷泉是一种常见的自然现象,如图是化学教材中常用的喷泉实验装置,在烧瓶中充满干燥气体,而胶头滴管
及烧杯中分别盛有液体。下列气体和液体的组合中不可能形成喷泉的是( )
A.氯化氢和水 B.氧气和水 C.氨和水 D.二氧化碳和氢氧化钠溶液
9、为了检验某固体物质中是否含有NH,你认为下列试纸或试剂一定用不到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A.①⑤ B.④⑤ C.①③ D.①④⑤
10、为了更简便地制取干燥的NH ,下列方法中适合的是( )
3
A.NH Cl与浓HSO 混合共热,生成的气体用碱石灰进行干燥
4 2 4
B.N+3H 2NH ,用烧碱进行干燥
2 2 3
C.加热浓氨水,气体用碱石灰干燥D.加热NH HCO ,气体用PO 干燥
4 3 2 5
11、以下有关氨及铵盐的叙述中,不正确的是( )
A.铵态氮肥不能与碱性物质如草木灰混合施用
B.氨的喷泉实验体现了氨的溶解性和氧化性
C.实验室里常用固体氯化铵与氢氧化钙反应制取少量氨气
D.氨具有还原性,一定条件下可与氧化性的物质如氧气发生反应
12、下列关于铵盐的叙述中正确的是( )
①所有铵盐中,氮元素化合价都是-3价 ②所有铵盐都溶于水
③铵态氮肥不宜与草木灰混合使用 ④铵盐都是离子化合物 ⑤铵盐都能与碱反应,不能与酸反应
A.①③④ B.②③④ C.①②③④ D.①②③④⑤
13、下列关于铵盐的叙述正确的是( )
①所有铵盐中,氮元素化合价都是-3 ②绝大多数铵盐都易溶于水 ③铵态氮肥不宜与碱性肥料混合施用
④铵盐是由离子构成的化合物 ⑤铵盐都能与碱反应,不能与酸反应 ⑥铵盐受热分解一定都会产生氨气
A.①③④ B.②③④ C.①②③④⑥ D.①②③④⑤⑥
14、下列离子方程式书写正确的是( )
A.实验室用氯化铵和熟石灰制氨:NH+OH- NH ↑+HO
3 2
B.NaOH溶液与NH Cl溶液混合加热:NH +OH- NH ·H O
4 3 2
C.氨水中加盐酸:NH ·H O+H+===NH+HO
3 2 2
D.氨水中加入氯化铁溶液:Fe2++2NH ·H O===2NH+Fe(OH) ↓
3 2 2
15、试管中盛有白色晶体,检验它是不是铵盐的方法中不可行的是( )
A.加热,将湿润的红色石蕊试纸放在管口
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口
16、下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A.①② B.③④ C.①③ D.②④
17、一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后再溶于水可得Z溶液,Y和Z反应又生
成X,则X是( )
A.(NH )SO B.NH NO C.NH Cl D.NH HCO
4 2 4 4 3 4 4 3
18、已知X、Y、Z、W(含同一元素)之间的转化关系为X――→Y――→Z――→W,且X能与W发生反应生成
一种易溶于水的盐,则X可能是( )
A.N B.NO C.NH D.NO
2 2 3
19、只用一种试剂就能将NH Cl、(NH )SO 、NaCl、NaSO 四种溶液区分开,这种试剂是( )
4 4 2 4 2 4
A.NaOH溶液 B.AgNO 溶液 C.Ba(OH) 溶液 D.BaCl 溶液
3 2 2
20、某同学仿照“喷泉”实验的原理,在实验室做了一个“喷烟”实验,如图所示。他在甲、乙两个烧瓶中分
别充入X、Y两种无色气体,在胶头滴管中盛有含酚酞的NaOH溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可以看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。
若已知X、Y是HCl、NH 、Cl、O、CH、SO 、NO气体中的两种,则下列判断中正确的是( )
3 2 2 4 2
A.X是NH ,Y是HCl B.X是Cl,Y是NH
3 2 3
C.X是SO ,Y是O D.X是NO,Y是O
2 2 2
21、某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生
装置,C为纯净、干燥的氯气与氨气反应的装置。请回答下列问题:
备选装置
Ⅰ Ⅱ Ⅲ
(1)装置F中发生反应的离子方程式是_______________________________
(2)装置A中的烧瓶内固体可选用________
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从如图的备选装置中选择,并将编号填入下列空格:
B:________、D:________、E:________
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:___________________
装置 C 内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体就是氯化铵:
__________________
(5)若从装置C的G处逸出的尾气中含有N 和少量Cl,应如何处理?______________________________
2 2
21、在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强
酸还是强碱时,都有如下的转化关系:
――→――→――→――→
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请
回答:
(1)A是________,Y是________,Z是________
(2)当X是强酸时,E是________,写出B生成C的化学方程式: ____________
(3)当X是强碱时,E是________,写出B生成C的化学方程式:_______________
【氨和铵盐】答案
【对点训练1】
1、D。解析:氨易液化,液氨常用来作制冷剂;氨的密度比空气小(常用向下排空气法收集);氨极易溶于水(可
用来做喷泉实验);氨溶于水,能与水反应生成电解质一水合氨,其水溶液能导电,但氨是非电解质。
2、D。解析:氨分子中氮元素是-3价,处于最低价态,只具有还原性,A项正确;NH 具有还原性,在催化
3
剂作用下可与氧气发生反应:4NH +5O=====4NO+6HO,B项正确;氨的催化氧化是NH 在催化剂作用下
3 2 2 3
被O 氧化为NO的反应,若O 过量,生成的NO与O 反应生成红棕色气体NO ,C项正确;NH 与酸的反应为
2 2 2 2 3
化合反应,D项错误。]
3、A。解析:NH 能与HCl发生化合反应,生成NH Cl白色固体;NH 也能与HSO 发生化合反应,生成
3 4 3 2 4(NH )SO ;NH 与氯化物溶液反应生成氢氧化物沉淀,该氯化物可以是氯化铝、氯化镁等;NH 溶于水生成
4 2 4 3 3
NH ·H O,NH ·H O属于碱,NH 不属于碱。
3 2 3 2 3
【对点训练2】
1、C。解析:A项适合用于工业生产;B项因为NH Cl分解生成的NH 、HCl遇冷又化合为NH Cl,不能制取
4 3 4
氨气;D项由于NH 极易溶于水,不适合制取NH 。
3 3
2、C。解析:①中氯化铵固体受热分解生成氨和氯化氢,而在试管口部温度降低,氨和氯化氢又重新化合成固
体氯化铵,无法得到氨;②中漏斗没入水下起不到防倒吸的作用,应使倒置漏斗的上边缘刚好没入水中;③氧
化钙能与浓氨水中的水反应生成氢氧化钙,同时放出大量热,使浓氨水分解放出氨;④中的收集装置应在试管
口塞一团棉花,防止因空气对流,而使氨逸出。
3、C。解析:氨极易溶于水,若用装置A、B、D吸收尾气氨时,容易发生倒吸。
4、A。解析:A项收集NH 集气瓶口无棉花;B项NH 通入CCl 中,NH 不溶于CCl ,不会产生倒吸,逸出的
3 3 4 3 4
NH 又可被稀硫酸吸收;C项向长颈漏斗中加一定量水,没过长颈漏斗的下端,关闭止水夹,再加一定量的水
3
液面不下降,可说明气密性良好,反之,气密性不好;D项,收集比空气密度小的气体NH ,应该短管进气长
3
管出气。
5、(1)B
(2)C
(3)②④
(4)d 利用氨气密度小于空气,采用短管进氨气,长管出空气,即可收集氨气
解析:(1)加热氯化铵产生氯化氢和氨气,遇冷又转化为氯化铵固体,不能制取氨气;用浓氨水与氢氧化钠固体
混合制氨气时,将氨水滴入氢氧化钠固体中更方便操作,而且节约氨水的用量;氨气极易溶于水,若用稀溶液
制取,产量较少。(2)根据所给试剂判断,不需要加热条件。(3)收集气体可采用排空气法(密度、气体不能被氧
气氧化等),也可采用排水法(不易溶于水),与其他性质无关。(4)氨气极易溶于水,采用向下排空气法收集。
【对点训练3】
1、C。解析:A项,有的铵盐受热分解产生氨(如NH Cl),有的铵盐受热分解不产生氨(如硝酸铵);D项,可用
4
加热法分离NH Cl和某些固体(不分解、不升华的固体)的混合物,但其过程为先受热分解,再降温化合,而不
4
是升华。
2、C。解析:铵盐受热均易分解,NH Cl加热分解,而NaCl受热没有明显变化,同时生成的NH 和HCl气体
4 3
导出后又能迅速化合生成NH Cl。]
4
3、B。解析:将固体放入试管中,加强碱溶液加热后,用湿润的红色石蕊试纸放在试管口,湿润的红色石蕊试
纸会变蓝色,证明产生的气体是氨,则该盐中含有铵根离子,B正确。
【对点训练4】
1、C。解析:氨气极易溶于水,使烧瓶内气压迅速小于大气压,从而形成喷泉,A项正确;若烧瓶内的氨气中
混有少量空气,由于空气中的氮气等难溶于水,也不与水反应,则喷泉实验后的水不能充满烧瓶,B项正确;
若将NH 换成HCl,因HCl也极易溶于水,也能形成喷泉,但由于HCl的水溶液显酸性,故滴有酚酞的水形成
3
的喷泉溶液显无色,C项错误;设烧瓶容积为V L,则标准状状况下烧瓶内氨气的物质的量n==mol,由于氨
水充满烧瓶,所以最终形成氨水的物质的量浓度c=== mol·L-1,D项正确。
2、C。解析:气体与液体易发生反应或易溶即可形成喷泉。CO→NaOH溶液反应,无色喷泉;NH →HO(酚
2 3 2
酞),易溶显红色,形成喷泉;SO →NaOH溶液反应,无色喷泉;HCl→AgNO 溶液反应,生成白色沉淀,形成
2 3
喷泉。
3、D。解析:Cl 在饱和氯化钠溶液中的溶解度很小,也不与NaCl反应,烧杯与烧瓶内压强相等,不能形成喷
2
泉,A错误;NO不溶于水,与水不反应,压强不变,不能形成喷泉,B错误;CO 在饱和NaHCO 溶液中的溶
2 3
解度很小,也不与其反应,烧杯与烧瓶内压强相等,不能形成喷泉,C错误;HCl极易与AgNO 溶液反应,从
3
而使烧瓶内压强减小,小于外界压强,能形成喷泉,D正确。
4、(1)2NHCl+Ca(OH) CaCl +2NH +2HO
4 2 2 3 2
①打开止水夹,挤压胶头滴管 NH 溶于少量水中,使圆底烧瓶内压强减小,烧杯内的水进入圆底烧瓶,
3
形成喷泉
②打开止水夹,用热毛巾捂住圆底烧瓶至有气泡从水中冒出,移去热毛巾
(2)D
(3)减小 增大 3解析:(1)图1引发喷泉,只需打开止水夹,挤压胶头滴管即可,图 2则需先打开止水夹,再用热毛巾捂住圆底
烧瓶,发现有气泡冒出后,移去热毛巾即可。
(2)能在锥形瓶内反应产生气体,压强大于圆底烧瓶内压强方可,故应选NH HCO 和稀盐酸,其他要么不反应,
4 3
要么反应不生成气体或产生气体很少。
(3)图1、2是上部压强减小导致喷泉,图3是下部压强增大导致喷泉,人造喷泉及火山爆发均与图3原理相似。
【课后作业】
1、D。解析:氨气极易溶于水,使容器内压强减小,可以用来做喷泉实验,①正确;氨气的水溶液呈碱性,可
用湿润的红色石蕊试纸检验氨气,②错误;氨气的密度比空气的小,可用向下排空气法收集氨气,③错误;氨
易液化,工业上可用氨作制冷剂,④正确;氨气是碱性气体,实验室制取的氨气可用碱石灰干燥,⑤正确;故
选D。
2、D。解析:溶于水的氨大部分与水反应生成NH ·H O,所以除水外,物质的量浓度最大的粒子是NH ·H O;
3 2 3 2
NH ·H O是一种弱碱,在水中发生部分电离使溶液呈碱性;氨水中共含有六种粒子,分别是 HO、NH 、
3 2 2 3
NH ·H O、NH、OH-和少量的H+,是一种混合物,液氨是纯净物。
3 2
3、A。解析:氨易溶于水,且与水反应生成一水合氨,一水合氨能电离产生氢氧根离子,使氨水具有弱碱性,
可使酚酞变红色;氨与水的反应是可逆反应,大部分氨能与水反应生成一水合氨,一水合氨只有少部分电离,
氨水中含有NH 、NH ·H O、HO、NH、OH-、H+6种粒子,其中一水合氨的物质的量浓度最大。
3 3 2 2
4、B。解析:氨之所以能做成喷泉实验,是由于胶头滴管挤入的少量水可使烧瓶内的氨迅速溶解,烧瓶内外形
成了压强差。
5、B。解析:氨的喷泉实验证明氨极易溶于水,不能体现氨的氧化性。
6、B。解析:检验氨方法,一是用湿润的红色石蕊试纸(或石蕊溶液),因为氨溶于水呈碱性,遇到红色石蕊试
纸(或石蕊溶液)变蓝;二是用蘸有浓盐酸的玻璃棒靠近盛有待检验气体的瓶口,发生的反应为 NH +
3
HCl===NHCl,现象是形成白烟。
4
7、D。解析:A项,NH 极易溶于水,可用来做喷泉实验;B项,氨水呈碱性,能使酚酞溶液变红色;C项,
3
NH 极易溶于水,使烧瓶内的气压小于大气压,在压强差的作用下,烧杯中的水沿导管迅速向上流动,从而形
3
成喷泉;D项,Cl 在水中的溶解度较小,不能用于做喷泉实验。
2
8、B。解析:氯化氢、氨都极易溶于水,挤压装置中的胶头滴管,它们被水吸收,烧瓶内的气压都迅速减小,
都可形成喷泉; 二氧化碳极易被氢氧化钠溶液吸收,烧瓶内的气压迅速减小,可形成喷泉;氧气难溶于水,烧
瓶内的气压几乎无变化,不能形成喷泉。
9、B。解析:NH检验一般是取少量样品与碱混合于试管中,加热,将湿润的红色石蕊试纸靠近试管口,看试
纸是否变蓝;也可将蘸有浓盐酸的玻璃棒靠近试管口,看是否有白烟生成。因此④、⑤一定用不到。
10、C
11、B。解析:氨的喷泉实验证明氨极易溶于水,不能体现氨的氧化性。
12、B。解析:NH NO 中的NO,氮元素是+5价,①错误;NH HCO 也能与酸反应,⑤错误;草木灰主要成
4 3 4 3
分为KCO,显碱性,混合使用会产生NH ,从而降低肥效,③正确。
2 3 3
13、B。解析:①硝酸铵中氮元素既有-3价又有+5价,错误;②绝大多数铵盐易溶于水,正确;③铵态氮肥
中含有NH,能与OH-结合形成NH ·H O,NH ·H O受热分解产生氨气并逸出,使铵态氮肥的肥效降低,因此
3 2 3 2
不应与碱性肥料混合施用,正确;④铵盐都是由铵根离子与酸根离子构成的,属于离子化合物,正确;⑤弱酸
的铵盐(如碳酸铵等)能与酸反应,错误;⑥铵盐受热分解不一定生成氨气,如硝酸铵等,错误。
14、C。解析:A项,该反应属于固体间的加热反应,不能书写相应的离子方程式;B项,加热条件下NH ·H O
3 2
应分解为NH 和HO,离子方程式应为NH+OH- NH ↑+HO;C项,符合反应原理及离子方程式书写要
3 2 3 2
求;D项,向氨水中滴加FeCl 溶液应生成Fe(OH) 沉淀,离子方程式为Fe3++3NH ·H O===Fe(OH) ↓+3NH。
3 3 3 2 3
15、A
16、C。解析:实验室制取氨气的方法有:铵盐与碱加热制取氨气,常用 NH Cl与Ca(OH) 反应,固体与固体
4 2
反应,试管口应略向下倾斜,③错误;在浓氨水中加入CaO,CaO与水反应使溶液中c(OH-)增大,消耗了水,
并且放出大量的热,使NH ·H O分解放出氨气;加热浓氨水,加快氨气挥发。①是错误的,因为氯化铵分解生
3 2
成的NH 与HCl冷却后又生成NH Cl,不能得到NH 。
3 4 3
17、B。解析:铵盐与烧碱共热产生NH ,Y为NH ,NH ――→NO――→NO ――→HNO――→NH NO 。Z
3 3 3 2 3 4 3
为HNO,X为NH NO 。
3 4 3
18、C。解析:根据题意可知X、Y、Z、W(含同一元素)均含N元素,由X能与W发生反应生成一种易溶于水的盐,知X是NH ,发生反应:4NH +5O=====4NO+6HO,2NO+O===2NO ,3NO +HO===2HNO +
3 3 2 2 2 2 2 2 3
NO;且HNO+NH ===NHNO 。
3 3 4 3
19、C。解析:四种盐溶液中有四种离子:NH、Na+、Cl-、SO,区分Na+与NH使用碱溶液,区分Cl-和SO
用Ba2+,故选用Ba(OH) 溶液。
2
20、A。解析:根据题中已知的气体,能产生白烟的是HCl和NH 或Cl 和NH ,再根据题中信息“甲烧瓶中的
3 2 3
溶液颜色逐渐变浅”可知X是NH ,Y是HCl,故A项正确。
3
21、(1)MnO +4H++2Cl- Mn2++Cl ↑+2HO
2 2 2
(2)ACE
(3)Ⅱ Ⅲ Ⅰ
(4)8NH +3Cl ===6NHCl+N 将固体在烧杯中溶解,取少量溶液于试管①中,然后滴加少量硝酸酸化的
3 2 4 2
AgNO 溶液,有白色沉淀产生,证明有Cl-;取少量溶液于试管②中,加入浓烧碱溶液,加热,再将湿
3
润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝证明有NH
(5)将导气管一端与G口连接,另一端插入盛有NaOH溶液的烧杯中
解析:(1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,MnO +4H++2Cl- Mn2++Cl↑+
2 2
2HO。
2
(2)利用物质溶解时放出的热量促进氨水的挥发来制取氨气,且该物质和氨气不反应,氨气是碱性气体,所以溶
解的物质必须是碱性物质,A.碱石灰、C.生石灰、E.烧碱都是碱性物质,且溶解于水时放出热量,D.五氧化二
磷、B.浓硫酸虽然溶于水时放热,但是属于酸性物质。
(3)氨气中混有水蒸气,氨气是碱性气体,要除去水蒸气只能用碱性物质,故选Ⅱ;制取的氯气中混有氯化氢气
体和水蒸气,氯化氢极易溶于水,氯气也能溶于水,所以不能用水除去氯化氢气体;氯气和水反应生成盐酸和
次氯酸,食盐水中含有氯离子,能抑制氯气的溶解,所以要想除去氯气中的氯化氢 E应选Ⅰ;水蒸气常用浓硫
酸除去,故D选Ⅲ。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气:8NH +3Cl===6NHCl+N ;氯化铵中含有氯离
3 2 4 2
子和铵根离子,氯离子用硝酸酸化的硝酸银溶液检验;氨气用红色石蕊试纸检验。(5)氯气有毒,所以不能直接
排入空气中,但氯气能和水反应生成盐酸和次氯酸,盐酸和次氯酸都能和氢氧化钠反应生成盐,所以除去氯气
可选用氢氧化钠溶液吸收,方法为:将导气管与G口连接,另一端插入盛有NaOH溶液的烧杯中。
21、(1)(NH )S O HO
4 2 2 2
(2)H SO 2HS+3O=====2SO +2HO
2 4 2 2 2 2
(3)HNO 4NH +5O=====4NO+6HO
3 3 2 2
解析:本题考查氮、硫及其化合物的转化关系。由D的相对分子质量比C的相对分子质量大16,容易联想D比
C增加1个氧原子,则D可能是氧化物,而E为酸,则应为含氧酸,而Y是能提供“O”的物质,A为正盐,与
碱 反 应 放 出 的 物 质 能 连 续 两 次 氧 化 最 后 得 一 含 氧 酸 , 可 推 知 A 可 能 是 铵 盐 :
A――→NH ――→NO――→NO ――→HNO ,而A与强酸反应时,生成的物质也会连续氧化两次,最后生成
3 2 3
含氧酸,则 A可能为硫化物(含S2-):A――→HS――→SO ――→SO ――→HSO ,综上所述可确定 A是
2 2 3 2 4
(NH )S。
4 2