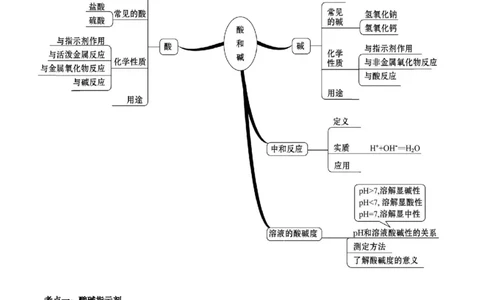
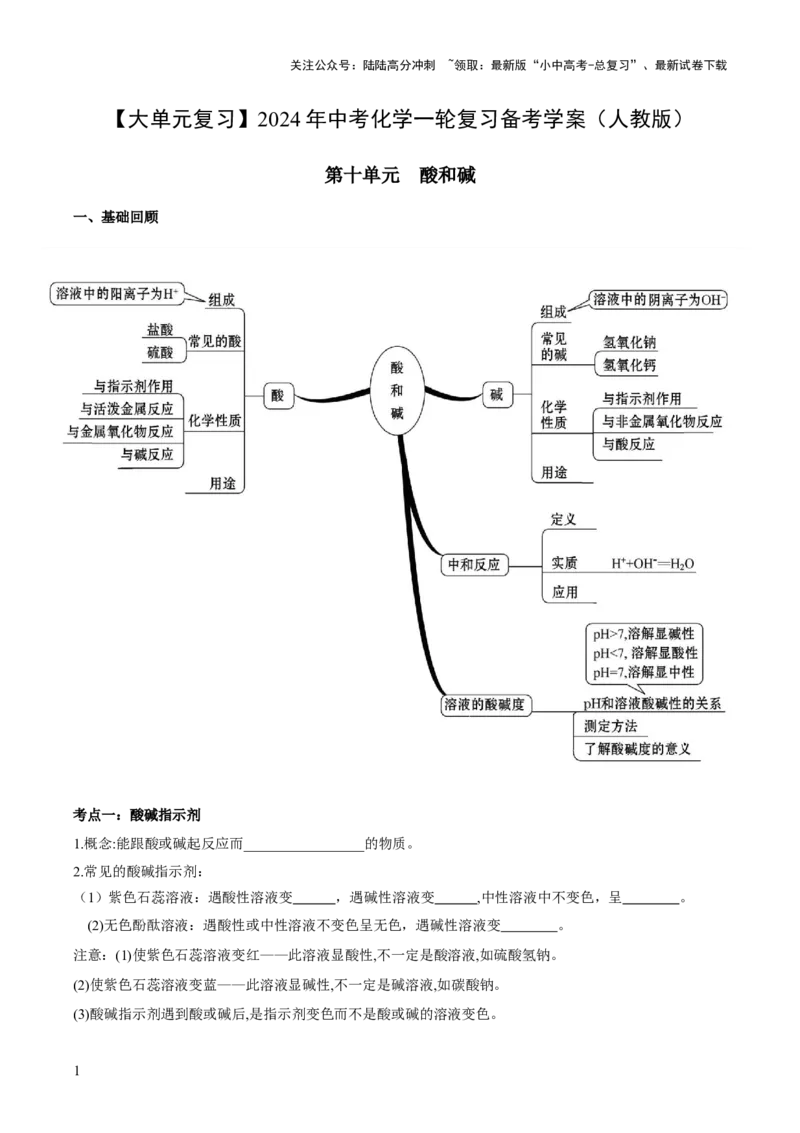
文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【大单元复习】2024 年中考化学一轮复习备考学案(人教版)
第十单元 酸和碱
一、基础回顾
考点一:酸碱指示剂
1.概念:能跟酸或碱起反应而_________________的物质。
2.常见的酸碱指示剂:
(1)紫色石蕊溶液:遇酸性溶液变 ,遇碱性溶液变 ,中性溶液中不变色,呈 。
(2)无色酚酞溶液:遇酸性或中性溶液不变色呈无色,遇碱性溶液变 。
注意:(1)使紫色石蕊溶液变红——此溶液显酸性,不一定是酸溶液,如硫酸氢钠。
(2)使紫色石蕊溶液变蓝——此溶液显碱性,不一定是碱溶液,如碳酸钠。
(3)酸碱指示剂遇到酸或碱后,是指示剂变色而不是酸或碱的溶液变色。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点二:几种常见的酸
1.酸的定义:在水中解离时产生的阳离子全部是 的化合物。
2.酸的组成=
3.盐酸、硫酸的物理性质及用途:
4.浓硫酸的特性与稀释:
(1)浓硫酸的特性。
①吸水性:浓硫酸具有吸水性,在实验室常用作某些气体的___________。如干燥中性气体(H 、O、CO等)
2 2
和酸性气体(HCl、CO、SO 等),可将浓硫酸装入如图的洗气瓶中,然后将气体从长导管通入,此过程属于
2 2
浓盐酸(HCl气体的水溶液) 浓硫酸
色味态 无色 气味的液体 无色黏稠,油状液体
不挥发, (可做干燥剂),
个性对 有挥发性,在空气里会生成 ,有刺激
(化学性质,使有机物炭化),
比 性气味
(化学性质)
腐蚀性 有腐蚀性,对活泼金属腐蚀性强 强腐蚀性
** 错误的表达式 ** ;** 错误的表
** 错误的表达式 ** ;** 错误的表达
达式 **胃液中含有盐酸可帮助消化;**
用途 式 **浓硫酸在实验室里常用作 。
错误的表达式 ** ;④实验室制取
** 错误的表达式 **重要化工原料
CO
2
变化。
②脱水性:能够夺取纸张、木材、布料、皮肤里的氢、氧元素,按水的组成比脱去,使它们脱水生成黑色的炭,
发生炭化,此过程属于 变化。
③强氧化性:与金属反应时一般不生成氢气。
(2)使用注意事项:由于浓硫酸具有脱水性,所以表现出强烈的腐蚀性,若不慎将浓硫酸沾到皮肤上,应立即用
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。
(3)浓硫酸的稀释。
注意:(1)浓盐酸在空气里会形成白雾不是白烟,这是因为浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气
接触,形成 的缘故。
(2)浓盐酸易挥发,露置在空气中溶液质量会 ,溶质质量分数会 。浓硫酸具有吸水性,露置在空气
中,溶液的质量会 ,溶质的质量分数 。
考三:酸的化学性质
1.与酸碱指示剂反应:使紫色石蕊溶液________,使无色酚酞溶液___________。
2.与某些金属反应生成盐和氢气:
例如,铁和盐酸:(写化学方程式,下同)__________________________
铝和稀硫酸:___________________________________
3.与某些金属氧化物反应生成盐和水:
例如,氧化铜和盐酸:__________________________
氧化铁和硫酸:______________________________
4.与碱反应生成盐和水:
例如,盐酸和氢氧化铜:______________________________
硫酸和氢氧化钡:________________________________
5.与某些盐反应生成新酸和新盐:
例如,氯化钡和硫酸:__________________________
硝酸银和盐酸:_____________________________
考点四:几种常见的碱
1.碱的定义:在水中解离时产生的阴离子全部是 的化合物。
2.碱的组成= (NH +相当于金属离子)
4
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3.常见碱的物理性质及用途:
俗名 特性 用途
氢 氧 化 钠 、 ① 溶于水且溶解放 ①气体 ;②生活中可用于除 ;③
NaOH 、 热;② ,③ 。 化工原料,用于制肥皂、石油、造纸等
。
氢 氧 化 钙 、 溶于水。溶解度随温 (①建筑上用来砌砖、刷墙。②农业上用来
Ca(OH) , 度的 ,配制农药(波尔多液) ③石灰水用于
2
溶液称为 。
一 水 合 氨 氨水 易挥发, 的液体 化肥
NH ·HO
3 2
4.Ca(OH) 的制取:
2
(1)第一步:煅烧石灰石(写化学方程式,下同):_____________________。
(2)第二步:生石灰和水反应:______________________。
注意:(1)由于氢氧化钠易潮解,故称量氢氧化钠固体时,要放在_________,不能放在纸上。
(2)强碱有强烈的腐蚀性,使用时须十分小心,若沾在皮肤上,应立即_________,然后再涂上_________。
5.用氢氧化钠和氧化钙干燥气体
氢氧化钠和氧化钙都有强吸水性,所以可作为干燥剂。它们是碱性干燥剂,故可干燥中性气体(CH、CO、
4
O、NO等)、碱性气体(NH )。它们是固体干燥剂,常装在干燥管或U形管里,装在干燥管中时气体流向是
2 3
“大进小出”。
考点五:碱的化学性质
1.能和酸碱指示剂反应:使紫色石蕊溶液_________,使无色酚酞溶液_______。
2.能和某些非金属氧化物反应生成盐和水:
例如,澄清石灰水中通入二氧化碳:(写化学方程式,下同)___________________。
氢氧化钠固体暴露在空气中:________________________。
3.能和酸发生中和反应生成盐和水:
例如,氢氧化钠与盐酸反应:________________________。
4.能和部分盐反应生成新碱和新盐(只有可溶性碱和可溶性盐的溶液才能反应):
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
例如,NaOH溶液与CuSO 溶液:___________________。
4
氢氧化钙溶液与碳酸钠溶液:__________________________。
考点六:中和反应
1.概念:___________作用生成___________的反应。
2.实验探究:
(1)原理:中和反应(如氢氧化钠溶液与盐酸的反应)中,往往无明显的实验现象,无法确定反应是否发生及反
应进行的程度,因此,需要借助指示剂或其他方法来判断。
(2)判断中和反应是否发生的方法及注意事项:
判断依据 注意事项
方法一 借助酸碱指示剂的颜色变化 ①先在碱溶液中滴加几滴酚酞溶液
(若用酸中和碱时)
②为防止酸过量,应逐滴加
入,并不断搅拌或振荡,当溶液恰好由红色变为无色时,恰好完
全中和
方法二 借助反应中的温度变化(若 ①先测量加入烧杯中的碱溶液的温度
用酸中和碱时)
②边加酸溶液,边不断搅拌并及时测量、记录溶液的温度
方法三 借助反应中溶液pH的变化 ①先测出酸溶液的pH
(若用碱中和酸时)
②逐滴加入碱溶液,并不断搅拌,同时测定溶液pH
③需保证溶液的pH≥7,才能证明反应发生了
3.实质:酸溶液中的______和碱溶液中的_______结合生成_______。
4.应用:
(1)改良土壤:农业上用__________改良酸性土壤。
(2)处理废水:如用熟石灰中和硫酸厂的污水,化学方程式为____________。
(3)用于医药:用含Al(OH) 或Mg(OH) 的药物中和过多的胃酸,反应的化学方程式为
3 2
______________________________、_____________________。
考点七:溶液酸碱度的表示——pH
1.溶液的酸碱性和酸碱度:
(1)溶液的酸碱性是指溶液显酸性、中性或碱性,可以用_______________来粗略测定。
(2)溶液酸碱性的强弱程度叫溶液的酸碱度,常用pH表示。pH的范围通常为_________。
2.pH与溶液的酸碱度:
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)pH<7溶液呈_________,pH越小,_________越强;
(2)pH>7溶液呈_________,pH越大,_________越强;
(3)pH=7溶液呈_________。
3.pH的测定方法:
(1)粗略测定(用pH试纸):在______________上放一片pH试纸,用玻璃棒蘸取待测液体滴到___________上,
把_____________________与_______________对照,即可得出待测液体的pH。此法只能粗略测出pH的整
数值(pH试纸必须是干燥的)。
(2)精确测定(用pH计):pH计又叫酸度计,是用来精确测定溶液pH的仪器,可以精确到0.1和0.01。
4.溶液酸碱度的应用:
(1)了解土壤的酸碱性,农作物一般适宜在pH为7或接近7的土壤中生长。
(2)测定雨水的pH(因溶解有CO,正常雨水的pH约为______,酸雨的pH_____),了解空气的污染情况。
2
(3)测定人体体液的pH,了解人体的健康状况。
考点八:氢氧化钠变质的探究
1.原因:NaOH与空气中的______ 反应生成碳酸钠,反应原理:________________
2
2.如何检验NaOH溶液是否变质:
(1)加入过量的稀盐酸,现象:______,
反应原理:________________________________
(2)加入澄清石灰水,现象:________________,
反应原理:________________________________
(3)加入Ba(OH) 或CaCl 溶液,现象:________________________________ ,反应原
2 2
理:__________________________ 、_________________________。
3.除杂:NaOH中混有NaCO:在溶液中滴入澄清石灰水至不再产生沉淀为止,过滤,反应
2 3
理:__________________________ 。
4.探究氢氧化钠是部分变质还是全部变质的方案设计
实验步骤 实验目的 现象 结论
a.取部分样品溶于水,加 除去NaOH 生成白色沉淀
过量BaCl (CaCl )
2 2 中的Na 2 CO 3 BaCl 2 +Na 2 CO 3
溶液 ====BaCO ↓+
3
2NaCl
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
b.________________,滴 检验是否含有NaOH 溶液变红 ________
加无色酚酞溶液
溶液不变色 ________
注意:要确认是否有NaOH,在检验NaOH时必须排除NaCO 的干扰,因为NaCO 溶液也呈碱性,也能使酚
2 3 2 3
酞溶液变红。在除NaCO 时,不能用盐酸,因为盐酸与NaOH也反应,也不能用Ca(OH) ,因为会与NaCO 反
2 3 2 2 3
应生成NaOH,干扰NaOH的检验。
二、基础达标
1.小刚同学用如图所示装置进行“粒子不断运动”的研究,一段时
间后,可观察到无色酚酞溶液变红,则物质X是( )
A.浓氨水 B.浓盐酸 C.浓硫酸 D.浓食盐水
2.消除铁制品表面的锈可用( )
A.水 B.稀盐酸 C.洗涤剂 D.食盐水
3.浓硫酸和浓盐酸敞口放置在空气中一段时间后,溶液中( )
A.溶质的质量分数都变小 B.溶液的质量都增大
C.溶质的质量分数都变大 D.溶质的质量分数前者变大,后者变小
4.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的
共同性质的是( )
A.能使紫色石蕊试液变为红色 B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀 D.能与锌反应生成氢气
5.下列物质常用于改良酸性土壤的是( )
A.熟石灰 B.烧碱 C.食盐 D.大理石
6.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
序号 实验 现象
A 将氢氧化钠固体放在表面皿上,放置一会儿 固体受潮,逐渐溶解
B 向盛有氢氧化钠溶液的试管中滴入无色酚酞试液 溶液变红
C 向盛有氢氧化钠溶液的试管中滴加稀盐酸 有氯化钠生成
D 向盛有氢氧化钠溶液的试管中滴加硫酸铜溶液 产生蓝色沉淀
7.氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质,其本质原因是( )
A.都能与指示剂作用 B.都能解离出氢氧根离子
C.都能解离出金属阳离子 D.都含有氢元素和氧元素
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
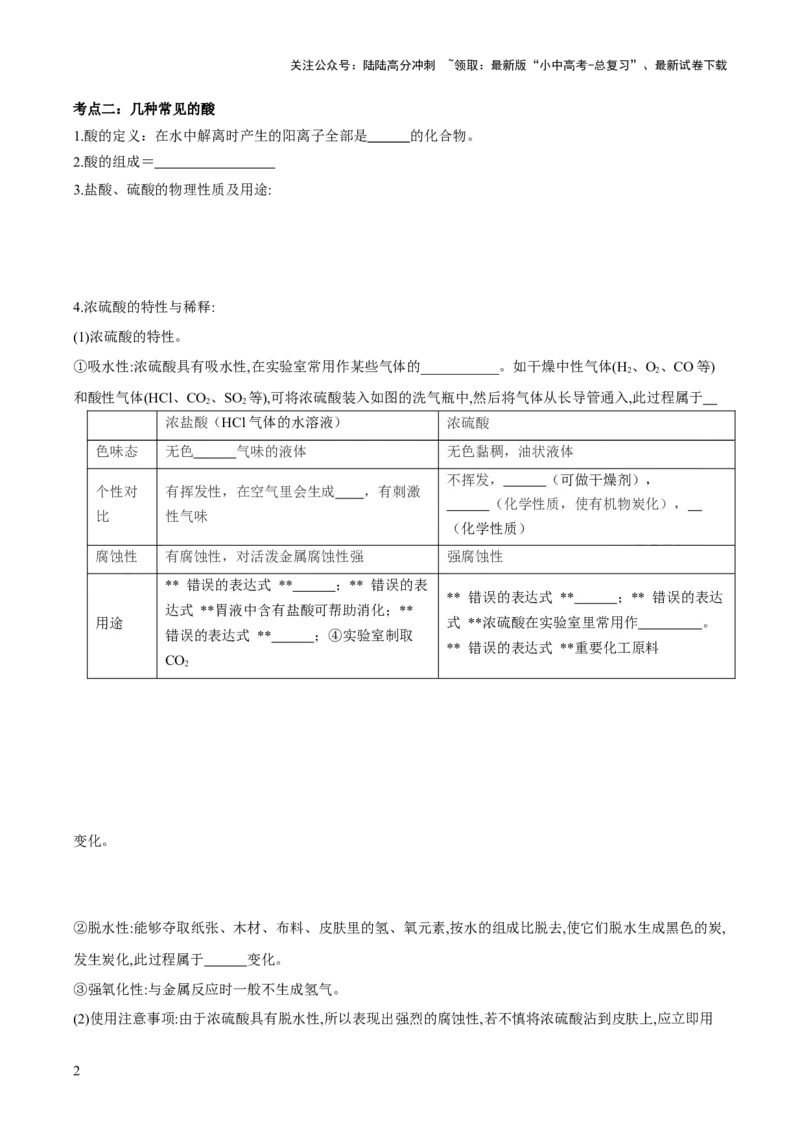
8.下列验证“CO 与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)(
2
)
A. B. C. D.
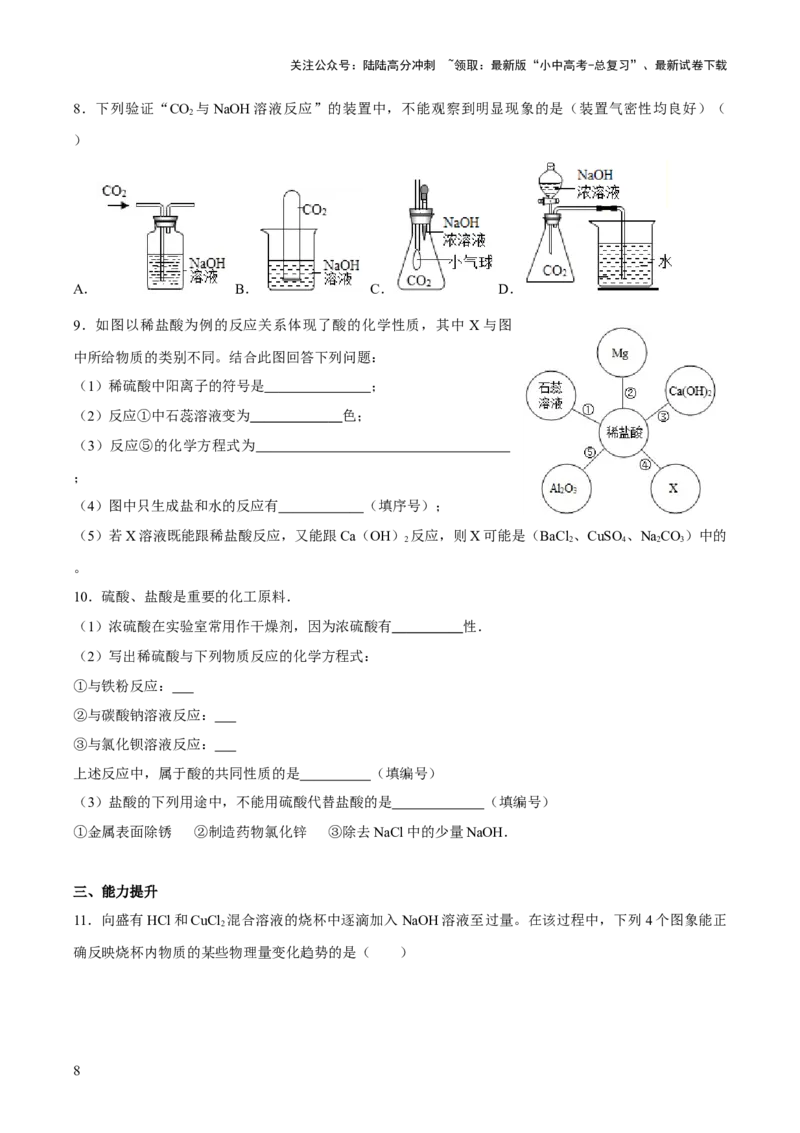
9.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中 X与图
中所给物质的类别不同。结合此图回答下列问题:
(1)稀硫酸中阳离子的符号是 ;
(2)反应①中石蕊溶液变为 色;
(3)反应⑤的化学方程式为
;
(4)图中只生成盐和水的反应有 (填序号);
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH) 反应,则X可能是(BaCl 、CuSO 、NaCO)中的
2 2 4 2 3
。
10.硫酸、盐酸是重要的化工原料.
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性.
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
三、能力提升
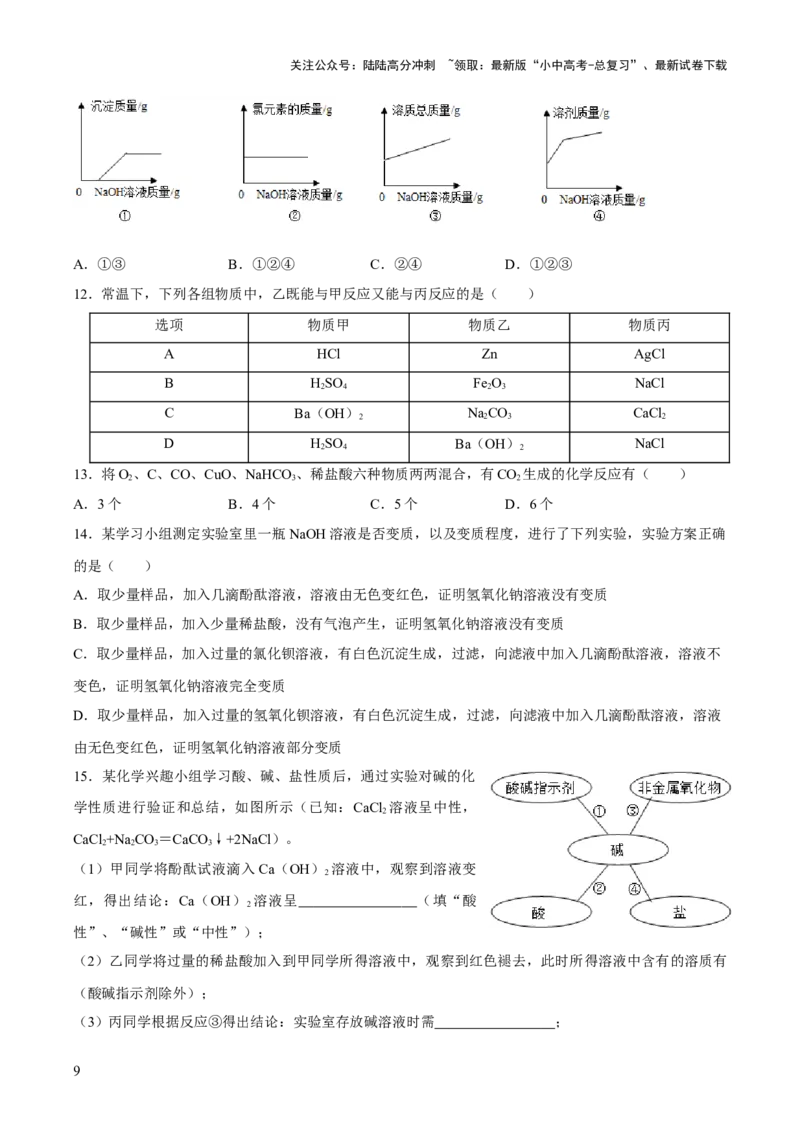
11.向盛有HCl和CuCl 混合溶液的烧杯中逐滴加入NaOH溶液至过量。在该过程中,下列4个图象能正
2
确反映烧杯内物质的某些物理量变化趋势的是( )
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.①③ B.①②④ C.②④ D.①②③
12.常温下,下列各组物质中,乙既能与甲反应又能与丙反应的是( )
选项 物质甲 物质乙 物质丙
A HCl Zn AgCl
B HSO Fe O NaCl
2 4 2 3
C Ba(OH) NaCO CaCl
2 2 3 2
D HSO Ba(OH) NaCl
2 4 2
13.将O、C、CO、CuO、NaHCO 、稀盐酸六种物质两两混合,有CO 生成的化学反应有( )
2 3 2
A.3个 B.4个 C.5个 D.6个
14.某学习小组测定实验室里一瓶NaOH溶液是否变质,以及变质程度,进行了下列实验,实验方案正确
的是( )
A.取少量样品,加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液没有变质
B.取少量样品,加入少量稀盐酸,没有气泡产生,证明氢氧化钠溶液没有变质
C.取少量样品,加入过量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液不
变色,证明氢氧化钠溶液完全变质
D.取少量样品,加入过量的氢氧化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液
由无色变红色,证明氢氧化钠溶液部分变质
15.某化学兴趣小组学习酸、碱、盐性质后,通过实验对碱的化
学性质进行验证和总结,如图所示(已知:CaCl 溶液呈中性,
2
CaCl +Na CO=CaCO ↓+2NaCl)。
2 2 3 3
(1)甲同学将酚酞试液滴入Ca(OH) 溶液中,观察到溶液变
2
红,得出结论:Ca(OH) 溶液呈 (填“酸
2
性”、“碱性”或“中性”);
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到红色褪去,此时所得溶液中含有的溶质有
(酸碱指示剂除外);
(3)丙同学根据反应③得出结论:实验室存放碱溶液时需 ;
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)丁同学将NaCO 溶液加入Ca(OH) 溶液中,充分反应后,与乙同学所得溶液混合,静置后发现:
2 3 2
上层为无色透明的溶液,底部有白色沉淀。则上层溶液中一定含有的溶质是 (酸碱指示剂除
外),可能含有的溶质是 ;为验证可能含有的溶质,应该补充的实验操作是
。
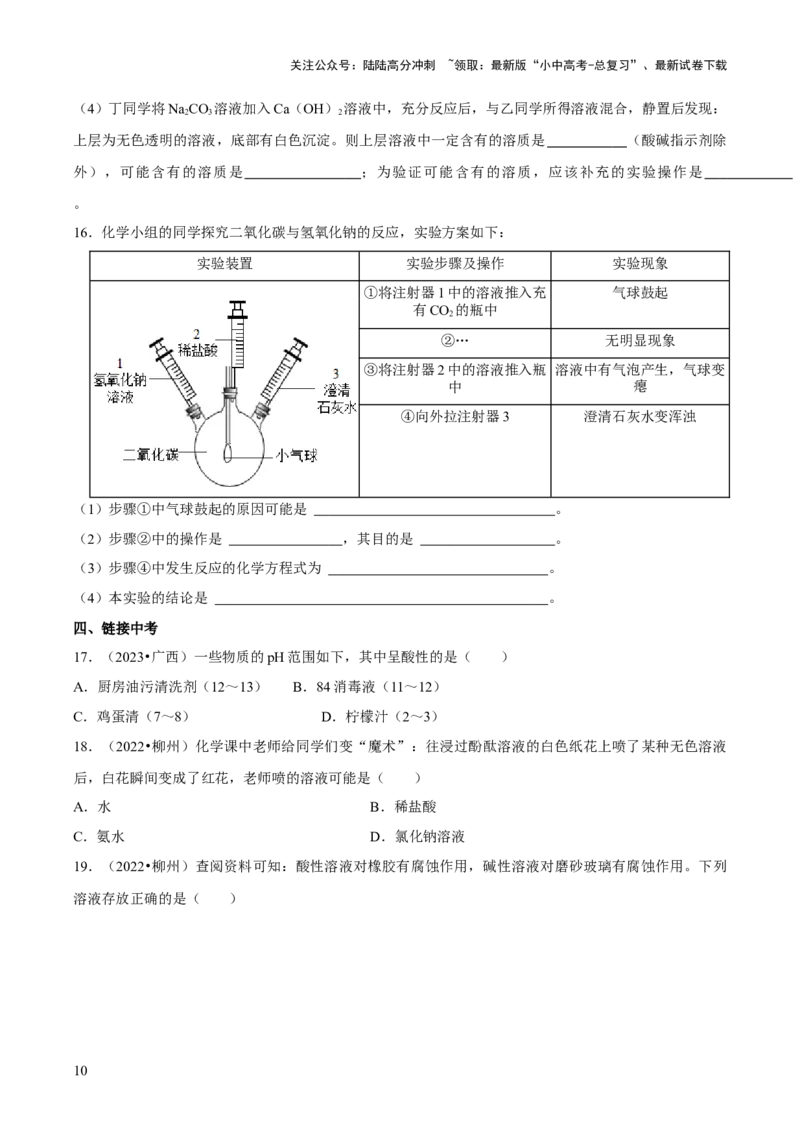
16.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液推入充 气球鼓起
有CO 的瓶中
2
②… 无明显现象
③将注射器2中的溶液推入瓶 溶液中有气泡产生,气球变
中 瘪
④向外拉注射器3 澄清石灰水变浑浊
(1)步骤①中气球鼓起的原因可能是 。
(2)步骤②中的操作是 ,其目的是 。
(3)步骤④中发生反应的化学方程式为 。
(4)本实验的结论是 。
四、链接中考
17.(2023•广西)一些物质的pH范围如下,其中呈酸性的是( )
A.厨房油污清洗剂(12~13) B.84消毒液(11~12)
C.鸡蛋清(7~8) D.柠檬汁(2~3)
18.(2022•柳州)化学课中老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花上喷了某种无色溶液
后,白花瞬间变成了红花,老师喷的溶液可能是( )
A.水 B.稀盐酸
C.氨水 D.氯化钠溶液
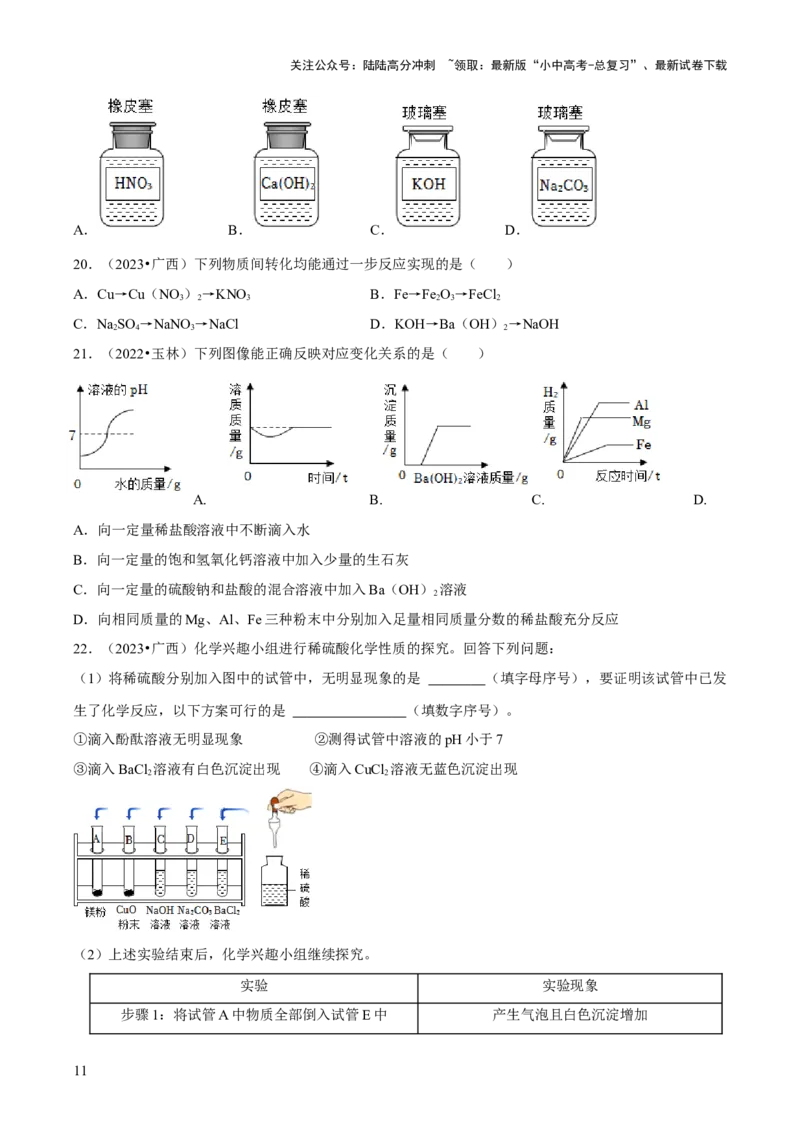
19.(2022•柳州)查阅资料可知:酸性溶液对橡胶有腐蚀作用,碱性溶液对磨砂玻璃有腐蚀作用。下列
溶液存放正确的是( )
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. B. C. D.
20.(2023•广西)下列物质间转化均能通过一步反应实现的是( )
A.Cu→Cu(NO )→KNO B.Fe→Fe O→FeCl
3 2 3 2 3 2
C.NaSO →NaNO →NaCl D.KOH→Ba(OH)→NaOH
2 4 3 2
21.(2022•玉林)下列图像能正确反映对应变化关系的是( )
A. B. C. D.
A.向一定量稀盐酸溶液中不断滴入水
B.向一定量的饱和氢氧化钙溶液中加入少量的生石灰
C.向一定量的硫酸钠和盐酸的混合溶液中加入Ba(OH) 溶液
2
D.向相同质量的Mg、Al、Fe三种粉末中分别加入足量相同质量分数的稀盐酸充分反应
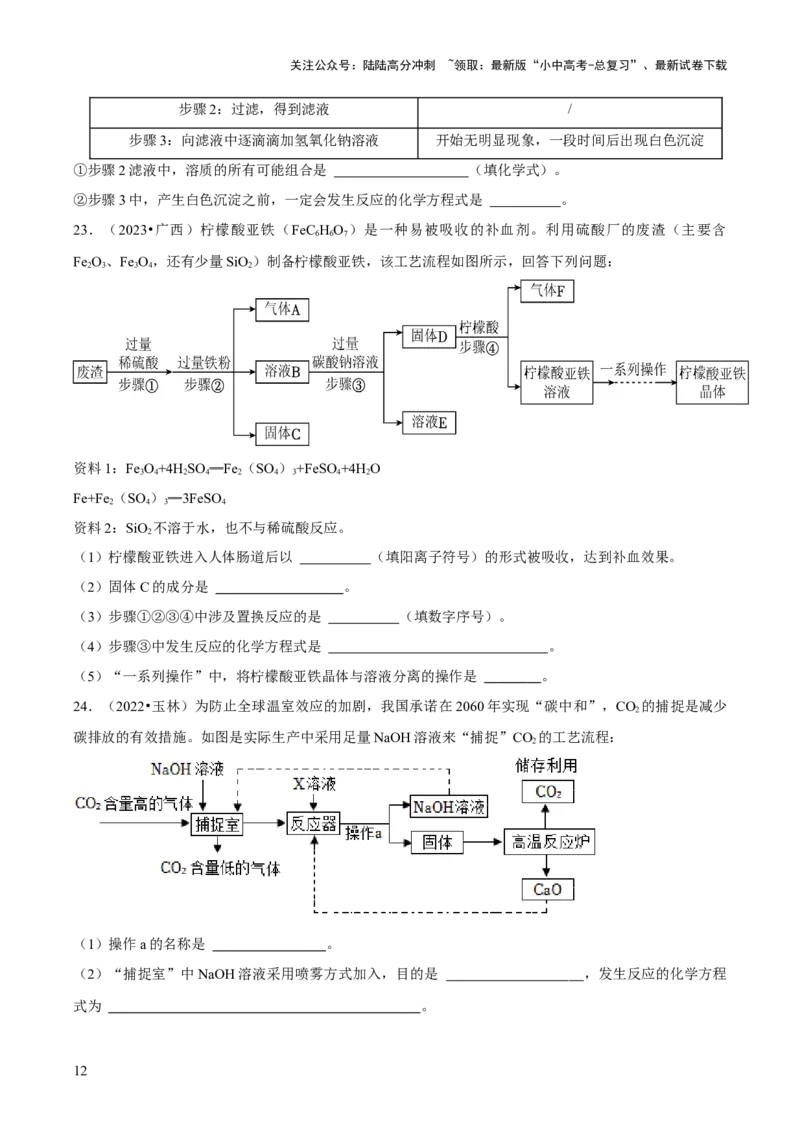
22.(2023•广西)化学兴趣小组进行稀硫酸化学性质的探究。回答下列问题:
(1)将稀硫酸分别加入图中的试管中,无明显现象的是 (填字母序号),要证明该试管中已发
生了化学反应,以下方案可行的是 (填数字序号)。
①滴入酚酞溶液无明显现象 ②测得试管中溶液的pH小于7
③滴入BaCl 溶液有白色沉淀出现 ④滴入CuCl 溶液无蓝色沉淀出现
2 2
(2)上述实验结束后,化学兴趣小组继续探究。
实验 实验现象
步骤1:将试管A中物质全部倒入试管E中 产生气泡且白色沉淀增加
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
步骤2:过滤,得到滤液 /
步骤3:向滤液中逐滴滴加氢氧化钠溶液 开始无明显现象,一段时间后出现白色沉淀
①步骤2滤液中,溶质的所有可能组合是 (填化学式)。
②步骤3中,产生白色沉淀之前,一定会发生反应的化学方程式是 。
23.(2023•广西)柠檬酸亚铁(FeC HO )是一种易被吸收的补血剂。利用硫酸厂的废渣(主要含
6 6 7
Fe O、Fe O,还有少量SiO)制备柠檬酸亚铁,该工艺流程如图所示,回答下列问题:
2 3 3 4 2
资料1:Fe O+4H SO ═Fe (SO )+FeSO+4H O
3 4 2 4 2 4 3 4 2
Fe+Fe (SO )═3FeSO
2 4 3 4
资料2:SiO 不溶于水,也不与稀硫酸反应。
2
(1)柠檬酸亚铁进入人体肠道后以 (填阳离子符号)的形式被吸收,达到补血效果。
(2)固体C的成分是 。
(3)步骤①②③④中涉及置换反应的是 (填数字序号)。
(4)步骤③中发生反应的化学方程式是 。
(5)“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是 。
24.(2022•玉林)为防止全球温室效应的加剧,我国承诺在2060年实现“碳中和”,CO 的捕捉是减少
2
碳排放的有效措施。如图是实际生产中采用足量NaOH溶液来“捕捉”CO 的工艺流程:
2
(1)操作a的名称是 。
(2)“捕捉室”中NaOH溶液采用喷雾方式加入,目的是 ,发生反应的化学方程
式为 。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
( 3 ) “ 捕 捉 室 ” 中 的 NaOH 溶 液 与 “ 反 应 器 ” 中 的 X 溶 液 可 否 互 换 ? 原 因 是
。
(4)整个流程中可以循环使用的物质是 (填化学式)。
25.(2022•桂林)实验室里有一瓶未盖瓶塞的碱石灰,某学习小组的同学在老师的指导下,以“碱石灰
成分和性质”为主题开展项目式学习。
任务一:查阅资料认识碱石灰
Ⅰ.制碱石灰的流程:
Ⅱ.Ca(OH) 的分解温度是580℃;NaOH受热不分解。
2
(1)煅烧石灰石发生反应的化学方程式是 。
(2)上述制得的碱石灰主要含有NaOH、 和少量水。
任务二:探究未盖瓶塞的“碱石灰”样品的成分
【作出猜想】样品中的成分可能有下列几种:
猜想1:Ca(OH)、NaOH
2
猜想2:CaCO 、Ca(OH)、NaOH
3 2
猜想3:C aCO、NaOH、NaCO
3 2 3
猜想4:CaCO 、NaCO
3 2 3
【实验探究】该小组同学设计并进行了如下实验(已知BaCl 溶液呈中性)。
2
实验步骤 现象 结论
①取5g“碱石灰”样品于烧杯中,加入50g水,充分搅拌 烧杯底部有白色 猜想1不正确
后,静置 固体
②取①烧杯中上层清液少许,加入试剂Ⅹ 无明显现象 猜想2不正确
③取①烧杯中上层清液少许,滴2滴酚酞溶液 溶液变红 猜想3正确,而猜想4不
正确
④取③变红的溶液,加入过量BaCl 溶液
2
【反思评价】
(3)实验①方案不严密,理由是 。
(4)试剂X可选用 (填字母序号)。
A.氯化铁溶液 B.稀盐酸 C.碳酸钠溶液
任务三:测定未盖瓶塞的“碱石灰”样品中各成分的含量
该小组同学另取“碱石灰”样品 10.00g,加入100.00g水,充分搅拌、过滤
后,按如图进行实验。实验记录如表。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
滤渣质量 活塞关闭时整个装置总质量(仪器+药 打开瓶塞和活塞反应完成后整个装置总质量
品) (仪器+药品)
8.00g 442.64g 442.20g
【结论与评价】
(5)根据数据可计算原样品中各成分的含量,其中NaOH的质量分数是 。
(6)该小组同学按上述实验规范操作,测得样品中 NaCO 的质量分数偏小,原因是
2 3
。
参考答案:
一、基础回顾
考点一:酸碱指示剂
1.显示不同颜色。 2.(1)紫色。 (2)红色,
考点二:几种常见的酸
1.H+。2.H++酸根离子
3.有刺激性;白雾;除锈;除水垢;有吸水性;有脱水性;有强氧化性;除锈;气体干燥剂
4.(1)①吸干燥剂。物理。②化学。(2)即用大量水冲洗,碳酸氢钠溶液。(3)注意:(1)盐酸小液滴。(2)减少,
减小。增大,变小。
考三:酸的化学性质
1.变红色,不变色。
2.Fe + 2HCl = FeCl + H ↑;2Al +3H SO = Al(SO ) +3 H ↑。
2 2 2 4 2 4 3 2
3.CuO + 2HCl = CuCl + H O;Fe O + 3H SO = Fe (SO ) + 3H O 。
2 2 2 3 2 4 2 4 3 2
4.2HCl + Cu(OH) = CuCl + 2HO;HSO + Ba(OH) == BaSO↓ + 2H O 。
2 2 2 2 4 2 4 2
5.HSO + BaCl == BaSO ↓ + 2HCl;HCl + AgNO == AgCl↓ + HNO
2 4 2 4 3 3
考点四:几种常见的碱
1.氢氧根离子(OH—)。2.金属离子+OH—
3.
俗名 特性 用途
氢 氧 化 钠 火碱、烧碱、 ①易溶于水且溶解放 ①气体干燥剂;②生活中可用于除油污;③化工
NaOH 苛性钠 热;②有吸水性, 原料,用于制肥皂、石油、造纸等
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
③易潮解
氢 氧 化 钙 熟石灰、消石 微溶于水。溶解度随温 (①建筑上用来砌砖、刷墙。②农业上用来改良
Ca(OH) 灰,溶液称为 度的升高而减小 酸性土壤,配制农药(波尔多液) ③石灰水用
2
石灰水 于检验CO 气体
2
一 水 合 氨 氨水 易挥发,有刺激性气味 化肥
NH ·HO 的液体
3 2
4.(1)CaCO CaO + CO ↑。 (2)CaO + H O = Ca(OH) 。
3 2 2 2
注意:(1)玻璃器皿里。(2)用大量水冲洗,硼酸溶液。
考点五:碱的化学性质
1.变蓝色,变红色。
2.Ca(OH) + CO = CaCO ↓+ H O。 2NaOH + CO = NaCO + H O。
2 2 3 2 2 2 3 2
3.HCl + NaOH = NaCl +H O 。
2
4.CuSO +2NaOH=Cu(OH) ↓+Na SO 。 Ca(OH) + Na CO = CaCO↓+ 2NaOH。
4 2 2 4 2 2 3 3
考点六:中和反应
1.酸与碱;盐和水。 3.H+;OH-;水。
4.(1)熟石灰。 (2)HSO + Ca(OH) = CaSO + 2H O。
2 4 2 4 2
(3)3HCl + Al(OH) = AlCl + 3H O、2HCl + Mg(OH) = MgCl + 2HO。
3 3 2 2 2 2
考点七:溶液酸碱度的表示——pH
1.(1)酸碱指示剂。 (2)0~14。
2.(1)酸性;酸性; (2)碱性;碱性; (3)中性。
3.(1)玻璃片或白瓷板;pH试纸;pH试纸显示的颜色;标准比色卡。
4.(2)5.6;<5.6。
二、基础达标
1.A:2.B:3.A:4.C:5.A:6.C:7.B:8.A
9.(1)H+;(2)红;(3)Al O+6HCl=2AlCl +3H O;(4)③⑤;(5)NaCO 。
2 3 3 2 2 3
10.(1) 吸水.(2)①Fe+H SO =FeSO +H ↑ ②NaCO+H SO ═NaSO +H O+CO↑
2 4 4 2 2 3 2 4 2 4 2 2
③HSO +BaCl ═BaSO↓+2HCl ①② ;(3) ②③
2 4 2 4
三、能力提升
11.B;12.C;13.C;14.C
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
15.(1) 碱性;(2) CaCl 、HCl ;(3)密封保存 ;
2
(4) NaCl ;CaCl ;取少量上层清液于试管中,向试管内滴加碳酸钠溶液,如果有白色沉淀生成,
2
说明含有氯化钙,如果没有白色沉淀生成,说明不含有氯化钙。
16.(1)NaOH溶液吸收CO 装置内压强变小,气球鼓起;
2
(2)向外拉注射器3(或充分振荡),证明步骤1中装置内的CO 已被完全吸收;
2
(3)Ca(OH)+CO ═HO+CaCO ↓;
2 2 2 3
(4)CO 能和NaOH反应且生成了碳酸盐。
2
四、链接中考
17.D;18.C;19.B;20.A;21.D
22.(1)C;①②④;(2)①MgCl 、HCl;MgCl 、HCl、BaCl ;MgCl 、HCl、MgSO ;
2 2 2 2 4
②NaOH+HCl=NaCl+H O。
2
23.(1)Fe2+;(2)SiO 和Fe;(3)②;(4)FeSO +Na CO=FeCO↓+Na SO ;(5)过滤。
2 4 2 3 3 2 4
24.(1)过滤。(2)增大反应物接触面积,使反应更快、更充分;2NaOH+CO ═NaCO+H O。
2 2 3 2
(3)不能互换,是因为氢氧化钙微溶于水,氢氧化钠易溶于水,相同条件下氢氧化钙吸收二氧化碳的效
果比氢氧化钠差。(4)NaOH、CaO。
25.(1)CaCO CaO+CO ↑;(2)Ca(OH)(或氢氧化钙);
3 2 2
【实验探究】有白色沉淀生成,溶液仍为红色;(3)Ca(OH) 微溶于水,白色固体可能是Ca(OH)
2
;(4)C;(5)9.4%;(6)装置中有CO 残留(或浓硫酸吸收了空气中的水分)。
2 2
16