文档内容
化学部分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39 Ca-40
Zn-65 Ba-137
一、选择题(本大题包括10个小题,每小题2分,共20分。每小题给出的四个选项中,只
有一个符合题目要求,请在答题卡选择题栏内用2B铅笔将对应题目的答案标号涂黑。)
1. 大自然是我们美丽的家园。下列不利于保护环境的是
A. 分类回收垃圾 B. 任意排放废水
C. 积极植树造林 D. 净化处理废气
【答案】B
2. KMnO 属于第三类易制毒化学品。下列说法错误的是
4
A. KMnO 只能发生分解反应 B. 不能将KMnO 带出化学实验室
4 4
C. 用KMnO 制毒品是化学变化 D. 应严格控制KMnO 流入非法渠道
4 4
【答案】A
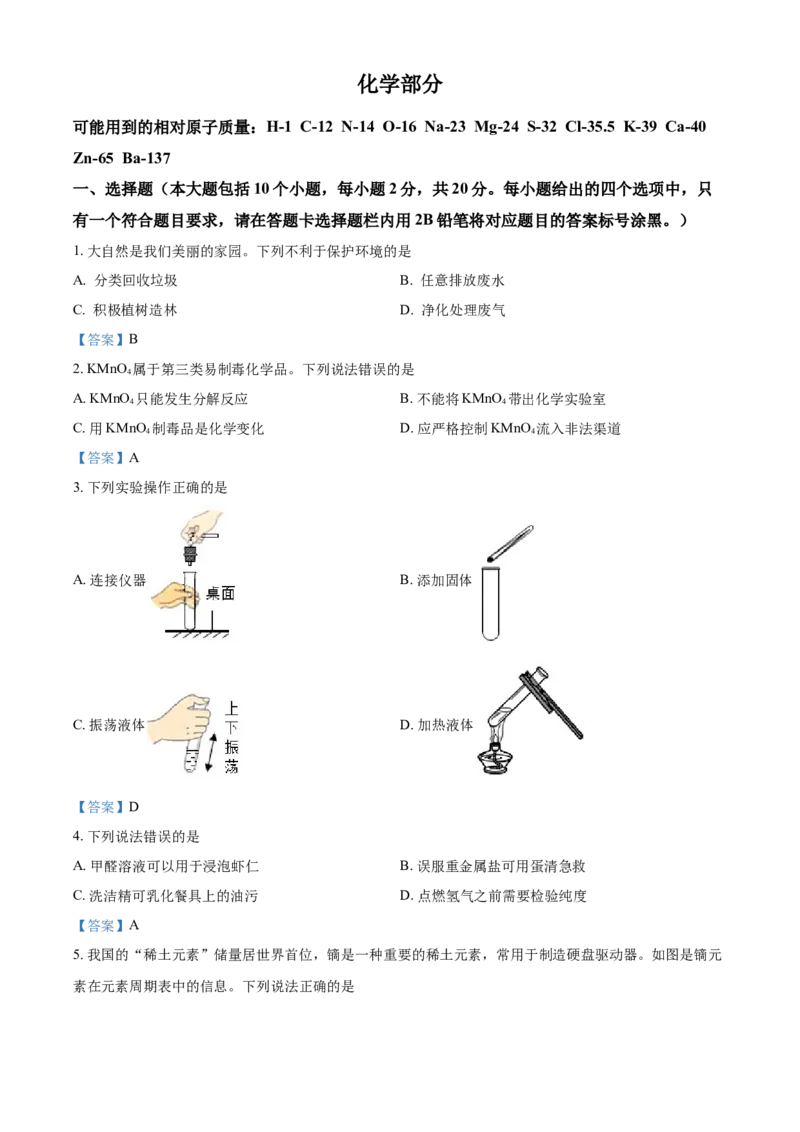
3. 下列实验操作正确的是
A. 连接仪器 B. 添加固体
C. 振荡液体 D. 加热液体
【答案】D
4. 下列说法错误的是
A. 甲醛溶液可以用于浸泡虾仁 B. 误服重金属盐可用蛋清急救
C. 洗洁精可乳化餐具上的油污 D. 点燃氢气之前需要检验纯度
【答案】A
5. 我国的“稀土元素”储量居世界首位,镝是一种重要的稀土元素,常用于制造硬盘驱动器。如图是镝元
素在元素周期表中的信息。下列说法正确的是A. 镝为非金属元素 B. 镝的元素符号可写为dy
C. 镝原子的质子数为66 D. 镝的相对原子质量为162.5g
【答案】C
6. 在成熟辣椒中能提取一种天然无害的红色素——辣椒红色素(C H O),广泛应用在食品加工、医药
40 56 3
等产业中、下列说法正确的是
A. 辣椒红色素是一种人工合成的氧化物
B. 辣椒红色素中碳元素的质量分数最大
C. 辣椒红色素由碳、氢、氧三种原子构成
D. 辣椒红色素中碳、氢、氧元素的质量比为40:56:3
【答案】B
7. 下列排序正确的是
A. 分子间的空隙: B. 原子核外电子层数:
C. 地壳中元素含量: D. 空气中物质的含量:
【答案】A
8. 探究燃烧的条件便于控制燃烧。可燃物燃烧的一般条件是:①可燃物与O 接触;②温度达到可燃物的着
2
火点。用如图装置探究,下列说法正确的是
A. 欲证明条件①:先通O,再通N
2 2
B. 欲证明条件②:先通N,再点燃酒精灯
2
C. 欲证明条件①②:先通O,再点燃酒精灯,然后立即改通N
2 2
D. 试管中的氢氧化钠溶液可以检验并吸收木炭燃烧生成的CO
2
【答案】C9. 下列实验方法不能达到目的的是
选项 实验目的 实验方法
A 除去O 中少量的水蒸气 将气体通过盛有足量浓硫酸的洗气瓶
2
B 鉴别浓盐酸和浓硫酸 打开瓶盖,利用煽动 的方法闻气味
取样于试管中,加入适量 的AgNO 溶液和足
C 检验某溶液中是否含有Cl- 3
量的稀硝酸
向混合溶液中加入过量的氢氧化钠溶液,搅
D 分离溶液中的NaSO 和MgSO 拌、过滤、洗涤,得滤液:再将滤渣放入烧
2 4 4
杯中,加入适量的稀硫酸
A. A B. B C. C D. D
【答案】D
10. 有一包不纯的KCO 样品,含有一定量的KOH和KCl。现需测定该样品中KCO 的质量分数,取10g
2 3 2 3
样品充分溶解后进行实验。下列方案合理的是
A. 加入过量的Ca(OH) 固体,充分反应后过滤,称滤渣的质量
2
B. 加入足量溶质质量分数为7.3%的稀盐酸,称反应后溶液的质量
C. 加入足量的MgCl 溶液,充分反应后过滤、洗涤,将滤渣干燥、称重
2
D. 加入足量的BaCl 溶液,充分反应后过滤,洗涤,将滤渣干燥、称重
2
【答案】D
二、非选择题(本大题包括7个小题,15题(4)②、16题(2)②各2分,其余每空1分,
共40分。请将下列各题应答内容,填写到答题卡相应题号的空格内。)
11. 化学使世界变得更加绚丽多彩。
(1). 我国新疆盛产的棉花是优质的长绒棉,棉属于______(填“合成”或“天然”)纤维。
(2). 天然气可用作汽车燃料,天然气的主要成分是______。
(3). 一些烟花中加入镁粉,利用镁燃烧产生了______的现象。
(4). 利用化学方法制取加碘食盐,适当补碘可以预防的疾病是______。
(5). 合理使用化肥能提高水稻的产量。尿素CO(NH ) 是一种肥效高的氮肥。现有一尿素样品,测得其中
2 2
氮元素的质量分数为43.2%,则该尿素样品中尿素的质量分数为______。(结果保留0.1%)
【答案】(1). 天然
(2). 甲烷 (3). 耀眼的白光
(4). 甲状腺肿大 (5). 92.6%
12. 实验室制备CO 并探究其性质。
2(1). 制取CO 可选择的发生装置是______。(填字母序号)
2
(2). 用C装置收集CO,验满的方法是______。
2
的
(3). D装置中,m、n处分别放有湿润、干燥 蓝色石蕊试纸,证明CO 能与水反应的现象是______;通过
2
E装置产生的现象可证明CO 具有______的性质。
2
(4). 中国将力争2030年前实现碳达峰、2060年前实现碳中和。中国承诺实现从碳达峰到碳中和的时间,远
远短于发达国家所用的时间。“低碳生活,人人有责”,提出一条合理的低碳出行建议______。
【答案】(1). B (2). 把燃着的木条放在导管口a处,木条熄灭说明满了
(3). ①. m处石蕊试纸变红色 ②. 密度大于空气、不燃烧也不支持燃烧
(4). 尽量少开私家车
13. 阅读短文,回答问题。
自制米酒
北魏贾思勰的著作《齐民要术》是世界上最早记录食品酿造的典籍,对我国传统的酿酒方法有较详细的叙
述,文中记载“浸曲三日,如鱼眼汤沸,酘米”,即曲要晒干,磨细,浸曲三日,待曲内的酵母菌和霉菌
等微生物初步繁殖至液体内不断有鱼眼般大小的气流冒出时,即可拌入蒸熟后摊凉的米饭中进行发酵。
《齐民要术》中对酿酒用水及酿酒季节的掌握也有记裁,“初冻后,尽年暮,水脉既定,收取则用,其春
酒及余月,皆须煮水为五沸汤,待冷,浸曲,不然则动。”这是对浸曲用水的要求。除初冻的冬月和年底
的腊月外,酿酒时一律要把浸曲的水煮沸五次,不然,酒就会变质,这说明古人已经知道天冷时水温低,
微生物活动能力弱,可以直接取水浸曲;天气稍暖,就要将水煮沸灭菌。古代没有控制温度的设备,只能
选择适宜的季节,通常在春,秋两季酿酒。
谷物酿造的发酵过程可以简单表示为:
(1). 酸米酒所用的原料主要是糯米,糯米富含的营养素是______。
(2). 天冷时,可以直接取水浸曲酿酒的原因是______。
(3). 葡萄糖(C H O)转化为乙醇(C HOH)的过程中还生成了二氧化碳,写出该转化过程的化学方程
6 12 6 2 5
式______。
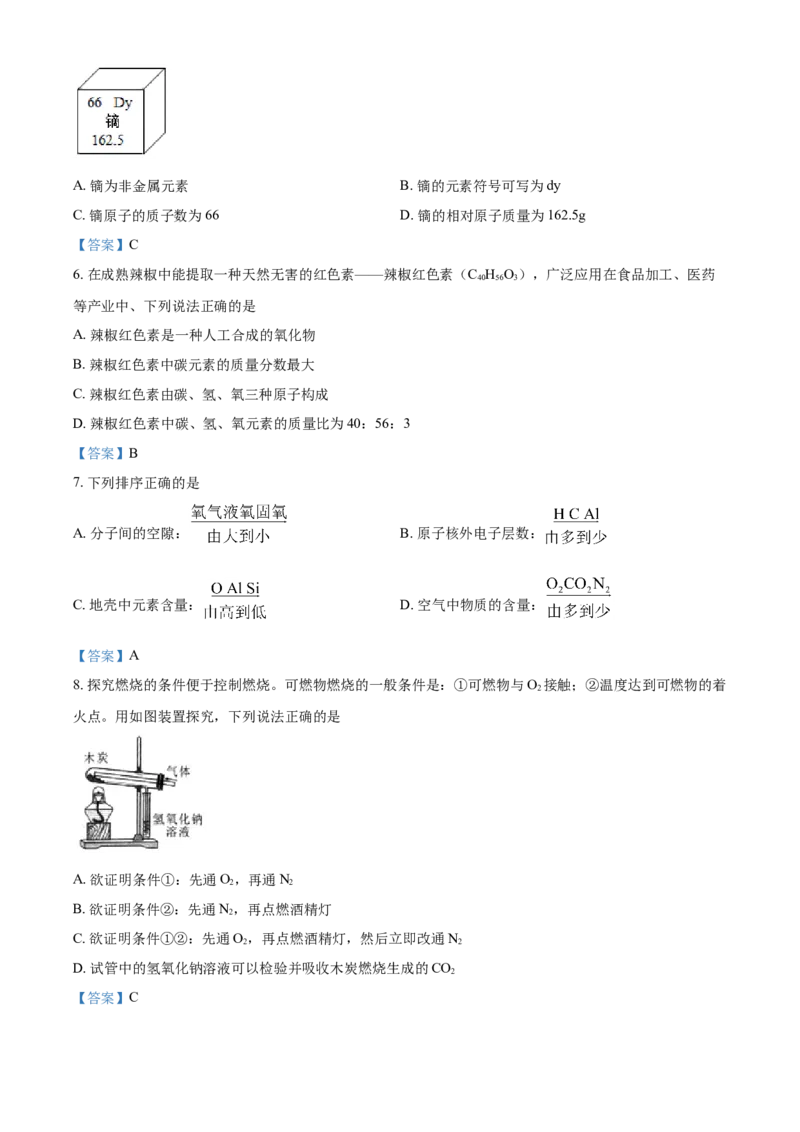
(4). 某兴趣小组自制米酒,测得某次米酒酿制过程中酒精度与pH随时间变化的实验数据如下图。据图分析,米酒的酒精度随时间的变化趋势是______;随时间推移,米酒的pH逐渐减小的原因是______。
【答案】(1). 糖类
(2). 天冷水温低,微生物活动能力弱
(3).
(4). ①. 开始几天酒精度不断变大,第7天以后酒精度几乎不再变化 ②. 部分乙醇转化为乙酸
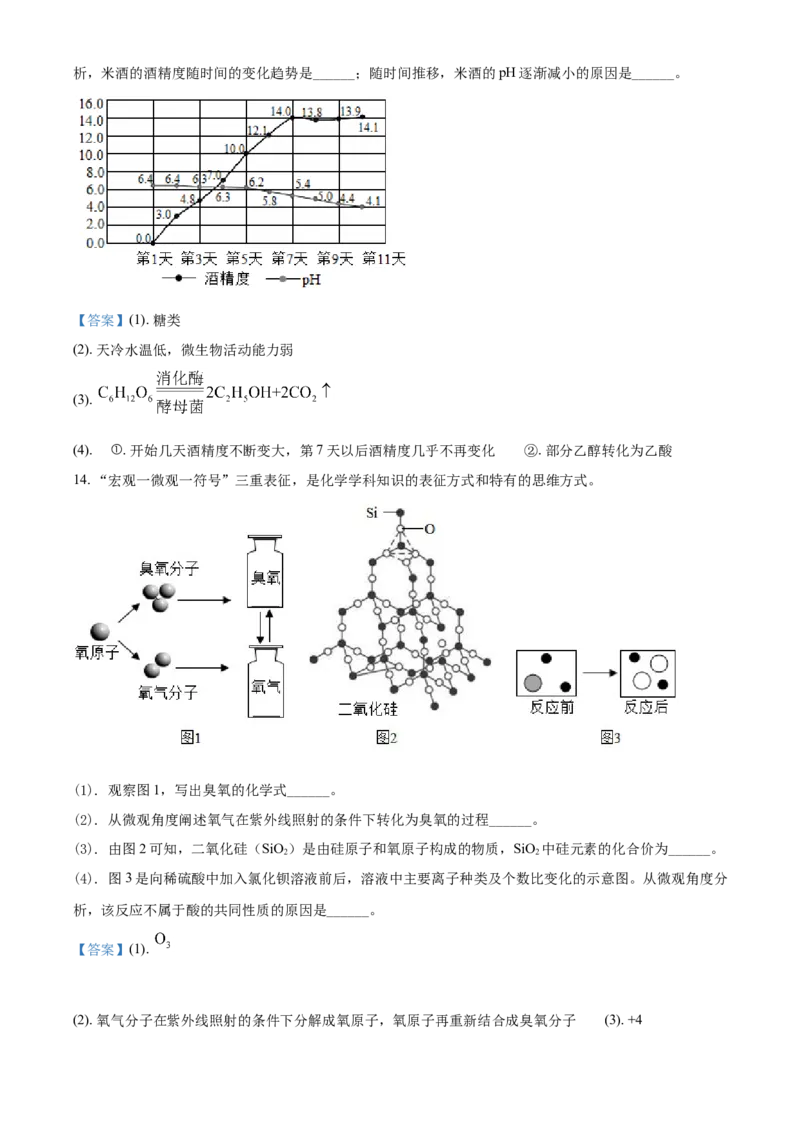
14. “宏观一微观一符号”三重表征,是化学学科知识的表征方式和特有的思维方式。
(1). 观察图1,写出臭氧的化学式______。
(2). 从微观角度阐述氧气在紫外线照射的条件下转化为臭氧的过程______。
(3). 由图2可知,二氧化硅(SiO)是由硅原子和氧原子构成的物质,SiO 中硅元素的化合价为______。
2 2
(4). 图3是向稀硫酸中加入氯化钡溶液前后,溶液中主要离子种类及个数比变化的示意图。从微观角度分
析,该反应不属于酸的共同性质的原因是______。
【答案】(1).
(2). 氧气分子在紫外线照射的条件下分解成氧原子,氧原子再重新结合成臭氧分子 (3). +4(4). 该反应的实质是硫酸根离子与钡离子反应生成硫酸钡沉淀,而酸的通性是酸中的氢离子参加反应
15. 水是生命之源。
(1). 遵义市有丰富的山泉水,大部分的山泉水是硬水,需煮沸后饮用。硬水中常含有可溶性的碳酸氢钙,
化学式为Ca(HCO ),在煮沸的过程中,碳酸氢钙发生分解生成碳酸钙、水和二氧化碳,该反应的化学
3 2
方程式为______。
(2). 研究水的组成须从纯净的水入手分析,通过电解水实验可知,水是由______组成的一种化合物。
的
(3). 水 转化如下图所示,箭头指向一步实现的物质转化方向,反应①②③④分别属于四种不同的基本反
应类型。其中②为置换反应,写出一个符合反应②的化学方程式______。
(4). 根据下表信息回答问题。
0 10 20 30 40
碳酸钠 7.1 12.5 21.5 39.7 49.0
.
碳酸氢钠 69 8.1 9.6 11.1 12.7
①表中物质的溶解度受温度影响较大的是______。
②现有两瓶失去标签的固体样品,分别是碳酸钠和碳酸氢钠中的一种。下列鉴别方案正确的是______。
A.取两只烧杯,分别加样品各4g,各加50g水溶解,观察现象
B.20℃时,取两只烧杯,分别加样品各6g,各加50g水溶解,观察现象
C.30℃时,取两只烧杯,分别配制两样品的100g饱和溶液,再降温到0℃,观察现象
D.40℃时,取两只烧杯,分别加样品各6g,各加50g水溶解,观察现象
【答案】(1).
(2). 氢元素、氧元素(3).
(4). ①. 碳酸钠 ②. BC
16. 黄铜(铜锌合金)和白铜(铜镍合金)是应用广泛的铜合金。某兴趣小组以黄铜和白铜及其组成金属
为例,进行了简单的项目式学习。
(1). 认识金属的性质
①锌在常温或加热条件下能与氧气反应,生成致密的氧化锌薄膜。一些金属制品可采用镀锌的方法来防锈,
其原理是______。
②按如图方案探究铜、锌、镍三种金属的活动性,观察到试管a中缓慢产生气泡,试管b中无明显现象,
试管c中的现象是______。则这三种金属的活动性由强到弱的顺序是______。(金属镍呈银白色,NiCl 和
2
NiSO 溶液都呈绿色)
4
(2). 认识合金的组成和性能
①合金因组分不同,性能和用途有差异。黄铜呈黄色,塑性好,适用于制造线材、管材等:白铜呈银白色,
耐腐蚀,适用于制造精密仪器、医疗器械等。验证黄铜和白铜中金属成分不同的化学方法是______。(写
出操作、现象和结论)
②我国发行的第五套人民币中,1元、5角和1角硬币的材料分别为钢芯镀镍、钢芯镀铜、铝合金,请分析
铸造硬币的金属材料除考虑成本、环保、美观、安全以外,还需要考虑的因素有______。(答两点)
(3). 认识金属的冶炼
金属冶炼的方法与金属的性质和科学技术的发展密切相关。
①湿法治铜为我国首创,原理是铁和硫酸铜溶液反应得铜,化学方程式为______。
②碳热还原硫化锌能制备单质锌,主要发生的反应有: ,,100万吨含硫化锌48.5%的闪锌矿,理论上最多能炼出含锌90%的粗锌质量为
______万吨。(结果保留一位小数)
【答案】(1). ①. 形成一层保护膜,保护了内部金属 ②. 生成红色固体、溶液变为绿色 ③. 锌>镍>
铜
(2). ①. 向硫酸镍溶液中分别加入两种合金,溶液由绿色变为无色的为黄铜合金,没有明显变化的为白铜
合金 ②. 有一定的硬度、耐腐蚀
(3). ①. ②. 36.1
17. 酸碱中和反应是两类物质的一类反应。某班同学分为五个小组对该类反应进行探究。
(1). 分组探究,收集证据
①第一组观察到______的现象,证明反应发生了。
②第二组将稀硫酸滴加到盛有氢氧化钠固体的试管中,测得该过程中温度升高。经讨论分析,此现象不能
作为该反应发生的证据,理由是______。
③第三组向滴有酚酞的氢氧化钠溶液中滴加稀硝酸至溶液恰好变为无色,回滴一滴氢氧化钠溶液,溶液又
变为红色,从溶液酸碱性的变化证明反应发生了,该反应的化学方程式为______。
④第四组将所选的酸碱溶液充分混合后,将混合溶液蒸发结晶,理论上可得固体______g,证明该反应发
生了。
⑤第五组将所选的酸碱溶液充分混合后,未观察到明显现象,再向混合后的溶液中滴加溶质质量分数为
5%的NaCO 溶液,烧杯中溶液质量与滴加NaCO 溶液的质量关系如第五组坐标图所示。图示信息______
2 3 2 3
(填“能”或“不能”)作为稀盐酸和氢氧化钙发生反应的证据,理由是______。
(2). 得出结论,解释应用
通过探究可知,不同的酸和不同的碱能发生中和反应,该类反应的共性是:不同酸中的H+和不同碱中的
OH-相互作用生成水分子,此类反应有广泛的用途,如农业上常用______改良酸性土壤。(填一种物质的
名称或化学式)
【答案】(1). ①. 有白色沉淀生成 ②. 氢氧化钠固体溶于水放出大量的热,温度也会升高 ③.④. 2.4 ⑤. 能 ⑥. 和碳酸钠溶液反应的盐酸质量小于原盐酸的质量
(2). 熟石灰(或Ca(OH) )
2