文档内容
考点 33 工业流程题解题策略
目录
.....................................................................................................................................................1
1.高考真题考点分布...................................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................................1
.....................................................................................................................................................2
考法01 微型工业流程...............................................................................................................................................2
考法02 综合工业流程...............................................................................................................................................5
...................................................................................................................................................15
1.高考真题考点分布
考点内容 考点分布
2024广东卷、2024湖南卷、2024河北卷、2024辽宁卷、2024安徽卷、2024新课标卷、
物质分离和提 2024全国甲卷、2023湖北卷、2023辽宁卷、2023广东卷、2023浙江卷、2023新课标
纯类 卷、
2022湖南卷、2022湖北卷、2022重庆卷、2022全国乙卷
2024北京卷、2024甘肃卷、2024浙江卷6月、2024江苏卷、2024山东卷、2024湖北
卷、2024浙江卷、2023全国甲卷、2023全国乙卷、2023湖南卷、2023山东卷、2023北
物质制备类 京卷、2023浙江卷、2022福建卷、2022辽宁卷、2022广东卷、2022北京卷、2022河北
卷、
2022全国甲卷
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,以化工流程或实验装置图为载体,考查物质的制备、回收、分离
提纯等仍是高考命题的热点。
【备考策略】
1.审题策略
(1)看原料:明确化工生产或化学实验所需的材料。
(2)看目的:把握题干中的“制备”或“提纯”等关键词,确定化工生产或化学实验的目的。
(3)看箭头:进入的是投料(即反应物);出去的是生成物(包括主产物和副产物)。(4)看三线:主线主产品;分支副产品;回头为循环。
(5)找信息:明确反应条件控制和分离提纯方法。
(6)关注所加物质的可能作用:参与反应、提供反应氛围、满足定量要求。
2.解题方法
(1)粗读题干,挖掘图示,明确目的
图示中一般会出现超出教材范围的知识,但题目有提示或者问题中不涉及,关注题目的每一个关键字,尽
量弄懂流程图,但不必将每一种物质都推出,只需问什么推什么。通过阅读明确生产目的,找到制备物质
所需的原料及所含杂质。
(2)携带问题,精读信息
读主干抓住关键字、词;读流程图,重点抓住物质流向(进入与流出)、实验操作方法。
(3)看清问题,准确规范作答
答题时要看清问题,不能答非所问,要注意语言表达的科学性和准确性,答题时不具有“连带效应”,即
前一问未答出,不会影响后面答题。
【命题预测】
预计2025年高考会以新的工业流程情境为载体考查物质的制备、分离、提纯、回收等知识,重点考查学
生分析问题、解决问题的能力,题目难度一般较大。
考法01 微型工业流程
化学工艺流程选择题是近几年高考的热点,将化工生产过程中的主要生产阶段即生产流程用框图的形式表
示出来,并根据生产流程中有关的化学知识设计选项,形成与化工生产紧密联系的化工工艺试题;主要涉
及物质的性质、分离提纯、反应原理、实验操作等知识点。由于此类试题陌生度高,对学生的能力要求也
大,加上有的试题文字信息量大,所以这类选择题容易出错。考查的内容主要有:
(1)金属冶炼类,常以Cr、Mn、V、Zn等元素化合物的制备流程为载体,考查不同价态物质转化规律,
条件控制、物质的分离提纯等关键能力。
(2)物质制备类,如胆矾、绿矾、明矾、氧化铁、硝酸铜等物质的制备。
考向01 考查物质的制备
【例1】(2024·湖南株洲·一模)铜的氯化物是重要的化工原料,常用作有机合成催化剂。实验室用粗铜
(含杂质Fe)制备氯化亚铜、氯化铜晶体的流程如下:
下列说法错误的是( )
A.固体1和固体2中Fe元素的价态相同B.检验溶液2中的杂质离子是否除尽可以选用KSCN溶液或铁氰化钾溶液
C.试剂X可能是CuO,操作②中结晶时需要通入HCl气体
D.反应②的离子方程式为2Cu2++SO +2HO+2Cl-===2CuCl↓+SO+4H+
2 2
考向02 考查物质的分离提纯、除杂
【例2】(2024·山西长治·模拟)某矿石中含有硅、铁、铝的氧化物,为综合开发资源提高矿石的利用率,
化工厂采取如图工艺制备铁红和AlCl ·6H O。下列说法错误的是( )
3 2
A.“酸浸”过程中选择盐酸比硫酸更为合适
B.“氧化”过程中少量多次添加双氧水可有效减少Fe3+催化HO 分解
2 2
C.“洗涤”的操作是将沉淀转移至洁净的烧杯中,加蒸馏水清洗2~3次
D.将SOCl 与AlCl ·6H O混合并加热,可得到无水AlCl
2 3 2 3
【对点1】(2024·河南商丘·模拟)高铁酸钾(K FeO)是一种环保、高效、多功能饮用水处理剂,制备流程
2 4
如图所示:
下列叙述不正确的是( )
A.用KFeO 作水处理剂时,既能杀菌消毒又能净化水
2 4
B.反应Ⅰ中尾气可用FeCl 溶液吸收再利用
2
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为2∶3
D.该条件下,物质的溶解性:NaFeO<KFeO
2 4 2 4
【对点2】(2024·浙江金华·模拟)电镀污泥(包含Ni、Ca、Fe、Al等金属阳离子)对环境污染极大,是典
型危险废弃物。某科研团队设计了从电镀污泥中提取镍的流程,如图所示。
根据以上信息,下列说法错误的是( )
A.“浸出渣”的主要成分可能是CaCO 、Fe(OH) 、Al(OH)
3 3 3
B.“氨浸”时适当提高氨水浓度和反应温度,有利于增大浸出率
C.该流程中“有机萃取剂”和“萃余液”均可重复使用,且重复使用的目的相同
D.“富集”与“还原”之间的操作可能是沉淀、过滤、洗涤、干燥、灼烧考法02 综合工业流程
一、工业流程试题的呈现形式
【方法技巧】读图要领
(1)箭头:进入的是 (反应物),出去的是含产品中元素的物质(流程方向)、副产物或 (支线方向)。
(2)三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
二、流程中原料的预处理
方法 目的
研
将块状或颗粒状的物质磨成粉末或将液体分散成微小液滴,增大反应物接触面积,以 反
磨、
应速率或使反应
雾化
水浸 与水接触反应或溶解
酸浸 与酸接触反应或溶解,使可溶性金属离子进入溶液,不溶物通过 除去
碱浸 除去油污,溶解 氧化物、铝及其氧化物
灼烧 除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除去可燃性杂质
煅烧 改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解,如煅烧高岭土
三、流程中反应条件的控制
1.控制溶液的pH
(1)控制反应的发生,增强物质的 性或 性,或改变水解程度。
(2)控制溶液的酸碱性使其中的某些金属离子形成 沉淀。
①控制溶液的酸碱性使其中的某些金属离子形成氢氧化物沉淀。如若要除去Al3+、Mn2+溶液中含有的Fe2
+,先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH。
②调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH增大;不引入新杂质。例如:若要除去
Cu2+溶液中混有的Fe3+,可加入CuO、Cu(OH) 、CuCO、Cu (OH) CO 等物质来调节溶液的pH。
2 3 2 2 3
2.控制反应的温度
(1)控制 。
(2)控制 方向。
(3)控制固体的 ,如趁热过滤能防止某物质降温时析出。
(4)促进溶液中气体的 或实现蒸馏。
(5)防止或实现某物质 或 。
(6)使催化剂达到最大 。
(7)防止副反应的发生。
3.调节反应物的浓度(1)根据需要选择适宜浓度,控制一定的 ,使平衡移动有利于目标产物的生成,减小对后续操
作产生的影响。
(2)反应物过量,能保证反应的完全发生或提高其他物质的 ,但对后续操作也会产生影响。
4.控制反应体系的压强
(1)改变化学 。
(2)影响 的方向。
5.使用催化剂
加快 ,提高生产效率。
四、物质的分离与提纯
(一)沉淀洗涤
1.对沉淀洗涤的原因
(1)若滤渣是所需要的物质,洗涤的目的是除去晶体表面的 杂质,得到更纯净的沉淀物。
(2)若滤液是所需要的物质,洗涤的目的是洗涤过滤所得到的 ,把有用的物质如目标产物尽可能洗出
来。
(3)防止污染环境:如果滤渣表面含有一些对环境有害的物质,如重金属或CN-,为了防止污染环境,往往
要对残渣进行洗涤。
2.洗涤剂的选择
洗涤试剂 适用范围 目的
除去固体表面吸附着的××杂质;可适当降低固体因
冷水 产物不溶于水
为溶解而造成的损失
蒸
有特殊的物质其溶解度随着温 除去固体表面吸附着的××杂质;可适当降低固体因
馏 热水
度升高而下降 为温度变化而造成溶解的损失
水
固体易溶于水,难溶于有机溶 减少固体溶解;利用有机溶剂的挥发性除去固体表面
有机溶剂
剂 的水分,产品易干燥
饱和溶液 对纯度要求不高的产品 减少固体溶解
除去固体表面吸附着的可溶于酸、碱的杂质;减少固
酸、碱溶液 产物不溶于酸、碱
体溶解
3.洗涤的方法
洗涤的方法 注意点 三个得分点
让过滤后的晶体继续留在过 在洗涤过程中不能搅 注洗涤液→加洗涤液→重复操作
滤器中,加入洗涤剂浸没晶 拌。因为滤纸已经润 (1)注洗涤液:沿 向漏斗中注入洗涤液
体,让洗涤液自然流下,重 湿,如果搅拌很容易搅 (2)加洗涤液:洗涤液 晶体
复2~3次即可 破滤纸,造成晶体损失 (3)重复操作:重复操作2~3次
(二)产品分离、提纯
1.结晶——固体物质从溶液中析出的过程。
(1)蒸发浓缩、冷却结晶:如制取含结晶水的物质、除去KNO 中的少量NaCl。
3
(2)蒸发结晶、趁热过滤:如除去NaCl中的少量KNO。
32.过滤——固、液分离。
3.洗涤——用冷水、酒精或电解质溶液洗去固体表面吸附的溶质。
4.蒸馏——分离 的液体混合物。
5.分液—— 的液体间的分离。
6.萃取——用一种溶剂将溶质从另一种溶剂中提取出来。(反萃取)
7.升华——将可直接汽化的固体分离出来。
8.盐析——加无机盐使溶质的 降低而析出。
9.冷却——利用气体易液化的特点分离气体,如工业合成氨中分离出液氨。
五、工业流程中的计算
化工流程题中涉及的计算主要有:样品的质量分数或纯度的计算,物质的转化率或产率、物质的量浓度、
物质的质量的计算。
1.计算公式
(1)n=,n=,n=cV(aq)
(2)物质的质量分数(或纯度)=×100%
(3)产品产率=×100%
(4)物质的转化率=×100%
2.计算方法——关系式法
关系式法常应用于一步反应或分多步进行的连续反应中,利用该法可以节省不必要的中间运算过程,避免
计算错误,并能迅速准确地获得结果。一步反应中可以直接找出反应物与目标产物的关系;在多步反应
中,若第一步反应的产物是下一步反应的反应物,可以根据化学方程式将某中间物质作为“中介”,找出
已知物质和所求物质之间量的关系。
如水中溶氧量(DO)的测定:
碱性条件下,O 将Mn2+氧化为MnO(OH) :①2Mn2++O+4OH-===2MnO(OH)↓
2 2 2 2
酸性条件下,MnO(OH) 将I-氧化为I:②MnO(OH) +2I-+4H+===Mn2++I+3HO
2 2 2 2 2
用NaSO 标准溶液滴定生成的I:③2SO2-+I===S O2-+2I-
2 2 3 2 2 3 2 4 6
可得关系式:O~2Mn2+~2MnO(OH) ~2I~4NaSO
2 2 2 2 2 3
考向01 物质制备型工业流程
【例1】(2024·湖北荆州·三模)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还
包括钾、镁的铝硅酸盐,以及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是_________________________________________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出VO+转化为VO反应
的离子方程式_______________________________________________。
(3)“中和沉淀”中,钒水解并沉淀为VO·xHO,随滤液②可除去金属离子K+、Mg2+、Na+、______,以
2 5 2
及部分的______。
(4)“沉淀转溶”中,VO·xHO转化为钒酸盐溶解。滤渣③的主要成分是________。
2 5 2
(5)“调pH”中有沉淀生成,生成沉淀反应的化学方程式是_________________________。
(6)“沉钒”中析出NH VO 晶体时,需要加入过量NH Cl,其原因是
4 3 4
___________________________________________________________________。
【思维建模】流程图建模——理清流程图的各环节
[识图方法]
图1箭头表示反应物加入同时生成物出来;
图2箭头表示反应物分步加入和生成物出来;
图3箭头表示循环反应。
考向02 分离提纯型工业流程
【例2】(2024·湖北武汉·模拟)V有“工业味精”之称。工业上提取钒的工艺有多种,一种从钒页岩(一
种主要含Si、Fe、Al、V元素的矿石)中提取V的工艺流程如下:
已知:①“酸浸”时有 生成。②“萃取”时离子萃取率的大小顺序为 。回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl-Na SO 与钒页岩形成混合物,这样做的目的是 。
2 4
(2)“滤渣Ⅰ”除掉的主要杂质元素是 (填元素符号)。
(3)H C O 作用是将 转化为 ,转化的目的是 ,发生的离子反应方程式为 。
2 2 4
(4)“沉钒”时,生成 沉淀,“步骤X”的目的是 ,写出“煅烧”时的化学反应方程式
。
(5)以“沉钒率”( 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于
80℃时沉钒率下降的原因是 。
【思维建模】解题思维建模——通过“三审”建立系统思维
(1)审题干——明确原料成分和目的要求
(2)审流程——明确各步转化原理和目的
①看箭头:进入的是原料(即反应物);出去的是生成物(包括主产物和副产物)。
②看三线:主线主产品、分支副产品、回头为循环。
③找信息:明确反应条件控制和分离提纯方法。
④关注所加物质的可能作用:参与反应、提供反应氛围、满足定量要求。
(3)审问题——明确答什么
①不要答非所问:要看清题目要求,按要求答题,防止答非所问。
②规范答题:回答问题要准确全面,注意语言表达的规范性,特别是化学用语的书写与表示要准确、规
范。
【对点1】(2024·江苏南京·模拟预测)重铬酸钾(K Cr O)在实验室和工业上都有广泛应用,如用于制铬
2 2 7矾、制火柴、电镀、有机合成等。工业上以铬铁矿[主要成分为Fe(CrO ),杂质主要为硅、铁、铝的氧化
2 2
物]制备重铬酸钾的工艺流程如下图所示:
已知:
①焙烧时Fe(CrO ) 中的Fe元素转化为NaFeO ,Cr元素转化为NaCrO。
2 2 2 2 4
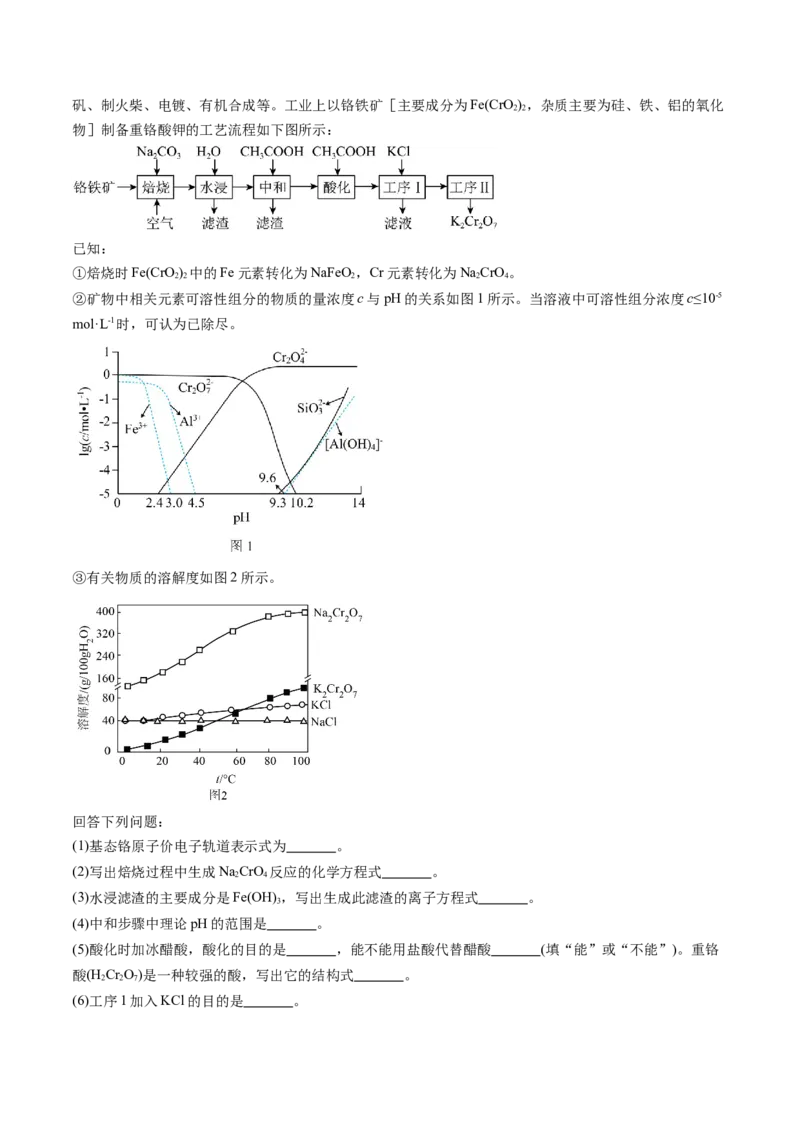
②矿物中相关元素可溶性组分的物质的量浓度c与pH的关系如图1所示。当溶液中可溶性组分浓度c≤10-5
mol·L-1时,可认为已除尽。
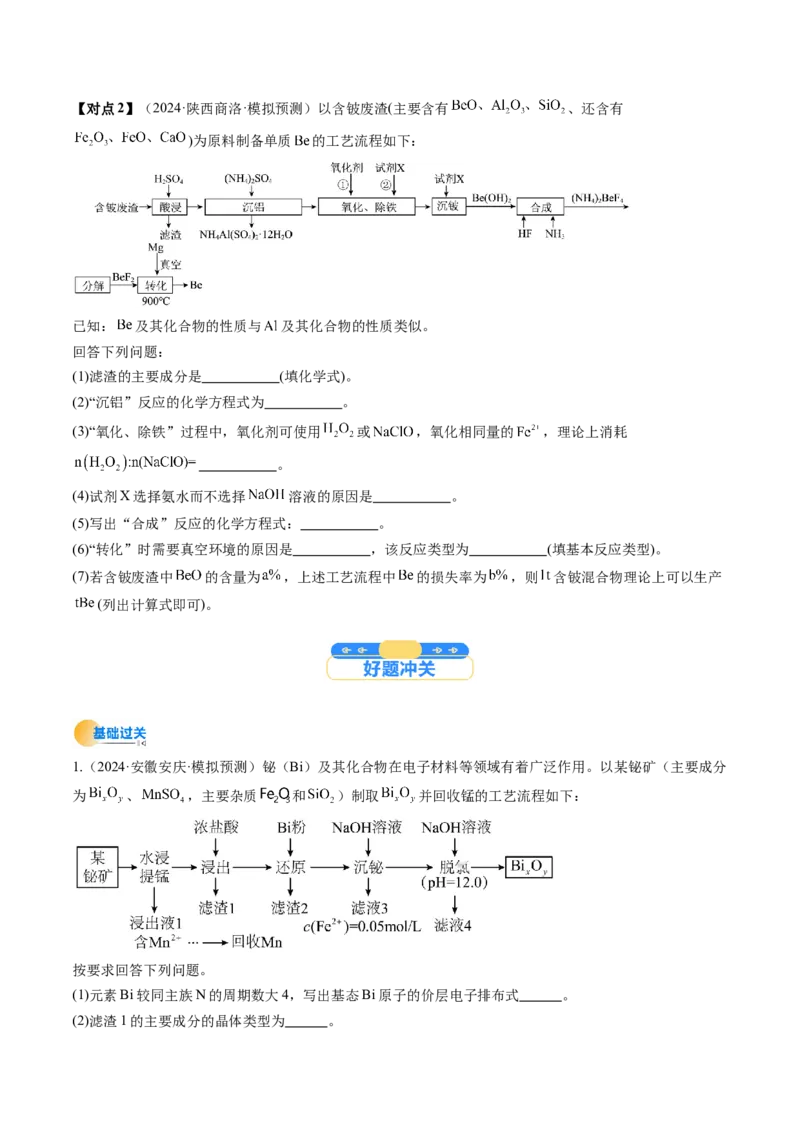
③有关物质的溶解度如图2所示。
回答下列问题:
(1)基态铬原子价电子轨道表示式为 。
(2)写出焙烧过程中生成NaCrO 反应的化学方程式 。
2 4
(3)水浸滤渣的主要成分是Fe(OH) ,写出生成此滤渣的离子方程式 。
3
(4)中和步骤中理论pH的范围是 。
(5)酸化时加冰醋酸,酸化的目的是 ,能不能用盐酸代替醋酸 (填“能”或“不能”)。重铬
酸(H Cr O)是一种较强的酸,写出它的结构式 。
2 2 7
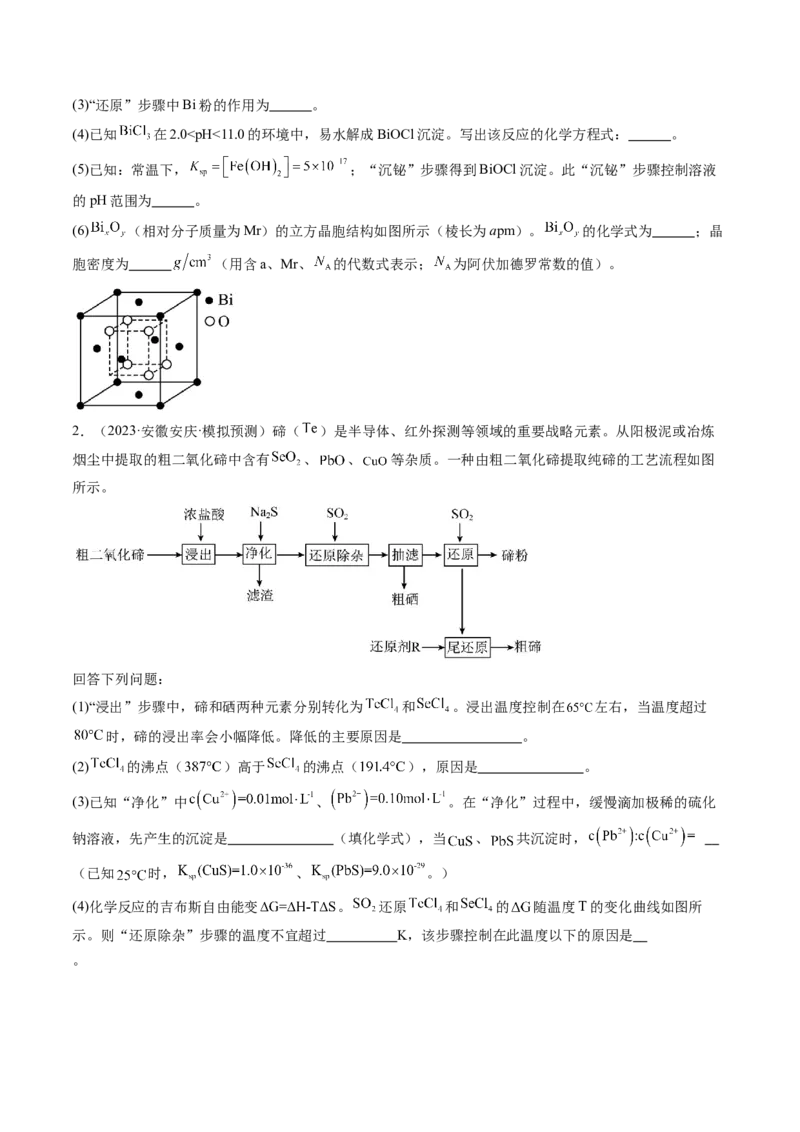
(6)工序1加入KCl的目的是 。【对点2】(2024·陕西商洛·模拟预测)以含铍废渣(主要含有 、还含有
)为原料制备单质 的工艺流程如下:
已知: 及其化合物的性质与 及其化合物的性质类似。
回答下列问题:
(1)滤渣的主要成分是 (填化学式)。
(2)“沉铝”反应的化学方程式为 。
(3)“氧化、除铁”过程中,氧化剂可使用 或 ,氧化相同量的 ,理论上消耗
。
(4)试剂X选择氨水而不选择 溶液的原因是 。
(5)写出“合成”反应的化学方程式: 。
(6)“转化”时需要真空环境的原因是 ,该反应类型为 (填基本反应类型)。
(7)若含铍废渣中 的含量为 ,上述工艺流程中 的损失率为 ,则 含铍混合物理论上可以生产
(列出计算式即可)。
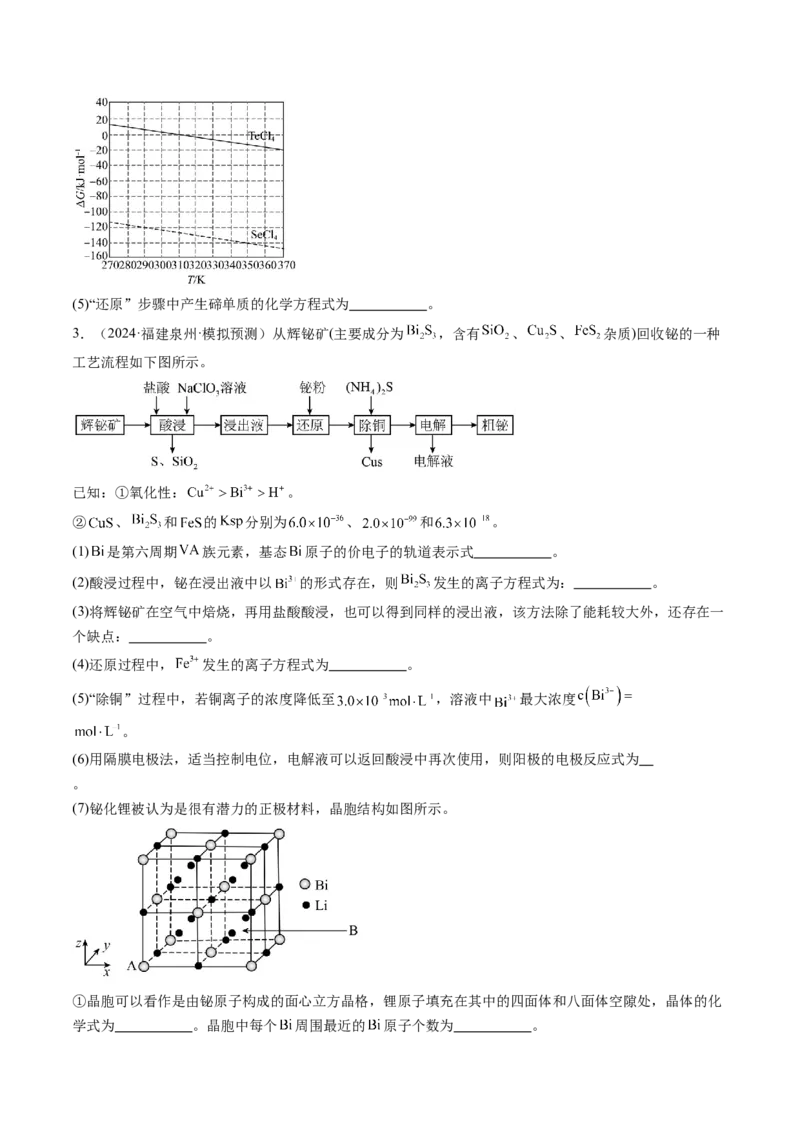
1.(2024·安徽安庆·模拟预测)铋(Bi)及其化合物在电子材料等领域有着广泛作用。以某铋矿(主要成分
为 、 ,主要杂质 和 )制取 并回收锰的工艺流程如下:
按要求回答下列问题。
(1)元素Bi较同主族N的周期数大4,写出基态Bi原子的价层电子排布式 。
(2)滤渣1的主要成分的晶体类型为 。(3)“还原”步骤中Bi粉的作用为 。
(4)已知 在2.03, 易发生水解为BiOCl。ii.几种离子沉淀与pH的关系如下。
离子 Mn2+ Fe2+ Fe3+
开始沉淀pH 8.1 6.3 1.9
沉淀完全pH 10.1 8.3 3.3
(1)“联合焙烧”时,BiS 和MnO 在空气中反应生成 BiO 和MnSO ,该反应的化学方程式为 。
2 3 2 2 3 4
(2)“酸浸”时需及时补充浓盐酸调节浸取液的 pH,一般控制浸取液pH小于1.4,其目的是 。
(3)“转化”时加入金属Bi的作用是 ,得到BiOCl的离子方程式为 。
(4)铋能被有机萃取剂(简称 TBP)萃取,其萃取原理可表示为
。“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,
萃取率随c(Cl-)变化关系如图所示,c(Cl-)最佳为1.3 mol·L-1。c(Cl-)>1.3mol·L−1 时,铋离子萃取率下降的可
能原因是 。
(5)“沉淀反萃取”时生成草酸铋[Bi (C O)·7H O] 晶体。为得到含 Cl- 较少的草酸铋晶体,“萃取”后有机
2 2 4 3 2
相与草酸溶液的混合方式为 。
5.(2024·辽宁沈阳·模拟预测)二氧化铈( )是一种用途广泛的稀土化合物。以氟碳铈矿(主要含)为原料制备 的一种工艺流程如图所示:
已知:① 能与 结合成 ,也能与 结合成 ;
②在硫酸体系中 能被萃取剂[ ]萃取,而 不能。
回答下列问题:
(1)氧化焙烧中氧化的目的是 。
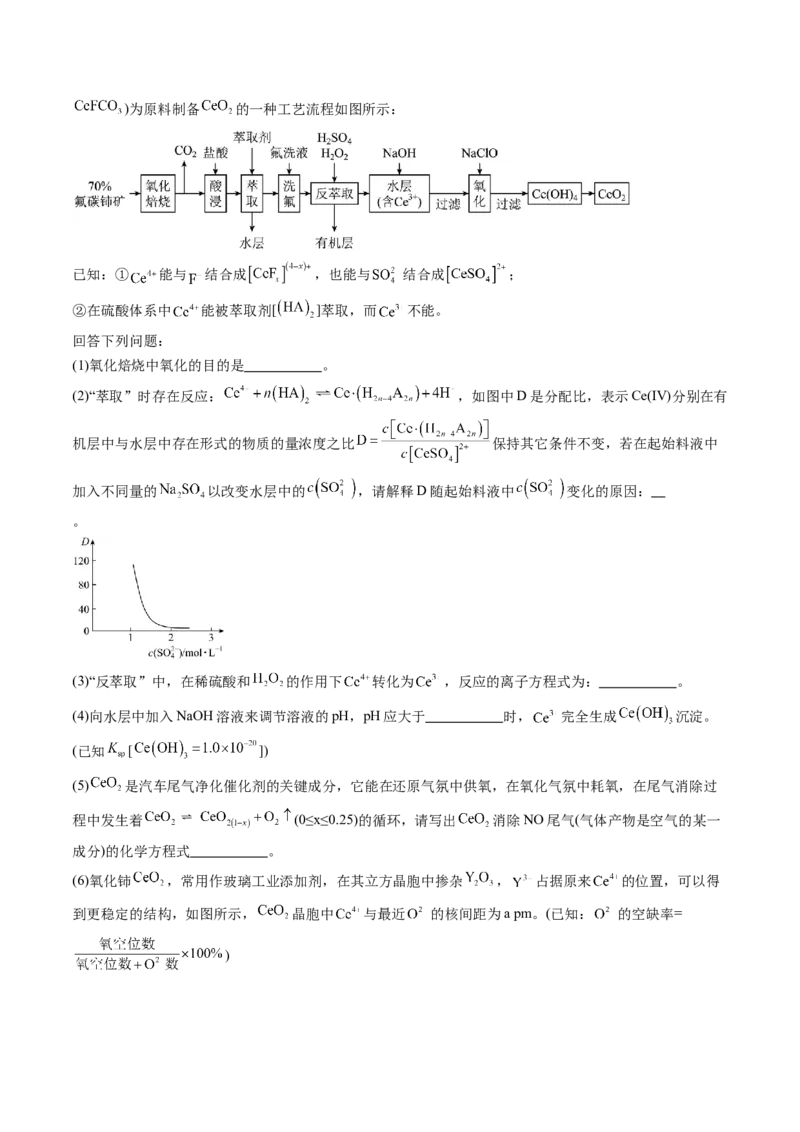
(2)“萃取”时存在反应: ,如图中D是分配比,表示Ce(IV)分别在有
机层中与水层中存在形式的物质的量浓度之比 保持其它条件不变,若在起始料液中
加入不同量的 以改变水层中的 ,请解释D随起始料液中 变化的原因:
。
(3)“反萃取”中,在稀硫酸和 的作用下 转化为 ,反应的离子方程式为: 。
(4)向水层中加入NaOH溶液来调节溶液的pH,pH应大于 时, 完全生成 沉淀。
(已知 [ ])
(5) 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过
程中发生着 (0≤x≤0.25)的循环,请写出 消除NO尾气(气体产物是空气的某一
成分)的化学方程式 。
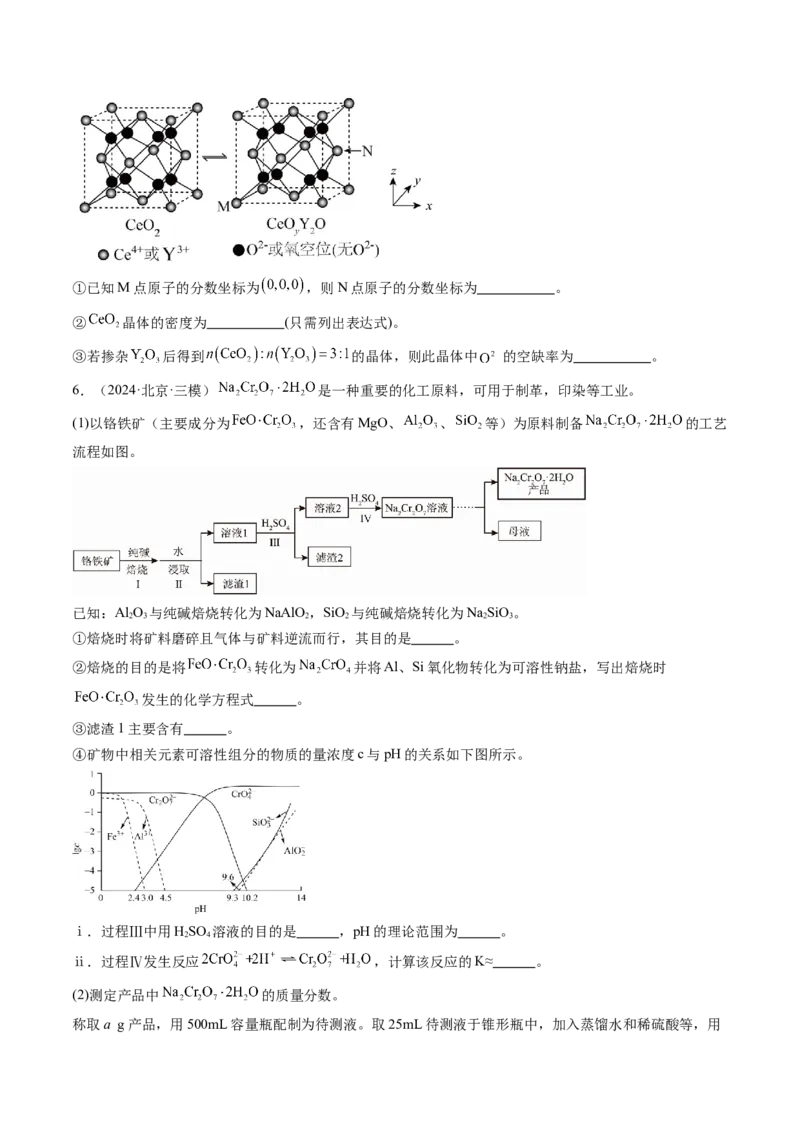
(6)氧化铈 ,常用作玻璃工业添加剂,在其立方晶胞中掺杂 , 占据原来 的位置,可以得
到更稳定的结构,如图所示, 晶胞中 与最近 的核间距为a pm。(已知: 的空缺率=
)①已知M点原子的分数坐标为 ,则N点原子的分数坐标为 。
② 晶体的密度为 (只需列出表达式)。
③若掺杂 后得到 的晶体,则此晶体中 的空缺率为 。
6.(2024·北京·三模) 是一种重要的化工原料,可用于制革,印染等工业。
(1)以铬铁矿(主要成分为 ,还含有MgO、 、 等)为原料制备 的工艺
流程如图。
已知:Al O 与纯碱焙烧转化为NaAlO ,SiO 与纯碱焙烧转化为NaSiO。
2 3 2 2 2 3
①焙烧时将矿料磨碎且气体与矿料逆流而行,其目的是 。
②焙烧的目的是将 转化为 并将Al、Si氧化物转化为可溶性钠盐,写出焙烧时
发生的化学方程式 。
③滤渣1主要含有 。
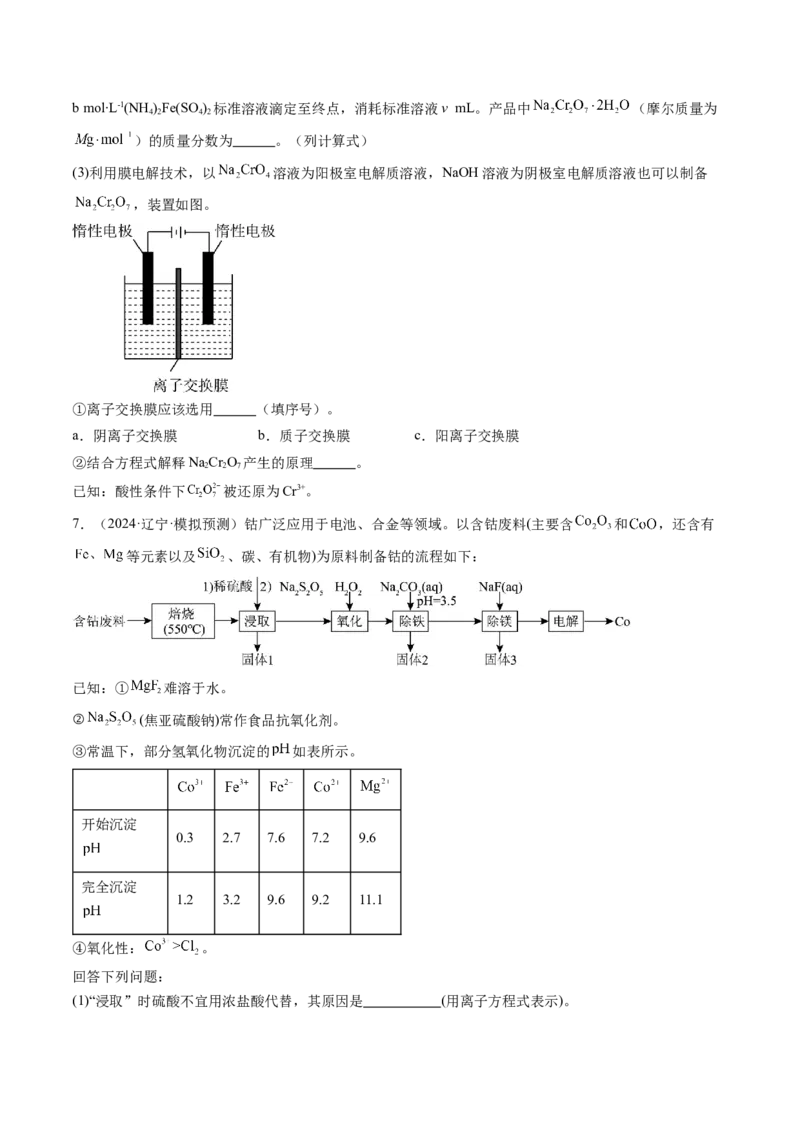
④矿物中相关元素可溶性组分的物质的量浓度c与pH的关系如下图所示。
ⅰ.过程Ⅲ中用HSO 溶液的目的是 ,pH的理论范围为 。
2 4
ⅱ.过程Ⅳ发生反应 ,计算该反应的K≈ 。
(2)测定产品中 的质量分数。
称取a g产品,用500mL容量瓶配制为待测液。取25mL待测液于锥形瓶中,加入蒸馏水和稀硫酸等,用b mol∙L-1(NH )Fe(SO ) 标准溶液滴定至终点,消耗标准溶液v mL。产品中 (摩尔质量为
4 2 4 2
)的质量分数为 。(列计算式)
(3)利用膜电解技术,以 溶液为阳极室电解质溶液,NaOH溶液为阴极室电解质溶液也可以制备
,装置如图。
①离子交换膜应该选用 (填序号)。
a.阴离子交换膜 b.质子交换膜 c.阳离子交换膜
②结合方程式解释NaCr O 产生的原理 。
2 2 7
已知:酸性条件下 被还原为Cr3+。
7.(2024·辽宁·模拟预测)钴广泛应用于电池、合金等领域。以含钴废料(主要含 和 ,还含有
等元素以及 、碳、有机物)为原料制备钴的流程如下:
已知:① 难溶于水。
② (焦亚硫酸钠)常作食品抗氧化剂。
③常温下,部分氢氧化物沉淀的 如表所示。
开始沉淀
0.3 2.7 7.6 7.2 9.6
完全沉淀
1.2 3.2 9.6 9.2 11.1
④氧化性: 。
回答下列问题:
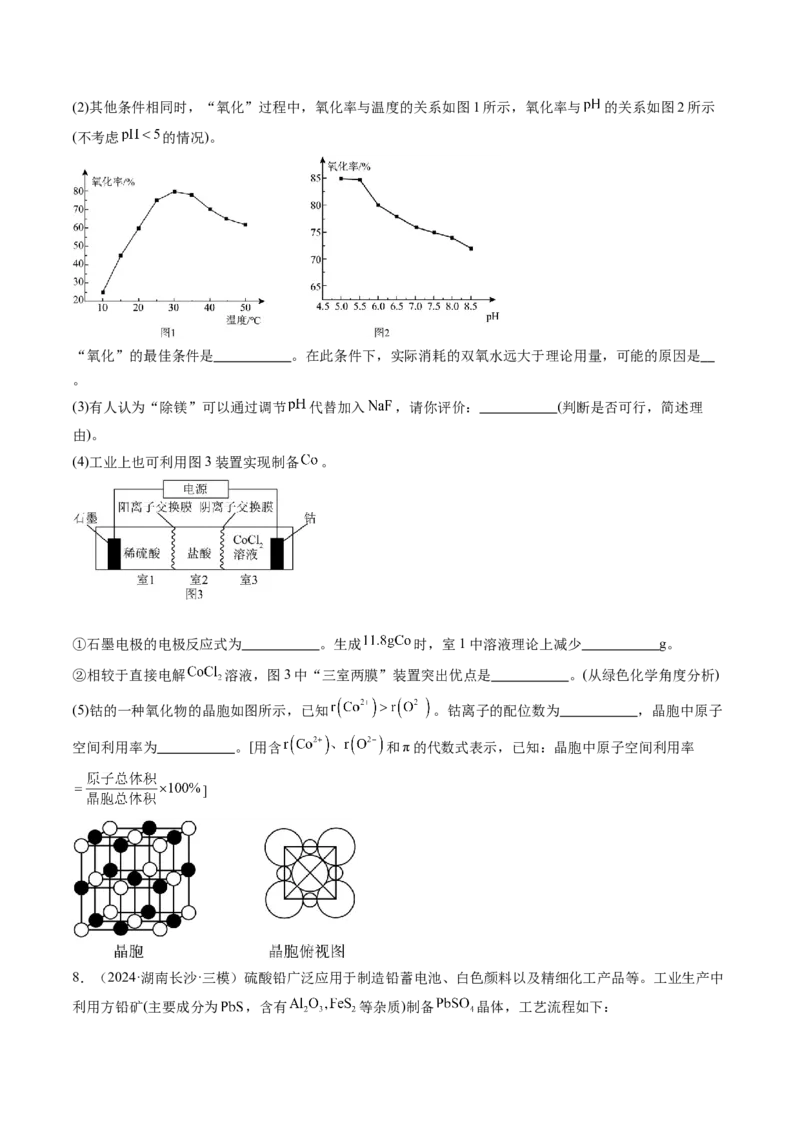
(1)“浸取”时硫酸不宜用浓盐酸代替,其原因是 (用离子方程式表示)。(2)其他条件相同时,“氧化”过程中,氧化率与温度的关系如图1所示,氧化率与 的关系如图2所示
(不考虑 的情况)。
“氧化”的最佳条件是 。在此条件下,实际消耗的双氧水远大于理论用量,可能的原因是
。
(3)有人认为“除镁”可以通过调节 代替加入 ,请你评价: (判断是否可行,简述理
由)。
(4)工业上也可利用图3装置实现制备 。
①石墨电极的电极反应式为 。生成 时,室1中溶液理论上减少 g。
②相较于直接电解 溶液,图3中“三室两膜”装置突出优点是 。(从绿色化学角度分析)
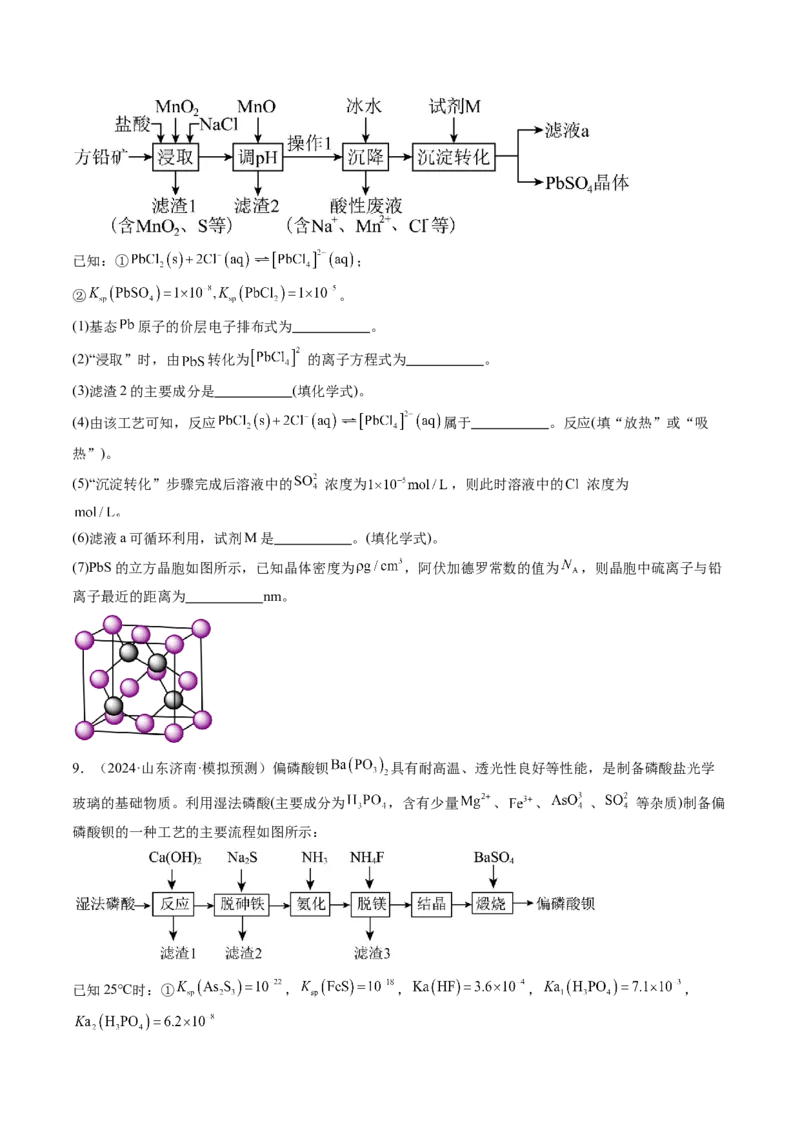
(5)钴的一种氧化物的晶胞如图所示,已知 。钴离子的配位数为 ,晶胞中原子
空间利用率为 。[用含 和π的代数式表示,已知:晶胞中原子空间利用率
]
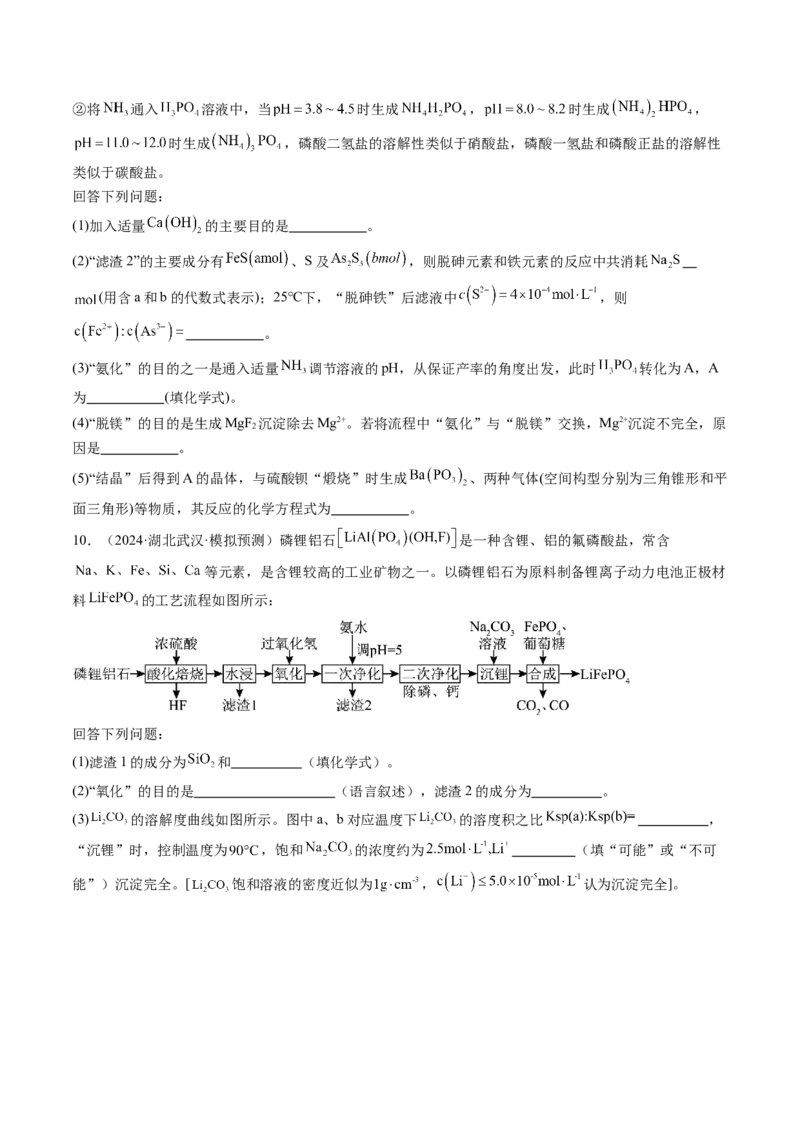
8.(2024·湖南长沙·三模)硫酸铅广泛应用于制造铅蓄电池、白色颜料以及精细化工产品等。工业生产中
利用方铅矿(主要成分为 ,含有 等杂质)制备 晶体,工艺流程如下:已知:① ;
② 。
(1)基态 原子的价层电子排布式为 。
(2)“浸取”时,由 转化为 的离子方程式为 。
(3)滤渣2的主要成分是 (填化学式)。
(4)由该工艺可知,反应 属于 。反应(填“放热”或“吸
热”)。
(5)“沉淀转化”步骤完成后溶液中的 浓度为 ,则此时溶液中的 浓度为
(6)滤液a可循环利用,试剂M是 。(填化学式)。
(7)PbS的立方晶胞如图所示,已知晶体密度为 ,阿伏加德罗常数的值为 ,则晶胞中硫离子与铅
离子最近的距离为 nm。
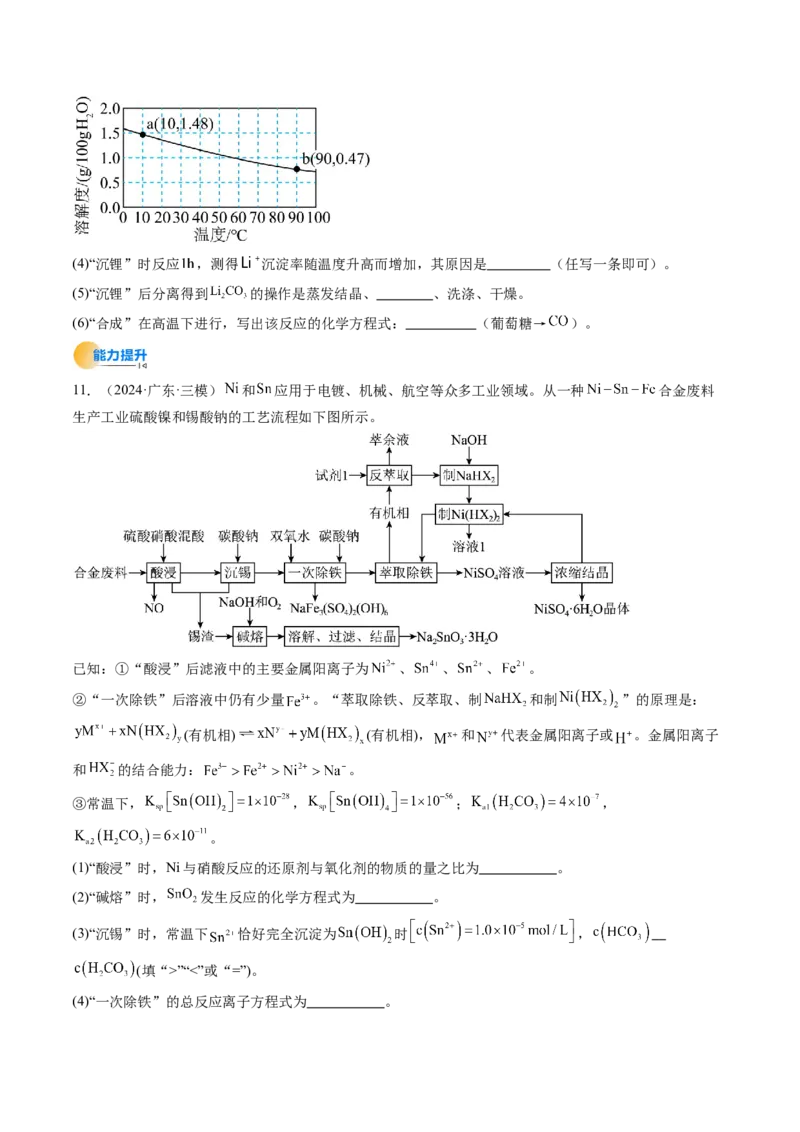
9.(2024·山东济南·模拟预测)偏磷酸钡 具有耐高温、透光性良好等性能,是制备磷酸盐光学
玻璃的基础物质。利用湿法磷酸(主要成分为 ,含有少量 、 、 、 等杂质)制备偏
磷酸钡的一种工艺的主要流程如图所示:
已知25℃时:① , , , ,②将 通入 溶液中,当 时生成 , 时生成 ,
时生成 ,磷酸二氢盐的溶解性类似于硝酸盐,磷酸一氢盐和磷酸正盐的溶解性
类似于碳酸盐。
回答下列问题:
(1)加入适量 的主要目的是 。
(2)“滤渣2”的主要成分有 、S及 ,则脱砷元素和铁元素的反应中共消耗
(用含a和b的代数式表示);25℃下,“脱砷铁”后滤液中 ,则
。
(3)“氨化”的目的之一是通入适量 调节溶液的pH,从保证产率的角度出发,此时 转化为A,A
为 (填化学式)。
(4)“脱镁”的目的是生成MgF 沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原
2
因是 。
(5)“结晶”后得到A的晶体,与硫酸钡“煅烧”时生成 、两种气体(空间构型分别为三角锥形和平
面三角形)等物质,其反应的化学方程式为 。
10.(2024·湖北武汉·模拟预测)磷锂铝石 是一种含锂、铝的氟磷酸盐,常含
等元素,是含锂较高的工业矿物之一。以磷锂铝石为原料制备锂离子动力电池正极材
料 的工艺流程如图所示:
回答下列问题:
(1)滤渣1的成分为 和 (填化学式)。
(2)“氧化”的目的是 (语言叙述),滤渣2的成分为 。
(3) 的溶解度曲线如图所示。图中a、b对应温度下 的溶度积之比 ,
“沉锂”时,控制温度为 ,饱和 的浓度约为 (填“可能”或“不可
能”)沉淀完全。[ 饱和溶液的密度近似为 , 认为沉淀完全]。(4)“沉锂”时反应 ,测得 沉淀率随温度升高而增加,其原因是 (任写一条即可)。
(5)“沉锂”后分离得到 的操作是蒸发结晶、 、洗涤、干燥。
(6)“合成”在高温下进行,写出该反应的化学方程式: (葡萄糖→ )。
11.(2024·广东·三模) 和 应用于电镀、机械、航空等众多工业领域。从一种 合金废料
生产工业硫酸镍和锡酸钠的工艺流程如下图所示。
已知:①“酸浸”后滤液中的主要金属阳离子为 、 、 、 。
②“一次除铁”后溶液中仍有少量 。“萃取除铁、反萃取、制 和制 ”的原理是:
(有机相) (有机相), 和 代表金属阳离子或 。金属阳离子
和 的结合能力: 。
③常温下, , ; ,
。
(1)“酸浸”时,Ni与硝酸反应的还原剂与氧化剂的物质的量之比为 。
(2)“碱熔”时, 发生反应的化学方程式为 。
(3)“沉锡”时,常温下 恰好完全沉淀为 时 ,
(填“>”“<”或“=”)。
(4)“一次除铁”的总反应离子方程式为 。(5)“萃取除铁”时,用 制取 进行萃取,而不用 直接进行萃取的原因是
。
(6)“反萃取”时,萃余液的溶质含 ,试剂1是 。
(7)“制 ”时,溶液1的主要成分是 (填化学式)。
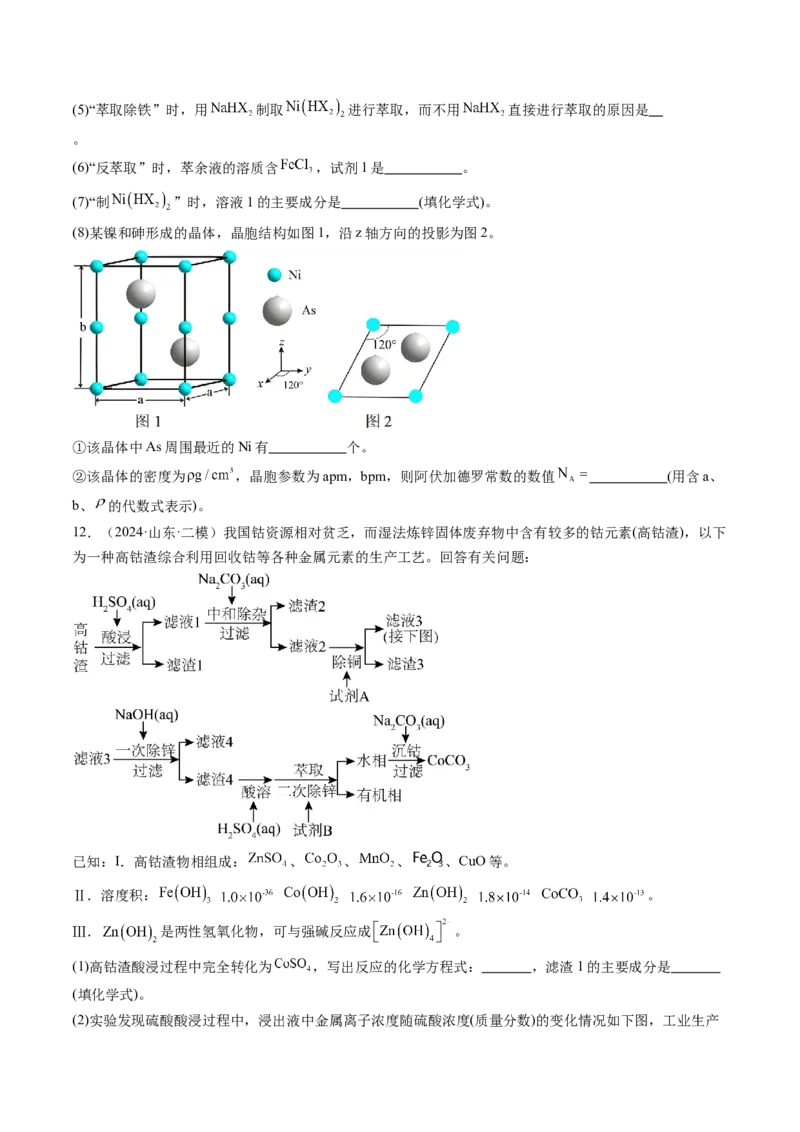
(8)某镍和砷形成的晶体,晶胞结构如图1,沿z轴方向的投影为图2。
①该晶体中As周围最近的Ni有 个。
②该晶体的密度为 ,晶胞参数为apm,bpm,则阿伏加德罗常数的数值 (用含a、
b、 的代数式表示)。
12.(2024·山东·二模)我国钴资源相对贫乏,而湿法炼锌固体废弃物中含有较多的钴元素(高钴渣),以下
为一种高钴渣综合利用回收钴等各种金属元素的生产工艺。回答有关问题:
已知:I.高钴渣物相组成: 、 、 、 、CuO等。
Ⅱ.溶度积: 。
Ⅲ. 是两性氢氧化物,可与强碱反应成 。
(1)高钴渣酸浸过程中完全转化为 ,写出反应的化学方程式: ,滤渣1的主要成分是
(填化学式)。
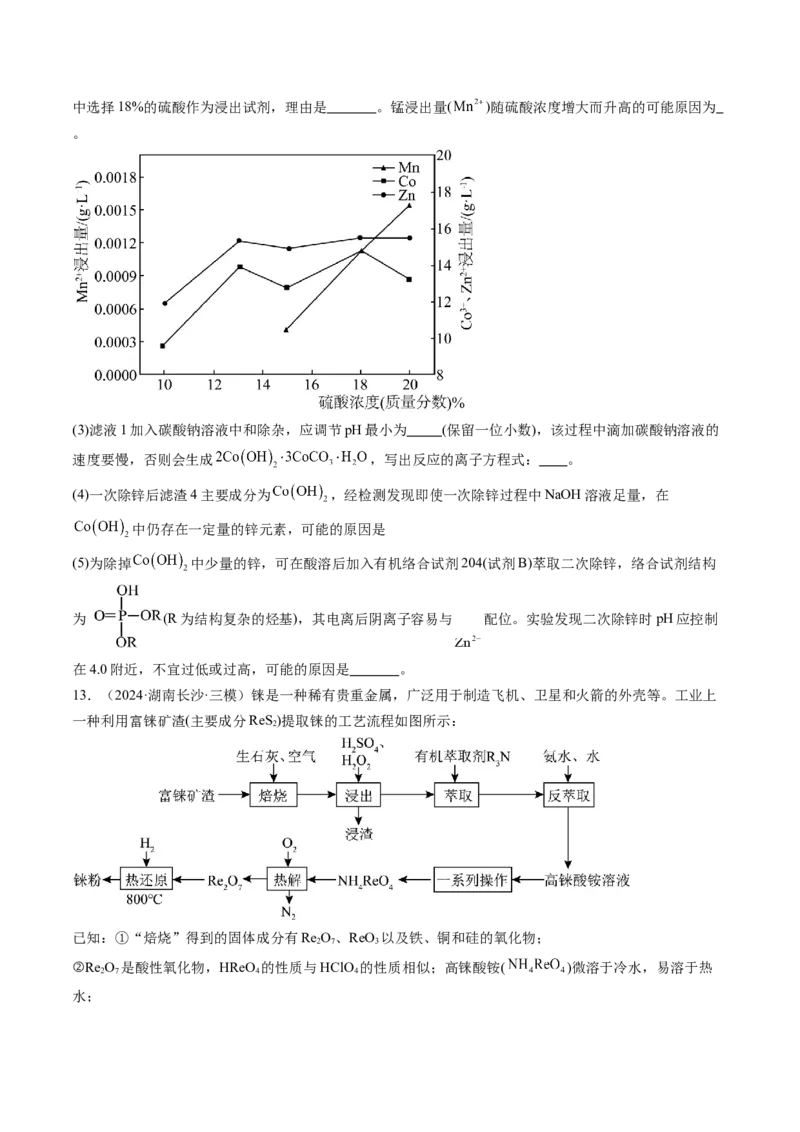
(2)实验发现硫酸酸浸过程中,浸出液中金属离子浓度随硫酸浓度(质量分数)的变化情况如下图,工业生产中选择18%的硫酸作为浸出试剂,理由是 。锰浸出量( )随硫酸浓度增大而升高的可能原因为
。
(3)滤液1加入碳酸钠溶液中和除杂,应调节pH最小为 (保留一位小数),该过程中滴加碳酸钠溶液的
速度要慢,否则会生成 ,写出反应的离子方程式: 。
(4)一次除锌后滤渣4主要成分为 ,经检测发现即使一次除锌过程中NaOH溶液足量,在
中仍存在一定量的锌元素,可能的原因是
(5)为除掉 中少量的锌,可在酸溶后加入有机络合试剂204(试剂B)萃取二次除锌,络合试剂结构
为 (R为结构复杂的烃基),其电离后阴离子容易与 配位。实验发现二次除锌时pH应控制
在4.0附近,不宜过低或过高,可能的原因是 。
13.(2024·湖南长沙·三模)铼是一种稀有贵重金属,广泛用于制造飞机、卫星和火箭的外壳等。工业上
一种利用富铼矿渣(主要成分ReS )提取铼的工艺流程如图所示:
2
已知:①“焙烧”得到的固体成分有Re O、ReO 以及铁、铜和硅的氧化物;
2 7 3
②Re O 是酸性氧化物,HReO 的性质与HClO 的性质相似;高铼酸铵( )微溶于冷水,易溶于热
2 7 4 4
水;③室温下, 。
回答下列问题:
(1)Re O 与水反应的离子方程式为 ;室温下,加入氨水后,测得溶液pH约为11,则溶液中
2 7
(填“>”“<”或“=”) 。
(2)“焙烧”时,空气从焙烧炉底部通入,粉碎后的矿渣从顶部加入,目的是 。
(3)写出“热解”时发生反应的主要化学方程式: 。
(4)测得制得的铼粉(含少量Re O)中Re与O的原子个数比为1∶0.35,则该产品的纯度为 %(保留
2 7
三位有效数字)。
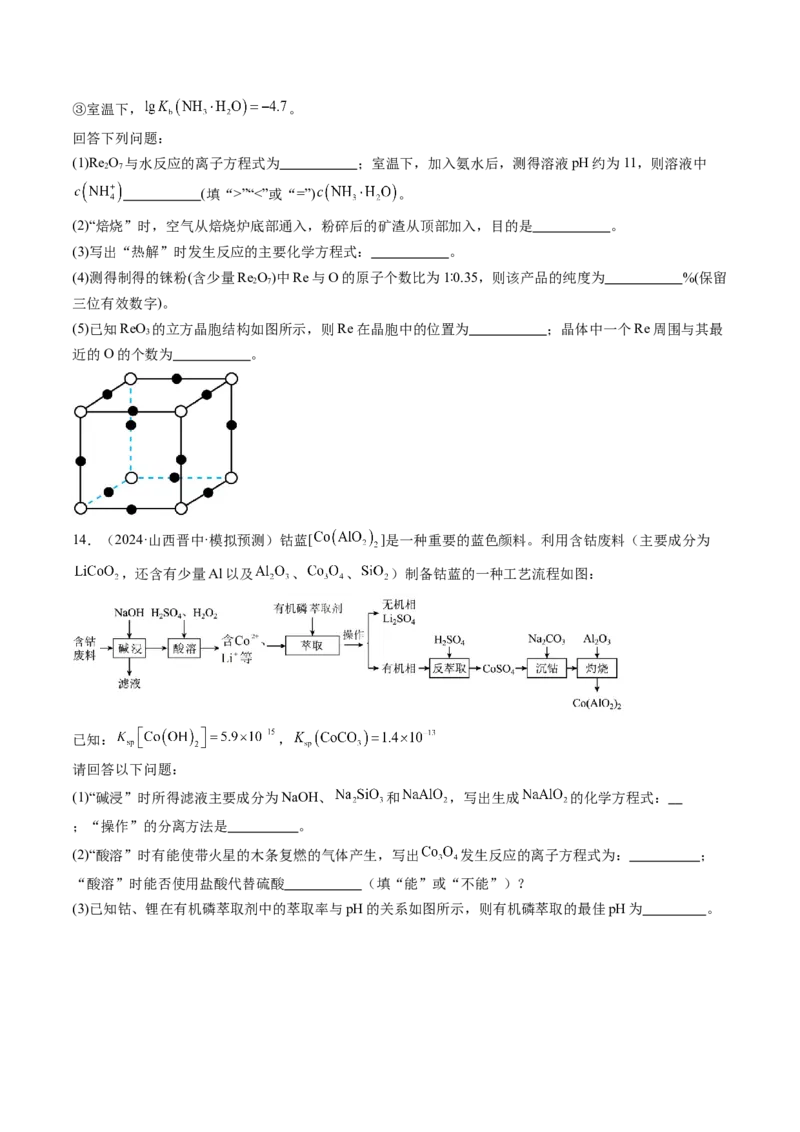
(5)已知ReO 的立方晶胞结构如图所示,则Re在晶胞中的位置为 ;晶体中一个Re周围与其最
3
近的O的个数为 。
14.(2024·山西晋中·模拟预测)钴蓝[ ]是一种重要的蓝色颜料。利用含钴废料(主要成分为
,还含有少量Al以及 、 、 )制备钴蓝的一种工艺流程如图:
已知: ,
请回答以下问题:
(1)“碱浸”时所得滤液主要成分为NaOH、 和 ,写出生成 的化学方程式:
;“操作”的分离方法是 。
(2)“酸溶”时有能使带火星的木条复燃的气体产生,写出 发生反应的离子方程式为: ;
“酸溶”时能否使用盐酸代替硫酸 (填“能”或“不能”)?
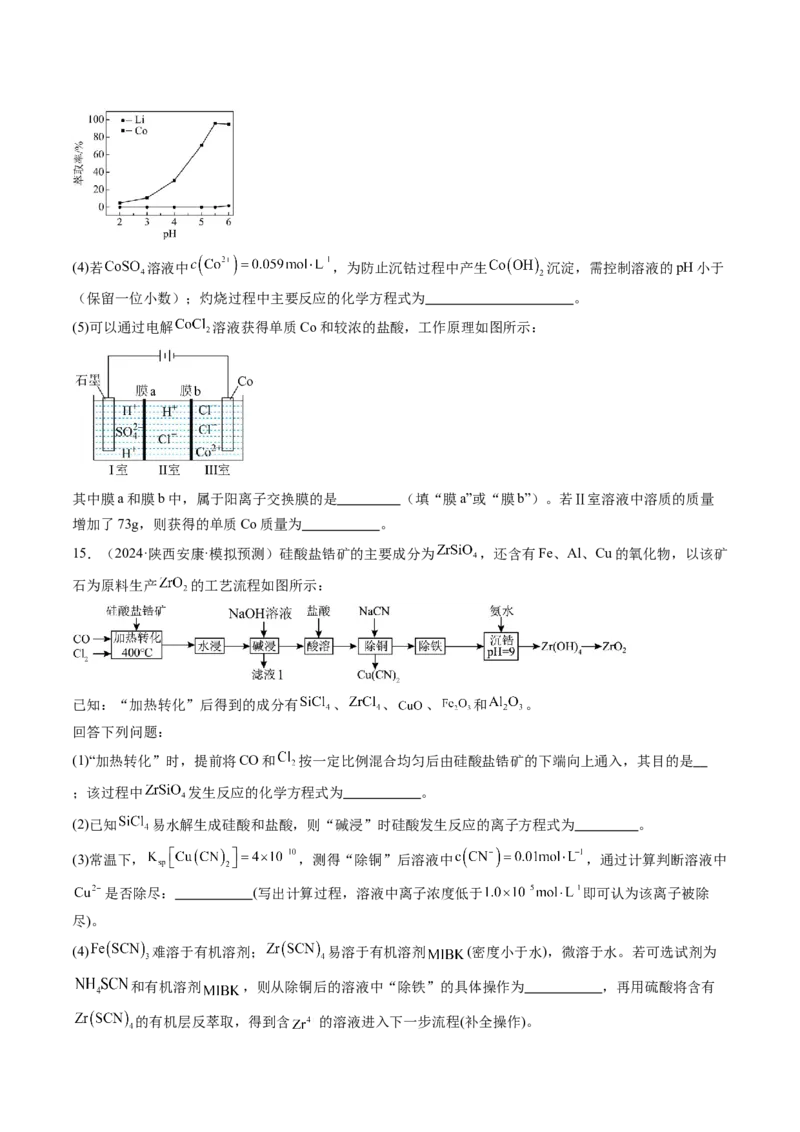
(3)已知钴、锂在有机磷萃取剂中的萃取率与pH的关系如图所示,则有机磷萃取的最佳pH为 。(4)若 溶液中 ,为防止沉钴过程中产生 沉淀,需控制溶液的pH小于
(保留一位小数);灼烧过程中主要反应的化学方程式为 。
(5)可以通过电解 溶液获得单质Co和较浓的盐酸,工作原理如图所示:
其中膜a和膜b中,属于阳离子交换膜的是 (填“膜a”或“膜b”)。若Ⅱ室溶液中溶质的质量
增加了73g,则获得的单质Co质量为 。
15.(2024·陕西安康·模拟预测)硅酸盐锆矿的主要成分为 ,还含有Fe、Al、Cu的氧化物,以该矿
石为原料生产 的工艺流程如图所示:
已知:“加热转化”后得到的成分有 、 、 、 和 。
回答下列问题:
(1)“加热转化”时,提前将CO和 按一定比例混合均匀后由硅酸盐锆矿的下端向上通入,其目的是
;该过程中 发生反应的化学方程式为 。
(2)已知 易水解生成硅酸和盐酸,则“碱浸”时硅酸发生反应的离子方程式为 。
(3)常温下, ,测得“除铜”后溶液中 ,通过计算判断溶液中
是否除尽: (写出计算过程,溶液中离子浓度低于 即可认为该离子被除
尽)。
(4) 难溶于有机溶剂; 易溶于有机溶剂 (密度小于水),微溶于水。若可选试剂为
和有机溶剂 ,则从除铜后的溶液中“除铁”的具体操作为 ,再用硫酸将含有
的有机层反萃取,得到含 的溶液进入下一步流程(补全操作)。(5)常温下, ,“沉锆”后 的溶液中, (填“
”“ ”或“ ”)。
(6)若 硅酸盐锆矿经上述流程后,最后制得 ,则原矿石中 的百分含量为 (忽
略过程中Zr的消耗,保留两位有效数字)。
1.(2024·辽宁卷)某工厂利用铜屑脱除锌浸出液中的 并制备 ,流程如下“脱氯”步骤仅 元素化合
价发生改变。下列说法正确的是
锌浸出液中相关成分(其他成分无干扰)
离子
浓度 145 0.03 1
A. “浸铜”时应加入足量 ,确保铜屑溶解完全
B. “浸铜”反应:
C. “脱氯”反应:
D. 脱氯液净化后电解,可在阳极得到
2.(2024·北京卷)硫酸是重要化工原料,工业生产制取硫酸的原理示意图如下。
下列说法不正确的是
A. I的化学方程式:
B. Ⅱ中的反应条件都是为了提高 平衡转化率
C. 将黄铁和换成硫黄可以减少废渣的产生
D. 生产过程中产生的尾气可用碱液吸收
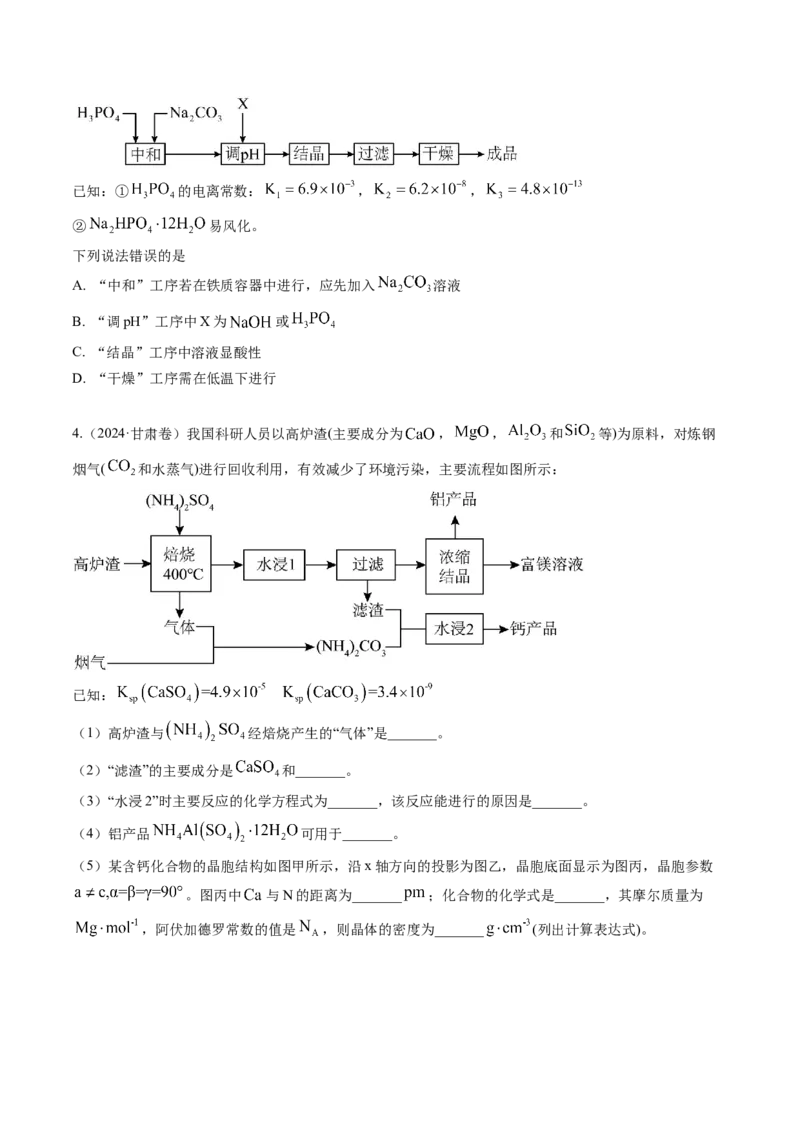
3.(2024·湖南卷)中和法生产 的工艺流程如下:已知:① 的电离常数: , ,
② 易风化。
下列说法错误的是
A. “中和”工序若在铁质容器中进行,应先加入 溶液
B. “调pH”工序中X为 或
C. “结晶”工序中溶液显酸性
D. “干燥”工序需在低温下进行
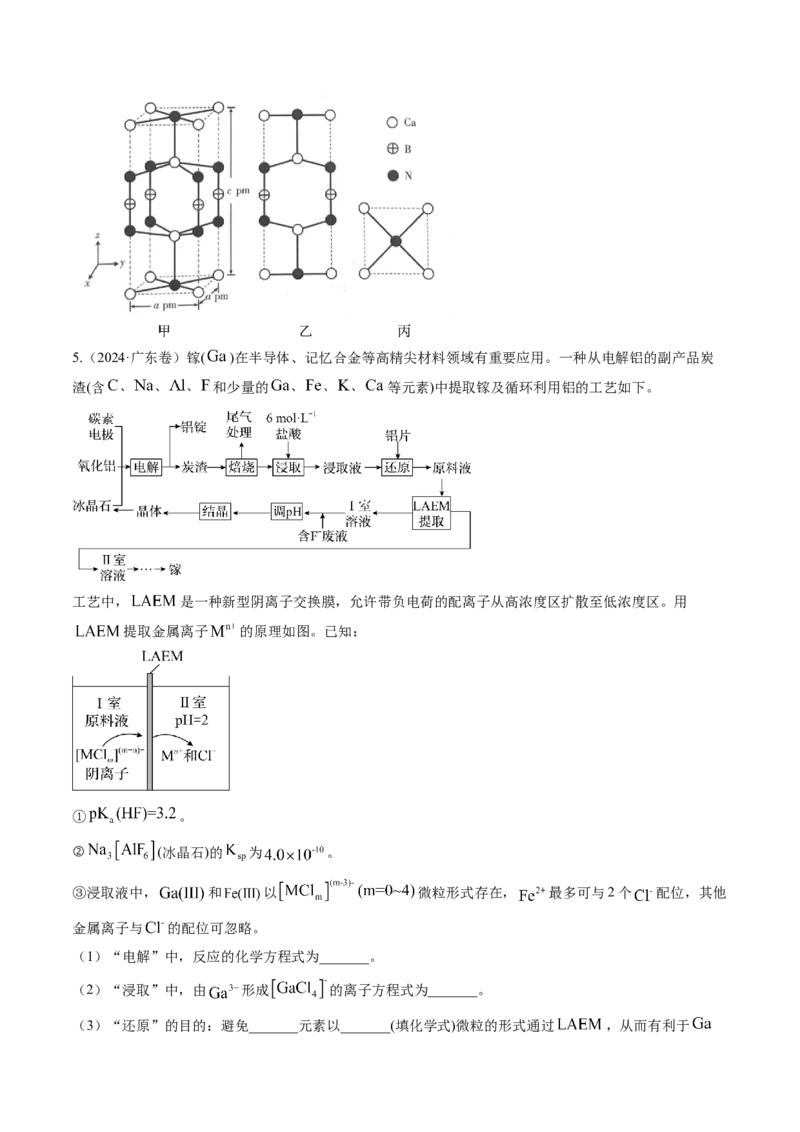
4.(2024·甘肃卷)我国科研人员以高炉渣(主要成分为 , , 和 等)为原料,对炼钢
烟气( 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
已知:
(1)高炉渣与 经焙烧产生的“气体”是_______。
(2)“滤渣”的主要成分是 和_______。
(3)“水浸2”时主要反应的化学方程式为_______,该反应能进行的原因是_______。
(4)铝产品 可用于_______。
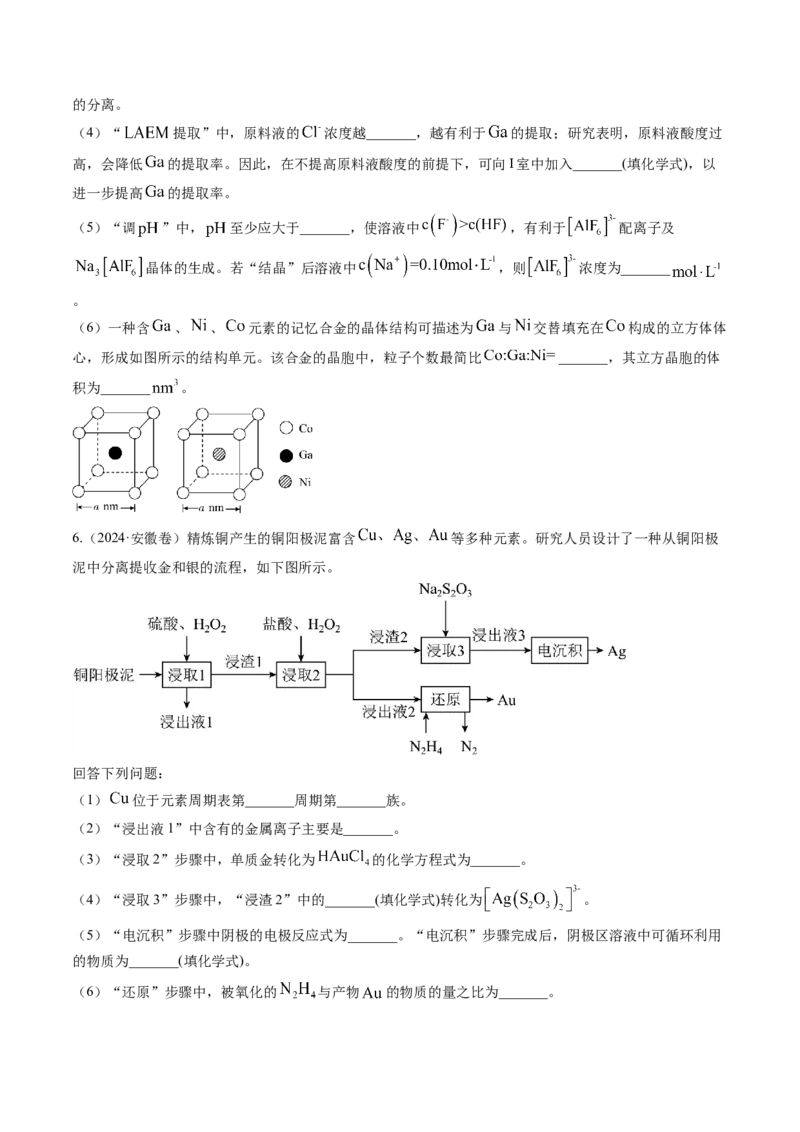
(5)某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞参数
。图丙中 与N的距离为_______ ;化合物的化学式是_______,其摩尔质量为
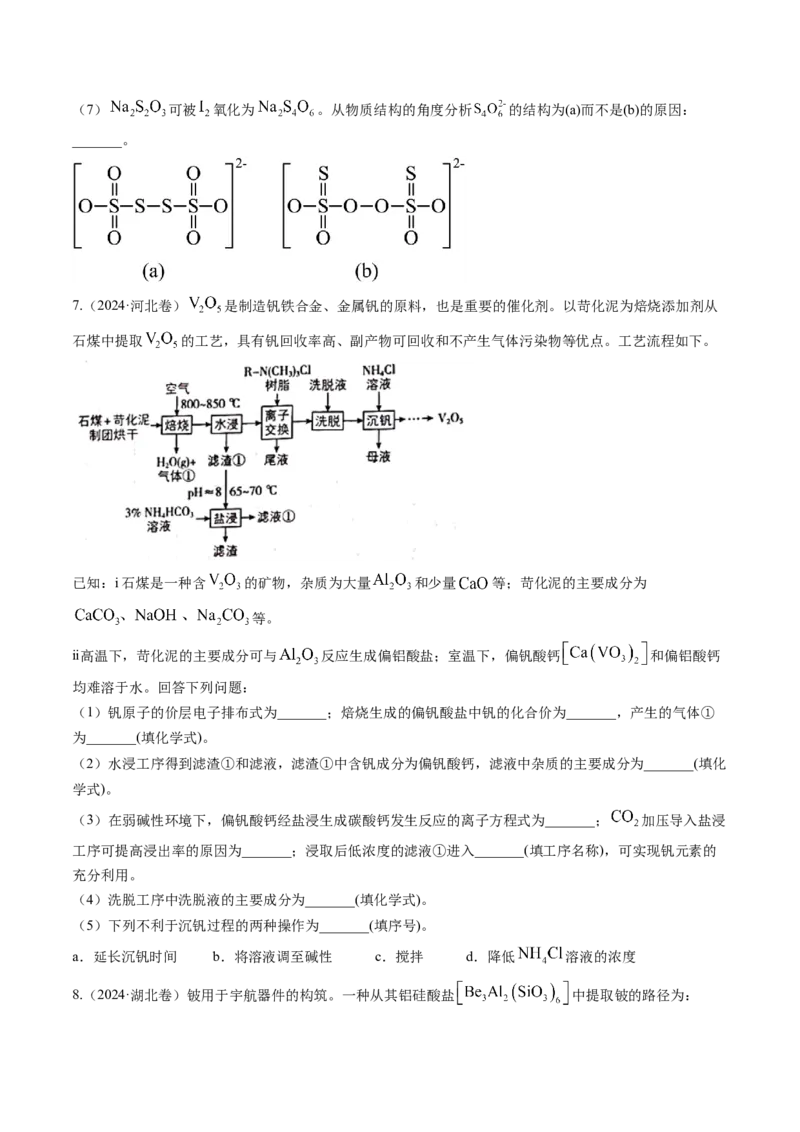
,阿伏加德罗常数的值是 ,则晶体的密度为_______ (列出计算表达式)。5.(2024·广东卷)镓( )在半导体、记忆合金等高精尖材料领域有重要应用。一种从电解铝的副产品炭
渣(含 和少量的 等元素)中提取镓及循环利用铝的工艺如下。
工艺中, 是一种新型阴离子交换膜,允许带负电荷的配离子从高浓度区扩散至低浓度区。用
提取金属离子 的原理如图。已知:
① 。
② (冰晶石)的 为 。
③浸取液中, 和 以 微粒形式存在, 最多可与2个 配位,其他
金属离子与 的配位可忽略。
(1)“电解”中,反应的化学方程式为_______。
(2)“浸取”中,由 形成 的离子方程式为_______。
(3)“还原”的目的:避免_______元素以_______(填化学式)微粒的形式通过 ,从而有利于的分离。
(4)“ 提取”中,原料液的 浓度越_______,越有利于 的提取;研究表明,原料液酸度过
高,会降低 的提取率。因此,在不提高原料液酸度的前提下,可向I室中加入_______(填化学式),以
进一步提高 的提取率。
(5)“调 ”中, 至少应大于_______,使溶液中 ,有利于 配离子及
晶体的生成。若“结晶”后溶液中 ,则 浓度为_______
。
(6)一种含 、 、 元素的记忆合金的晶体结构可描述为 与 交替填充在 构成的立方体体
心,形成如图所示的结构单元。该合金的晶胞中,粒子个数最简比 _______,其立方晶胞的体
积为_______ 。
6.(2024·安徽卷)精炼铜产生的铜阳极泥富含 等多种元素。研究人员设计了一种从铜阳极
泥中分离提收金和银的流程,如下图所示。
回答下列问题:
(1) 位于元素周期表第_______周期第_______族。
(2)“浸出液1”中含有的金属离子主要是_______。
(3)“浸取2”步骤中,单质金转化为 的化学方程式为_______。
(4)“浸取3”步骤中,“浸渣2”中的_______(填化学式)转化为 。
(5)“电沉积”步骤中阴极的电极反应式为_______。“电沉积”步骤完成后,阴极区溶液中可循环利用
的物质为_______(填化学式)。
(6)“还原”步骤中,被氧化的 与产物 的物质的量之比为_______。(7) 可被 氧化为 。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
_______。
7.(2024·河北卷) 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添加剂从
石煤中提取 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程如下。
已知:i石煤是一种含 的矿物,杂质为大量 和少量 等;苛化泥的主要成分为
等。
ⅱ高温下,苛化泥的主要成分可与 反应生成偏铝酸盐;室温下,偏钒酸钙 和偏铝酸钙
均难溶于水。回答下列问题:
(1)钒原子的价层电子排布式为_______;焙烧生成的偏钒酸盐中钒的化合价为_______,产生的气体①
为_______(填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为_______(填化
学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为_______; 加压导入盐浸
工序可提高浸出率的原因为_______;浸取后低浓度的滤液①进入_______(填工序名称),可实现钒元素的
充分利用。
(4)洗脱工序中洗脱液的主要成分为_______(填化学式)。
(5)下列不利于沉钒过程的两种操作为_______(填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低 溶液的浓度
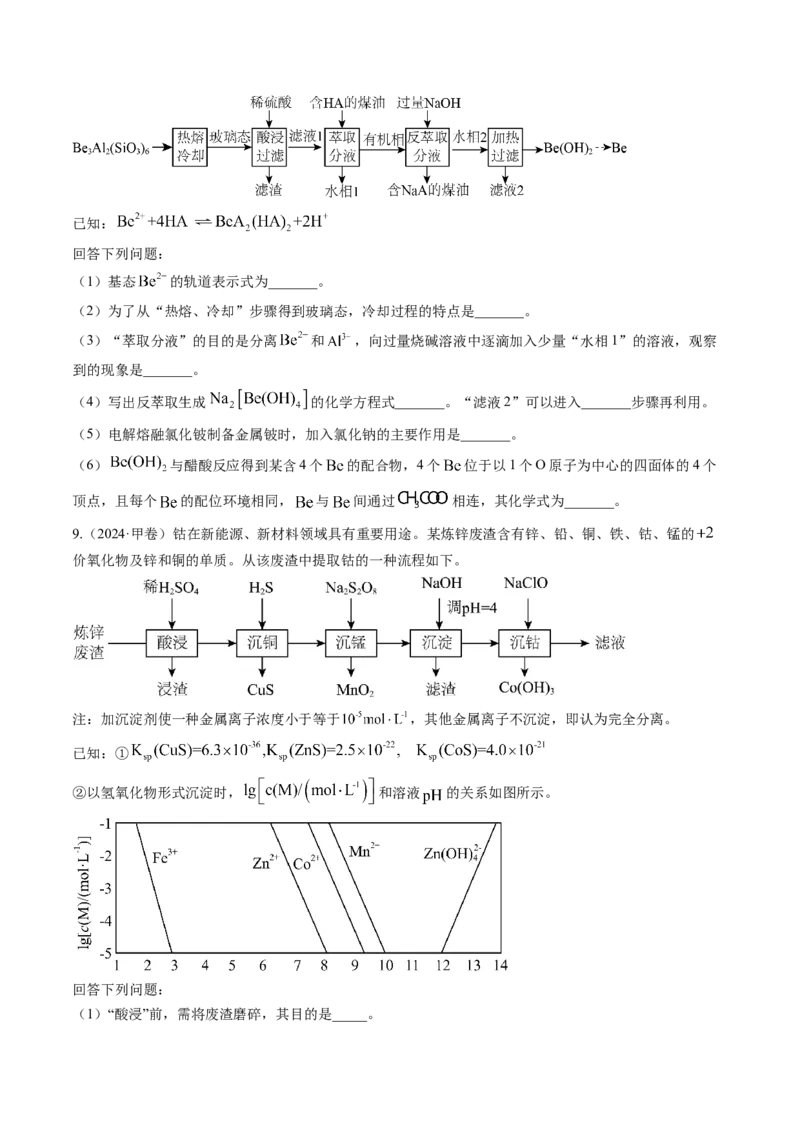
8.(2024·湖北卷)铍用于宇航器件的构筑。一种从其铝硅酸盐 中提取铍的路径为:已知:
回答下列问题:
(1)基态 的轨道表示式为_______。
(2)为了从“热熔、冷却”步骤得到玻璃态,冷却过程的特点是_______。
(3)“萃取分液”的目的是分离 和 ,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察
到的现象是_______。
(4)写出反萃取生成 的化学方程式_______。“滤液2”可以进入_______步骤再利用。
(5)电解熔融氯化铍制备金属铍时,加入氯化钠的主要作用是_______。
(6) 与醋酸反应得到某含4个 的配合物,4个 位于以1个O原子为中心的四面体的4个
顶点,且每个 的配位环境相同, 与 间通过 相连,其化学式为_______。
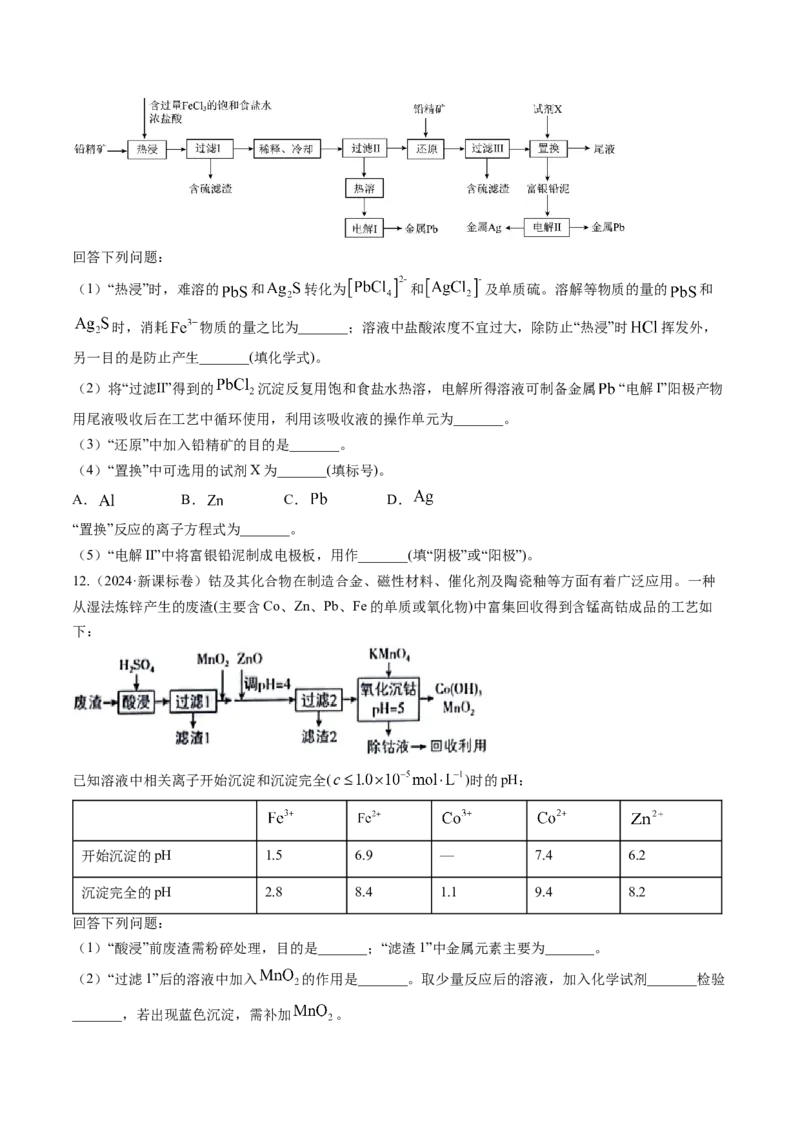
9.(2024·甲卷)钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
注:加沉淀剂使一种金属离子浓度小于等于 ,其他金属离子不沉淀,即认为完全分离。
已知:① 。
②以氢氧化物形式沉淀时, 和溶液 的关系如图所示。
回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是_____。(2)“酸浸”步骤中, 发生反应的化学方程式是_____。
(3)假设“沉铜”后得到的滤液中 和 均为 ,向其中加入 至 沉淀
完全,此时溶液中 _____ ,据此判断能否实现 和 的完全分离_____(填“能”或
“不能”)。
(4)“沉锰”步骤中,生成 ,产生 的物质的量为_____。
(5)“沉淀”步骤中,用 调 ,分离出的滤渣是_____。
(6)“沉钴”步骤中,控制溶液 ,加入适量的 氧化 ,其反应的离子方程式为
_____。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是_____。
10.(2024·辽宁卷)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧化”时转化为硫
酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的 颗粒被 、 包裹),以提高金的
浸出率并冶炼金,工艺流程如下:
回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为
_______(填化学式)。
(2)“细菌氧化”中, 发生反应的离子方程式为_______。
(3)“沉铁砷”时需加碱调节 ,生成_______(填化学式)胶体起絮凝作用,促进了含 微粒的沉降。
(4)“培烧氧化”也可提高“浸金”效率,相比“培烧氧化”,“细菌氧化”的优势为_______(填标
号)。
A. 无需控温 B. 可减少有害气体产生
C. 设备无需耐高温 D. 不产生废液废渣
(5)“真金不拍火炼”,表明 难被 氧化,“浸金”中 的作用为_______。
(6)“沉金”中 的作用为_______。
(7)滤液②经 酸化, 转化为 和 的化学方程式为_______。用碱中和
可生成_______(填溶质化学式)溶液,从而实现循环利用。
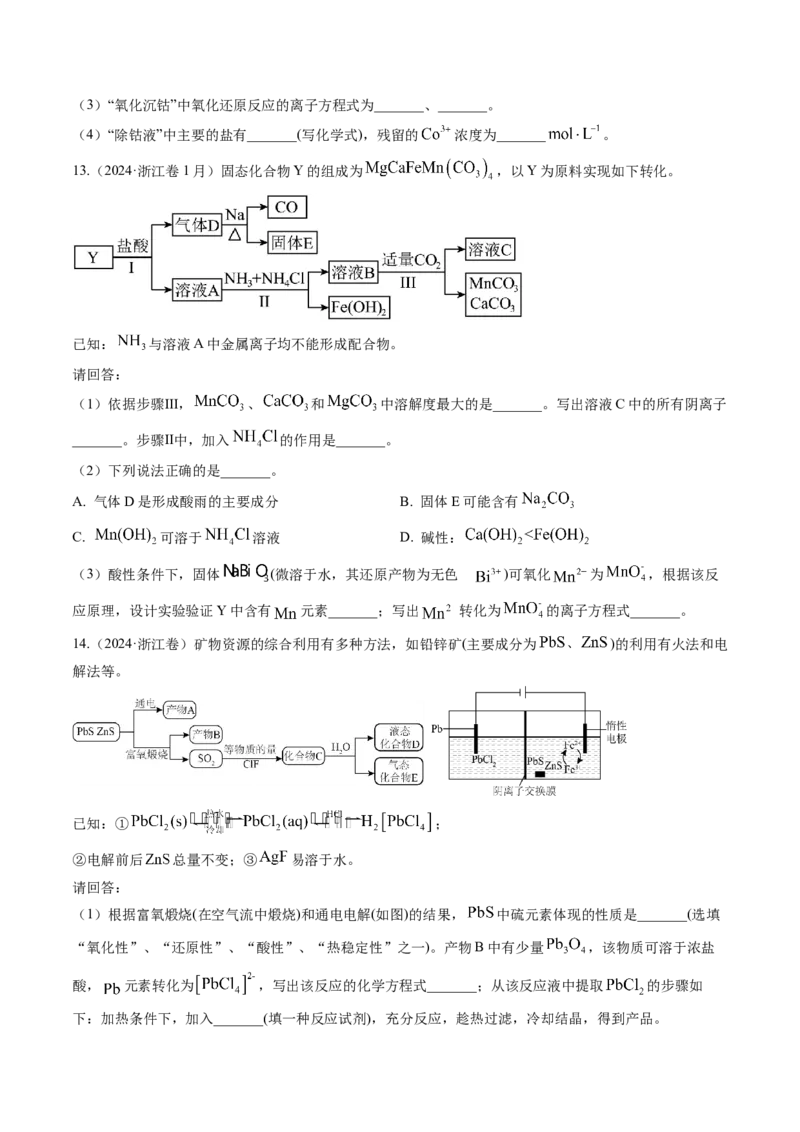
11.(2024·山东卷)以铅精矿(含 , 等)为主要原料提取金属 和 的工艺流程如下:回答下列问题:
(1)“热浸”时,难溶的 和 转化为 和 及单质硫。溶解等物质的量的 和
时,消耗 物质的量之比为_______;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,
另一目的是防止产生_______(填化学式)。
(2)将“过滤Ⅱ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极产物
用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为_______。
(3)“还原”中加入铅精矿的目的是_______。
(4)“置换”中可选用的试剂X为_______(填标号)。
A. B. C. D.
“置换”反应的离子方程式为_______。
(5)“电解II”中将富银铅泥制成电极板,用作_______(填“阴极”或“阳极”)。
12.(2024·新课标卷)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广泛应用。一种
从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成品的工艺如
下:
已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是_______;“滤渣1”中金属元素主要为_______。
(2)“过滤1”后的溶液中加入 的作用是_______。取少量反应后的溶液,加入化学试剂_______检验
_______,若出现蓝色沉淀,需补加 。(3)“氧化沉钴”中氧化还原反应的离子方程式为_______、_______。
(4)“除钴液”中主要的盐有_______(写化学式),残留的 浓度为_______ 。
13.(2024·浙江卷1月)固态化合物Y的组成为 ,以Y为原料实现如下转化。
已知: 与溶液A中金属离子均不能形成配合物。
请回答:
(1)依据步骤Ⅲ, 、 和 中溶解度最大的是_______。写出溶液C中的所有阴离子
_______。步骤Ⅱ中,加入 的作用是_______。
(2)下列说法正确的是_______。
A. 气体D是形成酸雨的主要成分 B. 固体E可能含有
C. 可溶于 溶液 D. 碱性:
(3)酸性条件下,固体 (微溶于水,其还原产物为无色 的)可氧化 为 ,根据该反
应原理,设计实验验证Y中含有 元素_______;写出 转化为 的离子方程式_______。
14.(2024·浙江卷)矿物资源的综合利用有多种方法,如铅锌矿(主要成分为 )的利用有火法和电
解法等。
已知:① ;
②电解前后 总量不变;③ 易溶于水。
请回答:
(1)根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果, 中硫元素体现的性质是_______(选填
“氧化性”、“还原性”、“酸性”、“热稳定性”之一)。产物B中有少量 ,该物质可溶于浓盐
酸, 元素转化为 ,写出该反应的化学方程式_______;从该反应液中提取 的步骤如
下:加热条件下,加入_______(填一种反应试剂),充分反应,趁热过滤,冷却结晶,得到产品。(2)下列说法正确的是_______。
A. 电解池中发生的总反应是 (条件省略)
B. 产物B主要是铅氧化物与锌氧化物
C. 化合物C在水溶液中最多可中和
D. 的氧化性弱于
(3)D的结构为 ( 或 ),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液
探究X为何种元素。
①实验方案:取D的溶液,加入足量 溶液,加热充分反应,然后_______;
②写出D(用 表示)的溶液与足量 溶液反应的离子方程式_______。
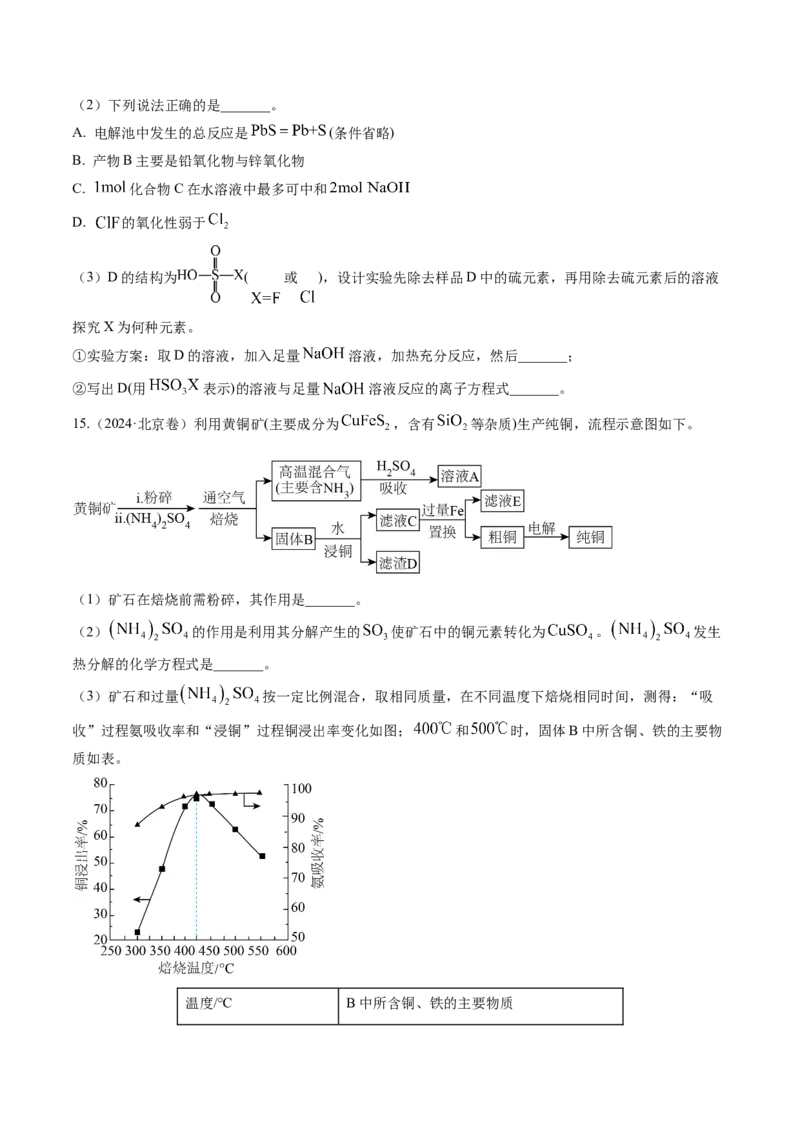
15.(2024·北京卷)利用黄铜矿(主要成分为 ,含有 等杂质)生产纯铜,流程示意图如下。
(1)矿石在焙烧前需粉碎,其作用是_______。
(2) 的作用是利用其分解产生的 使矿石中的铜元素转化为 。 发生
热分解的化学方程式是_______。
(3)矿石和过量 按一定比例混合,取相同质量,在不同温度下焙烧相同时间,测得:“吸
收”过程氨吸收率和“浸铜”过程铜浸出率变化如图; 和 时,固体B中所含铜、铁的主要物
质如表。
温度/℃ B中所含铜、铁的主要物质400
500
①温度低于 ,随焙烧温度升高,铜浸出率显著增大的原因是_______。
②温度高于 ,根据焙烧时可能发生的反应,解释铜浸出率随焙烧温度升高而降低的原因是
_______。
(4)用离子方程式表示置换过程中加入 的目的_______。
(5)粗铜经酸浸处理,再进行电解精炼;电解时用酸化的 溶液做电解液,并维持一定的 和
。粗铜若未经酸浸处理,消耗相同电量时,会降低得到纯铜的量,原因是_______。