文档内容
2019 年辽宁省沈阳市中考化学试卷
一、选择题(本部分包括13道小题,1-11小题,每题1分;12、13小题,每题2分
每小题只有一个最符合题目要求的选项.)
1.下列变化属于化学变化的是( )
A.谷物酿酒 B.汽油挥发 C.冰雪融化 D.西瓜榨汁
2.下列关于物质用途的说法不正确的是( )
A.熟石灰用于改良酸性土壤
B.氮气用作灯泡填充气
C.液态氧用作火箭的可燃剂
D.食盐用作调味品
3.下列符号表示2个氢原子的是( )
A.2H B.2H C.H D.2HO
2 2 2
4.下列实验操作中错误的是( )
A.蒸发溶剂 B.取用固体 C.滴加液体 D.量取液体
5.下列叙述属于CO化学性质的是( )
A.无色 B.无味 C.难溶于水 D.能燃烧
6.为预防甲状腺疾病,人体应补充的元素是( )
A.碘元素 B.氟元素 C.硒元素 D.氯元素
7.下列物质属于化合物的是( )
A.氦气 B.氯化钾 C.空气 D.金刚石
8.下列结构示意图表示阴离子的是( )
A. B.
C. D.
9.下列情况会造成环境污染的是( )
A.垃圾分类回收 B.燃放烟花爆竹
C.增加绿地面积 D.处理工业废气
10.下列早餐食物中富含蛋白质的是( )
A.鸡蛋 B.青椒 C.稀饭 D.馒头
11.下列物质能用作磷肥的是( )A.NHNO B.CO(NH) C.Ca(PO) D.KSO
4 3 2 2 3 4 2 2 4
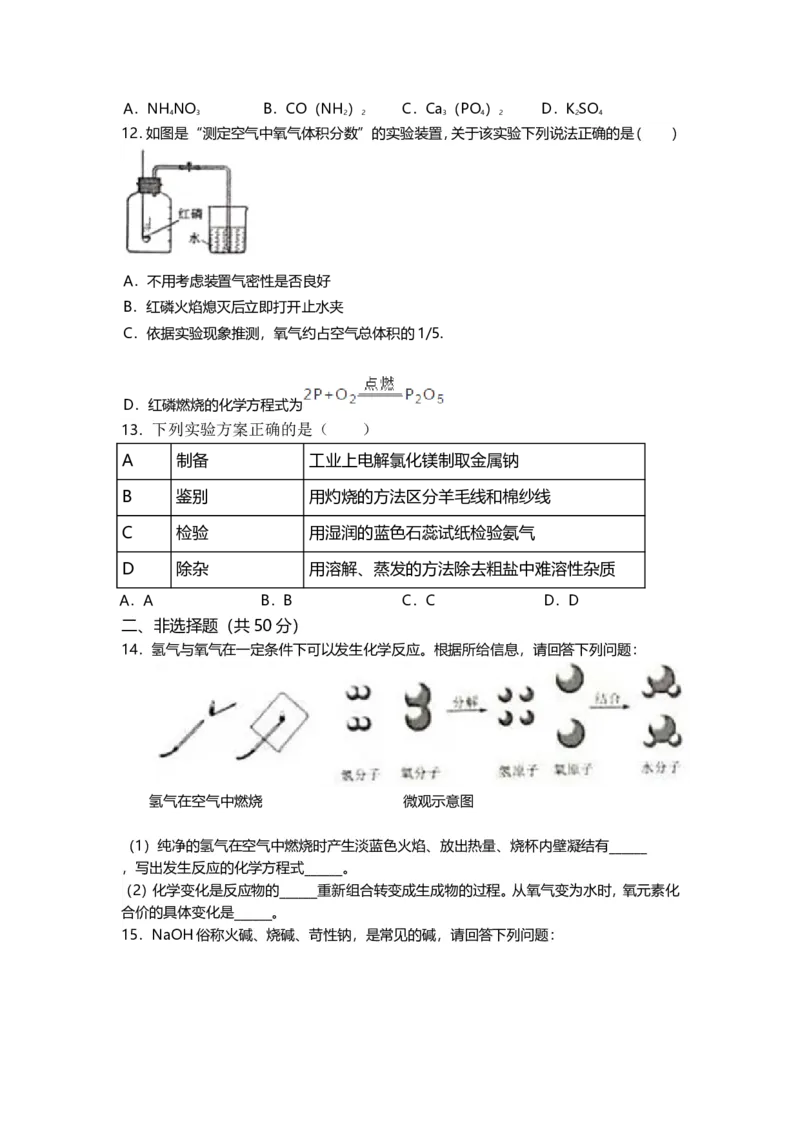
12.如图是“测定空气中氧气体积分数”的实验装置,关于该实验下列说法正确的是( )
A.不用考虑装置气密性是否良好
B.红磷火焰熄灭后立即打开止水夹
C.依据实验现象推测,氧气约占空气总体积的1/5.
D.红磷燃烧的化学方程式为
13.下列实验方案正确的是( )
A 制备 工业上电解氯化镁制取金属钠
B 鉴别 用灼烧的方法区分羊毛线和棉纱线
C 检验 用湿润的蓝色石蕊试纸检验氨气
D 除杂 用溶解、蒸发的方法除去粗盐中难溶性杂质
A.A B.B C.C D.D
二、非选择题(共50分)
14.氢气与氧气在一定条件下可以发生化学反应。根据所给信息,请回答下列问题:
氢气在空气中燃烧 微观示意图
(1)纯净的氢气在空气中燃烧时产生淡蓝色火焰、放出热量、烧杯内壁凝结有______
,写出发生反应的化学方程式______。
(2)化学变化是反应物的______重新组合转变成生成物的过程。从氧气变为水时,氧元素化
合价的具体变化是______。
15.NaOH俗称火碱、烧碱、苛性钠,是常见的碱,请回答下列问题:(1)NaOH的名称是______,易溶于水,溶于水生成自由移动的______(填微粒符号),所以
NaOH溶液能够导电。
(2)向NaOH溶液中滴加稀硫酸,溶液的pH______(填”增大”、“减小”或“不变”)。
(3)在试管中加入2mL 10%NaOH溶液,滴加5%CuSO 溶液4-5滴,生成______色的Cu
4
(OH)沉淀。用试管中的物质检验葡萄糖,发生如下反应:CH O+2Cu(OH)+NaOH
2 6 12 6 2
CH ONa+CuO↓+3X,推测X的化学式为______。
6 11 7 2
(4)参考如图,在( )内画出“→”或“-”补全图例(“→”表示物质间转化,“-”表示
物质间相互反应)。请写出图例中,能发生复分解反应的化学方程式:______(写出一个即可)。
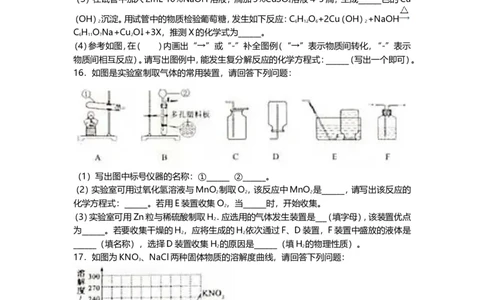
16.如图是实验室制取气体的常用装置,请回答下列问题:
(1)写出图中标号仪器的名称:①______ ②______。
(2)实验室可用过氧化氢溶液与MnO 制取O,该反应中MnO 是______,请写出该反应的
2 2 2
化学方程式:______。若用E装置收集O,当______时,开始收集。
2
(3)实验室可用Zn粒与稀硫酸制取H.应选用的气体发生装置是___(填字母),该装置优点
2
为______。若要收集干燥的H,应将生成的H 依次通过F、D装置,F装置中盛放的液体是
2 2
______(填名称),选择D装置收集H 的原因是______(填H 的物理性质)。
2 2
17.如图为KNO、NaCl两种固体物质的溶解度曲线,请回答下列问题:
3
(1)10℃时KNO 的溶解度______(填“<”、“=“或“>”)NaCl的溶解度。
3(2)80℃时140g KNO 溶于100g水中形成的溶液是______(填“饱和”或“不饱和”)溶
3
液。
(3)如图所示进行实验,再现结晶过程:
本实验条件下,影响析出晶体质量多少的主要因素是______、______。
18.化学是一门实用的基础科学,在人类社会的发展历程中起着重要作用。
正确认识物质
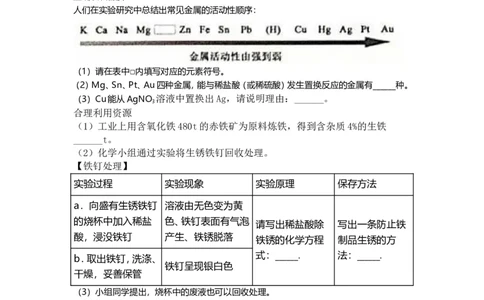
人们在实验研究中总结出常见金属的活动性顺序:
(1)请在表中□内填写对应的元素符号。
(2)Mg、Sn、Pt、Au四种金属,能与稀盐酸(或稀硫酸)发生置换反应的金属有______种。
(3)Cu能从AgNO 溶液中置换出Ag,请说明理由:______。
3
合理利用资源
(1)工业上用含氧化铁480t的赤铁矿为原料炼铁,得到含杂质4%的生铁
______t。
(2)化学小组通过实验将生锈铁钉回收处理。
【铁钉处理】
实验过程 实验现象 实验原理 保存方法
a.向盛有生锈铁钉 溶液由无色变为黄
的烧杯中加入稀盐 色、铁钉表面有气泡
请写出稀盐酸除 写出一条防止铁
酸,浸没铁钉 产生、铁锈脱落
铁锈的化学方程 制品生锈的方
b.取出铁钉,洗涤、
式:______. 法:______.
铁钉呈现银白色
干燥,妥善保管
(3)小组同学提出,烧杯中的废液也可以回收处理。
【废液处理】
同学们查阅相关资料,获知:
a.FeO 是一种红棕色粉末,俗称铁红,常用作红色油漆和涂料。
2 3
b.FeCl+2NaOH=Fe(OH)↓+2NaCl
2 2
c.4Fe(OH)+O+2HO=4Fe(OH)
2 2 2 3
d.不溶性碱受热易分解,生成对应的金属氧化物和水。
实验流程:①悬浊液A静置一天的原因是______。
②操作I是______。
③写出固体C转化为铁红的化学方程式______。
促进科技发展
化学学科在合成药物等方面发挥若巨大作用,以下是几种常见的合成药物,请根据信息回答
下列问题:
(1)解热镇痛药
阿司匹林是人们熟知的治感冒药,具有解热镇痛作用,化学式为CHO,相对分子质量是
9 8 4
______。
(2)抗生素
青霉素是最重要的抗生素,即消炎药,能治疗肺炎和外伤感染等。青霉素中用得较多的是青
霉素钠,化学式为C H ONSNa,其中氢、氧元素质量比为______。
16 17 4 2
(3)抗酸药
抗酸药是一类治疗胃痛的药物,能中和胃里过多的盐酸,缓解胃部不适。抗酸药的种类很多,
通常含有一种或几种化学物质,如NaHCO、MgCO、Mg(OH)等。请写出其中一个与盐酸
3 3 2
反应的化学方程式______。
19.某化学小组对石灰石灼烧后得到的固体进行相关探究。
成分分析
(1)检验灼烧过程中产生的新物质
①根据已有知识和经验判断:石灰石灼烧后固体中含有CaO,判断的依据是
______(用化学方程式表示)。
②设计实验方案进行验证:
实验内容 实验现象 实验分析
取灼烧后固体放入盛有冷水的烧杯
中,充分搅拌静置后,取少量上层澄 溶液由无色 反应后生成碱,请写出该反
清的液体置于试管中,向其中滴加2 变为____色 应的化学方程式:______.
滴酚酞试液
(2)检验灼烧后固体中是否含有CaCO
3
向盛有灼烧后固体的烧杯中滴加稀盐酸,有气泡产生,证明______。
数据分析
用反应前后质量差计算灼烧后固体中CaCO 的质量分数
3
化学小组设计以下两个实验方案,方案中反应前后质量差分别用m 与m 表示。(两方案中
1 2
实验操作误差忽略不计,取用的灼烧后固体成分均匀、质量相等,固体中除CaO、CaCO 其
3
余成分均不发生反应,所用稀盐酸经估算确保足量)数据测量 数据处理
实验方案
反应前后质量
反应前 反应后
差
方案一:取灼烧后
固体放入烧杯中, 灼烧后固体的质量、 烧杯中剩余物质的
m
1
加入稀盐酸充分反 所用稀盐酸质量 质量
应,不再产生气泡
方案二:取灼烧后
固体继续灼烧,至
灼烧后固体的质量 剩余固体的质量 m
2
固体的质量不再改
变
结合信息,比较m 与m 的关系。请写出两种不同猜想并分别说明理由。
1 2
猜想1及理由:______。
猜想2及理由:______。
经分析选择合理的实验方案,进行计算……
拓展研究
如图的酒精灯和酒精喷灯是常用的加热仪器,请回答下列问题:
(1)酒精灯是玻璃仪器,火焰温度通常可达300~500℃,______(填“焰心”、“内焰”或
“外焰”)温度最高。熄灭酒精灯的方法是______,采用此方法灭火的原理是______。
(2)酒精喷灯一般是铜质仪器,火焰温度通常可达800-1000℃.使用酒精喷灯时应先向引
火碗内注入2/3容量的酒精,用火柴将引火碗内酒精点燃,点燃引火碗内酒精的目的是
______、______。参考答案
第一部分选择题(共15分)
(本部分包括13道小题,1-11小题,每题1分;12、13小题,每题2分。每小题只
有一个最符合题目要求的选项。)
1.A 2.C 3.B 4.C 5.D 6.A 7.B 8.D 9.B 10.A
11.C 12.C 13.B
第二部分非选择题(共50分)
14.(1)水雾(或水珠,其他合理答案均可)
(2)原子0→-2
15.(1)氢氧化钠Na+、OH-(2)减小(3)蓝H O
2
(4)
16.(1)①试管②长颈漏斗(2)催化剂
导管口有连续气泡均匀冒出(其他合理答案均可)
(3)B 便于控制反应的发生和停止(其他合理答案均可)
浓硫酸 H 比密度小于空气(其他合理答案均可)
2
17.(1)<
(2)不饱和
(3)热水的温度(其他合理答案均可)
热水的量(其他合理答案均可)
18.正确认识物质
(1)Al
(2)2
(3)铜的金属活动性比银强(其他合理答案均可)合理利用资源(1)350
(2)【铁钉处理】
实验原理:Fe O +6HCI=2FeCl +3H O
2 3 3 2
保存方法:刷漆(电镀、涂油等其他合理答案均可)
(3)【废液处理】
①使Fe(OH) 转化为Fe(OH) (其他合理答案均可)
2 3
数据分析m1=m2,两方案固体中CaCO3质量相等,完全反应后生成CO2,质量相等,
反应前后质量差相等(其他合理答案均可)
m1>m2,两方案固体中CaCO3质量相等,完全反应后生成CO2质量相等,
溶液中水蒸气和氯化氢气体逸出,m1偏大(其他合理答案均可)
m1