文档内容
中国人民大学附属中学学生用书
高三化学二轮专题复习
班级:
_________
姓名:
_________
1目 录
高三实验板块复习——性质专题(P3-25)
高三实验板块复习——制备专题(P26-33)
高三实验板块复习——原理专题(P34-41)
高三实验板块复习——定量专题(P42-43)
高三实验板块复习——其它专题(P44-46)
高三实验板块复习——性质专题习题(P47-59)
高三实验板块复习——制备专题习题(P60-64)
高三实验板块复习——原理专题习题(P65-72)
高三实验板块复习——定量专题习题(P72-76)
高三实验板块复习——参考答案(P77-82)
2高三实验板块复习——性质专题
实验1:必修一 鲁科版p12 人教版p32
实验分类:性质
实验目的:金属钠的性质
实验步骤: 取一小块金属钠,用滤纸吸干表面
的煤油后,用刀切去一端的外皮,这时可以看到
钠的真面目。
实验现象:新切开的钠表面呈银白色,在空气中迅速变暗。
实验结论:钠质软,性质活泼,4Na+O =2Na O
2 2
注意事项:剩余钠,放回原试剂瓶。
实验2:必修一 鲁科版p12 人教版p33
实验分类:性质
实验目的:金属钠与氧气的反应
实验现象:与氧气剧烈反应,发出黄色火焰,生成一种淡黄色的固体。
实验仪器:三角架、泥三角、坩埚、坩埚钳、酒精灯等
实验结论:钠在燃烧时生成淡黄色的过氧化钠
2Na+O =Na O (点燃或加热)
2 2 2
注意事项:钠的燃烧实验在坩埚里进行比较规范。钠开始燃烧后立即撤掉酒精灯。
实验3:必修一 鲁科版p11 人教版p34
实验分类:性质
实验目的:金属钠与水的反应
实验步骤:在烧杯(表面皿)中加一些水,滴入几滴酚酞溶液,然后把一小块钠放入水中,
实验现象:钠浮在水面上,熔成一个闪亮的小球,小球四处游动,发出嘶嘶的响声,(有时
可能有火花,钠球周围有水雾),小球逐渐变小,最后消失。溶液变成红色。
实验结论:钠与水发生剧烈反应,生成碱性物质。
2Na+2H O = 2NaOH+H ↑ 2Na+2H O=2Na++2OH-+H ↑
2 2 2 2
实验4:必修一 人教版p35
实验分类:性质
实验目的:过氧化钠与水的反应
实验步骤:把水滴入盛有过氧化钠固体的试管中,立即把带火星的木条放在试管口,
检验生成的气体,用手轻轻一摸一摸试管外壁,然后向反应后的溶液中
滴入酚酞溶液,
实验现象:滴入水后有大量气泡产生,气体能使带有火星的木条复燃,试管外壁发热,向溶液里滴入酚酞溶液后,
溶液的颜色变红。
实验结论:2Na O +2H O=4NaOH+O ↑
2 2 2 2
3实验5:必修一 人教版p36
实验分类:性质
实验目的:碳酸钠与碳酸氢钠的性质
实验内容与步骤:
碳酸钠1g 碳酸氢钠1g
(1)观察碳酸钠和碳酸氢钠的外
白色粉末 白色晶体
观进行描述
(2)向两只试管中分别滴入几滴
水,振荡,观察现象;将温度计
结块变为晶体,伴随放热现象 溶解,伴随吸热现象
分别插入其中,温度计的示数有
何变化
(3)继续向(2)中加入5mL水,
固体全部溶解 固体部分溶解
用力振荡,有何现象
(4)分别向(3)中所得溶液滴
变红 变红(比碳酸钠略浅)
加1-2滴酚酞,有何现象
实验结论:
(1)相同温度下,碳酸钠的溶解度大于碳酸氢钠
(2)相同浓度下的碳酸钠溶液的碱性大于碳酸氢钠
(3)碳酸钠溶解放热,碳酸氢钠溶解吸热
实验6:必修一 鲁科版p34 人教版p36
实验分类:性质
实验目的:Na CO 和NaHCO 的热稳定性
2 3 3
实验装置:见右图
实验现象:碳酸氢钠受热分别,产生使澄清石灰水变浑浊的气体
实验结论:
现象 化学方程式 结论
Na CO 澄清的石灰水不变浑浊 无 受热不分解
2 3
NaHCO 3 澄清的石灰水变浑浊 2NaHCO 3 =Na 2 CO 3 +H 2 O+CO 2 ↑(加热) 受热易分解
实验7:必修一 鲁科版p34 人教版p38
实验分类:性质
实验目的:焰色反应
实验步骤:
1. 洗:将铂丝(或光洁无锈的铁丝)用盐酸洗净
2. 烧:在酒精灯外焰上灼烧至与原来的火焰颜色相同时
3. 蘸:蘸取待测液
4. 烧:在酒精灯外焰上灼烧,观察火焰的颜色。
实验现象:钠元素火焰颜色是黄色;钾元素火焰颜色是 紫色(透过蓝色钴玻璃观察)焰色反应为物理变化 。
4★实验8:必修一 鲁科版p84 人教版p68
实验分类:性质
实验目的:铁离子的检验
实验步骤:在2支试管里分别加入5mLFeCl 和5mLFeCl 溶液,各滴入几滴KSCN溶液,观察并描述发生的现象
2 3
实验现象与结论:
滴入KSCN溶液现象 离子方程式
FeCl 3 溶液 溶液变为血红色 Fe3++3SCN-=Fe(SCN) 3
FeCl 溶液 无明显现象 --------------------------------------
2
★实验9:必修一 鲁科版p83 人教版p68
实验分类:性质
实验目的:铁盐与亚铁盐的性质
实验1:在盛有2mLFeCl 溶液的试管中,加入少量铁粉,振荡试管,充分反应后中,滴入几滴KSCN溶液,观察
3
并记录实验现象,把上层清液倒入另一试管,再加入几滴氯水,
实验现象与结论:
现象 离子方程式
FeCl 溶液,加铁粉、KSCN 溶液由黄色变成浅绿色,加入KSCN溶液,不
3
2Fe3++Fe=3Fe2+
溶液 变色.
2Fe2++Cl =2Fe3++
加入氯水,溶液又变成黄色(可能看不到); 2
上层清液加氯水,振荡 2Cl-
由于试液中有KSCN溶液,最终成红色
Fe3++3SCN-=Fe(SCN)
3
实验2:在酸性高锰酸钾溶液中滴入少量硫酸亚铁溶液
实验现象与结论:紫色溶液褪色(变浅)5Fe2++MnO -+8H+=5Fe3++Mn2++4H O
4 2
实验3:探究实验
实验用品:硫酸亚铁溶液,氯化铁溶液,氢氧化钠溶液,酸性高锰酸钾溶液,氯水,硫氰化钾溶液,碘化钾溶液,
淀粉溶液,铁粉、铜片、锌片
物质 预测性质 选取试剂 实验现象 结论及离子方程式
硫酸亚铁
氯化铁
5实验10:必修一 鲁科版p85 人教版p66
实验分类:性质
实验目的:铁与水蒸气的反应
实验装置:见右图
实验现象:加热时试管内铁粉红热,导气管口有气泡冒出,
点燃肥皂泡可听到爆鸣声。
实验结论: 铁与水蒸气反应时会有氢气生成
高温
3Fe+4H O===Fe O +4H ↑
2 3 4 2
★实验11:必修一 鲁科版p88
实验分类:性质
实验目的:补铁剂中铁元素价态的检验
实验用品:某补铁口服液,硫酸溶液,氢氧化钠溶液,酸性高锰酸钾溶液,氯水,硫氰化钾溶液
实验方案设计及实施:
实验步骤 实验现象 实验结论
实验注意事项与反思:
实验12:必修一 鲁科版p95
实验分类:性质
实验目的:硫单质的性质
实验1:取少量硫粉放入试管中,观察颜色状态;在酒精灯上加热,观察发生的现象。
实验2:把研细的硫粉和铁粉按一定比例混合,放在石棉网上堆成条状或如下图形状,用灼热的玻璃棒触及一端,
当混合物呈红热状态时移开玻璃棒,观察现象。
实验3:取少量硫粉放入燃烧匙中,将燃烧匙放在酒精灯上加热至硫粉熔化,并燃烧后,迅速伸入盛满氧气的集气
瓶(底部有少量水),观察发生的现象。
实验现象和结论:
实验编号 实验现象 实验结论及方程式
1 硫为淡黄色晶体,加热后熔化 硫易熔化为液态
2 大量放热,生成黑色固体 Fe+S==FeS
3 集气瓶中有蓝紫色火焰 S+O ==SO
2 2
6★实验13:必修一 鲁科版p98 必修二 人教版p3
实验分类:性质
实验目的:二氧化硫的漂白性
实验步骤:将二氧化硫气体通入品红溶液,观察现象;然后加热试管,再次观察溶液中的变化
实验现象和结论:品红溶液褪色,加热后溶液恢复红色;二氧化硫有漂白性(可逆漂白)。
实验14:必修二 人教版p3
实验分类:性质
实验目的:二氧化硫的溶解性;二氧化硫与水反应
实验步骤:把充满二氧化硫,塞有橡胶塞的试管倒立在水中,在水面下打开橡胶塞,观察试管内
液面的情况;待液面高度不再明显变化时,在水下用橡胶塞塞紧试管口,取出试管,用pH试纸
测定试管中溶液的酸碱性
实验装置:
实验现象:试管内液面上升;pH试纸显红色;SO +H O=H SO
2 2 2 3
★实验15:必修一 鲁科版p98
实验分类:性质
实验目的:二氧化硫的氧化性
实验步骤:在试管中装有的氢硫酸溶液中通入二氧化硫气体,观察现象
实验现象和结论:试管内出现淡黄色浑浊;2H S+SO =3S+2H O
2 2 2
★实验16:必修一 鲁科版p99 必修二 人教版p5
实验分类:性质
实验目的:浓硫酸的氧化性
实验装置:
实验现象:铜表面变黑,形成棕黑色浊液,导管口有气泡产生,有刺激性气味气体产生,品红溶液逐渐褪色
实验结论及化学方程式:Cu+2H SO (浓)=CuSO +SO ↑+2H O
2 4 4 2 2
7★实验17:必修二 人教版p6
实验分类:性质
实验目的:硫酸根离子的检验
实验步骤:在三支试管中分别加入少量稀硫酸、硫酸钠溶液和碳酸钠溶液,然后各滴入几滴氯化钡溶液,观察现象;
再分别加入少量稀盐酸,振荡,观察现象
实验现象及结论:先用稀盐酸酸化,以排除碳酸根等可能造成的干扰,再加入氯化钡溶液来检验硫酸根离子的存在。
★实验18:必修一 鲁科版p99 必修二 人教版p4
实验分类:性质
实验目的:浓硫酸的脱水性和氧化性
实验步骤:在小烧杯中加入少量蔗糖,加入几滴水,再加入浓硫酸,边加边用玻璃棒搅拌,观察现象。
实验现象和结论:蔗糖变黑,体积膨胀,变成疏松多孔的海绵状的炭,并放出有刺激性气味的气体,体现了浓硫酸
的脱水性和强氧化性 。
化学方程式: C H O =12C+11H O C+2H SO (浓)=CO +2SO +2H O
12 22 11 2 2 4 2 2 2
★实验19:必修一 鲁科版p96
实验分类:性质
实验目的:不同价态硫元素之间的转化
实验用品:二氧化硫水溶液,亚硫酸钠溶液,浓硫酸,硫化钠溶液,稀硫酸,氢氧化钠溶液,酸性高锰酸钾溶液,
氯水,碘化钾溶液,淀粉溶液,品红溶液,铜片
实验方案设计及实施
预期转化 选取试剂 实验现象 结论及化学方程式
8★实验20:必修一,人教版p46
实验分类:性质
实验目的:氯气的性质
实验操作与现象 化学反应方程式
实验1 ①氯气是一种黄绿色气体,有刺激
氯气的物 性气味,密度比空气大。
理性质、 ②能溶于水,倒扣于水槽中,静置
氯水的制 一段时间后会有水倒吸进入试管
备 中,所得溶液呈现黄绿色。
③将氯水密闭放置一段时间后,氯
水的颜色会变浅。
实验2 干燥的氯气通入集气瓶 Cl +H O HCl+HClO
2 2
氯气与 ①干燥的红纸条不褪色 Cl 不具有漂白性,
2
漂白性 ②湿润的红纸条褪色 HClO具有漂白性。
用NaOH溶液吸收氯气的尾气。 Cl +2OH-=Cl-+ClO-
2
实验3 钠在氯气中燃烧
钠、铜、
铁分别在
氯气中燃
烧
铜在氯气中燃烧
铁在氯气中燃烧
钠熔化,黄色火焰, 产生大量棕红色的烟, 产生大量棕黄色的烟,
产生大量白烟,放热, 加水后,溶液呈黄色 加水后,溶液呈绿色
加水后,溶液无色
实验4 (1)在空气中点燃H ,然后把导管伸入盛满氯气的集
2
氢气与氯 气瓶中。现象:安静燃烧,苍白色火焰,瓶口有白雾,
气的反应 有刺激性气味气体生成。
(2)将氯气与氢气混合,光照。
现象:爆炸,瓶口有白雾。
反思:从以上实验可以看出氯气是一种助燃剂
9★实验21:必修一:人教版p46
实验分类:性质
实验目的:氯离子的检验
实验现象 解释或离子方程式
试剂 加入AgNO 加入稀硝酸后
3
稀盐酸 白色沉淀 沉淀不溶解 Cl-+Ag+=AgCl↓
NaCl溶液 白色沉淀 沉淀不溶解 Cl-+Ag+=AgCl↓
Na 2 CO 3 溶液 白色沉淀 沉淀溶解,放出气泡 2Ag++CO 3 2- =Ag 2 CO 3 ↓
自来水 白色沉淀(有些地区没有) 沉淀不溶解 Cl-+Ag+=AgCl↓
蒸馏水 无明显现象 无明显现象
思考:为什么滴加AgNO 溶液后还要再加稀硝酸呢?
3
★实验22:必修一:鲁科版p67
实验分类:性质
实验目的:探究物质“H O ”的氧化性或还原性
2 2
预测H O 的性质 实验操作 实验原理及实验现象
2 2
还原性(H 2 O 2 中氧元素的化合价为-1价, 将过氧 化氢溶液滴 入酸性 2MnO 4 -+5H 2 O 2 +6H+=
可被氧化,升价生成O 2 ) KMnO 4 ,溶液褪色。 2Mn2++5O 2 ↑+8H 2 O
氧化性(H 2 O 2 中氧元素的化合价为-1价, 向KI和淀粉的混合溶液中加入 2I-+H 2 O 2 +2H+=I 2 +2H 2 O
可被还原,降价生成H O) H O 溶液,溶液变为蓝色。
2 2 2
既有氧化性,又有还原性 向H O 溶液中加入催化剂
2 2
(H
2
O
2
中氧元素的化合价为-1价,可发 MnO
2
粉末,产生O
2
。 MnO2
生自身氧化还原反应,生成H O和O ) 2H 2 O 2 ===2H 2 O+O 2 ↑
2 2
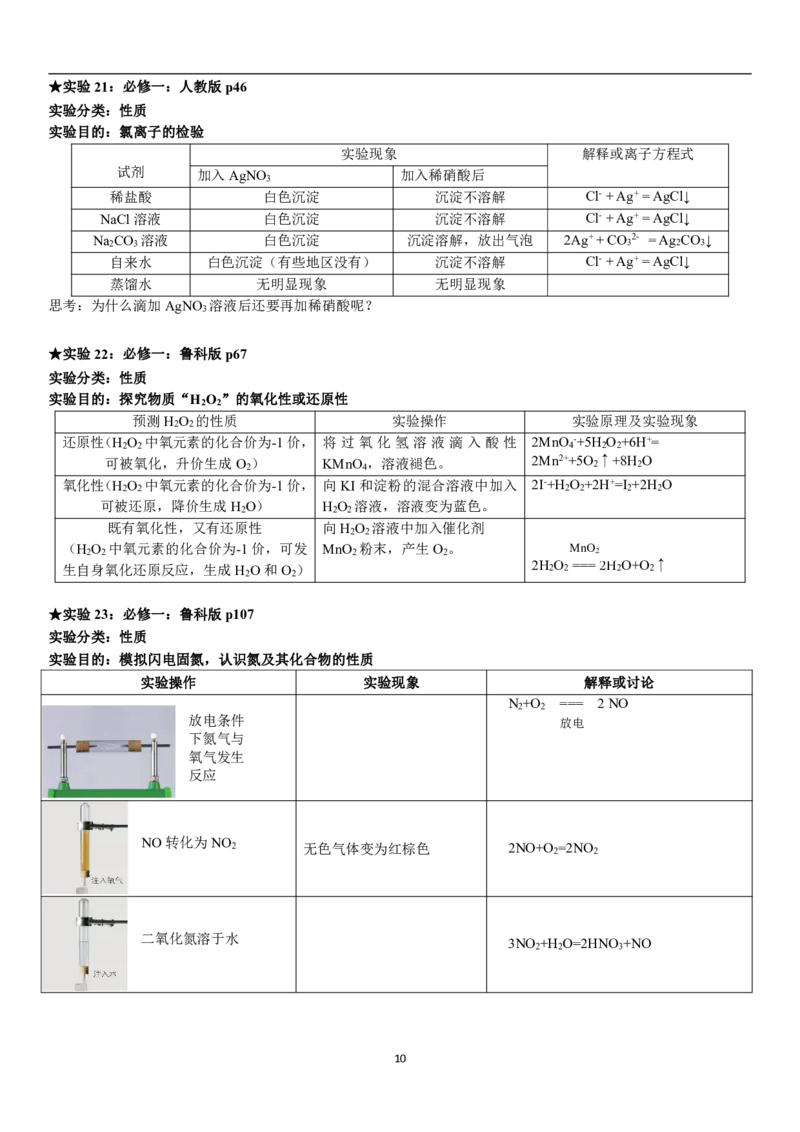
★实验23:必修一:鲁科版p107
实验分类:性质
实验目的:模拟闪电固氮,认识氮及其化合物的性质
实验操作 实验现象 解释或讨论
N +O === 2NO
2 2
放电条件 放电
下氮气与
氧气发生
反应
NO转化为NO
2 无色气体变为红棕色 2NO+O =2NO
2 2
二氧化氮溶于水
3NO +H O=2HNO +NO
2 2 3
10★实验24:必修一:鲁科版p111
实验分类:性质
实验目的:NH 的喷泉实验
3
实验操作 实验现象 解释或讨论
烧杯里的水由玻璃
氨气及易溶于水,且溶于水显碱性
管进入烧瓶,形成
H O+NH NH ·H O NH ++OH-
喷泉,烧瓶内液体 2 3 3 2 4
呈红色
轻轻挤压滴管,使少量水进入烧瓶,打开止水夹
★实验25:必修一:鲁科版113
实验分类:性质
实验目的:硝酸的性质——Cu与浓、稀硝酸
实验操作 实验现象 解释或讨论
取一瓶浓硝酸,打开瓶盖,小心地
有刺激性气味 HNO 具有挥发性
扇闻浓硝酸的气味。 3
在两个装置中各放入一小块铜片,
分别加入少量稀硝酸(4mol/L)和
浓硝酸(15mol/L)
稀硝酸:溶液变蓝,产生无色
气体,遇空气变为红棕色。 Cu+4HNO 3 (浓)=Cu(NO 3 ) 2 +2NO 2 ↑+2H 2 O
浓硝酸:溶液变为绿色,产生 3Cu+8HNO (稀)=3Cu(NO ) +2NO↑+4H O
3 3 2 2
红棕色气体。
稀硝酸:溶液变为黄色,产生
无色气体,遇空气变为红棕色。
将实验2中的铜片换成铁片进行相 Fe+4HNO 3 (稀)=Fe(NO 3 ) 3 +NO↑+2H 2 O
浓硝酸:铁片表面形成黑色固
同的实验,观察反应现象。 Fe遇浓硝酸发生钝化。
体,产生红棕色气体。片刻后
反应停止。
11★实验26:必修第二册:鲁科版P007、P020;人教版P094、P103(必修第一册)
实验分类:性质
实验目的:比较钾、钠、镁、铝元素原子的失电子能力
实验操作:切取绿豆大小的钠、钾,用滤纸吸干煤油;取表面积相同的镁条、铝条,用砂纸除去表面氧化膜。
实验装置:镊子、小刀、玻璃片、滤纸、铁圈、铁三角、坩埚、砂纸、表面皿,及常规仪器
实验操作 实验现象 解释或讨论
将干燥的坩埚加热,将钠钾迅速投
Na:燃烧,黄色火焰,得淡黄色固体 2Na+O =点燃=Na O
入到热坩埚中,金属熔化后撤掉酒 2 2 2
K:燃烧、紫色火焰,得固体 K不要求
精灯。
Na:浮、游、熔、响、红
取3个烧杯,分别放入等量混有酚 K:沉浮、游、火焰、响、红
2Na+2H O=2NaOH+H ↑
2 2
酞的水,投入钠、镁、钾,立即盖 Mg:室温下未见明显变化,加热后有 2K+2H O=2KOH+H ↑
2 2
上表面皿。 气体放出,反应一段时间后冷却至室 Mg+2H O=Mg(OH) +H ↑
2 2 2
温,溶液为红色。
向试管中加入2mL3mol/L盐酸, 均有无色气体生成,并放热。 Mg+2H+=Mg2++H ↑
2
将打磨后的镁条、铝条投入其中。 Mg产生气体的速率更快,放热更多。2Al+6H+=2Al3++3H
2
↑
向试管中加入2mL1mol/LAlCl 溶
3
液,滴加氨水至不再产生沉淀。静
AlCl :向沉淀中滴加盐酸或NaOH溶 Al3++3NH 3 ·H 2 O=Al(OH) 3 ↓+3NH 4 +
置后将沉淀平分至两支试管。分别 3 Al(OH) +3H+=Al3++3H O
液,沉淀均溶解。 3 2
滴加 2 mol/L 盐酸、2 mol/LNaOH Al(OH) +OH−=AlO −+2H O
MgCl :沉淀可溶于盐酸,不能溶解于 3 2 2
溶液,同时振荡。 2 Mg2++2NH ·H O=Mg(OH) ↓+2NH +
3 2 2 4
将 AlCl 溶液更换为 2 mL 1 mol/L
NaOH溶液。
Mg(OH) 2 +2H+=Mg2++2H 2 O
3
MgCl 溶液,重复上述实验。
2
鲁科版教材实验在此处希望比较Mg(OH) 、Al(OH) 的碱性。但两种饱和溶液的c(OH−)取决于K ,即受限于溶解过
2 3 sp
程(晶格能、水合能),不能直观反映简单氢氧化物的电离能力。
若想分析两种氢氧化物的碱式电离能力,可通过对比同浓度Mg2+、Al3+的水解能力来间接实现。详见水解部分。
实验结论:
1.根据金属与酸、水置换出H 的难易程度判断,失电子能力:K>Na>Mg>Al。
2
2.Mg(OH) 是碱,Al(OH) 是两性氢氧化物。
2 3
12★实验27:必修第二册:鲁科版P023;人教版P098、P115(必修第一册)
实验分类:性质
实验目的:卤族元素性质的相似性和递变性
实验操作 实验现象 解释或讨论
分别向盛有4mLKBr 溶液和4mL 滴加氯水后,分别呈橙红色、黄色、 Cl +2Br−=2Cl−+Br
2 2
KI溶液、4mL水的三支试管中加入 浅黄绿色。 Cl
2
+2I−=2Cl−+I
2
1mL氯水。对比颜色。 加入CCl
4
并静置后均分层,上层均无 Cl
2
、Br
2
、I
2
均为非极性分子,在水中溶
分别向三支试管中加入1mLCCl
4
,色,下层分别呈红色、紫色、浅黄绿 解度差,颜色亦发生变化;易溶于CCl
4
,
振荡,静置。 色。 颜色呈自身单质颜色。
分别向盛有4mLKI溶液、4mL水
滴加溴水后分别呈黄色、橙红色。 Br +2I−=2Br−+I
的两支试管中加入1mL溴水。对比 2 2
加入溴水后,第一支溶液变蓝,第二 淀粉与I 相遇,可呈特征蓝色;淀粉与
颜色。 2
支试管无明显变化。 Br 不显色。
分别向两支试管中加入淀粉溶液。 2
实验结论:
1.氯溴碘的单质均具有氧化性,顺序为氧化性:Cl >Br >I
2 2 2
.非金属性:Cl>Br>I
2
13实验28:必修第二册,鲁科版 – 无,人教版P064
实验分类:性质
实验目的:甲烷与氯气反应
实验装置:水槽、试管、铝箔
实验操作 实验现象 解释或讨论
取两支试管,均通过排饱和 NaCl
静置足够长时间后,用铝箔包套上的
溶液的方法收集半试管CH 和半试
4 试管无明显变化;放在光亮处的试管
管Cl ,分别用铁架台固定好。将其 CH 与Cl 在光照条件下发生反应。
2 内,气体颜色变浅,液面上升,试管 4 2
中一支试管用铝箔套上,另一支试
内壁出现油状液滴。
管放在光亮处。静置。
实验结论:
CH 与Cl 在光照下生成HCl和CH 的氯代物。
4 2 4
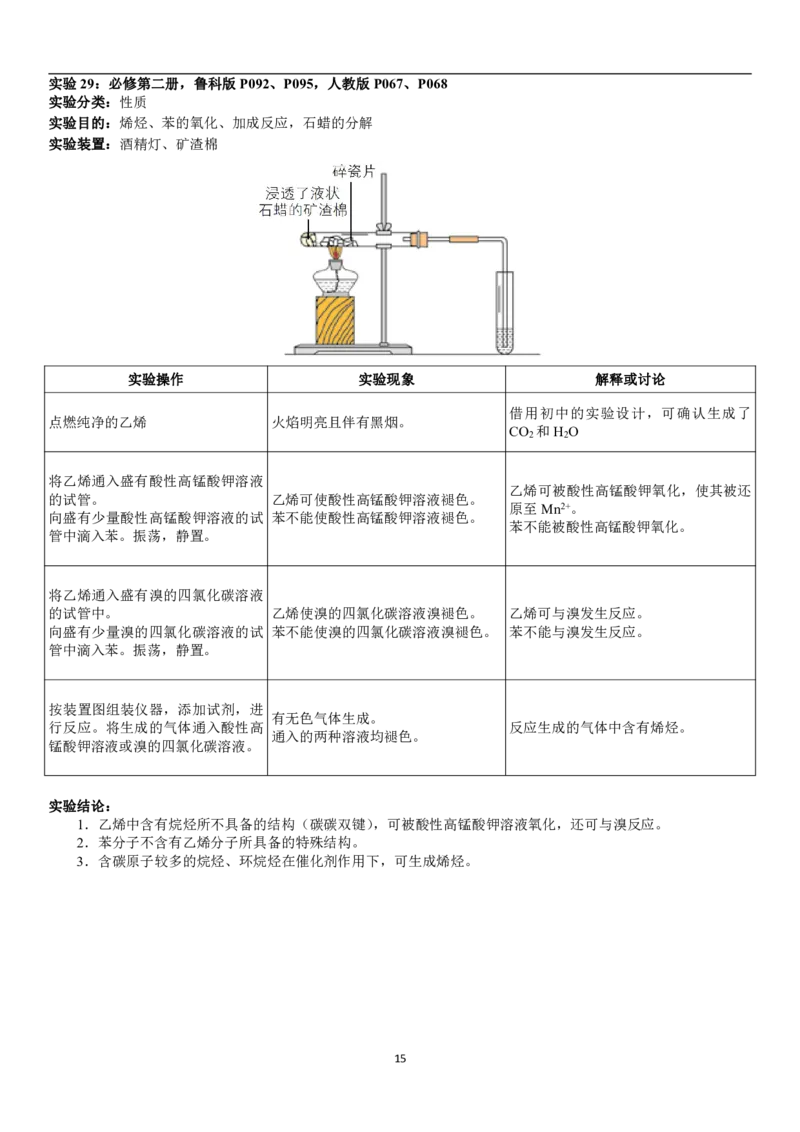
14实验29:必修第二册,鲁科版P092、P095,人教版P067、P068
实验分类:性质
实验目的:烯烃、苯的氧化、加成反应,石蜡的分解
实验装置:酒精灯、矿渣棉
实验操作 实验现象 解释或讨论
借用初中的实验设计,可确认生成了
点燃纯净的乙烯 火焰明亮且伴有黑烟。
CO 和H O
2 2
将乙烯通入盛有酸性高锰酸钾溶液
乙烯可被酸性高锰酸钾氧化,使其被还
的试管。 乙烯可使酸性高锰酸钾溶液褪色。
原至Mn2+。
向盛有少量酸性高锰酸钾溶液的试 苯不能使酸性高锰酸钾溶液褪色。
苯不能被酸性高锰酸钾氧化。
管中滴入苯。振荡,静置。
将乙烯通入盛有溴的四氯化碳溶液
的试管中。 乙烯使溴的四氯化碳溶液溴褪色。 乙烯可与溴发生反应。
向盛有少量溴的四氯化碳溶液的试 苯不能使溴的四氯化碳溶液溴褪色。 苯不能与溴发生反应。
管中滴入苯。振荡,静置。
按装置图组装仪器,添加试剂,进
有无色气体生成。
行反应。将生成的气体通入酸性高 反应生成的气体中含有烯烃。
通入的两种溶液均褪色。
锰酸钾溶液或溴的四氯化碳溶液。
实验结论:
1.乙烯中含有烷烃所不具备的结构(碳碳双键),可被酸性高锰酸钾溶液氧化,还可与溴反应。
2.苯分子不含有乙烯分子所具备的特殊结构。
3.含碳原子较多的烷烃、环烷烃在催化剂作用下,可生成烯烃。
15实验30:必修第二册,鲁科版P104、P107,人教版P077、P078、P080
实验分类:性质
实验目的:乙醇、乙酸的化学性质
实验装置:
实验操作 实验现象 解释或讨论
向烧杯中加入约2mL无水乙醇,点 出现蓝色的火焰,没有黑烟。
燃。 放大量的热。
向试管中加入约2mL无水乙醇,取
铜丝被加热时,表面变黑。伸入乙醇
一根光洁的铜丝绕成螺旋状,置于 CH CH OH 在 Cu 催化下被 O 氧化为
后,铜丝表面复原,变为红色。乙醇 3 2 2
酒精灯外焰上加热,然后伸入无水 CH CHO
中有刺激性气体生成。 3
乙醇中,反复几次。
向试管中加入约 2 mL 酸性高锰酸
酸性高锰酸钾溶液褪为无色。 乙醇可被酸性高锰酸钾溶液氧化。
钾溶液,滴入数滴无水乙醇。
向试管中加入约2mL无水乙醇,再
钠沉于乙醇底部,有无色气体生成。 2CH CH OH+Na=2CH CH ONa+H ↑
放入一小块金属钠。 3 2 3 2 2
分别向盛有 2 mL 冰醋酸的试管中
加入碳酸钙、锌粒、饱和碳酸钠溶
现象略。 乙酸具有酸性。不具有碱性。
液、NaOH 溶液、酚酞溶液、石蕊
溶液。
在试管中加入无水乙醇、浓硫酸、
冰醋酸的混合物,再加入2~3块碎
瓷片。按装置图连接装置。用酒精
有无色油状液体生成,具有香味。
灯小心均匀地加热试管。将产生的
气体经导管通到饱和碳酸钠溶液的
液面上。
实验结论:
1.乙醇具有还原性;可与Na反应。
2.乙酸具有酸性。
3.乙酸与乙醇在浓硫酸催化下可生成具有香味的乙酸乙酯。
16实验31:有机化学基础,鲁科版P29,人教版P35-36
实验分类:性质
实验目的:乙炔的性质
实验装置:
实验操作 实验现象 解释或讨论
(1)在圆底烧瓶中放入
几小块电石,打开分液漏
斗的活塞,逐滴加入适量 电石与水剧烈反应,产生大量气泡 CaC +2H O=Ca(OH) +HC≡CH↑
2 2 2
饱和氯化钠溶液,将产生 硫酸铜溶液中产生黑色浑浊 Cu2++H S=CuS↓+2H+
2
的气体通入硫酸铜溶液,
得到纯净的乙炔
(2)将纯净的乙炔通入
盛有酸性高锰酸钾溶液 溶液紫红色褪去 碳碳三键可被酸性高锰酸钾氧化
的试管中
(3)将纯净的乙炔通入
盛有溴的四氯化碳溶液 溶液橙红色褪去 碳碳三键可与Br 发生加成反应
2
的试管中
乙炔碳含量高,易燃烧不充分产生黑烟
(4)点燃纯净的乙炔 明亮的火焰,有浓烟
(碳的颗粒)
实验结论:___碳碳三键可发生氧化反应和加成反应____________________________________________________
注意事项或反思:
1. 饱和食盐水的作用
降低电石与水的反应速率,使反应安全可控
2. 硫酸铜溶液的作用
吸收乙炔气体中的H S等杂质,防止其干扰乙炔与高锰酸钾、溴的反应
2
17实验32:有机化学基础,鲁科版P33,人教版P44
实验分类:性质
实验目的:苯及其同系物的性质
实验操作 实验现象 解释或讨论
(1)向两支分别盛
有2mL苯和甲苯 有机物与溴水分层,苯与甲苯在上层,无色,溴 苯或甲苯与水不互溶,苯或甲苯密度小于
的试管中各加入几 水在下层,呈黄色 水
滴溴水,静置
(2)将上述试管用 混合液静置后分层,苯与甲苯在上层,呈橙色, 溴在苯或甲苯中的溶解度远大于在水中
力振荡,静置 水在下层,近无色 的溶解度,发生萃取
(3)向两支分别盛
有2mL苯和甲苯
有机物与水溶液分层,苯与甲苯在上层,无色, 苯或甲苯与水不互溶,苯或甲苯密度小于
的试管中各加入几
高锰酸钾溶液在下层,呈紫色 水
滴酸性高锰酸钾溶
液,静置
高锰酸钾在水中溶解度远大于在苯或甲
混合液静置后分层,苯与甲苯在上层,无色。盛
(4)将上述试管用 苯中的溶解度,不会发生萃取;
有苯的试管中下层水溶液仍为紫色,盛有甲苯的
力振荡,静置 苯不与酸性高锰酸钾反应,但甲苯可被酸
试管中下层水溶液褪为无色
性高锰酸钾氧化。
实验结论:______苯与甲苯均不与溴水反应,但可萃取溴;苯不被酸性高锰酸钾氧化,但甲苯可以____________
注意事项或反思:
1. 苯和甲苯在什么条件下可与Br 反应?
2
液溴+FeBr 催化
3
2. 甲苯被酸性高锰酸钾氧化的产物是什么?
苯甲酸
18★实验33:有机化学基础,鲁科版P55,人教版P53-54
实验分类:性质
实验目的:卤代烃的取代反应与消去反应
实验装置:
实验操作 实验现象 解释或讨论
(1)取一支试管,滴入
1-溴丁烷不溶于水且密度大于水;
10-15滴1-溴丁烷,再加 1-溴丁烷与水溶液分层,加热后
在碱性水溶液中加热可发生取代反应:
入1mL5%NaOH溶 有机层略变薄
液,振荡后加热,静置。
(2)待溶液分层后,用
胶头滴管小心吸取少量
上层水溶液,移入另一 1-溴丁烷水解同时生成Br-溶于水溶液中,并与Ag+形
滴入硝酸银后产生淡黄色沉淀
支盛有1mL2mol/L稀 成淡黄色的AgBr沉淀
硝酸的试管中,然后加
入2滴2%AgNO 溶液
3
(3)向圆底烧瓶中加入
2.0gNaOH和15mL无
1-溴丁烷在NaOH的乙醇溶液中可发生消去反应,产
水乙醇,搅拌。再向其 导管口不断有气泡冒出
生1-丁烯
中加入5mL1-溴丁烷和
几片碎瓷片,微热。
(4)将产生的气体通入
盛水的试管后,再通入 高锰酸钾的紫色褪去 烯烃可被酸性高锰酸钾氧化使其褪色
酸性高锰酸钾溶液中
实验结论:____卤代烃在NaOH水溶液中加热发生取代反应,在NaOH水溶液中加热发生消去反应___________
注意事项或反思:
1. 取代反应中,为什么要将溶液移入稀硝酸中
取代反应在NaOH溶液中进行,碱性环境下AgNO 会与OH-反应,干扰Br-的检验
3
2. 消去反应中,为什么要将产生的气体通入水中。除了高锰酸钾溶液,还可以方法检验丁烯,此时是否还有必
要将气体通入水中
消去反应产生的气体中会有挥发的乙醇,会干扰产物1-丁烯与高锰酸钾反应,利用乙醇与水混溶的特点可用
水将乙醇吸收除去;
还可以将气体通入溴水检验1-丁烯,由于乙醇不与溴水反应,所以可以不需要将气体通入水中。
19实验34:有机化学基础,鲁科版P66-68,人教版P62
实验分类:性质
实验目的:苯酚的化学性质
实验操作 实验现象 解释或讨论
(1)向两支盛有0.3g苯酚
晶体的试管中加入2mL蒸
固体变少,但未完全溶解 苯酚在室温下的溶解度不太大
馏水,振荡试管,分别记为
试管a、试管b
苯酚具有弱酸性,可与强碱反应生成可盐:
(2)向试管a中逐滴加入
加NaOH后,苯酚晶体完全溶解;
5%NaOH溶液并振荡试
再加盐酸后,出现白色浑浊 苯酚钠又可与强酸反应生成苯酚:
管,后再向其中加入稀盐酸
苯酚的酸性弱于碳酸,但强于HCO -:
3
(3)向试管b中逐滴加入
加Na CO 后,苯酚晶体完全溶解;
Na CO 溶液并振荡试管, 2 3
2 3 再通入CO 后,出现白色浑浊
后再向其中通入CO 气体 2
2
(4)另取两支试管,分别
加入0.1g 苯酚和3mL水,
—————————————— ————————————
振荡,得到苯酚稀溶液,分
别记为试管c、试管d。
(5)向试管c中逐滴加入
饱和溴水,边加边振荡,观 溶液中产生白色浑浊
察现象
白色
(6)向试管d中滴入几滴
FeCl 溶液,振荡,观察实 溶液由无色变为紫色 酚羟基可与Fe3+配位,生成紫色物质
3
验现象。
实验结论:___苯酚是一种弱酸,酸性弱于碳酸、强于碳酸氢根;苯酚易与溴水发生取代反应生成三溴苯酚,可与
Fe3+配位而显紫色____
注意事项或反思:
1. 注意苯酚与碳酸钠、苯酚钠与碳酸氢钠反应的产物
2. 苯酚的溴代与苯的溴代相比有何特点?
反应条件:苯酚溴代反应只需要溴水且不需催化剂
溴代数目:苯酚一次可以发生三溴代反应
溴代位置:苯酚的溴代只发生在酚羟基的邻位和对位
3. 酚的溴代反应和与Fe3+的显色反应均可用于酚类物质的检验
20★实验35:有机化学基础,鲁科版P77,人教版P67
实验分类:性质
实验目的:醛的氧化
实验操作 实验现象 解释或讨论
(1)在洁净的试管
中加入1mL2%
AgNO 溶液,然后边
3 硝酸银溶液中先产生白色沉淀,后沉淀溶 Ag++NH •H O=AgOH↓+NH +
振荡试管边逐滴滴 3 2 4
解,得到无色溶液 AgOH+2NH •H O=Ag(NH ) ++OH-+2H O
入2%氨水,使最初 3 2 3 2 2
产生的沉淀恰好溶
解,制得银氨溶液
(2)再滴入3滴乙
醛,振荡后将试管放
试管壁附着一层银镜 CH 3 CHO+2Ag(NH 3 ) 2 OH
在60~70oC热水浴
CH COONH +2Ag↓+3NH +H O
3 4 3 2
中温热。观察现象
(3)在试管里加入2
mL10%NaOH溶液,
加入5滴5%CuSO
4
溶液中产生蓝色沉淀 Cu2++2OH-=Cu(OH)
2
↓
溶液,得到新制的
Cu(OH)
2
(4)加入0.5mL乙
蓝色沉淀逐渐变为砖红色沉淀 CH 3 CHO+2Cu(OH) 2 +NaOH
醛溶液,加热 CH COONa+Cu O↓+3H O
3 2 2
实验结论:____醛基具有较强的还原性,可以被银氨溶液、新制氢氧化铜等弱氧化剂氧化_____________
注意事项或反思:
1. 配制银氨溶液时加入的氨水要适量,注意滴加顺序。
2. 配制银氨溶液时,中间产生的白色沉淀会变灰甚至变黑,是由于AgOH不稳定,易分解为黑色的Ag O,但
2
Ag O亦可溶于氨水,不影响银氨溶液的制备。
2
3. 实验后可以用硝酸来清洗试管内的银镜。
4. 配制新制氢氧化铜时,CuSO 溶液的质量分数不宜过大,且NaOH溶液应过量,Cu(OH)2只有在强碱性环境
4
下才具有足够的氧化性。
21实验36:有机化学基础,鲁科版P79,人教版P101、P104、P106
实验分类:性质
实验目的:糖类的性质
实验操作 实验现象 解释或讨论
(1)在一支洁净的试管中
配制约2mL银氨溶液,加
试管壁附着一层银镜 葡萄糖可被银氨溶液氧化,发生银镜反应
入1mL10%葡萄糖溶液,
平稳地放在水浴中加热。
(2)在一支洁净的试管中
加入2mL10%NaOH溶
液,加入5滴5%CuSO 溶 试管中产生砖红色沉淀 葡萄糖可被新制氢氧化铜氧化
4
液,再加入2mL10%葡萄
糖溶液,加热
(3)取两支试管,分别加
入1mL 蔗糖溶液,向一份
中加入2~3滴稀硫酸,水浴 蔗糖是非还原糖;
未加硫酸的试管中未产生砖红色沉淀;
加热几分钟,再加入NaOH 蔗糖在酸性条件下可水解,产生还原糖
加硫酸并加热的试管中产生砖红色沉淀
溶液调节至碱性;向两支试 ——葡萄糖和果糖,
管中分别加入新制氢氧化
铜悬浊液,加热
(4)取两支试管,分别加
入1mL 淀粉溶液,向一份
中加入2~3滴稀硫酸,水浴 未加硫酸的试管加碘水后出现较深的蓝
加热几分钟,取出试管冷却 色,加新制氢氧化铜并加热后未产生砖红
至室温;从两支试管中分别 色沉淀; 淀粉是非还原糖;
取出少量溶液,滴加碘水, 加硫酸并加热的试管中加碘水后出现较浅 淀粉在酸性条件下可水解,产生葡萄糖
观察现象;将两支试管中的 的蓝色,加新制氢氧化铜并加热后产生了
溶液分别用NaOH溶液调 砖红色沉淀
至碱性,加入新制氢氧化铜
悬浊液,加热
(5)在试管中放入少量脱
脂棉,加入几滴蒸馏水和几
滴浓硫酸,用玻璃棒将混合
物搅拌成糊状,小火微热, 纤维素在酸性条件下可发生水解(比淀粉
试管中产生砖红色沉淀
得到亮棕色溶液。加入过量 水解困难),产生葡萄糖
NaOH溶液中和至碱性,再
滴入3滴5%CuSO 溶液,
4
加热
实验结论:___葡萄糖是还原糖,可产生银镜反应,可被新制氢氧化铜氧化;蔗糖、淀粉
、纤维素都是非还原糖,但都可在酸性条件下水解产生还原糖______________________________________
注意事项或反思:
1. 蔗糖、淀粉、纤维素都是在酸性条件下水解,与新制氢氧化铜反应时必须先用NaOH将溶液调至碱性。
2. 淀粉与碘的显色需在室温下进行,因此淀粉溶液加碘水前必须先冷却。
3. 思考如何判断淀粉是否发生水解以及是否完全水解。
22实验37:有机化学基础,人教版P112-113
实验分类:性质
实验目的:蛋白质的性质
实验操作 实验现象 解释或讨论
(1)在试管中加入2mL
饱和(NH ) SO 溶液,向
4 2 4 鸡蛋清溶液中产生一些白色沉淀 蛋白质溶液在一些浓盐溶液中发生盐析
其中加入几滴鸡蛋清溶
液,振荡,观察现象。
(2)再继续加入蒸馏水, 盐析是可逆的,溶液盐浓度降低后可重新
白色沉淀加水后又溶解
振荡,观察现象 溶解,蛋白质的生物活性也能恢复
(3)在三支试管中各加
入2mL鸡蛋清溶液,将
加热、重金属离子、有机物等能使蛋白质
一支试管加热,向另两支 三支试管中均产生白色沉淀
发生变性
试管中分别加入硝酸银
溶液和乙醇,观察现象
(4)再向试管中加入蒸
变性是不可逆的,加水不能使变性后的蛋
馏水,观察产生的沉淀能 三支试管的白色沉淀加水后不能溶解
白质重新溶解,生物活性也不能恢复
否溶解
(5)向盛有2mL鸡蛋清 强酸会使蛋白质变性而产生沉淀;
加硝酸后产生白色沉淀,加热后变为沉淀变
溶液的试管中加入5滴浓 硝酸可与蛋白质中一些含苯环的氨基酸
为黄色
硝酸,加热 反应,使蛋白质变为黄色
注意事项或反思:
1. 盐析是可逆的,可用于蛋白质的分离提纯。
2. 想想生活中哪些地方利用了蛋白质的变性?
3. 蛋白质与硝酸反应可变黄,称为蛋白质的“颜色反应”,可用于蛋白质的检验。
23实验设计/实验探究:
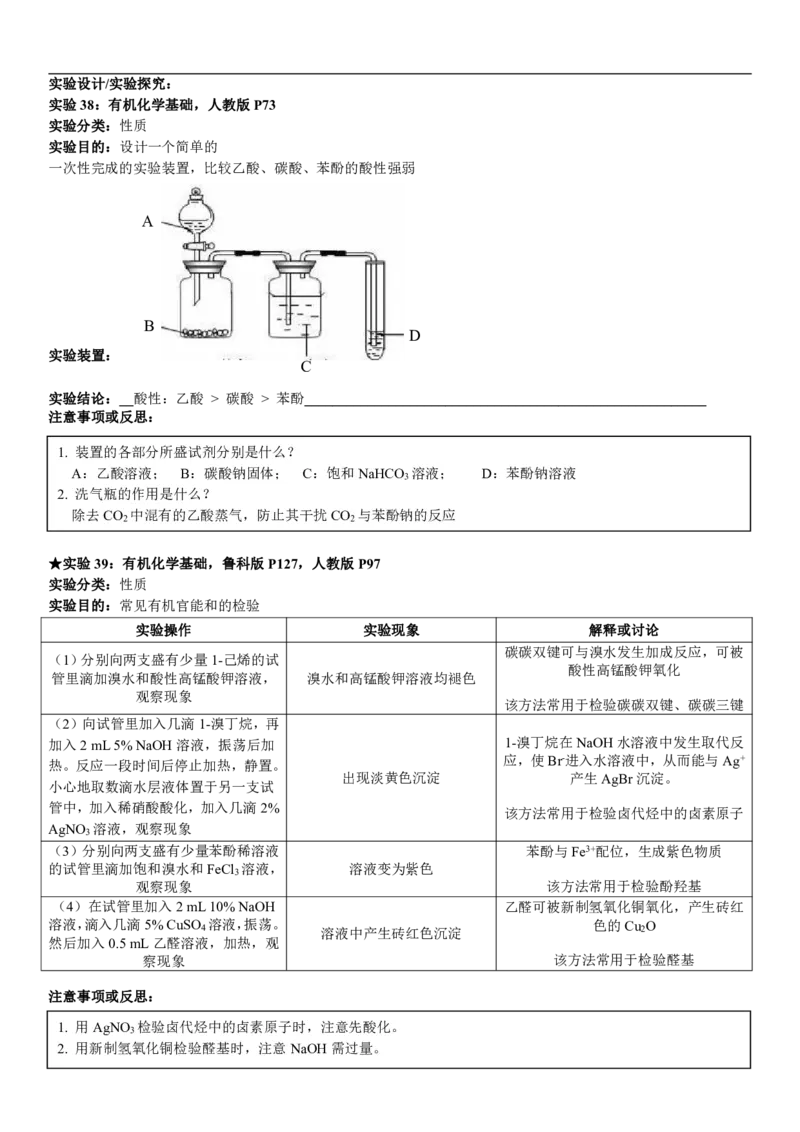
实验38:有机化学基础,人教版P73
实验分类:性质
实验目的:设计一个简单的
一次性完成的实验装置,比较乙酸、碳酸、苯酚的酸性强弱
A
B
D
实验装置:
C
实验结论:__酸性:乙酸 > 碳酸 > 苯酚_________________________________________________________
注意事项或反思:
1. 装置的各部分所盛试剂分别是什么?
A:乙酸溶液; B:碳酸钠固体; C:饱和NaHCO 溶液; D:苯酚钠溶液
3
2. 洗气瓶的作用是什么?
除去CO 中混有的乙酸蒸气,防止其干扰CO 与苯酚钠的反应
2 2
★实验39:有机化学基础,鲁科版P127,人教版P97
实验分类:性质
实验目的:常见有机官能和的检验
实验操作 实验现象 解释或讨论
碳碳双键可与溴水发生加成反应,可被
(1)分别向两支盛有少量1-己烯的试
酸性高锰酸钾氧化
管里滴加溴水和酸性高锰酸钾溶液, 溴水和高锰酸钾溶液均褪色
观察现象
该方法常用于检验碳碳双键、碳碳三键
(2)向试管里加入几滴1-溴丁烷,再
加入2mL5%NaOH溶液,振荡后加 1-溴丁烷在NaOH水溶液中发生取代反
热。反应一段时间后停止加热,静置。
应,使Br-进入水溶液中,从而能与Ag+
出现淡黄色沉淀 产生AgBr沉淀。
小心地取数滴水层液体置于另一支试
管中,加入稀硝酸酸化,加入几滴2%
该方法常用于检验卤代烃中的卤素原子
AgNO 溶液,观察现象
3
(3)分别向两支盛有少量苯酚稀溶液 苯酚与Fe3+配位,生成紫色物质
的试管里滴加饱和溴水和FeCl 溶液, 溶液变为紫色
3
观察现象 该方法常用于检验酚羟基
(4)在试管里加入2mL10%NaOH 乙醛可被新制氢氧化铜氧化,产生砖红
溶液,滴入几滴5%CuSO 4 溶液,振荡。 溶液中产生砖红色沉淀 色的Cu 2 O
然后加入0.5mL乙醛溶液,加热,观
察现象 该方法常用于检验醛基
注意事项或反思:
1. 用AgNO 检验卤代烃中的卤素原子时,注意先酸化。
3
2. 用新制氢氧化铜检验醛基时,注意NaOH需过量。
24★实验40:有机化学基础,鲁科版P128,人教版P98
实验分类:性质
实验目的:利用化学方法检测阿司匹林的官能团
实验操作 实验现象 解释或讨论
(1)将一片阿司匹林
(C H O )研碎后放入适量水 ——————————— ———————————
9 8 4
中,振荡后静置,取用上清液
(2)取少量清液滴入几滴
溶液未变为紫色 阿司匹林中无酚羟基
FeCl 溶液,振荡,观察现象
3
(3)取少量清液滴入2滴石
滴入石蕊后溶液变红 阿司匹林溶液呈酸性,可能有羧基
蕊溶液,观察现象
(4)取少量清液加入2mL
NaOH和几滴CuSO 溶液,加 未出现砖红色沉淀 阿司匹林中无醛基
4
热,观察现象
(5)向另一支试管中滴入2
滴稀硫酸,加热后滴入几滴 阿司匹林酸性条件下可发生水解,且水解
NaHCO 溶液将pH调至弱酸 加FeCl 后溶液变为紫色 产物含有酚羟基
3 3
性。再向其中滴入几滴FeCl 阿司匹林可能含酚酯结构
3
溶液,振荡,观察现象
实验结论:___阿司匹林中无醛基、无酚羟基,可能含有羧基和酚酯结构_______________________________
注意事项或反思:
1. 阿司匹林在稀硫酸中水解后,溶液酸性太强会干扰Fe3+的显色反应,故使用少量NaHCO 调节溶液的pH。
3
2. 综合阿司匹林的分子式和官能团检测结果,推断其可能的结构
苯环上分别连接有羧基和乙酰氧基(CH COO–),它们可能处于邻、间、对三种相对位置,最终结构可通过
3
1HNMR等方法确定。
25高三实验板块复习——制备专题
★实验1:必修一 鲁科版p87 人教版p67
实验分类:制备
实验目的:氢氧化铁与氢氧化亚铁的制备
实验步骤:在2支试管里分别加入少量FeCl 和FeSO 溶液,然后滴入NaOH溶液,观察并描述发生的现象
3 4
实验现象与结论:
FeCl 溶液 FeSO 溶液
3 4
溶液由浅绿色变为无色,产生白色絮状沉淀,迅速变为
滴入NaOH 有红褐色沉淀生成
灰绿色,最终变为红褐色.
离子方程式或 FeSO +2NaOH=Fe(OH) ↓+Na SO
4 2 2 4
FeCl +3NaOH=Fe(OH) ↓+3NaCl
化学方程式 3 3 4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 3
★实验2:必修一,人教版p8
实验分类:制备
实验目的:1、氢氧化铁胶体的制备和性质实验
实验操作 实验现象 解释或讨论
向沸水中逐滴滴加5-6滴饱
.
和 . 氯化铁溶液,继续煮沸至溶液 所得胶体应透明、呈红 FeCl 3 +3H 2 O(沸水)=
呈红褐色,停止加热。 褐色。 Fe(OH) (胶体)+3HCl
3
光亮的“通路”是由于胶体
把盛有CuSO 溶液和Fe(OH) 胶体的烧杯置于暗处,分
4 3 前者没有光亮的通路, 粒子对光散射形成的,叫做
别用红色激光笔照射烧杯中的液体,在与光束垂直的方向进
后者形成光亮的通路。 丁达尔效应。可用来区分胶
行观察。
体和溶液。
注意事项:
①烧杯里蒸馏水煮沸后,滴加FeCl 溶液要不断振荡,但不宜用玻璃棒搅拌,也不宜使液体沸腾时间过长,以免生
3
成沉淀。
②观察丁达尔效应方法:用激光灯照射烧杯中的液体,在与光束垂直的方向进行观察。制胶体、做丁达尔效应的实
验时,所用的FeCl 溶液要饱和但不能浑浊。
3
实验目的:2、电泳
胶体的分散质具有巨大的比表面积,能吸附带有某种电荷的离子,从
而形成带电微粒。有些胶体的分散质微粒吸附带有正电荷的离子,有些则
吸附带有负电荷的离子。这些带电微粒在外电场的作用下会发生定向移动。
例如,氢氧化铁胶体的分散质微粒带有正电荷,在通电的情况下会向与直
流电源负极相连的一极移动,这种现象称为电泳。电泳具有很高的实用价
值,如电泳电镀就是利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀
件上的。
26实验目的:3、聚沉
把酸、碱、盐等物质加入胶体中时,它们溶解产生的阳离子或阴离子所带电荷与胶
体的分散质微粒所带电荷中和,会使胶体的分散质微粒聚集成较大的微粒,在重力作用
下沉淀出来。这种胶体形成沉淀析出的现象称为聚沉。加热或搅拌也可能引起胶体的聚
沉。胶体的聚沉在生产和生活中有着重要的应用,如向豆浆(一种胶体)中加入硫酸钙
使蛋白质等聚沉可制成可口的豆腐。
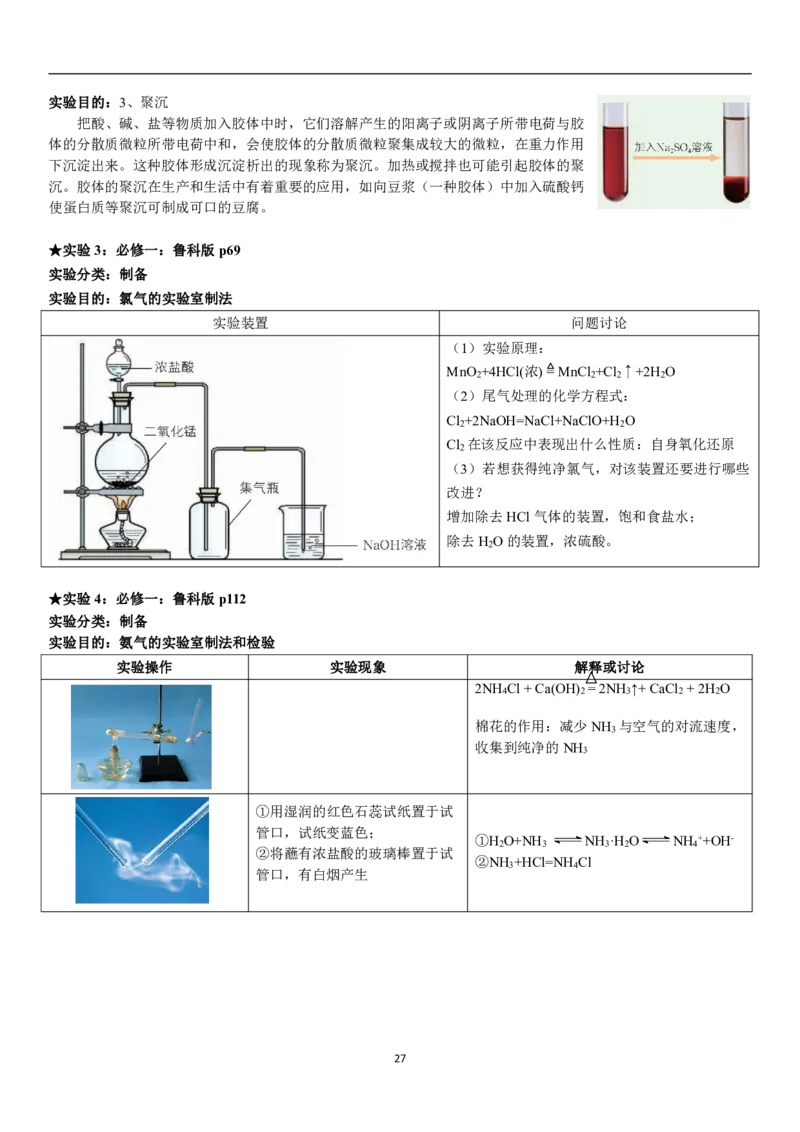
★实验3:必修一:鲁科版p69
实验分类:制备
实验目的:氯气的实验室制法
实验装置 问题讨论
(1)实验原理:
MnO +4HCl(浓)=MnCl +Cl ↑+2H O
2 2 2 2
(2)尾气处理的化学方程式:
Cl +2NaOH=NaCl+NaClO+H O
2 2
Cl 在该反应中表现出什么性质:自身氧化还原
2
(3)若想获得纯净氯气,对该装置还要进行哪些
改进?
增加除去HCl气体的装置,饱和食盐水;
除去H O的装置,浓硫酸。
2
★实验4:必修一:鲁科版p112
实验分类:制备
实验目的:氨气的实验室制法和检验
实验操作 实验现象 解释或讨论
2NH Cl+Ca(OH) =2NH ↑+CaCl +2H O
4 2 3 2 2
棉花的作用:减少NH 与空气的对流速度,
3
收集到纯净的NH
3
①用湿润的红色石蕊试纸置于试
管口,试纸变蓝色;
①H O+NH NH ·H O NH ++OH-
2 3 3 2 4
②将蘸有浓盐酸的玻璃棒置于试
②NH +HCl=NH Cl
3 4
管口,有白烟产生
27★实验5:必修第二册:鲁科版P030;人教版 − 无(P106,必修第二册)。
实验分类:制备
实验目的:海带提碘
实验装置:分液漏斗,及常规仪器
实验操作 实验现象 解释或讨论
1.取一定量干海带于坩埚中,充分
将海带中的有机物灼烧除去,
灼烧。灼烧后,待坩埚冷却至室温
碘元素以碘化物形式存在于海带灰中,
后,向坩埚中加入适量蒸馏水,搅
被水浸出。
拌。将所得混合物过滤,取滤液。
2.将滤液用稀硫酸酸化,加入适量
H O +2H++2I−=I +2H O
30%H O 溶液。充分反应后,煮沸,溶液变为黄色。 2 2 2 2
2 2 2H O =Δ=2H O+O ↑
除去过量的H O 。 2 2 2 2
2 2
3.将上一步所得溶液转移至分液漏
斗,加入一定量CCl 。振荡,静置。 I 易溶于CCl ,难溶于水;
4 液体分层,上层无色,下层紫色。 2 4
待分层后,将下层溶液从下口放出, CCl 密度大于水。
4
上层液体从上口弃去。
4.将上一步所得 CCl 溶液转移至
4
分液漏斗,加入少量浓NaOH溶液,
振荡,静置。待分层后,将下层溶 液体分层,上层无色,下层无色。 3I +6OH−=5I−+IO −+3H O
2 3 2
液从下口放出,弃去。上层液体从
上口倒出,置于烧杯中。
5.向烧杯中加入45%的H SO 。充
2 4 有紫色固体生成。 5I−+IO −+6H+=3I +3H O
分反应后过滤。 3 2 2
实验结论:
注意事项或反思:
1. 针对不同杂质的特点设计不同除杂方法。有机杂质:灼烧;无机杂质:萃取分液。
2. 得到目标产物后,为除杂等目的,可能会将目标产物先转化为其他物质。
3. 使用分液漏斗时,上层液体必须从上口倒出,不能从下口放出。
4. 第3、4、5步,将水溶液中的I 富集,使其超过溶解度,可以通过过滤方法分离。
2
5. 第4步,借助化学反应或其他原理,将非极性、弱极性分子从有机溶剂萃取至水溶液中,称为反萃取法。
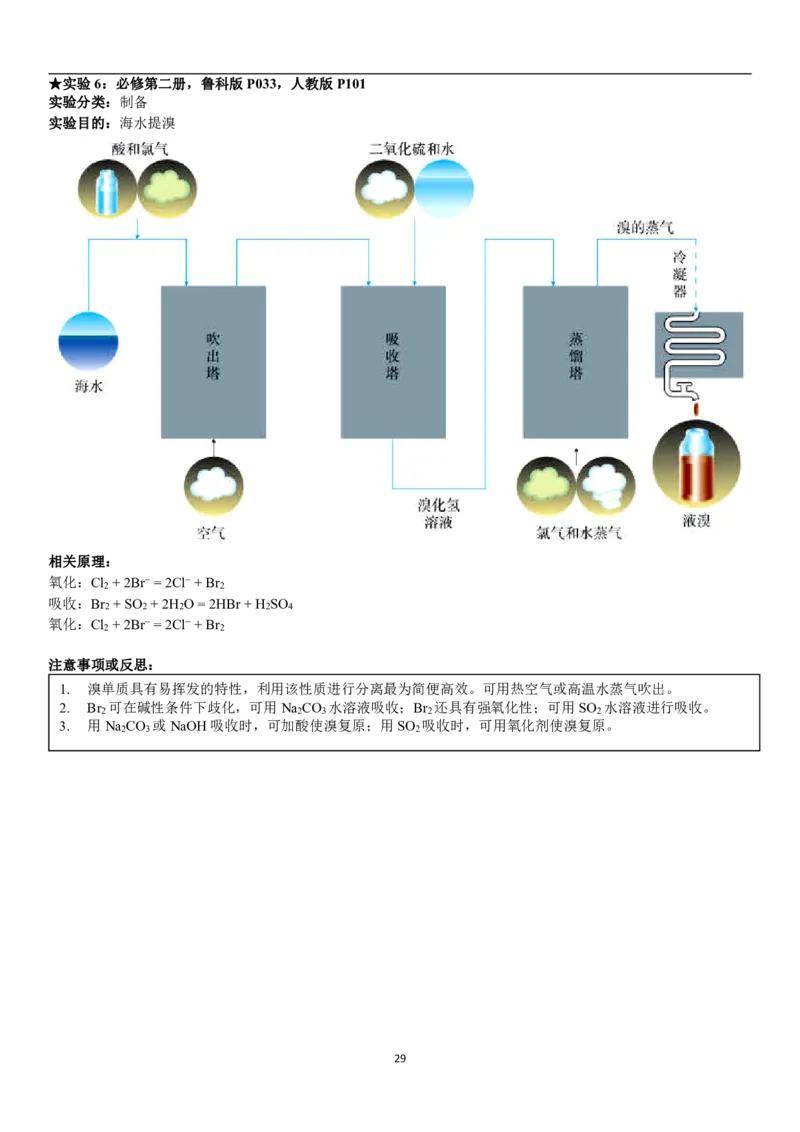
28★实验6:必修第二册,鲁科版P033,人教版P101
实验分类:制备
实验目的:海水提溴
相关原理:
氧化:Cl +2Br−=2Cl−+Br
2 2
吸收:Br +SO +2H O=2HBr+H SO
2 2 2 2 4
氧化:Cl +2Br−=2Cl−+Br
2 2
注意事项或反思:
1. 溴单质具有易挥发的特性,利用该性质进行分离最为简便高效。可用热空气或高温水蒸气吹出。
2. Br 可在碱性条件下歧化,可用Na CO 水溶液吸收;Br 还具有强氧化性;可用SO 水溶液进行吸收。
2 2 3 2 2
3. 用Na CO 或NaOH吸收时,可加酸使溴复原;用SO 吸收时,可用氧化剂使溴复原。
2 3 2
29★实验7:物质结构与性质,鲁科版P63,人教版P95-97P104
实验分类:制备
实验目的:制备配合物,体验形成配合物对物质性质的影响
实验操作 实验现象 解释或讨论
(1)分别取少量无 无水硫酸铜为白色固体,溶于水后得到
水硫酸铜粉末与硫 蓝色溶液; Cu2++4H O Cu(H O) 2+
2 2 4
酸钾粉末于两试管 硫酸钾为白色固体,溶于水后得到无色 无色 蓝色
中,分别加水溶解。 溶液
绿色固体溶解解得到绿色溶液,随水的
(2)向氯化铜固体 CuCl 2-+4H O Cu(H O) 2++4Cl-
加入,溶液颜色逐渐变为蓝绿色,最终 4 2 2 4
中逐滴加入水 绿色 蓝色
变从蓝色
(3)向0.1mol/L Cu2++2NH ∙H O=Cu(OH) ↓+2NH +
先产生蓝色沉淀,后沉淀溶解,得到深 3 2 2 4
CuSO 溶液中滴加 蓝色
4 蓝色溶液;加入乙醇后析出深蓝色的晶
1mol/L 氨水,再加 Cu(OH) + 4NH ∙H O = Cu(NH ) 2+ + 2OH- + 4H O
体 2 3 2 3 4 2
入8mL95%乙醇 深蓝色
(4)向0.1mol/L
NaCl溶液中滴几滴
0.1mol/LAgNO ,
滴加AgNO
3
后产生白色沉淀;再滴加氨 Ag++Cl-=AgCl↓
3 水后沉淀溶解,得到无色溶液 AgCl+2NH ∙H O=Ag(NH ) ++Cl-+2H O
再滴入1mol/L 氨 3 2 3 2 2
水
(5)向 Fe(NO )
3 3 滴加硝酸时,溶液的黄色逐渐变浅至近
溶液中滴加少量硝 Fe3+的水合离子接近无色,但Fe3+发生部分水解或
无色;再滴加NaCl溶液后溶液重新变为
酸,再滴入少量 与Cl-配位后,会产生黄色物质
黄色
NaCl溶液
(6)分别向两支盛
有少量蒸馏水的试
FeCl 溶液中滴加KSCN后溶液变红; Fe3++3SCN- Fe(SCN)
管中滴加2滴FeCl 3 3
溶液或K [Fe(CN) 3 ] K 3 [Fe(CN) 6 ]溶液中滴加KSCN后溶液不 [Fe(CN) 6 ]3-中,由于Fe3+与CN-配位,溶液中c(Fe3+)
3 6 变红 太小,难以被KSCN检测到
溶液,然后再各滴
加2滴KSCN溶液
注意事项或反思:
1. 以上实验通过什么现象说明制得了配合物?
颜色发生变化,溶解性发生变化
2. 从平衡移动和配位键两个角度分析上述实验。
30★实验8:有机化学基础,鲁科版P52,人教版P59
实验分类:制备
实验目的:利用乙醇的消去反应制备乙烯
实验操作:在圆底烧瓶中加入乙醇和浓硫酸(体积比约为1:3)的混合液20mL,放入几片碎瓷片,以避免混合液
在受热时暴沸。加热混合液,使液体温度迅速升到170oC,将生成的气体先通入氢氧化钠溶液除去杂质,再分别通
入酸性高锰酸钾溶液和溴的四氯化碳溶液中,观察实验现象。
实验装置:
实验操作 实验现象 解释或讨论
乙醇在浓硫酸催化下发生脱水,在170oC
(1)加热乙醇与浓 温度计示数不断升高,混合液逐渐由无色变黄、 时,发生分子内脱水,生成乙烯:
硫酸的混合液 变棕,甚至变黑,洗气瓶导管处不断产生气泡
(2)将洗涤后的气
体通入酸性高锰酸 高锰酸钾溶液的紫色褪色 碳碳双键可被酸性高锰酸钾氧化
钾溶液
(3)将洗涤后的气
溴水的黄色褪色 碳碳双键可与溴水发生加成反应
体通入溴水
实验结论:_____乙醇在浓硫酸催化下在170oC时发生消去反应生成乙烯___________________________________
注意事项或反思:
1. 预先向烧瓶中加几片碎玻璃片(碎瓷片),是何目的?
防止暴沸
2. 温度计的水银球位置和作用如何?
温度计水银球置于混合液液面下,用于测混合液的温度(控制温度)。
3. 反应后期,反应液有时会变黑,且有刺激性气味的气体产生,为何?
浓硫酸有强氧化性,可使乙醇等有机物氧化、碳化,从而使混合液变黄、变黑。
碳化后还会发生反应: ,从而产生有刺激性气味的SO
2
4. 氢氧化钠溶液的作用是什么?
吸收气体中的SO ,防止其干扰乙烯与酸性高锰酸钾、溴水的反应
2
31★实验9:有机化学基础,鲁科版P93-94,人教版P75
实验分类:制备
实验目的:乙酸乙酯的制备
实验操作:在试管中依次加入乙醇、浓硫酸、乙酸,管口用带长导管的塞子塞好,长导管另一端放入盛有饱和Na CO
2 3
溶液的试管中,导管口置于液面上方1~2cm。
实验装置:
实验操作 实验现象 解释或讨论
左侧试管中产生大量气泡,气体在右侧 乙醇与乙酸在浓硫酸催化下发生酯化反应:
(1)加热左侧试管 导管冷凝并流出,在水面上方产生一层
无色、有香味的液体
(2)将右侧试管取下, 冷凝的乙酸乙酯中溶解有挥发出的乙醇和乙
右侧水面上方的有机层变薄
振荡、静置 酸,它们可以被碳酸钠溶液吸收而溶于水层中
(3)将1mL乙酸乙
酯加入三支试管中,再
三支试管均分层,上层为乙酸乙酯,下
分别加入2mL水、 乙酸乙酯不溶于水,密度小于水
层为水溶液
2mL 稀硫酸、2mL 氢
氧化钠溶液
乙酸乙酯在酸性、碱性条件下均可水解:
(4)将三支试管加热 加水的试管中有机层没有明显变少,加
相同时间后冷却、静 酸或加碱的试管中有机层均变薄,有机
置,观察有机层的厚度 层的厚度为NaOH< 稀硫酸 < 水
在碱性条件下水解速率更快
实验结论:__乙醇与乙酸可发生酯化反应生成乙酸乙酯;乙酸乙酯在酸性或碱性条件下均可水解,在碱性条件水解
更充分、反应速率也更快________________________________________________________________________
注意事项或反思:
1. 为什么导管口不能伸入Na CO 溶液中?
2 3
防止发生倒吸
2. 浓硫酸的作用如何?
催化剂、吸水剂
3. 饱和Na CO 溶液的作用如何?
2 3
溶解乙醇;与乙酸反应而吸收乙酸;降低乙酸乙酯在水中的溶解度
4. 有哪些提高乙酸乙酯产率的措施
增大反应物浓度:使用过量的乙醇
降低产物浓度:蒸出乙酸乙酯,使用浓硫酸吸水
升温提高反应速率;
使用酸作催化剂提高反应速率
32实验10:有机化学基础,人教版P136
实验分类:制备
实验目的:酚醛树脂的制备
实验操作:在两支大试管中各加入2g苯酚、3mL质量分数为40%的甲醛溶液,再分别加入3滴浓盐酸或0.5mL
浓氨水,在水浴中加热。当试管中反应物接近沸腾时,从水浴中取出试管,并用玻璃棒搅拌,得到酚醛树脂固体。
实验装置:
实验操作 实验现象 解释或讨论
酸性条件下得到的是线型酚醛树脂
(1)将酸性条件下
得到的酚醛树脂放 酚醛树脂溶于乙醇
入乙醇中搅拌。
(2)将碱性条件下
得到的酚醛树脂放 酚醛树脂不溶于乙醇 碱性条件下得到的是网状酚醛树脂
入乙醇中搅拌。
实验结论:___酸或碱均可催化苯酚与甲醛反应产生酚醛树脂;酸催化下可制得线形产物,碱催化下一般会得到网
状产物______
注意事项或反思:
1. 制酚醛树脂的反应是缩聚反应,苯酚的邻、对位均可参与反应。
2. 苯酚与甲醛为什么可以得到网状高分子?
苯酚中酚羟基的邻、对位均可反应,有3个反应位点,因此可以使不同的高分子链互相连接成网状
3. 思考为何线形酚醛树脂可溶于乙醇,而网状酚醛树脂不溶于乙醇?
线形高分子链与链间为分子间相互作用,作用力弱,易被溶剂分子破坏,可以溶于合适的溶剂;
网状高分子链与链间被共价键边接,作用力强,难以被破坏,一般不能溶解
33高三实验板块复习——原理专题
★实验1:必修第二册,鲁科版P047,人教版P032
实验分类:原理
实验目的:感受化学反应中的能量变化
实验操作:
实验装置:砂纸、温度计、玻璃片、木片,及常规仪器
实验操作 实验现象 解释或讨论
向三支试管中分别加入 2 mL 2
mol/L盐酸,分别测定其温度。分别 均有无色气体生成,放热。
活泼金属与酸的反应是放热反应
加入打磨后的镁条、锌粉、铁粉。 最大升温程度:镁条 > 锌粉 > 铁粉
测定其温度随时间变化情况。
向试管中加入2mL柠檬酸溶液,
测定其温度。加入NaHCO 溶液。 有无色气体生成,溶液温度升高。 强酸制备弱酸的反应通常是放热的。
3
测定其温度随时间变化情况。
将20gBa(OH) ·8H O研细,与10g
2 2
NH Cl晶体一起放入烧杯。将烧杯
4 有刺激性气味气体生成
放在滴有几滴水的木片上。用玻璃 Ba(OH) ·8H O+2NH Cl
烧杯壁温度下降,外壁有无色液滴凝 2 2 4
棒快速搅拌,闻到气味后迅速用玻 =BaCl +2NH +10H O
结,烧杯与木板之间的液滴被冻结。 2 3 2
璃片盖上烧杯,用手触摸杯壁下部,
试着用手拿起烧杯。
实验结论:
1.活泼金属与酸的反应、(酸碱中和反应、)强酸制备弱酸的反应是放热反应。
2.Ba(OH) ·8H O与NH Cl的反应是吸热反应。
2 2 4
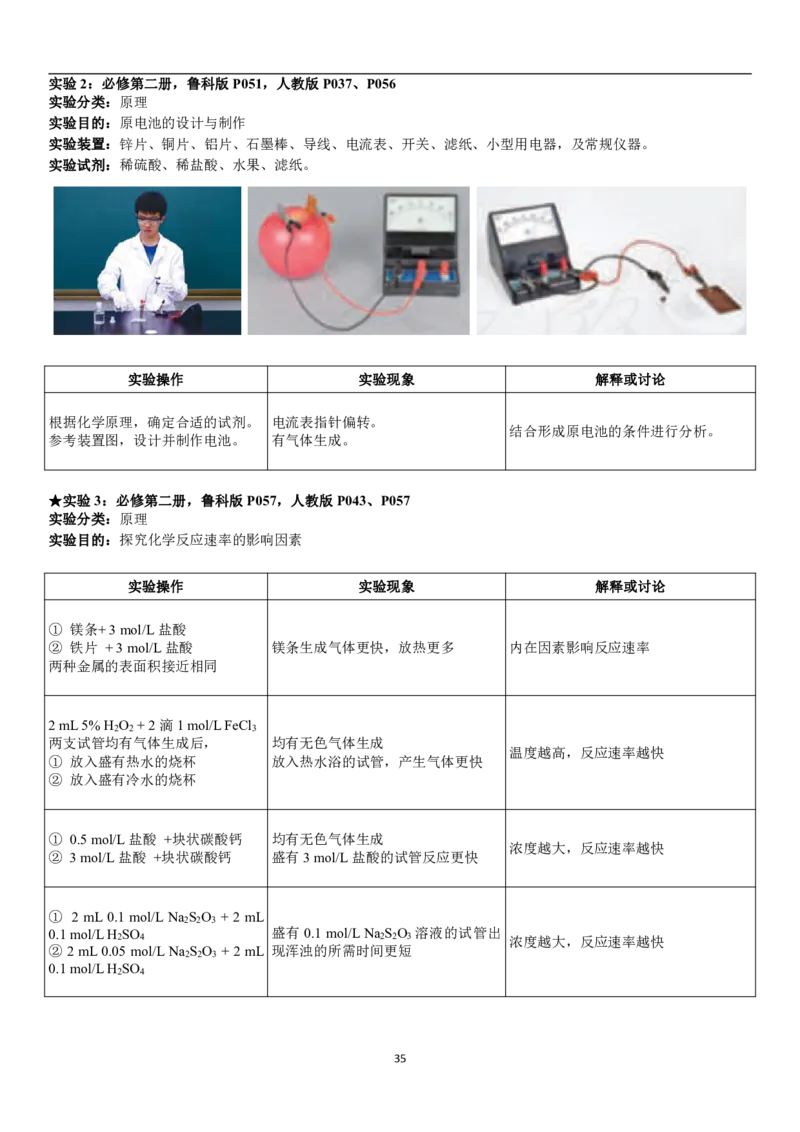
34实验2:必修第二册,鲁科版P051,人教版P037、P056
实验分类:原理
实验目的:原电池的设计与制作
实验装置:锌片、铜片、铝片、石墨棒、导线、电流表、开关、滤纸、小型用电器,及常规仪器。
实验试剂:稀硫酸、稀盐酸、水果、滤纸。
实验操作 实验现象 解释或讨论
根据化学原理,确定合适的试剂。 电流表指针偏转。
结合形成原电池的条件进行分析。
参考装置图,设计并制作电池。 有气体生成。
★实验3:必修第二册,鲁科版P057,人教版P043、P057
实验分类:原理
实验目的:探究化学反应速率的影响因素
实验操作 实验现象 解释或讨论
① 镁条+3mol/L盐酸
② 铁片 +3mol/L盐酸 镁条生成气体更快,放热更多 内在因素影响反应速率
两种金属的表面积接近相同
2mL5%H O +2滴1mol/LFeCl
2 2 3
两支试管均有气体生成后, 均有无色气体生成
温度越高,反应速率越快
① 放入盛有热水的烧杯 放入热水浴的试管,产生气体更快
② 放入盛有冷水的烧杯
① 0.5mol/L盐酸 +块状碳酸钙 均有无色气体生成
浓度越大,反应速率越快
② 3mol/L盐酸 +块状碳酸钙 盛有3mol/L盐酸的试管反应更快
① 2 mL 0.1 mol/L Na S O + 2 mL
2 2 3
0.1mol/LH 2 SO 4 盛有 0.1 mol/LNa 2 S 2 O 3 溶液的试管出 浓度越大,反应速率越快
② 2 mL0.05 mol/LNa S O + 2 mL 现浑浊的所需时间更短
2 2 3
0.1mol/LH SO
2 4
35① 块状碳酸钙 +0.5mol/L盐酸 均有无色气体生成
固体反应的表面积越大,反应速率越快
② 碳酸钙粉末 +0.5mol/L盐酸 盛有碳酸钙粉末的试管反应更快
盛有MnO 粉末的试管迅速产生大量
① 3%H O 2
2 2 无色气体,并放热; 加入催化剂可提高反应速率
② 3%H O + 少量MnO 粉末
2 2 2 另一支试管间或产生一些无色气泡
实验结论:
反应物自身性质可影响反应速率
提高温度、提高反应物浓度、增大固体反应物表面积、使用催化剂可提高反应速率。
注意事项或反思:
1. 对照实验注意控制变量
★实验4:必修第二册,鲁科版P059、P061,人教版 – 无
实验分类:原理
实验目的:认识化学反应存在限度
实验装置:止水夹
实验操作 实验现象 解释或讨论
2Fe3++2I− ≒ 2Fe2++I
向2mL0.01mol/LKI溶液中加入1 2
滴入FeCl 后,溶液变黄(I ) Fe3++3SCN− ≒ Fe(SCN)
mL0.01mol/LFeCl 溶液。在加入几 3 2 3
3 加入KSCN后,溶液变红。 在反应足够时间后,溶液内仍同时存在
滴0.1mol/LKSCN溶液。
Fe3+、I−、Fe2+、I 。
2
2NO ≒ N O ΔH>0
将封装有 NO 和 N O 混合气体的 2 2 4
2 2 4 浸入冷水中的气体颜色变浅, 外界条件改变后,平衡状态也将发生改
装置两端的球形容器分别浸入热水
浸入热水中的气体颜色变深 变。温度降低时,向生成NO 的方向移
和冷水中,观察实验现象。 2
动。
实验结论:
1.某些反应在反应足够长时间后,反应物、生成物可同时存在。这些反应是可逆反应,所达状态是化学平衡
状态。
2.化学平衡是在一定条件下建立起来的。外界条件发生改变时,平衡状态也将发生改变。
注意事项或反思:
1. 注意:Fe3+与I−的反应实际上是比较彻底的,在无其他物质影响的条件下,可认为按计量关系进行反应。
36★实验5:化学反应原理,人教P54
实验分类:原理
实验目的:浓度对平衡移动的影响
实验操作:已知在K Cr O 的溶液中存在如下平衡:Cr O 2- +H O 2CrO 2- +2H+;K Cr O 为橙色,K CrO
2 2 7 2 7 2 4 2 2 7 2 4
为黄色。取两支试管各加入5mL0.1mol/LK Cr O 溶液,然后按下表步骤操作,观察并记录溶液颜色变化。
2 2 7
步骤 滴加3~10滴浓H SO 滴加10~20滴6mol/LNaOH
2 4
K Cr O 溶液 溶液橙色加深 溶液由橙色变为黄色
2 2 7
★实验6:化学反应原理,P53人教
实验分类:原理
实验目的:浓度对平衡移动的影响
实验操作:向盛有5mL0.005mol/LFeCl 溶液的试管中加入5mL0.01mol/LKSCN溶液,溶液显红色。在这个反应
3
体系中存在下述平衡:Fe3+ + 3SCN- Fe(SCN) (红色)。(1)将上述溶液均分置于两支试管中;向其中一
3
支试管中加入饱和FeCl 溶液4滴,充分振荡,观察溶液颜色变化;向另一支试管滴加4滴1mol/LKSCN溶液,观
3
察溶液颜色变化。(2)向上述两支试管中各滴加0.01mol/LNaOH溶液3~~5滴,观察现象。
编号 1 2
步骤(1) 滴加饱和FeCl 溶液 滴加1mol/LKSCN溶液
3
现象 溶液红色加深 溶液红色加深
步骤(2) 加入少量铁粉 加入少量铁粉
现象 红色溶液变浅 红色溶液变浅
在0.005mol/L的FeCl 溶液中加入0.01mol/L的KSCN溶液,振荡,所得溶液的红色较浅。本实验的关键是第
3
一次获得的Fe(SCN) 溶液浓度要小,然后滴加浓的FeCl 、KSCN溶液时才会有明显的颜色变化。
3 3
因为铁粉与溶液中的Fe3+反应生成Fe2+,减小Fe3+浓度,平衡逆移,Fe(SCN) 浓度减小,混合液的颜色变浅。
3
★实验7:化学反应原理, P54人教
实验分类:原理
实验目的:温度对平衡移动的影响
实验操作:在CuCl 溶液中存在如下平衡 [Cu(H O)]2++4Cl- [CuCl ]2-+4H O ΔH>0
2 2 4 2
蓝色 黄色
取两只试管分别加入2mL0.5mol/LCuCl 溶液,将其中一支试管先加热,然后置于冷水中,与另一支试管对比。
2
实验步骤 实验现象 结论
(1)加热试管 溶液由蓝色变绿 升温平衡向吸热方向移动
(2)将上述试管置于冷水中 溶液由绿色变蓝 降温溶液向放热方向移动
37★实验8:化学反应原理,P37人教
实验分类:原理
实验目的:温度对平衡移动的影响
实验操作:
NO 球浸泡在冰水、热水中,观察颜色变化。
2
2NO (g) N O (g) ΔH=-56.9kJ/mol
2 2 4
红棕色 无色
实验 浸泡在热水中 浸泡再冰水中
现象 气体颜色变深 气体颜色变浅
结论 升温,平衡向着吸热方向移动,降温平衡向放热方向移动
★实验9:化学反应原理,人教
实验分类:原理
实验目的:压强对平衡移动的影响
实验操作:用50mL注射器吸入20mLNO 和N O 的混合气体(使注射器活塞位于Ⅰ处)
2 2 4
然后将活塞拉至2处,观察管内气体颜色的变化。
实验 体系压强增大 体系压强减小
现象 先变深,后略变浅 先变浅,后略变深
结论 加压平衡向着气体分子数减小的方向移动,减压平衡向着气体分子数增大的方向移动。
★实验10:化学反应原理,人教
实验分类:原理
实验目的:弱酸的电离
实验操作:分别试验等体积.等浓度的盐酸、醋酸溶液与等量镁条的反应;并测这两种酸的pH。
1mol/LHCl 1mol/LCH COOH
3
与镁条反应的现象 产生气泡速率快 产生气泡速率慢
溶液的pH pH=1 pH>1
★实验11:化学反应原理,P69人教
实验分类:原理
实验目的:盐的水解
实验操作:取少量NaCl、Na CO 、NaHCO 、NH Cl、Na SO 、CH COONa、(NH ) SO 的溶液,分别用pH试纸检
2 3 3 4 2 4 3 4 2 4
验酸碱性,并把盐按照强酸强碱盐、强酸弱碱盐、强碱弱酸盐分类。
盐溶液 NaCl Na CO NaHCO NH Cl Na SO CH COONa (NH ) SO
2 3 3 4 2 4 3 4 2 4
酸碱性 中性 碱性 碱性 酸性 中性 碱性 酸性
盐类型 强酸强碱 强碱弱酸 强碱弱酸 强酸弱碱 强酸强碱 强碱弱酸 强酸弱碱
分析上述实验结果,归纳其与盐的类型间的关系。
盐的类型 强酸强碱盐 强酸弱碱盐 强碱弱酸盐
溶液的酸碱性 中性 酸性 碱性
38实验12:化学反应原理,P80人教
实验分类:原理
实验目的:沉淀的溶解
实验操作:向3支盛有少量Mg(OH) 沉淀的试管中分别滴加适量的蒸馏水.盐酸和氯化铵溶液,观察并记录现象。
2
滴加试剂 蒸馏水 盐酸 氯化铵溶液
现象 固体无明显溶解现象 迅速溶解 可溶
★实验13:化学反应原理,P81人教
实验分类:原理
实验目的:沉淀转化
实验操作:向盛有1mL0.1mol/LMgCl 溶液的试管中滴加1~2滴2mol/LNaOH溶液,有白色沉淀生成,再滴加2
2
滴0.1mol/LFeCl 溶液,静置。观察现象。
3
步骤 MgCl 溶液中滴加NaOH溶液 向白色沉淀中滴加FeCl 溶液 静置
2 3
现象 有白色沉淀析出 白色沉淀变红褐色 红褐色沉淀析出,溶液褪至无色
实验14:化学反应原理,P112鲁科
实验分类:原理
实验目的:沉淀转化
实验操作:向一支试管中加入2mL0.1mol/LZnSO 溶液,再加入1滴1mol/LNa S 溶液, 向上述试管滴加2滴0.1
4 2
mol/LCuSO 溶液,振荡试管,观察现象
4
步骤 ZnSO 溶液中滴加Na S 溶液, 向白色沉淀中滴加CuSO 溶液
4 2 4
现象 有白色沉淀析出 白色沉淀变黑
★实验15:化学反应原理, P81人教
实验分类:原理
实验目的:沉淀转化
实验操作:(1)向盛有2mL0.1mol/LNaCl溶液的试管中,用滴加2滴0.1mol/LAgNO 溶液,振荡试管观察现象;
3
(2)然后向其中加入4滴 0.1mol/LKI溶液振荡观察现象;
(3)再向其中加入8滴0.1mLmol/LNa S溶液。振荡。
2
步骤 (1) (2) (4)
现象 有白色沉淀析出 白色沉淀变黄 黄色沉淀变黑
39实验16:化学反应原理,P94人教
实验分类:原理
实验目的:双液原电池的制作
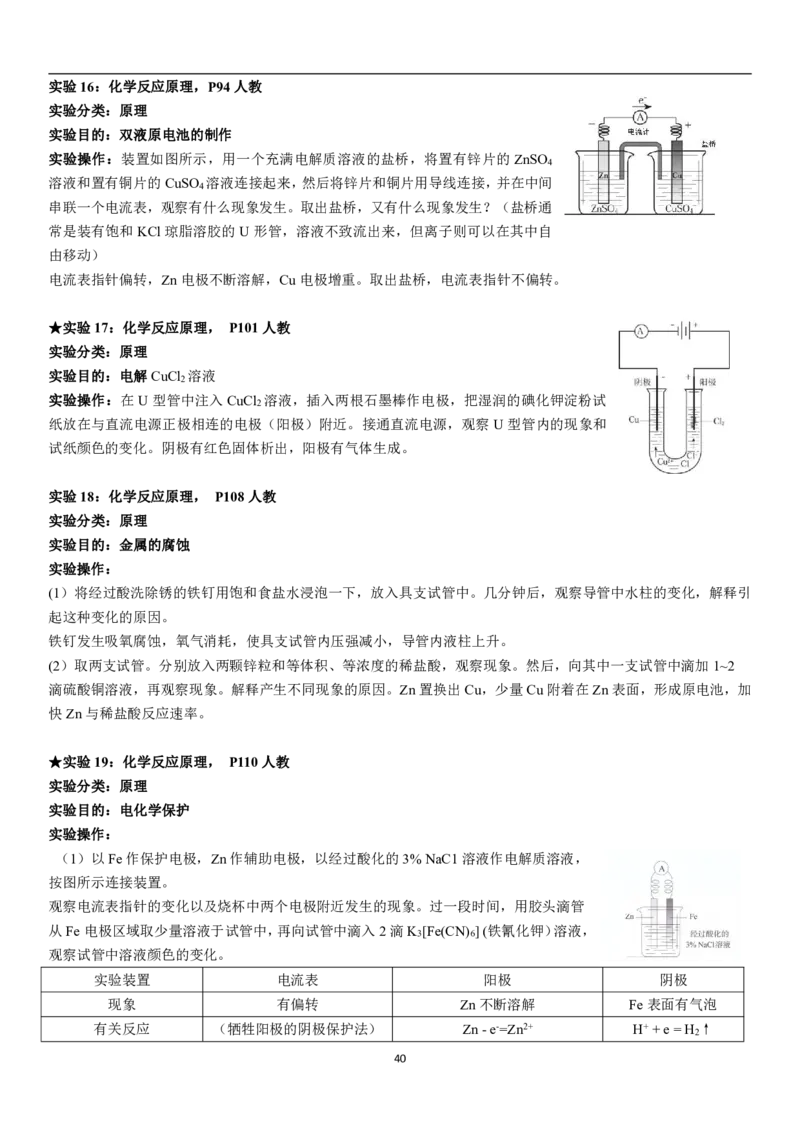
实验操作:装置如图所示,用一个充满电解质溶液的盐桥,将置有锌片的ZnSO
4
溶液和置有铜片的CuSO 溶液连接起来,然后将锌片和铜片用导线连接,并在中间
4
串联一个电流表,观察有什么现象发生。取出盐桥,又有什么现象发生?(盐桥通
常是装有饱和KCl琼脂溶胶的U形管,溶液不致流出来,但离子则可以在其中自
由移动)
电流表指针偏转,Zn电极不断溶解,Cu电极增重。取出盐桥,电流表指针不偏转。
★实验17:化学反应原理, P101人教
实验分类:原理
实验目的:电解CuCl 溶液
2
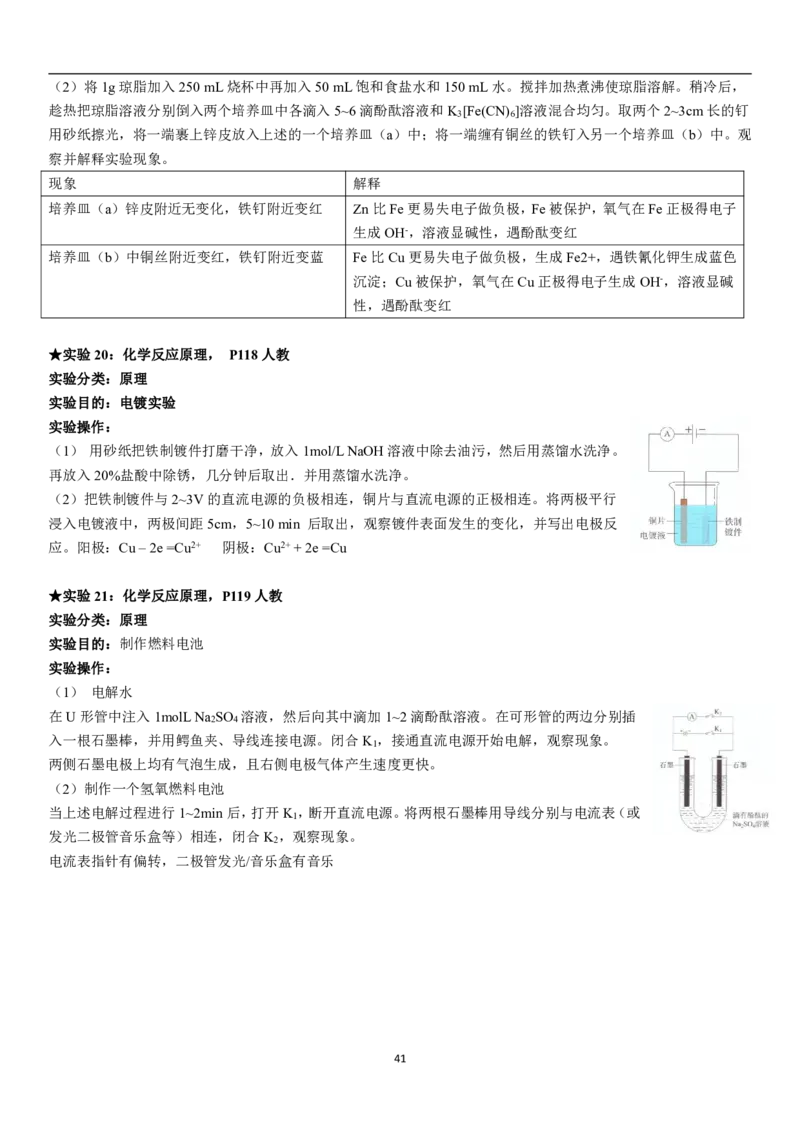
实验操作:在U型管中注入CuCl 溶液,插入两根石墨棒作电极,把湿润的碘化钾淀粉试
2
纸放在与直流电源正极相连的电极(阳极)附近。接通直流电源,观察U型管内的现象和
试纸颜色的变化。阴极有红色固体析出,阳极有气体生成。
实验18:化学反应原理, P108人教
实验分类:原理
实验目的:金属的腐蚀
实验操作:
(1)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入具支试管中。几分钟后,观察导管中水柱的变化,解释引
起这种变化的原因。
铁钉发生吸氧腐蚀,氧气消耗,使具支试管内压强减小,导管内液柱上升。
(2)取两支试管。分别放入两颗锌粒和等体积、等浓度的稀盐酸,观察现象。然后,向其中一支试管中滴加1~2
滴硫酸铜溶液,再观察现象。解释产生不同现象的原因。Zn置换出Cu,少量Cu附着在Zn表面,形成原电池,加
快Zn与稀盐酸反应速率。
★实验19:化学反应原理, P110人教
实验分类:原理
实验目的:电化学保护
实验操作:
(1)以Fe作保护电极,Zn作辅助电极,以经过酸化的3%NaC1溶液作电解质溶液,
按图所示连接装置。
观察电流表指针的变化以及烧杯中两个电极附近发生的现象。过一段时间,用胶头滴管
从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K [Fe(CN) ](铁氰化钾)溶液,
3 6
观察试管中溶液颜色的变化。
实验装置 电流表 阳极 阴极
现象 有偏转 Zn不断溶解 Fe表面有气泡
有关反应 (牺牲阳极的阴极保护法) Zn-e-=Zn2+ H++e=H ↑
2
40(2)将1g琼脂加入250mL烧杯中再加入50mL饱和食盐水和150mL水。搅拌加热煮沸使琼脂溶解。稍冷后,
趁热把琼脂溶液分别倒入两个培养皿中各滴入5~6滴酚酞溶液和K [Fe(CN) ]溶液混合均匀。取两个2~3cm长的钉
3 6
用砂纸擦光,将一端裹上锌皮放入上述的一个培养皿(a)中;将一端缠有铜丝的铁钉入另一个培养皿(b)中。观
察并解释实验现象。
现象 解释
培养皿(a)锌皮附近无变化,铁钉附近变红 Zn比Fe更易失电子做负极,Fe被保护,氧气在Fe正极得电子
生成OH-,溶液显碱性,遇酚酞变红
培养皿(b)中铜丝附近变红,铁钉附近变蓝 Fe比Cu更易失电子做负极,生成Fe2+,遇铁氰化钾生成蓝色
沉淀;Cu被保护,氧气在Cu正极得电子生成OH-,溶液显碱
性,遇酚酞变红
★实验20:化学反应原理, P118人教
实验分类:原理
实验目的:电镀实验
实验操作:
(1) 用砂纸把铁制镀件打磨干净,放入1mol/LNaOH溶液中除去油污,然后用蒸馏水洗净。
再放入20%盐酸中除锈,几分钟后取出.并用蒸馏水洗净。
(2)把铁制镀件与2~3V的直流电源的负极相连,铜片与直流电源的正极相连。将两极平行
浸入电镀液中,两极间距5cm,5~10min 后取出,观察镀件表面发生的变化,并写出电极反
应。阳极:Cu–2e=Cu2+ 阴极:Cu2++2e=Cu
★实验21:化学反应原理,P119人教
实验分类:原理
实验目的:制作燃料电池
实验操作:
(1) 电解水
在U形管中注入1molLNa SO 溶液,然后向其中滴加1~2滴酚酞溶液。在可形管的两边分别插
2 4
入一根石墨棒,并用鳄鱼夹、导线连接电源。闭合K ,接通直流电源开始电解,观察现象。
1
两侧石墨电极上均有气泡生成,且右侧电极气体产生速度更快。
(2)制作一个氢氧燃料电池
当上述电解过程进行1~2min后,打开K ,断开直流电源。将两根石墨棒用导线分别与电流表(或
1
发光二极管音乐盒等)相连,闭合K ,观察现象。
2
电流表指针有偏转,二极管发光/音乐盒有音乐
41高三实验板块复习——定量专题
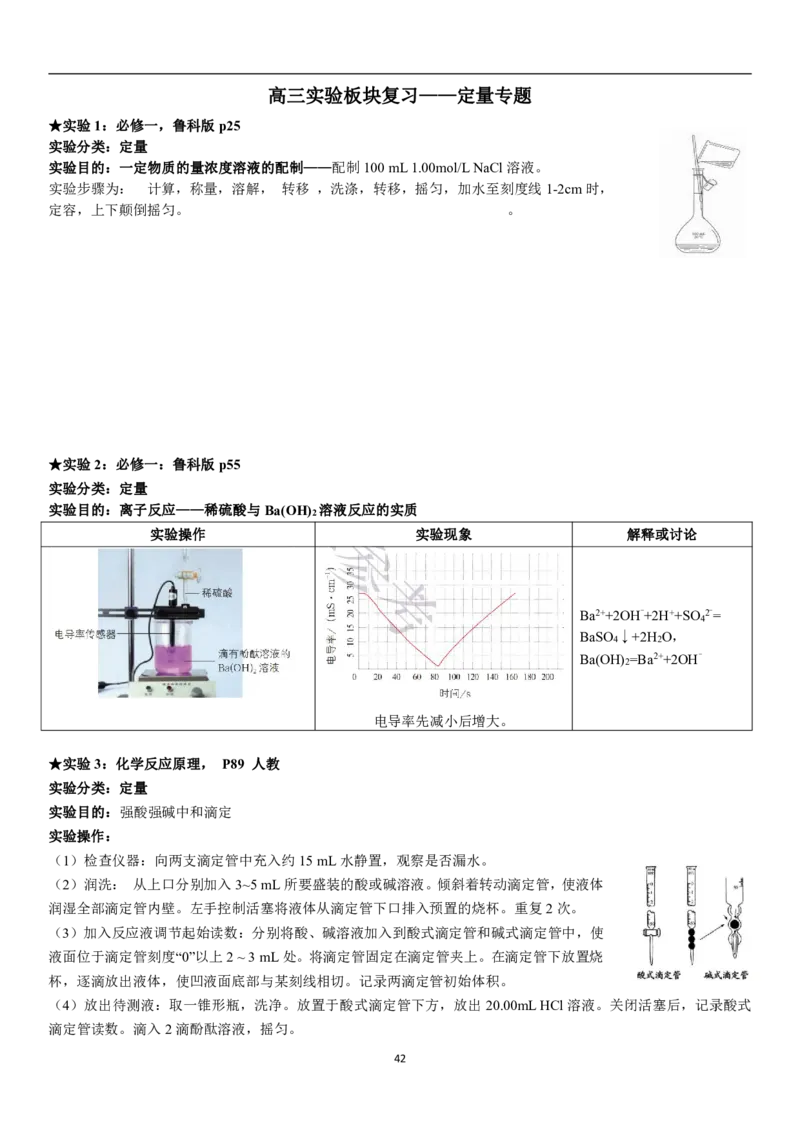
★实验1:必修一,鲁科版p25
实验分类:定量
实验目的:一定物质的量浓度溶液的配制——配制100mL1.00mol/LNaCl溶液。
实验步骤为: 计算,称量,溶解, 转移 ,洗涤,转移,摇匀,加水至刻度线1-2cm时,
定容,上下颠倒摇匀。 。
★实验2:必修一:鲁科版p55
实验分类:定量
实验目的:离子反应——稀硫酸与Ba(OH) 溶液反应的实质
2
实验操作 实验现象 解释或讨论
Ba2++2OH-+2H++SO 2-=
4
BaSO ↓+2H O,
4 2
Ba(OH) =Ba2++2OH-
2
电导率先减小后增大。
★实验3:化学反应原理, P89 人教
实验分类:定量
实验目的:强酸强碱中和滴定
实验操作:
(1)检查仪器:向两支滴定管中充入约15mL水静置,观察是否漏水。
(2)润洗: 从上口分别加入3~5mL所要盛装的酸或碱溶液。倾斜着转动滴定管,使液体
润湿全部滴定管内壁。左手控制活塞将液体从滴定管下口排入预置的烧杯。重复2次。
(3)加入反应液调节起始读数:分别将酸、碱溶液加入到酸式滴定管和碱式滴定管中,使
液面位于滴定管刻度“0”以上2~3mL处。将滴定管固定在滴定管夹上。在滴定管下放置烧
杯,逐滴放出液体,使凹液面底部与某刻线相切。记录两滴定管初始体积。
(4)放出待测液:取一锥形瓶,洗净。放置于酸式滴定管下方,放出20.00mLHCl溶液。关闭活塞后,记录酸式
滴定管读数。滴入2滴酚酞溶液,摇匀。
42(5)用标准溶液滴定:左手控制碱式滴定管,向上述锥形瓶中逐滴加入0.1000mol/LNaOH溶液,同时摇匀。直至
加入一滴溶液后溶液30秒不褪色为止,记录碱式滴定管读数。
1 2 3
待测盐酸的体积/mL 20.00 20.00 20.00
V(NaOH)/mL初始读数 0.00 0.1 0.00
V(NaOH)/mL滴定后读数 14.98 15.12 15.59
V(NaOH)/mL 消耗 14.98 15.02 15.59
将4、5步重复三次
(6)计算HCl溶液浓度为:0.0750mol/L 注:第三组数据误差大,舍去
实验4:化学反应原理,人教P5
实验分类:定量
实验目的:中和反应反应热的测定
实验操作:
(1)反应物温度的测量
①用量筒量取50mL0.50mol/L盐酸,打开杯盖,倒入量热计的内筒中,盖上杯盖,
插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸冲洗
干净,擦干备用。
②用另一个量筒量取50mL0.55mol/LNaOH溶液(为了保证盐酸被完全中和,采用稍过量的NaOH溶液),用温
度计测量并记录NaOH溶液的温度(数据填入下表)。
(2)反应后体系温度的测量
打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内筒中,立即盖上杯盖,插入温度计,用搅拌器匀速搅拌。密
切关注温度变化,将最高温度记为反应后体系的温度。
(3)重复上述步骤(1)至步骤(2)两次。
【数据处理】
(1)取盐酸温度和NaOH溶液温度的平均值记为反应前体系的温度(t )。计算温度差(t -t ),将数据填入下表。
1 2 1
实验次数 反应物的温度/℃ 反应前体系温度 反应后体系温度 温度差
盐酸 NaOH溶液 t /℃ t /℃ (t -t )/℃
1 2 2 1
1 27.0 27.4 27.2 31.3 4.1
2 26.2 26.0 26.1 29.4 3.3
3 26.2 26.2 26.3 29.4 3.1
(2)取三次测量所得温度差的平均值作为计算依据。
(3)根据温度差和比热容等计算反应热。
为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,则:
①50mL0.50mol/L盐酸的质量m =50g,50mL0.55mol/LNaOH溶液的质量m =50g。
1 2
②反应后生成的溶液的比热容c=4.18J/(g·℃),50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液发生中和
反应时放出的热量为:(m +m )·c·(t -t )=1.34kJ 注:第一组数据误差大,舍去
1 2 2 1
③生成1molH O时放出的热量为53.6kJ
2
强酸强碱的中和热是57.3kJ/mol,分析实验测量值偏低的原因:氢氧化钠溶液倒入过慢,溶液倒入量热计有液体溅
出,搅拌速度过慢,温度计未达到最高温度就读数等
43★实验5:化学反应原理,人教P24
实验分类:定量
实验目的:化学反应速率的测定
实验操作:按图安装两套装置,在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),通
过分液漏斗分别加入40mL1mol/L和40mL4mol/L的硫酸,比较二者收集10mLH 所
2
用的时间。
加入试剂 反应时间/min 反应速率/mL·min-`1
1mol/LH SO
2 4
4mol/LH SO
2 4
高三实验板块复习——其它专题
★实验1:必修一,鲁科版p59,人教版p
实验分类:分离提纯
实验目的:食盐的精制
粗盐中含有较多的杂质,如不溶性的泥沙,可溶性的CaCl 和MgCl ,以
2 2
及一些硫酸盐。
实验操作:
1.过滤与蒸发
注意事项:一贴,二低,三靠
实验原理:利用泥沙不溶于水来分离出来操作步骤及现象:
实验操作 现象
(1)溶解:称取约4g粗盐加到盛有约12ml水的烧杯中,边加边用玻璃 固体食盐逐渐溶解减少,食盐水
棒搅拌,直到粗盐不再溶解为止; 略显浑浊
(2)过滤:将烧杯中的液体沿玻璃棒倒入过滤器中,过滤器中的液面不 不溶物留在滤纸上,液体渗过滤
能超过滤纸的边缘。若滤液浑浊,再过滤一次; 纸,沿漏斗颈流入另一个烧杯中;
(3)蒸发:将滤液倒入蒸发皿中,然后用酒精灯加热,同时用玻璃棒不
水分蒸发,逐渐析出固体。
断的搅拌溶液,待出现较多固体时停止加热。
2.除去食盐中的可溶杂质——硫酸盐、CaCl 和MgCl
2 2
原理:利用碳酸钙是沉淀除去钙离子,利用硫酸钡除去硫酸根,利用氢氧化镁除去氢氧根
实验操作 化学原理(方程式)
加入过量的BaCl 溶液 BaCl +Na SO =BaSO ↓+2NaCl
2 2 2 4 4
加入过量的NaOH溶液 MgCl +2NaOH=Mg(OH) ↓+2NaCl
2 2
加入过量的Na CO 溶液 Na CO +CaCl =CaCO ↓+2NaCl,Na CO +BaCl =BaCO ↓+2NaCl
2 3 2 3 2 3 2 3 2 3
过滤
滴加适量盐酸至恰好不再产生气体 HCl+NaOH=NaCl+H O,2HCl+Na CO =2NaCl+H O+CO ↑
2 2 3 2 2
蒸发溶液,析出NaCl晶体。
注意事项:
(1)碳酸钠一定要加到氯化钡之后,碱可以随便加。试剂要加过量。
(2)思考:如何检验杂质离子是否去除干净?
取少量洗涤沉淀后的溶液,加入检测试剂,若无沉淀产生,则该杂质离子已去除干净。
44★实验2:必修一,人教版p46
实验分类:分离提纯
实验目的:蒸馏自来水
实验原理:对于液态互溶混合物,利用各组分沸点的不同除去杂质
实验操作 实验现象 解释或讨论
有不溶于稀硝酸 Ag++Cl-=AgCl
在试管中加入少量自来水,滴入几滴稀硝酸和几滴硝酸银溶液。
的白色沉淀。 自来水中有氯离子
加热,烧瓶中水
在100mL烧瓶中加入约1/3体积的自来水,再加入几粒沸石(或
温升高至100摄氏度
碎瓷片),按图连接好装置,向冷凝管中通入冷却水。加热烧瓶,弃 蒸馏可以制得蒸馏水
后沸腾。在锥形瓶中
去开始馏出的部分液体,用锥形瓶收集约10ml液体,停止加热。
收集到蒸馏水。
取少量收集到的液体加入试管中,然后滴入几滴稀硝酸和几滴
蒸馏水中无沉淀。 蒸馏水中无氯离子。
硝酸银溶液。
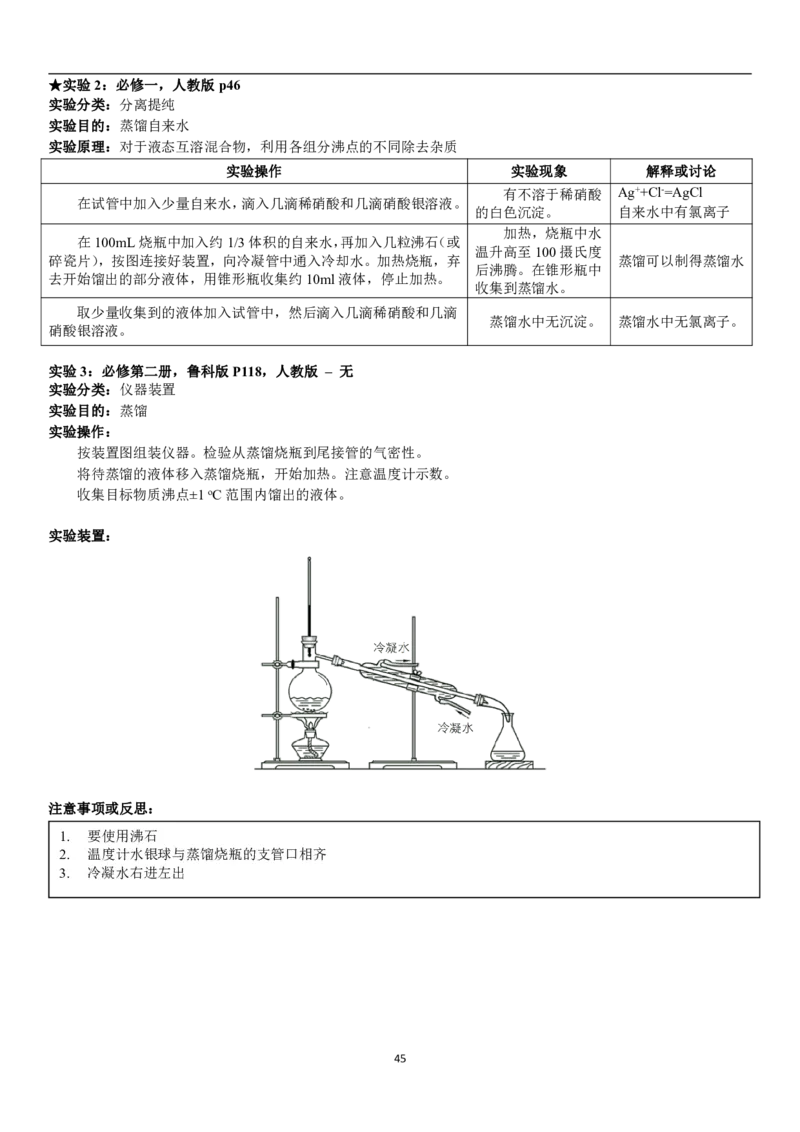
实验3:必修第二册,鲁科版P118,人教版 – 无
实验分类:仪器装置
实验目的:蒸馏
实验操作:
按装置图组装仪器。检验从蒸馏烧瓶到尾接管的气密性。
将待蒸馏的液体移入蒸馏烧瓶,开始加热。注意温度计示数。
收集目标物质沸点±1oC范围内馏出的液体。
实验装置:
注意事项或反思:
1. 要使用沸石
2. 温度计水银球与蒸馏烧瓶的支管口相齐
3. 冷凝水右进左出
45实验4:有机化学基础,人教版P13
实验分类:分离提纯
实验目的:重结晶法分离提纯苯甲酸
实验操作:
(1)观察粗苯甲酸样品的状态
(2)将1.0g粗苯甲酸放放100mL烧杯,加入50mL蒸馏水。加热,搅拌,使粗苯甲酸充分溶解。
(3)使用漏斗趁热将溶液过滤至另一烧杯中,将滤液静置,使其缓慢冷却结晶。
(4)待滤液完全冷却后滤出晶体,并用少量蒸馏水洗涤。将晶体铺在干燥的滤纸上,晾干后称其质量。
实验流程:
实验结论:___重结晶法是用于分离提纯固体有机物的重要方法,它可用于含有难溶和易溶杂质,而自身溶解度随
温度升高而明显增大的物质________
注意事项或反思:
1. 溶解粗苯甲酸时,加热的作用是什么?趁热过滤的目的是什么?
加热是为了尽可能多地溶解苯甲酸,得到浓的苯甲酸溶液,便于冷却时能析出更多的苯甲酸固体。
趁热过滤是为了在尽量不析出苯甲酸的情况下除于不溶性的杂质。
2. 实验中多次使用了玻璃棒,分别起到了哪些作用?
溶解时起搅拌作用,过滤时起引流作用。
3. 如何检验提纯后的苯甲酸中氯化钠已被除净
取少量固体,溶于水后加入硝酸酸化的硝酸银,若无白色沉淀,则氯化钠已被除净。
46高三实验板块复习——性质专题习题(选择题均为不定项)
无机物性质练习一
1. 下列实验中,对应的现象以及结论都正确且两者具有因果关系是
选项 实验 现象 结论
将稀硝酸加入过量铁粉中,充分 有气体生成,溶液呈 稀硝酸将Fe氧化为Fe3
A
反应后滴加KSCN溶液 血红色 +
将铜粉加入1.0mol·L-1 溶液变蓝、有黑色固
B 金属铁比铜活泼
Fe (SO ) 溶液中 体出现
2 4 3
用坩埚钳夹住一小块用砂纸仔细 熔化后的液态铝不滴 金属铝的熔点较低,氧
C
打磨过的铝箔在酒精灯上加热 落下来 化铝熔点较高
将0.1mol·L-1MgSO 溶液滴入
4
先有白色沉淀生成后 Cu(OH) 的溶解度比
2
D NaOH溶液至不再有沉淀产生,
变为浅蓝色沉淀 Mg(OH) 的小
2
再滴加0.1mol·L-1CuSO 溶液
4
2.由下列实验及现象不
.
能
.
推出相应结论的是
实验 现象 结论
A 向2 mL0.1 molL1的FeCl 溶液中加足量 黄色逐渐消失,加KSCN 还原性:Fe>Fe2+
3
溶液颜色不变
铁粉,振荡,加1滴KSCN溶液
B 将金属钠在燃烧匙中点燃,迅速伸入集满 集气瓶中产生大量白烟, CO 具有氧化性,白
2
CO 的集气瓶 瓶内有黑色颗粒产生 烟为Na O固体
2 2
C 加热盛有少量NH HCO 固体的试管,并在 石蕊试纸变蓝 NH HCO 显碱性
4 3 4 3
试管口放置湿润的红色石蕊试纸
D 向2支盛有2mL相同浓度银氨溶液的试管 一只试管中产生黄色沉 K (AgI)K (AgCl)
sp sp
中分别加入2滴相同浓度NaCl和NaI溶液 淀,另一支中无明显现象
3. 用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验合理的是
A.③中选用NaOH溶液吸收多余的SO
2
B.上下移动①中铜丝可控制SO 的量
2
C.②中选用品红溶液验证SO 的生成
2
D.为确认CuSO 生成,向①中加水,观察颜色
4
474.根据SO
2
通入不同溶液中实验现象,所得结论不
.
正
.
确
.
的是
溶液 现象 结论
A 含HCl、BaCl 的FeCl 溶液 产生白色沉淀 SO 有还原性
2 3 2
B H S溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
D Na SiO 溶液 产生胶状沉淀 酸性:H SO >H SiO
2 3 2 3 2 3
5.由下列实验及现象推出相应结论不
.
正
.
确
.
的是
实验 现象 结论
先有白色沉淀生成,加
某溶液中加入Ba(NO ) 溶液,
3 2
A 盐酸后白色沉淀不消 原溶液中可能有SO 2-
3
再加足量盐酸
失
将湿润的淀粉碘化钾试纸放在
B 试纸变蓝 红棕色气体为溴蒸气
盛有红棕色气体的集气瓶口
将碳酸钠与盐酸反应产生的气
C 体通入盛有硅酸钠溶液的烧杯 烧杯中液体变浑浊 非金属性:Cl>C>Si
中
将0.1mol/LMgSO 溶液加入等
4
先有白色沉淀生成,后 溶解度:Cu(OH) <
2
D 体积0.25mol/LNaOH溶液,
生成蓝色沉淀 Mg(OH)
2
再滴加0.1mol/LCuSO 溶液
4
6.喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是
气体 溶液
A H S 稀盐酸
2
B HCl 稀氨水
C NH 水
3
D CO 饱和NaHCO 溶液
2 3
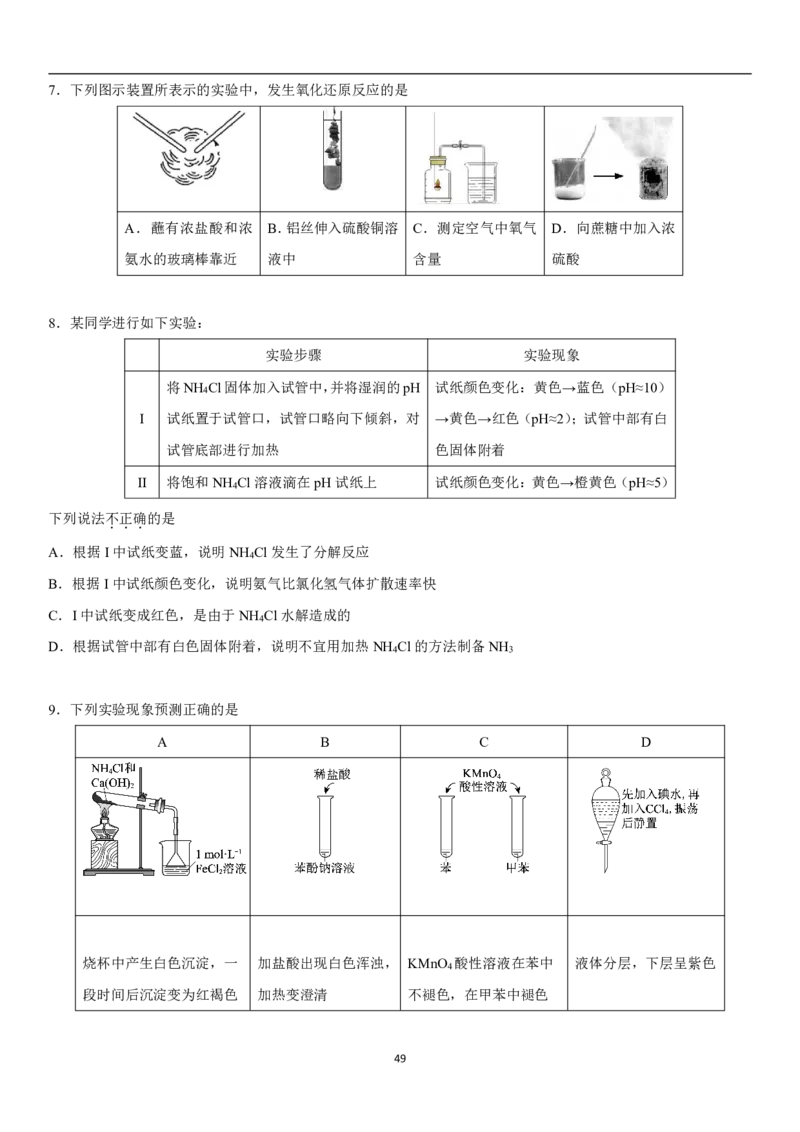
487.下列图示装置所表示的实验中,发生氧化还原反应的是
A.蘸有浓盐酸和浓 B.铝丝伸入硫酸铜溶 C.测定空气中氧气 D.向蔗糖中加入浓
氨水的玻璃棒靠近 液中 含量 硫酸
8.某同学进行如下实验:
实验步骤 实验现象
将NH Cl固体加入试管中,并将湿润的pH 试纸颜色变化:黄色→蓝色(pH≈10)
4
I 试纸置于试管口,试管口略向下倾斜,对 →黄色→红色(pH≈2);试管中部有白
试管底部进行加热 色固体附着
II 将饱和NH Cl溶液滴在pH试纸上 试纸颜色变化:黄色→橙黄色(pH≈5)
4
下列说法不正确的是
...
A.根据I中试纸变蓝,说明NH Cl发生了分解反应
4
B.根据I中试纸颜色变化,说明氨气比氯化氢气体扩散速率快
C.I中试纸变成红色,是由于NH Cl水解造成的
4
D.根据试管中部有白色固体附着,说明不宜用加热NH Cl的方法制备NH
4 3
9.下列实验现象预测正确的是
A B C D
烧杯中产生白色沉淀,一 加盐酸出现白色浑浊, KMnO 酸性溶液在苯中 液体分层,下层呈紫色
4
段时间后沉淀变为红褐色 加热变澄清 不褪色,在甲苯中褪色
4910.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl 液中需加入少量铁屑,其目的
2
是 。
(2)甲组同学取2mlFeCl 溶液。加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将Fe2+氧化。FeCl
2 2 2
溶液与氯水反应的离子方程式为 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl 溶液中先加入0.5ml煤油,再于液面下依次加入几
2
滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
。
(4)丙组同学取10mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl 溶液混合。分别取2mL此溶液于3 支试管中进行如
3
下实验:
① 第一支试管中加入1mLCCl 充分振荡、静置,CCl 层呈紫色;
4 4
② 第二只试管中加入1滴K [Fe(CN) ] 溶液,生成蓝色沉淀;
3 6
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是__ ___(填离子符号);实验①和③说明:在I—过量的情况
下,溶液中仍含有_ _____(填离子符号),由此可以证明该氧化还原反应
为 。
(5)丁组同学向盛有H O 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离子方程式
2 2 2
为 ;一段时间后,溶液中有气泡出现,
并放热。随后有红褐色沉淀生成。产生气泡的原因
是 ;
生成沉淀的原因是
(用平衡移动原理解释)。
11.一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是 。
(2)推测A中可能含有的金属阳离子:①Fe3+;②只有Fe2+;③ 。
甲同学为探究溶液的组成,实验如下:
实验步骤 实验现象 实验结论及反应离子方程式
假设②不成立,假设①或③成立;
取少量溶液A于试管中,
反应的离子方程式是:
加入KSCN溶液。
(3)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO =2KCl+2MnCl +5Cl ↑+8H O
4 2 2 2
实验过程:另取少量溶液A于试管中,逐滴加入酸性KMnO 溶液,充分振荡,KMnO 紫色褪去。实验结论:
4 4
(填写字母序号)。
a.可能有Fe2+ b.可能无Fe2+ c.一定有Fe2+
根据你选择的实验结论,简述理由: 。
5012.为了探究NH 的催化氧化反应,某小组同学按下图装置进行实验。A、B装置内可选药品有:浓氨水、HO、蒸
3 2 2
馏水、NaOH固体、MnO 。
2
(1)NH 催化氧化的化学方程式是 。
3
(2)甲乙两同学分别按上述装置进行实验。一段时间后,装置G中溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是 。
②乙观察到装置F中只有白烟生成,白烟的成分是(写化学式) 。
③用离子方程式解释装置G中溶液变成蓝色的原因: 。
(3)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进。
①甲认为可调节K 和K 控制A、B装置中的产气量,应(填“增加”或“减少”)
1 2
装置A中的产气量,或(填“增加”或“减少”) 装置B中的产气量。
②乙认为可在装置E、F间增加一个装置,该装置可以是(填序号) 。
无机物性质练习二
1.下列实验操作和现象得出的结论正确的是
实验操作 现象 结论
A 将某溶液与稀盐酸反应产生的 石灰水变浑浊 该溶液中一定含有CO 2-
3
气体通入澄清石灰水
B 常温下,将铁片浸入足量浓硫酸 铁片不溶解 常温下,铁与浓硫酸中钝化
中
C 向某食盐溶液中滴加淀粉溶液 溶液颜色不变 该食盐中一定没有添加碘酸钾
D 向苯酚钠溶液中滴加乙酸溶液 溶液变浑浊 相同条件下,乙酸的酸性一定比
苯酚强
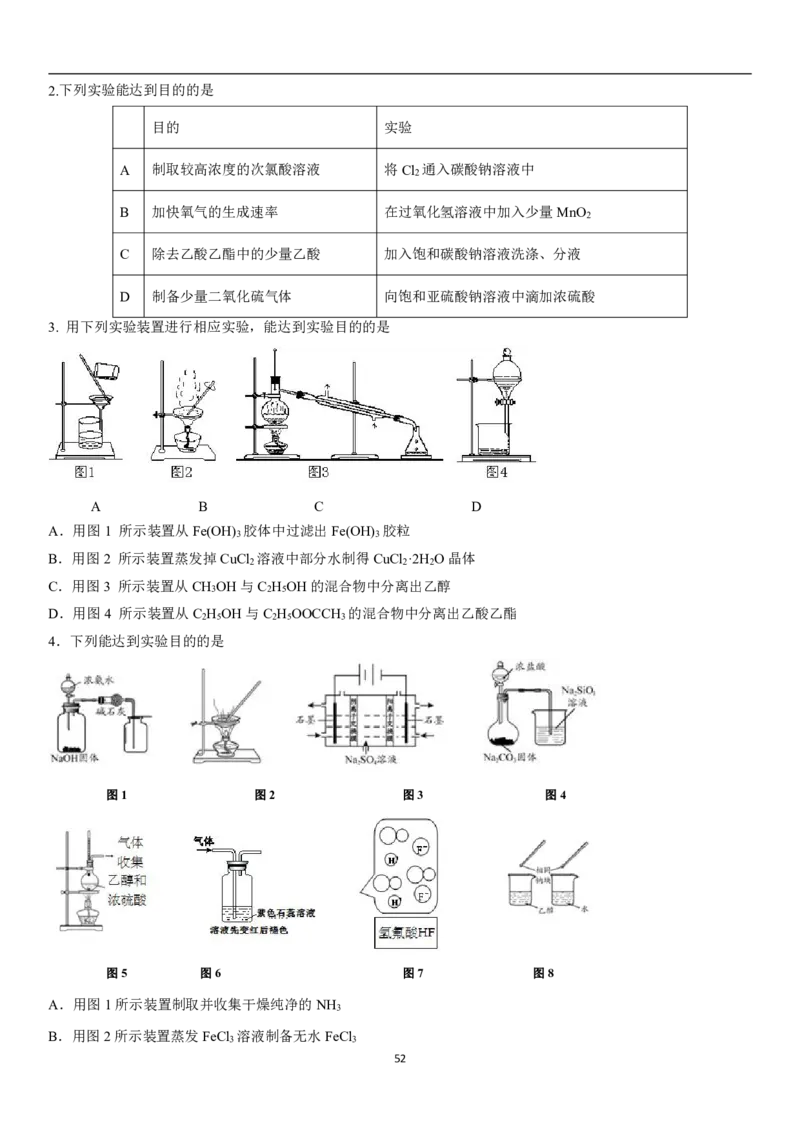
512.下列实验能达到目的的是
目的 实验
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸
3. 用下列实验装置进行相应实验,能达到实验目的的是
A B C D
A.用图1 所示装置从Fe(OH) 胶体中过滤出Fe(OH) 胶粒
3 3
B.用图2 所示装置蒸发掉CuCl 溶液中部分水制得CuCl ·2H O晶体
2 2 2
C.用图3 所示装置从CH OH与C H OH的混合物中分离出乙醇
3 2 5
D.用图4 所示装置从C H OH与C H OOCCH 的混合物中分离出乙酸乙酯
2 5 2 5 3
4.下列能达到实验目的的是
图1 图2 图3 图4
图5 图6 图7 图8
A.用图1所示装置制取并收集干燥纯净的NH
3
B.用图2所示装置蒸发FeCl 溶液制备无水FeCl
3 3
52C.用图3所示装置制硫酸和氢氧化钠
D.用图4所示装置比较HCl、H CO 和H SiO 的酸性强弱
2 3 2 3
E.图5利用乙醇的消去反应制取乙烯
F. 图6验证该气体可能为SO
2
G. 图7 说明HF为弱电解质
H.图8比较乙醇中羟基氢原子和水分子中氢原子的活泼性
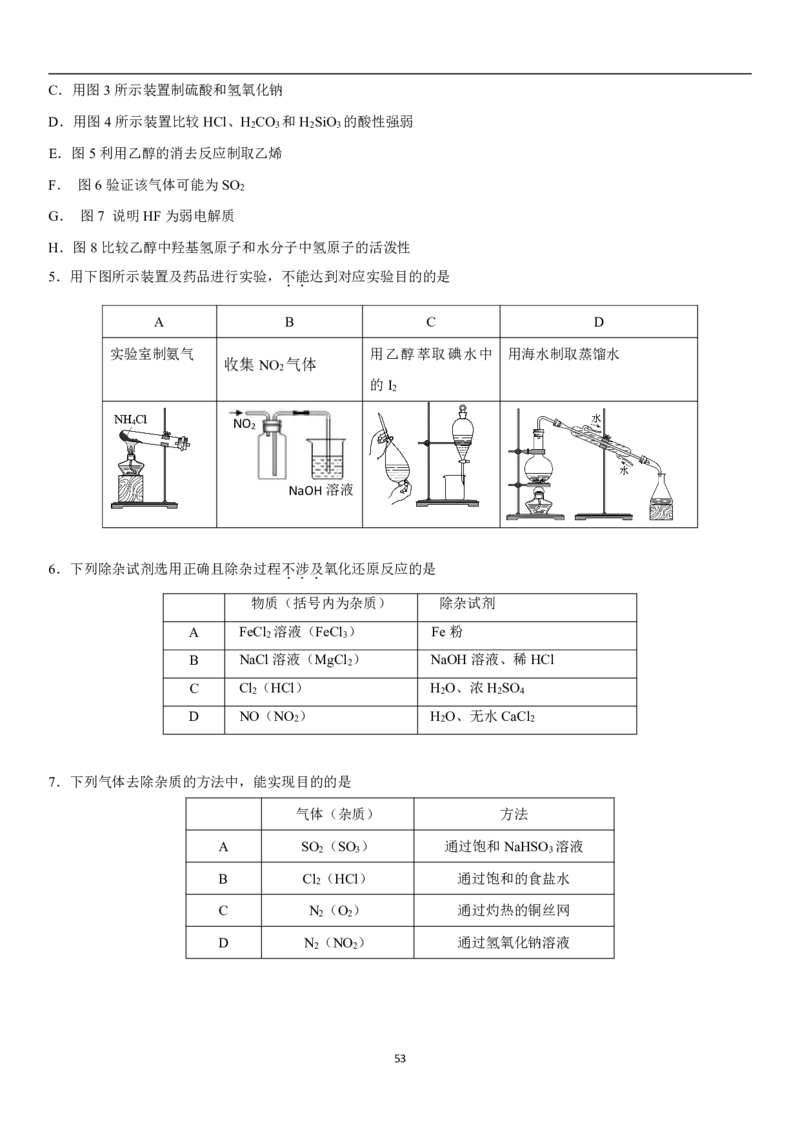
5.用下图所示装置及药品进行实验,不
.
能
.
达到对应实验目的的是
A B C D
实验室制氨气 用乙醇萃取碘水中 用海水制取蒸馏水
收集NO 气体
2
的I
2
NO
2
NaOH溶液
6.下列除杂试剂选用正确且除杂过程不
.
涉
.
及
.
氧化还原反应的是
物质(括号内为杂质) 除杂试剂
A FeCl 2 溶液(FeCl 3 ) Fe粉
B NaCl溶液(MgCl 2 ) NaOH溶液、稀HCl
C Cl 2 (HCl) H 2 O、浓H 2 SO 4
D NO(NO 2 ) H 2 O、无水CaCl 2
7.下列气体去除杂质的方法中,能实现目的的是
气体(杂质) 方法
A SO (SO ) 通过饱和NaHSO 溶液
2 3 3
B Cl (HCl) 通过饱和的食盐水
2
C N (O ) 通过灼热的铜丝网
2 2
D N (NO ) 通过氢氧化钠溶液
2 2
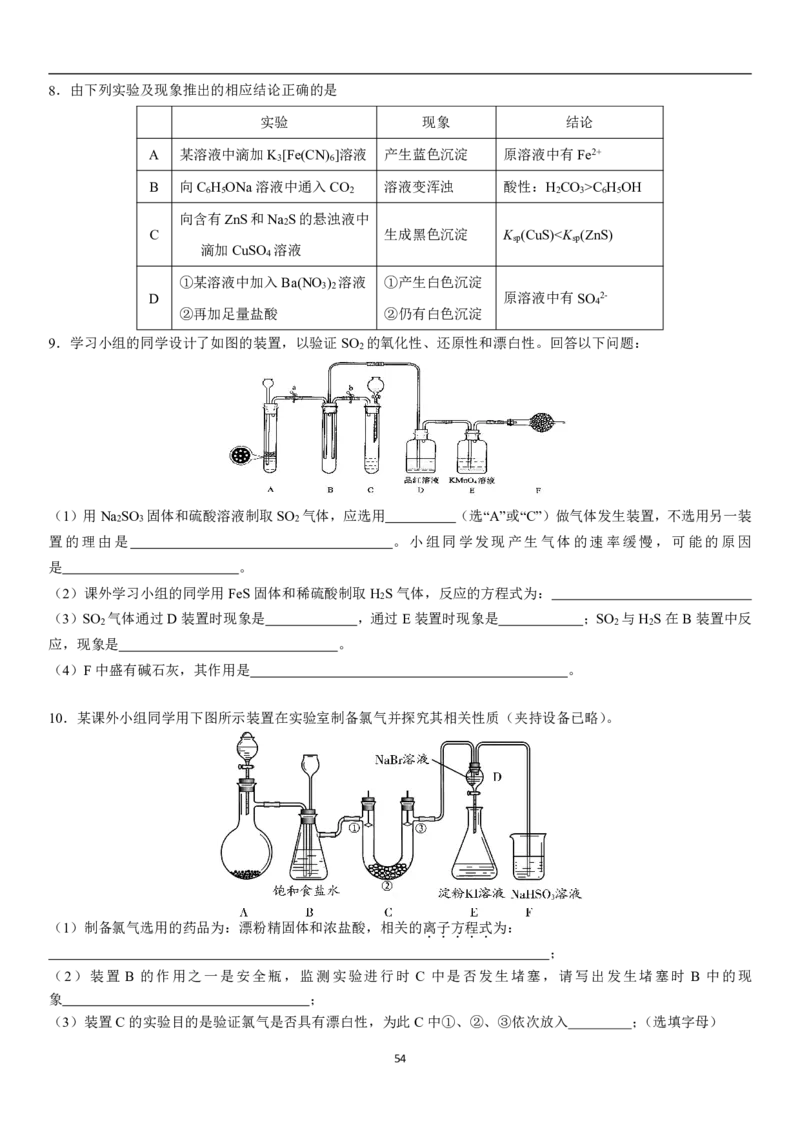
538.由下列实验及现象推出的相应结论正确的是
实验 现象 结论
A 某溶液中滴加K [Fe(CN) ]溶液 产生蓝色沉淀 原溶液中有Fe2+
3 6
B 向C H ONa溶液中通入CO 溶液变浑浊 酸性:H CO >C H OH
6 5 2 2 3 6 5
向含有ZnS和Na S的悬浊液中
2
C 生成黑色沉淀 K (CuS)H CO , NaHCO +H C O =NaHC O +CO ↑+H O
2 2 4 2 3 3 2 2 4 2 4 2 2
C.H C O 有还原性,2MnO -+5C O 2-+16H+=2Mn2++10CO ↑+8H O
2 2 4 4 2 4 2 2
D.H C O 可发生酯化反应,HOOCCOOH+2C H OH C H OOCCOOC H 2H O
2 2 4 2 5 2 5 2 5 2
3.下列实验操作或装置不
.
能
.
达到目的的是
酸性高锰
酸钾溶液
C.检验 CH CH Br
3 2
A.实验室制取乙酸 B. 用CuSO 溶液 D.证明乙醇与浓硫
4
消去反应的产物
乙酯 除去H S和PH 等杂质 酸共热生成乙烯
2 3
乙烯
4.下列制备实验能成功的是
A.将冰醋酸、乙醇和浓硫酸混合共热制取乙酸乙酯
B.将乙醇和3mol/L硫酸按体积比1:3混和共热至170℃制乙烯
C.检验CH CH Br中的溴元素,加AgNO 溶液产生淡黄色沉淀
3 2 3
D.用苯、液溴和还原铁粉制溴苯
575.下列有关除去杂质(括号内物质)的操作中,正确的是
A.FeCl (FeCl ):加入过量铁粉振荡,然后过滤
2 3
B.苯(苯酚):加入NaOH溶液振荡,然后分液
C.乙醛(乙酸):加入新制的生石灰,然后蒸馏
D.乙酸乙酯(乙酸):加入稀硫酸,然后加热
6.混合物的提纯,括号内为杂质。
混合物 除杂试剂 操作方法
C H (C H )
2 6 2 4
C H (SO )
2 4 2
苯(苯酚)
苯(甲苯)
肥皂溶液(甘油)
溴苯(溴)
硝基苯(混酸)
乙醛(乙酸)
乙醇(乙酸)
乙酸乙酯(乙酸)
石油
7. 实验室常用右图装置制备乙炔气体。
(1)CaC 中含有的化学键类型是 ,
2
乙炔的电子式是 。
(2)制备乙炔的化学方程式是 。
(3)洗气瓶的作用是除去乙炔中含有的臭味的H S杂质,
2
洗气瓶中反应的离子方程式是
。
(4)欲证明乙炔分子中 3 个碳碳键中有 2 个碳碳键的性质和另外 1 个碳碳键的性质不同,应选用的化学试剂
是 。
(5)利用不饱和烃通过加聚反应可以合成高分子。下图为其中一种高分子膜的片段:
该高分子的单体是 。
588.实验室制备苯甲醇和苯甲酸的化学原理是:
O
C H CH OH COOK
2 + KOH 2 +
COOK COOH
+HCl + KCl
已知苯甲醛易被空气氧化:苯甲醇沸点为205.3℃;苯甲酸熔点121.7℃,沸点为249℃,溶解度为0.34g;乙醚
(C H OC H )沸点为34.8℃,难溶于水,制备苯甲醇和苯甲酸的主要过程如下所示:
2 5 2 5
(1)操作I的名称是 ,乙醚溶液中所溶解的主要成份是 。
(2)操作II的名称是 。
(3)操作Ⅲ 的名称是 ,产品乙是 。
(4)操作II中温度计水银球上沿x放置的位置应为 (图a、b、c或d),该操作中,
除需带支管烧瓶、温度计外,还需的玻璃仪器是 ,收集产品甲的适宜温度
为 。
9.某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
(1)制备粗品。
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应
完全,在试管C内得到环己烯粗品。
① A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是 。
② 试管C置于冰水浴中的目的是 。
(2)制备精品。
① 环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己
烯在 层(填上或下),分液后用 (填入编号)洗涤。
a.KMnO 溶液 b.稀H SO c.Na CO 溶液
4 2 4 2 3
② 再将环己烯按右图装置蒸馏,冷却水从 口进入,目的是 。
(3)以下区分环己烯精品和粗品的方法,合理的是 。
a.用酸性高锰酸钾溶液 b.用氢氧化钠 c.测定沸点
59高三实验板块复习——制备专题习题
1.用所给试剂与图示装置能够制取相应气体的是(加热及夹持仪器略)
A B C D
酸性高锰酸
X中试剂 稀硝酸 双氧水 浓氨水
钾溶液
Y中试剂 Cu MnO MnO NaOH
2 2
气体 NO Cl O NH
2 2 3
2.利用下图装置可以进行实验并能达到实验目的的是
实验目的 X中试剂 Y中试剂
A MnO 和浓盐酸制取并收集纯净干燥Cl 饱和食盐水 浓硫酸
2 2
B Cu与稀硝酸制取并收集纯净干燥的NO 水 浓硫酸
验证电石与饱和食盐水反应生成的气体
C CuSO 溶液 KMnO 溶液
4 4
的性质并收集
CaCO 和稀盐酸制取并收集纯净干燥的
3
D 饱和NaHCO 溶液 浓硫酸
3
CO
2
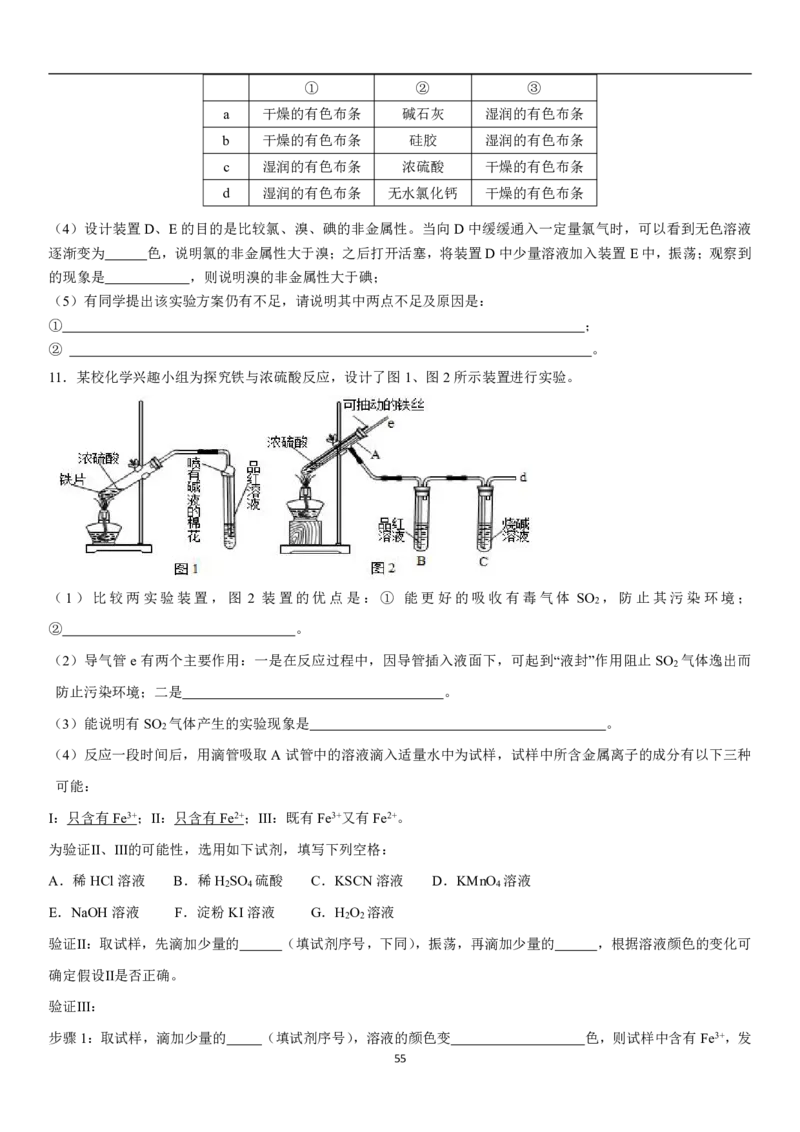
3. 下表所列实验探究,利用右图所示实验装置,能得出相应实验结论的是
① ② ③ 实验结论
A 水 电石 CuSO 溶液 乙炔具有还原性
4
B 浓硝酸 Cu KI-淀粉溶液 氧化性:NO >KI
2
C 浓盐酸 KMnO
4
KI-淀粉溶液 氧化性:KMnO
4
>Cl
2
>I
2
D 稀硫酸 Na 2 S AgNO 3 与AgCl的浊液 溶解度:AgCl>Ag 2 S
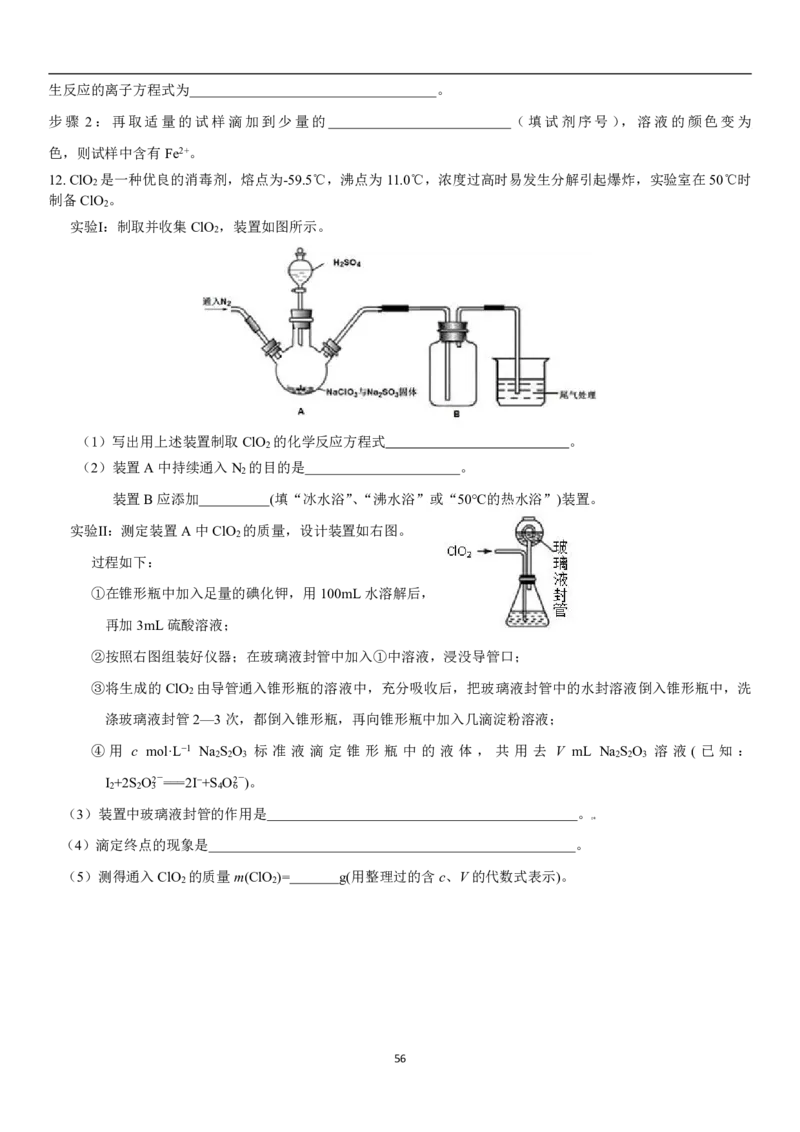
4.利用下列各组中的物质制备并收集少量相应的气体,能采用右图装置的是
① 浓氨水和固体NaOH制NH ; ② 大理石和稀盐酸制CO ;
3 2
③ 过氧化氢溶液和二氧化锰制O ; ④ 稀硝酸和铜片制NO;
2
⑤ 浓盐酸和二氧化锰制Cl ; ⑥ 电石和水制C H ;
2 2 2
⑦ 锌粒和稀硫酸制H ; ⑧ 乙醇和浓硫酸制C H 。
2 2 4
A.②③ B.①⑥⑦ C.②⑤⑧ D.①④⑥
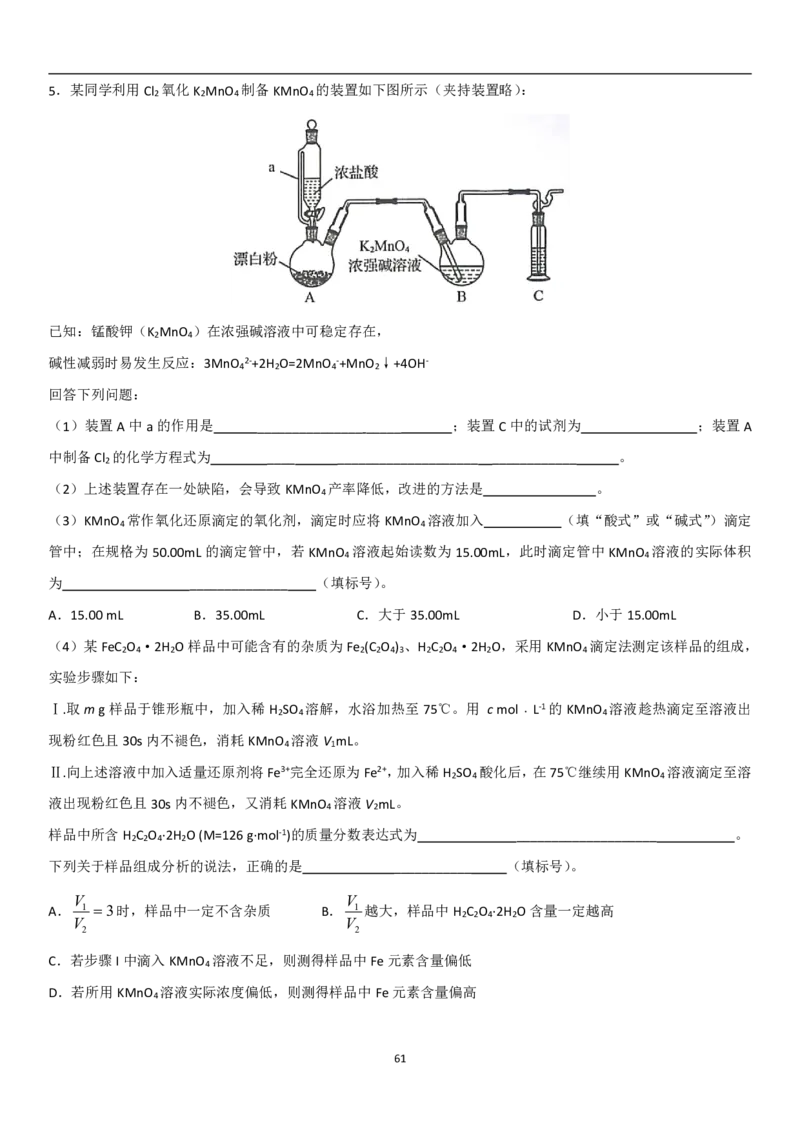
605.某同学利用Cl 氧化K MnO 制备KMnO 的装置如下图所示(夹持装置略):
2 2 4 4
已知:锰酸钾(K MnO )在浓强碱溶液中可稳定存在,
2 4
碱性减弱时易发生反应:3MnO 2-+2H O=2MnO -+MnO ↓+4OH-
4 2 4 2
回答下列问题:
(1)装置A中a的作用是 ____________________ ;装置C中的试剂为 ;装置A
中制备Cl 的化学方程式为 ____ ____________________ ____________ 。
2
(2)上述装置存在一处缺陷,会导致KMnO 产率降低,改进的方法是 。
4
(3)KMnO 常作氧化还原滴定的氧化剂,滴定时应将KMnO 溶液加入 (填“酸式”或“碱式”)滴定
4 4
管中;在规格为50.00mL的滴定管中,若KMnO 溶液起始读数为15.00mL,此时滴定管中KMnO 溶液的实际体积
4 4
为 ______________ (填标号)。
A.15.00mL B.35.00mL C.大于35.00mL D.小于15.00mL
(4)某FeC O ·2H O样品中可能含有的杂质为Fe (C O ) 、H C O ·2H O,采用KMnO 滴定法测定该样品的组成,
2 4 2 2 2 4 3 2 2 4 2 4
实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀H SO 溶解,水浴加热至75℃。用 cmol﹒L-1的KMnO 溶液趁热滴定至溶液出
2 4 4
现粉红色且30s内不褪色,消耗KMnO 溶液V mL。
4 1
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H SO 酸化后,在75℃继续用KMnO 溶液滴定至溶
2 4 4
液出现粉红色且30s内不褪色,又消耗KMnO 溶液V mL。
4 2
样品中所含H C O ·2H O(M=126g·mol-1)的质量分数表达式为 ____________________ 。
2 2 4 2
下列关于样品组成分析的说法,正确的是 ___________ (填标号)。
V V
A. 1 3时,样品中一定不含杂质 B. 1 越大,样品中H C O ·2H O含量一定越高
2 2 4 2
V V
2 2
C.若步骤I中滴入KMnO 溶液不足,则测得样品中Fe元素含量偏低
4
D.若所用KMnO 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
4
616.水合肼(N H ·H O)可用作抗氧剂等,工业上常用尿素[CO(NH ) ]和NaClO溶液反应制备水合肼。
2 4 2 2 2
已知:Ⅰ.N H ·H O的结构如右图(…表示氢键)。
2 4 2
Ⅱ.N H ·H O沸点118℃,具有强还原性。
2 4 2
(1)将Cl 通入过量NaOH溶液中制备NaClO,得到溶液X,离子方程式是_______。
2
(2)制备水合肼:将溶液X滴入尿素水溶液中,控制一定温度,装置如图a(夹持及控温装置已略)。充分反应
后,A 中的溶液经蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品 NaCl 和
Na CO ·10H O。
2 3 2
图a 图b
①A中反应的化学方程式是______。
②冷凝管的作用是______。
③若滴加NaClO溶液的速度较快时,水合肼的产率会下降,原因是______。
④NaCl和Na CO 的溶解度曲线如图b。由蒸馏后的剩余溶液获得NaCl粗品的操作是______。
2 3
(3)水合肼在溶液中可发生类似NH ·H O的电离,呈弱碱性;其分子中与N原子相连的H原子易发生取代
3 2
反应。
①水合肼和盐酸按物质的量之比1∶1反应的离子方程式是______。
②碳酰肼(CH N O)是目前去除锅炉水中氧气的最先进材料,由水合肼与DEC( )发
6 4
生取代反应制得。碳酰肼的结构简式是______。
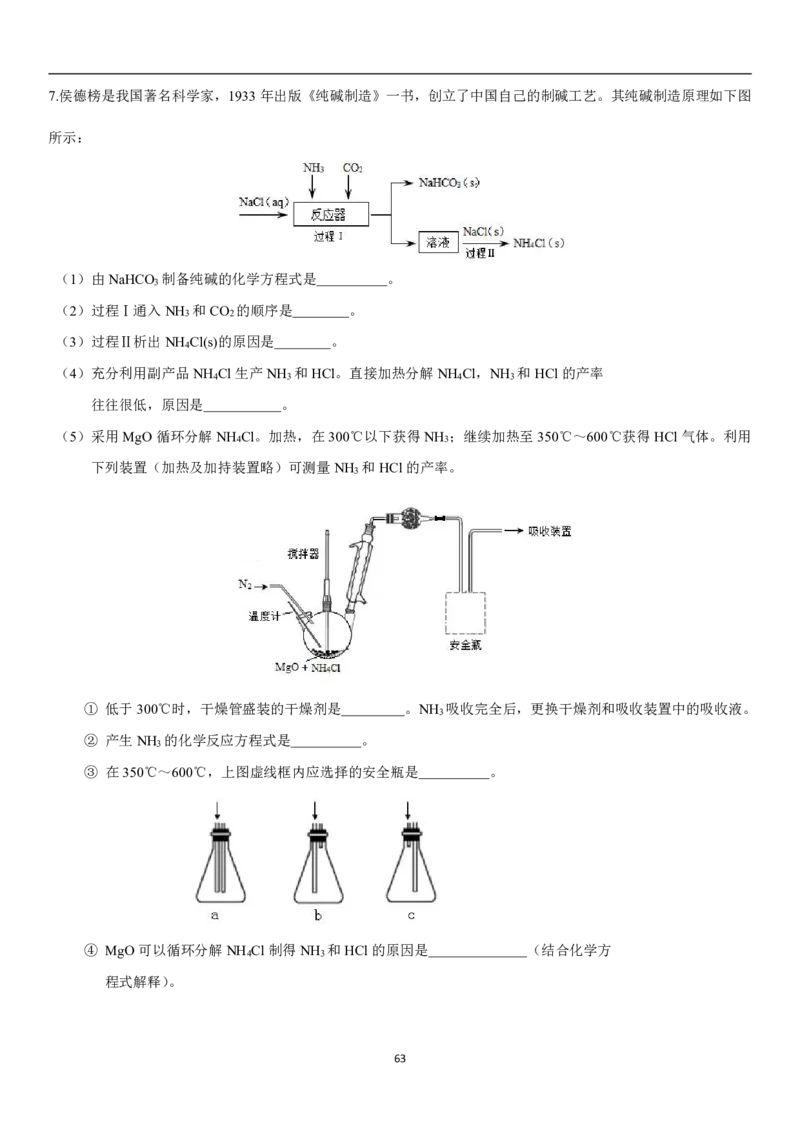
627.侯德榜是我国著名科学家,1933年出版《纯碱制造》一书,创立了中国自己的制碱工艺。其纯碱制造原理如下图
所示:
(1)由NaHCO 制备纯碱的化学方程式是 。
3
(2)过程Ⅰ通入NH 和CO 的顺序是 。
3 2
(3)过程Ⅱ析出NH Cl(s)的原因是 。
4
(4)充分利用副产品NH Cl生产NH 和HCl。直接加热分解NH Cl,NH 和HCl的产率
4 3 4 3
往往很低,原因是 。
(5)采用MgO循环分解NH Cl。加热,在300℃以下获得NH ;继续加热至350℃~600℃获得HCl气体。利用
4 3
下列装置(加热及加持装置略)可测量NH 和HCl的产率。
3
① 低于300℃时,干燥管盛装的干燥剂是 。NH 吸收完全后,更换干燥剂和吸收装置中的吸收液。
3
② 产生NH 的化学反应方程式是 。
3
③ 在350℃~600℃,上图虚线框内应选择的安全瓶是 。
④ MgO可以循环分解NH Cl制得NH 和HCl的原因是 (结合化学方
4 3
程式解释)。
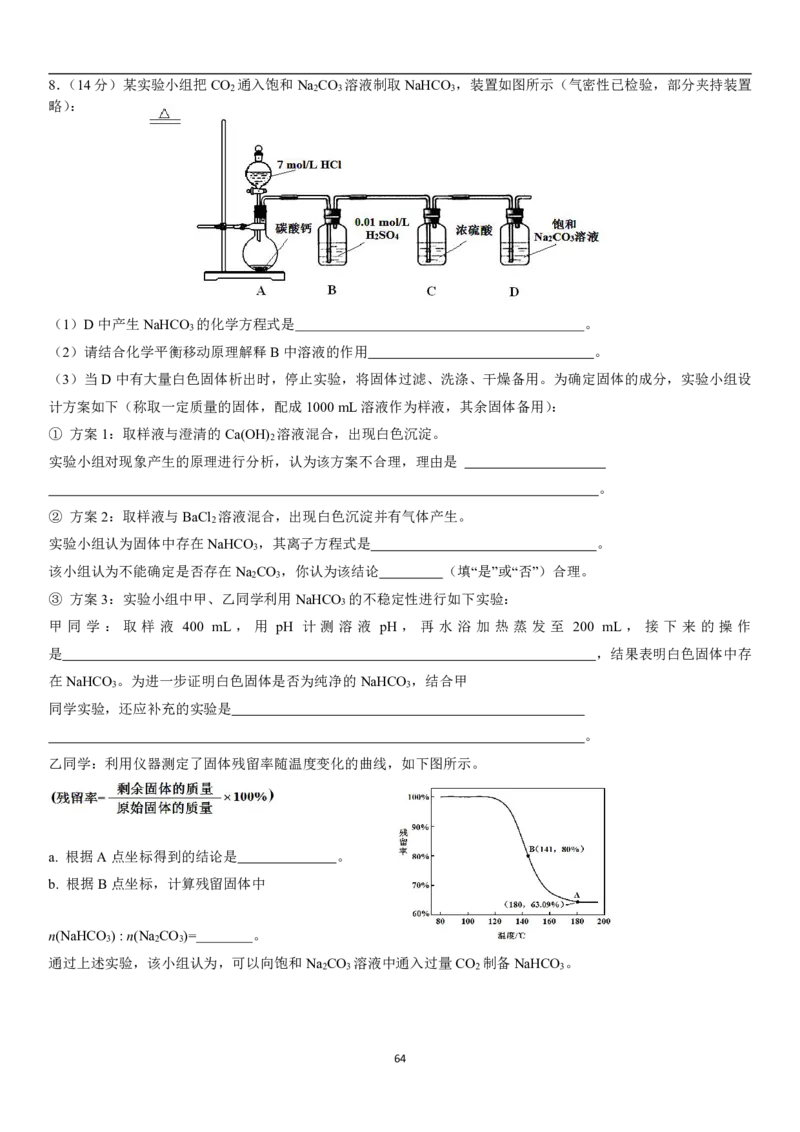
638.(14分)某实验小组把CO 通入饱和Na CO 溶液制取NaHCO ,装置如图所示(气密性已检验,部分夹持装置
2 2 3 3
略):
(1)D中产生NaHCO 的化学方程式是 。
3
(2)请结合化学平衡移动原理解释B中溶液的作用 。
(3)当D中有大量白色固体析出时,停止实验,将固体过滤、洗涤、干燥备用。为确定固体的成分,实验小组设
计方案如下(称取一定质量的固体,配成1000mL溶液作为样液,其余固体备用):
① 方案1:取样液与澄清的Ca(OH) 溶液混合,出现白色沉淀。
2
实验小组对现象产生的原理进行分析,认为该方案不合理,理由是
。
② 方案2:取样液与BaCl 溶液混合,出现白色沉淀并有气体产生。
2
实验小组认为固体中存在NaHCO ,其离子方程式是 。
3
该小组认为不能确定是否存在Na CO ,你认为该结论 (填“是”或“否”)合理。
2 3
③ 方案3:实验小组中甲、乙同学利用NaHCO 的不稳定性进行如下实验:
3
甲 同 学 : 取 样 液 400 mL , 用 pH 计 测 溶 液 pH , 再 水 浴 加 热 蒸 发 至 200 mL , 接 下 来 的 操 作
是 ,结果表明白色固体中存
在NaHCO 。为进一步证明白色固体是否为纯净的NaHCO ,结合甲
3 3
同学实验,还应补充的实验是
。
乙同学:利用仪器测定了固体残留率随温度变化的曲线,如下图所示。
a. 根据A点坐标得到的结论是 。
b. 根据B点坐标,计算残留固体中
n(NaHCO ):n(Na CO )= 。
3 2 3
通过上述实验,该小组认为,可以向饱和Na CO 溶液中通入过量CO 制备NaHCO 。
2 3 2 3
64高三实验板块复习——原理专题习题
一、催化剂对化学反应速率的影响
1.有X、Y、Z三种物质。常温下分别用Y或Z与X混合时,反应速率几乎相同的是
X Y Z
A 2mL5%H O 溶液 1mL1mol·L-1CuSO 溶液 1mL1mol·L-1FeCl 溶液
2 2 4 3
B 1mL1mol·L-1NaHCO 3 溶液 1mL1mol·L-1HCl溶液 1mL0.5mol·L-1H 2 SO 4 溶液
C 钠块 10mL 乙醇 10mL 水
D 经过酸洗除锈的铁钉 5mL 海水 5mL 蒸馏水
2.下列说法正确的是
能量 pH n(Mn2+) V(H 2 ) a
13
b
2NO2(g)+O3(g)
7
N2O5(g)+O2(g)
反应过程 0 20 V(酸)/mL 0 时间 0 t
① ② ③ ④
A.①表示化学反应2NO (g)+O (g) N O (g)+O (g) △H < 0
2 3 2 5 2
B.②表示25℃时,用0.1mol/LCH COOH溶液滴定20mL0.1mol/LNaOH溶液,溶液的pH随加入酸体积的变化
3
C.③表示10mL0.01mol/L KMnO 酸性溶液与过量的0.1mol/LH C O 溶液混合时,n(Mn2+)随时间的变化
4 2 2 4
D.④表示体积和pH均相同的HCl和CH COOH两种溶液中,分别加入足量的锌,产生H 的体积随时间的变化,
3 2
则a表示CH COOH溶液
3
3.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO +5H C O +3H SO ===K SO +2MnSO +10CO ↑+8H O
4 2 2 4 2 4 2 4 4 2 2
【实验内容及记录】
室温下,试管中所加试剂及其用量 /mL
实验 室温下溶液颜色褪至
0.6mol/L H O 0.2mol/L 3mol/L
编号 2 无色所需时间 /min
H C O 溶液 KMnO 溶液 稀硫酸
2 2 4 4
1 3.0 2.0 3.0 2.0 4.0
2 3.0 3.0 2.0 2.0 5.2
3 3.0 4.0 1.0 2.0 6.4
(1)根据上表中的实验数据,可以得到的结论是 。
(2)利用实验1中数据计算,用KMnO 的浓度变化表示的反应速率为:υ(KMnO )= 。
4 4
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发
现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的图假设是 图 。
65②请你帮助该小组同学完成实验方案,并填写表中空白。
实验 室温下,试管中所加试剂及其用量 /mL 再向试管 室温下溶液颜色
编号 0.6mol/L H O 0.2mol/L 3mol/L 中加入少 褪至无色所需时
2
H C O 溶液 KMnO 溶液 稀硫酸 量固体 间 /min
2 2 4 4
4 3.0 2.0 3.0 2.0 t
③若该小组同学提出的假设成立,应观察到的现象是 。
4.某小组同学查到一份研究过氧化氢溶液与氢碘酸(HI)反应的实验资料,具体如下。
资料1∶室温下,
过氧化氢溶液可与氢碘酸反应∶H O +2HI=I +2H O
2 2 2 2
资料2∶碘单质溶于水后,溶液为棕黄色。
资料3∶实验数据见下表。
实验编号 ① ② ③ ④ 5
c(H O )/(mol/L) 0.1 0.1 0.1 0.2 0.3
2 2
c(H O )/(mol/L) 0.1 0.2 0.3 0.1 0.1
2 2
从混合到出现棕黄色的时间/(s) 13 6.5 4.3 6.6 4.4
(1)通过资料3中的数据,可以得出的结论是 。
(2)资料3中编号为①的实验中反应继续进行,20s后测得过氧化氢的浓度为0.08mol/L,则v(HI)=_____。
(3)该小组同学欲用碘化钾替代氢碘酸验证上述实验结论。在实验过程中,未观察到溶液变为棕黄色。却观察到
有无色气体产生。于是,小组同学提出假设∶碘化钾可能是过氧化氢分解反应的催化剂。
①该小组同学提出上述假设的依据是 。
②请设计实验方案验证∶碘化钾能提高过氧化氢分解反应的速率(仪器和试剂可自选)。
实验方案∶
二、浓度对化学平衡的影响
5.下列各项中“操作或现象”能达到预期“实验目的”的是
实验目的 操作或现象
检验碳与浓硫酸反应后的气 将产生的气体依次通过无水CuSO 、品红溶液和澄清石灰水(每
4
A
体产物 一步气体均完全反应)
证明蛋白质在某些无机盐溶 向鸡蛋清溶液中加入饱和硫酸钠溶液,有沉淀析出;再把沉淀加
B
液作用下发生盐析 入蒸馏水中
将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,向上层
C 检验溴乙烷中的溴元素
清液中加稀HNO 酸化,再滴加AgNO 溶液
3 3
证明溶液中存在平衡: 将1mLKSCN溶液与1mL 同浓度 FeCl 溶液充分混合;再继续
3
D
Fe3++3SCN- Fe(SCN) 加入FeCl 溶液,溶液颜色加深
3 3
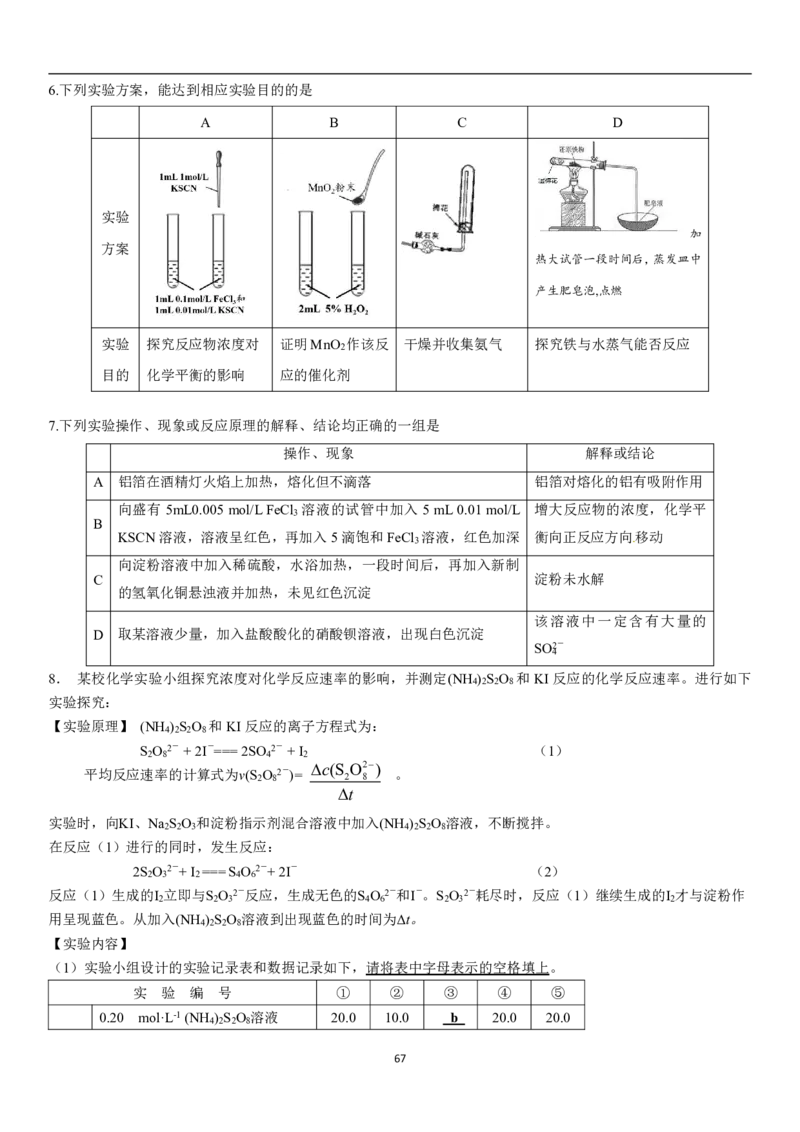
666.下列实验方案,能达到相应实验目的的是
A B C D
实验
加
方案
热大试管一段时间后,蒸发皿中
产生肥皂泡,点燃
实验 探究反应物浓度对 证明MnO 作该反 干燥并收集氨气 探究铁与水蒸气能否反应
2
目的 化学平衡的影响 应的催化剂
7.下列实验操作、现象或反应原理的解释、结论均正确的一组是
操作、现象 解释或结论
A 铝箔在酒精灯火焰上加热,熔化但不滴落 铝箔对熔化的铝有吸附作用
向盛有 5mL0.005 mol/LFeCl 溶液的试管中加入 5 mL0.01 mol/L 增大反应物的浓度,化学平
3
B
KSCN溶液,溶液呈红色,再加入5滴饱和FeCl 溶液,红色加深 衡向正反应方向移动
3
向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制
C 淀粉未水解
的氢氧化铜悬浊液并加热,未见红色沉淀
该溶液中一定含有大量的
D 取某溶液少量,加入盐酸酸化的硝酸钡溶液,出现白色沉淀
SO2-
4
8. 某校化学实验小组探究浓度对化学反应速率的影响,并测定(NH ) S O 和KI反应的化学反应速率。进行如下
4 2 2 8
实验探究:
【实验原理】 (NH ) S O 和KI反应的离子方程式为:
4 2 2 8
S O 2- +2I-===2SO 2- +I (1)
2 8 4 2
平均反应速率的计算式为v(S 2 O 8 2 -)= c(S 2 O 8 2) 。 kcx(S O2)cy(I)
t 2 8
实验时,向KI、Na S O 和淀粉指示剂混合溶液中加入(NH ) S O 溶液,不断搅拌。
2 2 3 4 2 2 8
在反应(1)进行的同时,发生反应:
2S O 2-+I ===S O 2-+2I- (2)
2 3 2 4 6
反应(1)生成的I 立即与S O 2-反应,生成无色的S O 2-和I-。S O 2-耗尽时,反应(1)继续生成的I 才与淀粉作
2 2 3 4 6 2 3 2
用呈现蓝色。从加入(NH ) S O 溶液到出现蓝色的时间为Δt。
4 2 2 8
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
实 验 编 号 ① ② ③ ④ ⑤
0.20 mol·L-1(NH ) S O 溶液 20.0 10.0 b 20.0 20.0
4 2 2 8
670.20 mol·L-1KI溶液 20.0 20.0 20.0 10.0 5.0
试剂 0.010 mol·L-1Na S O 溶液 a 8.0 8.0 8.0 8.0
2 2 3
用量 0.2% 淀粉溶液 2.0 2.0 2.0 2.0 2.0
(mL) 0.20 mol·L-1KNO 溶液 0 0 0 10.0 c
3
0.20 mol·L-1(NH ) SO 溶液 0 10.0 15.0 0 0
4 2 4
20℃时,反应时间Δt(s) 32 67 130 66 135
为了使溶液的离子强度和总体积保持不变,减少的(NH ) S O 溶液或KI溶液的用量,
4 2 2 8
分别用(NH ) SO 溶液或KNO 溶液补足;溶液混合后体积不变
4 2 4 3
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是
。
(3)第①组实验的v(S O 2-)= mol·(L·s)-1。
2 8
(4) 根据上表数据分析,可以得到的结论有(写出一条即可) 。
三、温度对化学平衡的影响
9.根据下列图示的实验操作,能实现实验目的的是
A.目的:浓度对化学反应速率的影响 B.目的:温度对化学平衡的影响
均为1mL2mol/L 硫酸硫酸
2mLNa S O 溶液 1mLNa S O 溶液+1mL水
2 2 3 2 2 3
(Na S O 溶液浓度均为 0.1mol·L-1 ) 试剂:烧瓶中各充入等质量的NO
2 2 3 2
C.目的:探究醋酸、碳酸、苯酚溶液的酸性强弱 D.目的:鉴别碳酸钠和碳酸氢钠
醋酸 CO 均为澄清石灰水
2
1mol/LNaHCO 溶液 1mol/L苯酚钠溶液 0.1mol/LNa CO 溶液 0.1mol/L NaHCO 溶液
3 2 3 3
四、难溶电解质溶解平衡 沉淀的溶解
10.已知Mg(OH) 能溶于浓度均为3mol/L的①盐酸、②NH Cl溶液、③CH COONH 溶液(中
2 4 3 4
性),下列说法正确的是
68A.c(NH +): ②>③ B.pH:①>②>③
4
C.Mg(OH) 溶于②的主要原因是由于NH +水解使溶液显酸性,导致平衡
2 4
Mg(OH) (s) Mg2+(aq)+2OH-(aq)向溶解方向移动
2
D. 将等体积的①和③混合,所得溶液中 c(Cl-)>c(NH +)>c(H+)>c(CH COO-)>c(OH-)
4 3
11下列实验操作能达到实验目的的是
实验目的 实验操作
A 证明乙烯能发生加成反应 将乙烯气体通入酸性溴水中
证 明 NH Cl 溶 液 能 促 进向两份等量 Mg(OH) 固体中分别加入等体积蒸馏水和
4 2
B
Mg(OH) 固体的溶解 NH Cl溶液
2 4
C 证明Al O 的熔点比Al高 把砂纸打磨过的铝箔在酒精灯上加热到熔化
2 3
将Fe(OH) 胶体过滤后所得滤液置于暗处,再用激光笔照
3
D 证明胶体的分散质能透过滤纸
射滤液
12.下列实验方案不
.
能
.
达到实验目的的是
实验目的 实验方案
A 证明溴乙烷发生消去反应 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将
有乙烯生成 反应产生的气体通入溴的四氯化碳溶液
B 证明 Mg(OH) 沉淀可以转 向2 mL1mol/LNaOH 溶液中先加入 3滴1mol/LMgCl 溶
2 2
化为Fe(OH) 沉淀 液,再加入3滴1mol/LFeCl 溶液
3 3
C 检验蔗糖水解产物具有还 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中
原性 加入新制的银氨溶液,并水浴加热
D 测定铝箔中氧化铝的含量 取ag铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰
后,测其体积为bL(已转化为标准状况下)
13.下列实验“操作和现象”与“结论”对应关系正确的是
操作和现象 结论
处理锅炉水垢中的CaSO 时,依次加入饱和Na CO 溶液和盐 溶解度:
4 2 3
A
酸,水垢溶解 S(CaCO )<S(CaSO )
3 4
B 用石墨作电极电解MgSO 溶液,某电极附近有白色沉淀生成 该电极为阴极
4
C 向FeCl 和CuCl 混合溶液中加入铁粉,有红色固体析出 氧化性:Cu2+>Fe3+
3 2
向某溶液中先滴加硝酸酸化,再滴加BaCl 溶液,有白色沉淀
2
D 该溶液中一定含有Ag+
生成
6914.下列实验能达到预期目的是
实验内容 实验目的
A 向苯和苯酚的混合溶液中加入溴水 除去苯中混有的苯酚
向10mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl 溶液, 证明在相同温度下的溶解
2
B
产生白色沉淀后,再滴加2滴0.1mol/LFeCl 溶液,又生成红褐色沉淀 度:Mg(OH) >Fe(OH)
3 2 3
证明Na CO 溶液中存在水
2 3
C 向含有酚酞的Na CO 溶液中加入少量BaCl 固体,溶液红色变浅
2 3 2
解平衡
D 将浓盐酸加入到碳酸钠溶液中,产生能使澄清石灰水变浑浊的气体 证明非金属性Cl>C
五、金属的腐蚀
15.右图是探究铁发生腐蚀的装置图。发现开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水
柱又上升。下列说法正确的是
A.开始时发生的是析氢腐蚀
B.一段时间后发生的是吸氧腐蚀
红
C.两种腐蚀负极的电极反应均为:Fe-2e-==Fe2+ pH=3的
墨
雨水浸
水
泡过的
D.吸氧腐蚀的总反应为:2Fe+O +2H O==2Fe(OH)
2 2 2 铁钉
16.如图所示的钢铁腐蚀中,下列说法正确的是
① ②
A.碳表面发生还原反应 B.钢铁被腐蚀的最终产物为FeO
C.生活中钢铁制品的腐蚀以图②所示为主 D.图②中,正极反应式为O +4e-+2H O=4OH-
2 2
7017.下述实验方案能达到实验目的的是
A B C D
实验
方案
片刻后在Fe电极附近滴入 置于光亮处
食盐水
K [Fe(CN) ]溶液
3 6
实验 验证铁钉发生 验证甲烷与氯气发生
验证Fe电极被保护 验证乙炔的还原性
目的 吸氧腐蚀 化学反应
18.图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法正确的是
图Ⅰ 图Ⅱ
A.图Ⅰ中a为纯铜 B.图Ⅰ中SO 2—向b极移动
4
C.图Ⅱ中如果a、b间连接电源,则a连接负极
D.图Ⅱ中如果a、b间用导线连接,则X可以是Zn
19.原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错
.
误
.
的是
装置① 装置② 装置③
A.装置①研究的是电解CuCl 溶液,a电极上有红色固体析出
2
B.装置②研究的是金属的吸氧腐蚀,可以观察到右侧导管有一小段液柱
C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl--2e-=Cl ↑
2
D.三个装置中涉及的主要反应都是氧化还原反应
7120.NaCl为主要成分的融雪剂会腐蚀桥梁、铁轨等钢铁设备。某研究小组探究NaCl溶液对钢铁腐蚀的影响。
(1)将滤纸用3.5%的NaCl溶液润湿,涂上铁粉、碳粉的混合物,贴在表面皿上。在滤纸上加几滴检验试剂,再
缓慢加入NaCl溶液至没过滤纸,操作如下所示:
① 实验ⅰ的现象说明,得电子的物质是 。
② 碳粉的作用是 。
③ 为了说明NaCl的作用,需要补充的对照实验是 。
(2)向图示装置的烧杯a、b中各加入30mL3.5%的NaCl溶液,
闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
①取a、b中溶液少量,滴加K [Fe(CN) ]溶液,a中出现蓝色沉淀,b中无变化,b中铁片作 极。
3 6
②加热后,指针发生偏转的原因可能是 。
(3)用图示装置探究不同浓度NaCl溶液对钢铁腐蚀的影响,
向烧杯a、b中各加入30mL不同质量分数的NaCl溶液,实验记录如下表所示。
实验 a b 指针偏转方向
Ⅰ 0.1% 0.01% 向右
Ⅱ 0.1% 3.5% 向左
Ⅲ 3.5% 饱和溶液 向右
①Ⅱ中,b中电极发生的电极反应式是 。
② Ⅲ中,铁在饱和NaCl溶液中不易被腐蚀。
查阅资料可知:在饱和NaCl溶液中O 浓度较低,钢铁不易被腐蚀。设计实验证明: 。
2
(4)根据上述实验,对钢铁腐蚀有影响的因素是 。
高三实验板块复习——定量专题习题
1.充满HCl的烧瓶做完喷泉实验后得到的稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下
列问题:
(1)用标准Na CO 溶液滴定这种盐酸时,Na CO 溶液应装在 式滴定管中,若用甲基橙作指示剂达到滴定
2 3 2 3
终点时,溶液从 色变为 色。
(2)现配制三种浓度的标准Na CO 溶液,你认为最合适的是下列第 种。
2 3
①2.500mol/L②0.25mol/L③0.025mol/L
(1)配制Na CO 标准溶液的主要操作步骤:
2 3
计算称量→溶解→洗涤(并将洗涤液移入容量瓶)→ → →将配制好的溶液倒入试剂瓶中,贴上标
签。
(2)若采用上述合的标准Na CO 溶液滴定,用c(Na CO )表示,滴定时实验数据列表如下:
2 3 2 3
72①求这种待测稀盐酸的物质的量浓度(用数据和符号列式即可 c(HCl)= 。
②排去碱式滴定管中气泡的方法应采用如图所示操作中的 ,然后轻轻挤压玻璃球使尖嘴部分充满
碱液。
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的
有 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测卦酸润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失
2. 下列对几种具体的滴定分析(待测液置于锥形瓶内)中所用指示剂及滴定终点时的溶液颜色的判断不正确的是
A.用标准酸性KMnO 溶液滴定Na SO 溶液以测量其浓度:KMnO 一浅红色
4 2 3 4
B.利用“Ag++SCN-===AgSCN”原理,可用标准KSCN溶液测量AgNO溶液浓度:Fe(NO)--红色
C.利用“2Fe3++2I-===I +2Fe2+”,用FeCl 溶液测量KI样品中KI的百分含量:淀粉--蓝色
2 3
D.利用OH-+H+===H O来测量某盐酸的浓度时:酚酞--浅红色
2
3.加碘食盐中加入的碘酸钾是一种强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。
【问题1】工业生产碘酸钾的流程如下:
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同。请写出反应器中发生反应的化学方程
式: ;
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是 。
温度/℃ 20 40 60 80
KIO g/100g水 8.08 12.6 18.3 24.8
3
【问题2】已知:KIO +5KI+3H SO =3K SO +3I +3H O;
3 2 4 2 4 2 2
I +2S O 2-=2I-+S O 2-。
2 2 3 4 6
(1)检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。
用四氯化碳检验碘时,用到的主要玻璃仪器有 。
(2)测定加碘食盐中碘的含量,学生乙设计的实验步骤如下:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO 与KI反应完全;
3
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10−3mol/L的Na S O 溶液10.0mL,恰好反应完全。则加碘食
2 2 3
盐样品中的碘元素含量是 mg/kg(以含w的代数式表示)。
(3)学生丙又进行了下列实验:
操作步骤 实验现象
取1g纯净的NaCl,加3mL水配成溶液。 溶液无变化
滴入5滴淀粉溶液和1mL0.1mol/LKI溶液,振荡。 溶液无变化
然后再滴入1滴1mol/L的H SO ,振荡。 溶液变蓝色
2 4
①请推测实验中产生蓝色现象的可能原因,用离子方程式表示
。
②根据学生丙的实验结果,请对学生乙的实验结果作出简要评价
..
734.一组滴定问题的讨论
(1)氯的测定:准确称取样品X,配成溶液后用AgNO 标准溶液滴定,K CrO 溶液为指示剂,至出现淡红色沉淀不
3 2 4
再消失为终点(Ag CrO 为砖红色)。测定氯的过程中,使用棕色测定管的原因是 ;滴定终点时,若
2 4
溶液中c(Ag+)=2.00×10-5mol/L,则c(CrO 2-)= mol/L(已知:Ksp(Ag CrO )=1.12×10-12)
4 2 4
(2)利用间接酸碱滴定法可测定Ba”的含量,实验分两步进行。已知:2CrO 2-+2H+=Cr O 2-+H O,Ba2++CrO 2-=BaCrO
4 2 7 2 4 4
↓
步骤I:移取xmL一定浓度的Na CrO 溶液于锥形瓶中,加入酸碱指示剂,用bmol/L盐酸标准液滴定至终点,测得
2 4
滴加盐酸体积为V mL。
0
步骤Ⅱ:移取ymLBaCl 溶液于锥形瓶中,加入xmL与步骤I相同浓度的Na CrO 溶液,待Ba2+完全沉淀后,再加入
2 2 4
酸碱指示剂,用bmol/L盐酸标准液滴定至终点,测得滴加盐酸的体积为VmL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的 (填“上方”或“下方”)。 BaCl
2
溶液的浓度为 mol,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将
(填偏大”或“偏小”)。
(3)将固氧后的水样酸化,MnO(OH) 被 I-还原为 Mn2+,在暗处静置 5min 然后用标准 Na S O 溶液滴定生成的
2 2 2 3
I (2S O 2-+I =2I-+S O 2-)。
2 2 3 2 4 6
①取 100.00mL 水样经固氧、酸化后,用 amol/LNa S O 溶液滴定:以淀粉溶液作指示剂,终点现象
2 2 3
为 ;若消耗Na S O 溶液的体积为bmL,则水样中溶解氧
2 2 3
的含量为 mg/L。
②上述滴定完成时,若滴定管尖嘴处留有气泡会导致测量结果偏 (填“高”或“低”)。
745.某烧碱样品因部分变质含Na CO 。某化学课外小组的同学用滴定法测定该烧碱样品中NaOH的质量分数。
2 3
【资料】常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2 无色 8.210 红色
甲基橙:pH<3.1 红色 3.14.4 黄色
【实验步骤】
I. 迅速地称取烧碱样品0.50g,溶解后配制成100mL溶液,备用。
Ⅱ. 将0.1000mol/LHCl标准溶液装入酸式滴定管,调零,记录起始读数V ;用碱式滴定管取20.00mL样品溶液
0
于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO ),记录酸式滴定管的
3
读数V ;然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数V 。
1 2
重复上述操作两次,记录数据如下:
实验序号 1 2 3
V /mL 0.00 0.00 0.00
0
V /mL 21.72 21.68 21.70
1
V /mL 23.72 23.68 23.70
2
(1)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(2)下列有关步骤I中样品溶液的说法正确的是________(填字母序号)。
a. 样品溶液中水的电离程度比相同pH的NaOH溶液中的小
b.c(OH-)>c(CO 2-)>c(HCO -)
3 3
c.c(H+)+c(Na+)=c(CO 2-)+c(HCO -)+c(OH-)
3 3
d. 向该溶液中滴加盐酸至第一终点时,n(Cl-)+n(CO 2-)+n(HCO -)+n(H CO )=n(Na+)
3 3 2 3
(3)酸式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是________。
(4)滴定至第一终点的过程中,发生反应的离子方程式为________。
(5)判断滴定至第二终点的现象是溶液由________色变为橙色。
(6)样品中NaOH的质量分数w(NaOH)= %。(计算结果保留小数点后1位)
(7)下列操作会导致测得的NaOH质量分数偏高的是________(填字母序号)。
a. 达到第一终点前,锥形瓶中有气泡产生
b. 记录酸式滴定管读数V 时,俯视标准液液面
1
c. 第一终点后继续滴定时,锥形瓶中有少许液体溅出
756.(11分)某铜合金中Cu的质量分数为80%~90%,还含有Fe等。通常用间接碘量法测定其中Cu的含量,步骤
如下:
Ⅰ.称取ag样品,加入稀H SO 和H O 溶液使其溶解,煮沸除去过量的H O ,冷却后过滤,滤液定容于250
2 4 2 2 2 2
mL容量瓶中;
Ⅱ.取50.00mL滤液于锥形瓶中,加入NH F溶液,控制溶液pH为3~4,充分反应后,加入过量KI溶液,
4
生成白色沉淀,溶液呈棕黄色;
Ⅲ.向Ⅱ的锥形瓶中加入c mol·L−1Na S O 溶液滴定,至锥形瓶中溶液为浅黄色时,加入少量淀粉溶液,继续
2 2 3
滴至浅蓝色,再加入KSCN溶液,剧烈振荡后滴至终点;
Ⅳ.平行测定三次,消耗Na S O 溶液的体积平均为vmL,计算铜的质量分数。
2 2 3
已知:ⅰ.F−与Fe3+生成稳定的FeF 3−(无色)。
6
ⅱ.I 在水中溶解度小,易挥发。
2
ⅲ.I +I− I −(棕黄色)。
2 3
ⅳ.I +2Na S O ==2NaI+Na S O (无色)。
2 2 2 3 2 4 6
(1)Ⅰ中Cu溶解的离子方程式是 。
(2)Ⅱ中Cu2+和I−反应生成CuI白色沉淀和I 。
2
①加入NH F溶液的目的是 。
4
②Cu2+和I−反应的离子方程式是 。
③加入过量KI溶液的作用是 。
(3)室温时,CuSCN的溶解度比CuI小。CuI沉淀表面易吸附I 和I −,使测定结果不准确。Ⅲ中,在滴定至终
2 3
点前加入KSCN溶液的原因是 。
(4)样品中Cu的质量分数为 (列出表达式)。
76高三实验板块复习——性质专题习题参考答案
无机物性质练习一
1 2 3 4 5 6 7 8 9
CD BC ABC C BC BC BCD C ABCD
10.(1)防止Fe2+被氧化
(2)2Fe2++Cl =2Fe3++2Cl-
2
(3)隔绝空气(排除氧气对实验的影响)
(4)Fe2+;Fe3+;可逆反应
(5)H O +2Fe2++2H+=2Fe3++2H O;
2 2 2
Fe3+催化H O 分解产生O ;
2 2 2
H O 分解反应放热,促进Fe3+的水解平衡Fe3++3H O Fe(OH) +3H+正向移动。
2 2 2 3
11.(1)2Fe+3Cl =2FeCl (2)③含有Fe3+和Fe2+
2 3
实验现象 实验结论及反应离子方程式
溶液呈红色 Fe3++3SCN-=Fe(SCN)
3
(3)a 因为还原性Fe2+>Cl-,逐滴加入的酸性KMnO 溶液,先将Fe2+氧化,而使KMnO 紫色褪去,故可能含有
4 4
Fe2+
b 溶液中可能无Fe2+,加入的酸性KMnO 溶液,将Cl-氧化,而使KMnO 紫色褪去
4 4
12.(11分)
催化剂
(1)4NH +5O 4NO+6H O(2分)
3 2 2
(2)①2NO+O =2NO (2分) ②NH NO (1分)
2 2 4 3
③3Cu+8H++2NO —=3Cu2++2NO↑+4H O(2分)
3 2
(3)①增加(1分) 减少(1分) ②abc(2分)
无机物性质练习二
1 2 3 4 5 6 7 8
BD BCD C CGH ABC B ABCD AB
9.(1)C Na SO 是可溶性固体,不能用具“随开随用”功能的装置
2 3
i.Na SO 已部分变质 ii.硫酸溶液太稀
2 3
(2)FeS+H SO =FeSO +H S↑
2 4 4 2
(3)溶液红色褪去 溶液紫色褪去 有无色液滴生成试管壁变模糊,有淡黄色固体生成
(4)吸收尾气(H S或SO ),避免污染空气
2 2
10.(1)ClO-+Cl-+2H+ = Cl ↑ +H O (2)B中长颈漏斗中液面明显上升,形成水柱
2 2
(3)d (4)黄(或橙) 溶液变蓝色
(5)①E处未能排除D中过量Cl 的干扰,而置换出I (或:C、D装置之间无干燥装置, ③处布条不干燥,
2 2
也可褪色)
7711.(1)便于控制反应的发生和停止
(2)停止加热时,防止倒吸或平衡压强(凡合理答案均可)
(3)品红溶液褪色
(4)验证Ⅱ: C G
验证Ⅲ:步骤1:C(或F) 红(或蓝) Fe3++3SCN—=Fe(SCN) (或2Fe3++2I—=2Fe2++I )
3 2
步骤2:D 浅红色褪去或变浅
12.(1)
(2) 降低ClO 的浓度,防止ClO 的浓度过高而发生分解,引起爆炸; 冰水浴
2 2
(3) 防止ClO 逸出,使ClO 全部反应,准确测定ClO 的质量
2 2 2
(4) 溶液由蓝色变为无色,并且在30s内颜色不发生变化
(5) 1.35×10-2CV
有机化学
1 2 3 4 5
AD C CD AD ABC
6.混合物的提纯
混合物 除杂试剂 操作方法
C H (C H ) 溴水 洗气
2 6 2 4
C H (SO ) NaOH 洗气
2 4 2
苯(苯酚) NaOH 洗气
苯(甲苯) 酸性高锰酸钾、NaOH 分液
肥皂溶液(甘油) NaCl 盐析、过滤
溴苯(溴) NaOH 分液
硝基苯(混酸) NaOH 分液
乙醛(乙酸) CaO 蒸馏
乙醇(乙酸) CaO 蒸馏
乙酸乙酯(乙酸) Na CO 分液
2 3
石油 分馏
7. (1)离子键、非极性(共价)键
(2)CaC +2H O Ca(OH) +HC≡CH↑
2 2 2
(3)H S+Cu2+==CuS↓+2H+ (H S+2OH−==S2−+H O也给分)
2 2 2
(4)过量溴水(或足量溴的CCl 溶液)
4
78(5)
8.(1)分液 苯甲醇 (2)蒸馏 (3)过滤 苯甲酸 (4)b 酒精灯、冷凝管、尾接管、锥形瓶 205.3℃。
9.(1)①防暴沸 冷凝 ②防止环己烯挥发
(2)①上层 C ②g 冷却水与气体形成逆流 ③83℃ b (3)C
高三实验板块复习——制备专题习题参考答案
1 2 3 4
AC D C A
5.(1)平衡气压,使浓盐酸顺利滴下; NaOH溶液;
Ca(ClO) +4HCl=CaCl +2Cl ↑+2H O
2 2 2 2
(2)在装置A、B之间加装盛有饱和食盐水的洗气瓶
(3)酸式;C
0.315c V 3V
(4) 1 2 100%;B、D
m
6.(1)Cl +2OH-==Cl-+ClO-+H O
2 2
(2)①NaClO+CO(NH ) +2NaOH 一 == 定 == 温 == 度 =N H ·H O+NaCl+Na CO
2 2 2 4 2 2 3
②冷凝回流水合肼
③N H ·H O被NaClO氧化
2 4 2
④加热至有大量固体析出,趁热过滤
(3)①N H ·H O+H+==N H ++H O ②
2 4 2 2 5 2
7. (1)2NaHCO Na CO +H O+CO ↑
3 2 3 2 2
(2)先通NH ,后通CO
3 2
(3)NH Cl(s) NH +(aq)+Cl-(aq),增大c(Cl-),平衡左移,促进氯化铵析出
4 4
(4)NH +HCl=NH Cl
3 4
(5)① 碱石灰
② MgO+2NH Cl 2NH ↑+MgCl +H O↑
4 3 2 2
③ c
④ 因为MgO+2NH Cl 2NH ↑+MgCl +H O↑, 而MgCl 水解生成Mg(OH) 和HCl,
4 3 2 2 2 2
MgCl +2H O Mg(OH) +2HCl↑;Mg(OH) 受热生成MgO,Mg(OH) MgO+H O,
2 2 2 2 2 2
所以MgO可以循环应用与NH Cl反应制得NH 和HCl。
4 3
8.(1)Na CO +CO +H O==2NaHCO
2 3 2 2 3
(2)CO 在水中存在平衡:CO +H O H CO H CO HCO -+H+,有H SO 存在时,可使上述平衡向左移动,
2 2 2 2 3 2 3 3 2 4
从而减少CO 在水中的溶解,同时吸收挥发出来的HCl气体
2
79(3)① Na CO 和NaHCO 都能跟Ca(OH) 溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO
2 3 3 2 3
②2HCO -+Ba2+=BaCO ↓+CO ↑+H O 合理
3 3 2 2
③接下来的操作:冷却到室温,加水至溶液体积为400mL,再次测定pH
补充实验:取相同质量的纯净的NaHCO 配成1000mL溶液,取400mL,重复甲的实验,进行对照。
3
a.白色固体为NaHCO
3
b.71:42(或1.69)
高三实验板块复习——原理专题习题参考答案
一、催化剂对化学反应速率的影响
1 2
B AD
3. (1)其他条件相同时,增 . 大 .K.M.n.O.4. 浓 . 度 . (或 . 反 . 应 . 物 . 浓 . 度 . ),反 . 应 . 速 . 率 . 增 . 大 .
(2)1.5×10-2mol/(L·min)(2分)
(3) ①生成物中的MnSO 为该反应的催化剂(或Mn2+对该反应有催化作用)
4
[2分,不指出MnSO (或Mn2+)扣1分]
4
②MnSO
4
③与实验1比较,溶液褪色所需时间短(2分,不写“与实验1比较”扣1分)
或:所用时间(t)小于4min(或其他合理答案)
4.(1)在 H O 浓度一定时,HI 浓度每增加1倍,速率就增加1倍;在 HI浓度一定时,H O 浓度每增加1倍,
2 2 2 2
速率也增加1倍;或用反应速率方程表示v=kc(H O )c(HI)
2 2
(2)0.002mol/(L·s)
(3)①未观察到棕黄色,说明没有碘单质生成,过氧化氢没有与碘化钾发生氧化还原反应;有无色气体产生,说
明发生了过氧化氢分解反应,而没有加入碘化钾前,没有观察到无色气体产生
②取两支试管,加入5%H O 溶液,向其中一支试管中加入少量KI固体,若观察到加入 KI 的试管中有无色气体
2 2
产生,则证明 KI能提高过氧化氢分解反应的速率
二、浓度对化学平衡的影响
5 6 7
ABCD BCD B
8. (1)a 8.0 b 5.0 c 15.0 (2)搅拌 (3)2.5×10-5
(4)反应物浓度增大反应速率加快,反应速率变化与反应物的起始浓度变化成比例等。
三、温度对化学平衡的影响
9.ABC
四、难溶电解质溶解平衡
10 11 12 13 14
AD ABCD BC AB C
80五、金属的腐蚀
15 16 17 18 19
ABCD ACD AD ABCD AC
20. (1)① O
2
② 与铁组成原电池,作原电池的正极
③ 用水代替NaCl溶液进行上述实验
(2)① 正
② 温度升高,Fe还原性增强 ,反应速率加快
(3)① Fe-2e-=Fe2+
②另取两个烧杯,分别往其中加入铁片和一定量的饱和NaCl溶液,再分别滴加几滴
K Fe(CN) 溶液,然后往其中一个烧杯中通入O ,观察现象。
3 6 2
(4)温度、NaCl溶液的浓度、O 的浓度
2
高三实验板块复习——定量专题习题参考答案
1(1)碱 红 橙 (2) ③ (3)转移 定容 摇匀
(4) 或 丙 D
2.C
3.(1)6I +11KClO +3H O=6KH(IO )+5KCl+3Cl ↑
2 3 2 3 2
(2)加热浓缩,冷却结晶,过滤,洗涤,干燥
【问题2】(1)分液漏斗(多选烧杯玻璃棒等合理答案不扣分)
(2)1270/3W(或423.33/W)
(3)①4I-+4H++O =2I +2H O ②学生乙实验结果会偏大
2 2 2
4.(1)防止硝酸银见光分解 2.80×10-3
(2)上方 偏大
(3)蓝色刚好褪去 80ab 低
5. (1)100mL容量瓶
(2)bd
(3)用HCl标准溶液润洗酸式滴定管
(4)H++OH-===H O H++CO 2-===HCO -
2 3 3
(5)黄
81(6)78.8
(7)ac
6.(1)Cu+H O +2H+==Cu2++2H O
2 2 2
(2)①将溶液中的Fe3+转化为FeF 3−,防止其氧化I−
6
②2Cu2++4I−==2CuI↓+I
2
③将Cu2+充分还原为CuI;I−与I 结合生成I −,减少I 的挥发
2 3 2
(3)将CuI沉淀转化为溶解度更小的CuSCN沉淀,释放出吸附的I 和I −,提高
2 3
测定结果的准确程度
(4)(63.5×5×cv×10−3/a)×100%
82