文档内容
参照秘密级管理★启用前 试卷类型:A
德州市二 O 一九年初中学业水平考试
化学试题
注意事项:
1.本试卷选择题共36分,非选择题共64分,全卷满分100分;考试时间70分钟。
2.答题前,考生务必将自己的县(市、区)、学校、姓名、准考证号用0.5毫米黑色墨水签字笔
填写在答题卡的相应位置上。
3.答选择题时,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,请用橡皮擦干净后,
再选涂其他答案;答非选择题时,必须用0.5毫米黑色墨水签字笔写在答题卡指定的位置上,不
在答题区域内的答案一律无效,不得用其他笔答题。
4.考生答案全部写在答题卡上,写在本试卷和草稿纸上无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 K-39 Mn-55
一、选择题(本题包括16个小题,1-12题每小题2分,13-16题每小题3分,共36分。每小题只
有一个选项符合题意)
1. 2019年世界地球日的主题是“珍爱美丽地球 守护自然资源”。下列做法不符合这一主题的是
A. 合理施用化肥和农药,减少负面作用 B. 工业废水达标后排放,防治水体污染
C. 露天焚烧废旧塑料,减少白色污染 D. 垃圾分类回收,节约资源、减少污染
【答案】C
【解析】
【详解】A、合理施用化肥和农药,减少负面作用,符合主题,故A正确;
B、工业废水达标后排放,防治水体污染,符合主题,故B正确;
C、露天焚烧废旧塑料,会造成白色污染,不符合主题,故C不正确;
D、垃圾分类回收,节约资源、减少污染,符合主题,故D正确。故选C。
2. 下面是实验室常见的玻璃仪器,其中能够在酒精灯上直接加热的是
A. B.C. D.
【答案】A
【解析】
【详解】A、试管可以 在酒精灯上直接加热,故A正确;
B、量筒用来量取液体 的一种玻璃仪器,不能加热,故B不正确;
C、烧杯加热要垫石棉网,故C不正确;
D、集气瓶不能加热,故D不正确。故选A。
3. 空气是一种宝贵的自然资源。下列对空气的相关叙述正确的是
A. 空气是由空气分子构成的 B. 空气中的氧气可以作燃料
C. 稀有气体化学性质很不活泼 D. 化石燃料的使用不会污染空气
【答案】C
【解析】
【详解】A、空气是由氮气、氧气、稀有气体等组成的混合物,故A不正确;
B、空气中的氧气支持燃烧,但不燃烧,不能做燃料,故B不正确;
C、稀有气体化学性质很不活泼,故C正确;
D、化石燃料的使用会产生二氧化硫等污染空气的气体,故D不正确。故选C。
4. 中国诗词、成语和谚语中有些蕴含着化学知识。下列说法正确的是
A. “遥知不是雪,为有暗香来”说明分子在不断地运动
B. “只要功夫深,铁杵磨成针”描述的是化学变化
C. “真金不怕火炼"说明金具有熔点高的物理性质
D. “釜底抽薪”体现的灭火原理是隔绝氧气(或空气)
【答案】A
【解析】
【详解】A、“遥知不是雪,为有暗香来”说明分子在不断地运动,故A正确;
B、“只要功夫深,铁杵磨成针”描述的是物理变化,故B不正确;
C、“真金不怕火炼"说明黄金的化学性质稳定,故C不正确;
D、“釜底抽薪”体现的灭火原理是清除可燃物,故D不正确。故选A。
5. 下列化学用语书写正确的是
A. 2个氮原子-N B. 钙离子-Ca+2 C. 氯化铁-FeCl D. 氦气-He
2 2
【答案】D【解析】
【详解】A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上
相应的数字,则2个氮原子化学式为 ,故A不正确;
B、离子符号在元素符号右上角写带几个单位的正(或)负电荷,数字在前,正负号在后,则钙离子化学
式为 ,故B不正确;
C、组成化合物的元素的化合价代数和为零,铁离子为+3价,则氯化铁化学式为 ,故C不正确;
D、氦是稀有气体,则氦气化学式为 ,故D正确。故选D。
6. 碳酸氢铵(NH HCO )可用作食品添加剂,有关它的说法正确的是
4 3
A. 碳酸氢铵是有机物 B. 氮、氢元素质量比为1: 5
.
C 碳酸氢铵由10个原子构成 D. 碳酸氢铵由四种元素组成
【答案】D
【解析】
【分析】
有机物是含碳的化合物,但是不包括碳的氧化物和硫化物、碳酸、碳酸盐等,化合物里各元素的质量比是
原子个数与相对原子质量的乘积之比。
【详解】A、有机物是含碳的化合物,但是不包括碳的氧化物和硫化物、碳酸、碳酸盐等,碳酸氢铵是碳
酸盐,不属于有机物,故A不正确;
B、氮、氢元素质量比为 ,故B不正确;
C、1个碳酸氢铵分子是由1个氮原子、5个氢原子、1个碳原子和3个氧原子构成的,故C不正确;
D、碳酸氢铵由氮元素、氢元素、碳元素和氧元素四种元素组成,故D正确。故选D。
7. 下面是某同学在制取二氧化碳时选用的实验装置或操作方法,正确的是
A. 发生装置 B. 收集C. 干燥 D. 验满
【答案】D
【解析】
【分析】
实验室用大理石或石灰石和稀盐酸常温反应制取。
【详解】A、实验室用大理石或石灰石和稀盐酸常温反应制取,为不加热的装置,故A不正确;
B、二氧化碳易溶于水,不能用排水法收集,故B不正确;
C、为了使混合气体充分与浓硫酸接触,浓硫酸干燥二氧化碳,二氧化碳要长管进,短管出,故C不正确;
D、二氧化碳验满方法:用燃着的木条被在集气瓶口(不能伸入瓶内),如果火焰熄灭,证明已集满,故
D正确。故选D。
【点睛】
8. 石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。
关于石墨烯的认识错误的是
A. 可作散热材料 B. 是一种新型化合物
C. 常温下化学性质稳定 D. 可作新型电池的电极
【答案】B
【解析】
【分析】
单质是由同种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
【详解】A、石墨烯具有超强导热的性能,则可作散热材料 ,故A正确;
B、石墨烯化学性质和石墨相似,属于单质,故B不正确;
C、常温下石墨烯不和其他物质反应,则化学性质稳定,故C正确;
D、石墨烯超强导电性能,则可作新型电池的电极,故D正确。故选B。
9. 化学反应不仅有新物质生成,而且还伴随能量变化。以下能量变化不是由化学变化引起的是
A. 鞭炮爆炸发声 B. 蜡烛燃烧发光 C. 煤燃烧火力发电 D. 电水壶通电放热
【答案】D
【解析】
【分析】物理变化是物质在变化过程中没有新物质生成。
【详解】A、鞭炮爆炸发声,有新物质生成,是化学变化,故A正确;
B、蜡烛燃烧发光,有新物质生成,是化学变化,故B正确;
C、煤燃烧火力发电,有新物质生成,是化学变化,故C正确;
D、电水壶通电放热,没有新物质生成,是物理变化,故D不正确。故选D。
10. 根据如图所示的实验现象分析,下列说法错误的是
A. ①②对比说明物质燃烧需要与空气接触
B. ①中使温度达到白磷着火点是利用了铜的导热性
C. 烧杯中的热水只起提高温度的作用
D. ①③对比说明红磷着火点高于白磷
【答案】C
【解析】
【分析】
燃烧条件:物质是可燃物、有氧气参与、达到可燃物的着火点。
【详解】A、①白磷在空气中,②白磷在水中,则①②对比说明物质燃烧需要与空气接触,故A正确;
B、热水通过铜把温度传给了白磷,则①中使温度达到白磷着火点是利用了铜的导热性,故B正确;
C、烧杯中的热水不但起提高温度的作用,而且还具有隔绝氧气的作用,故C不正确;
D、相同的温度和氧气浓度,白磷燃烧,红磷不燃烧,则①③对比说明红磷着火点高于白磷,故D正确。
故选C。
【点睛】灭火原理:清除可燃物、隔绝氧气、降低温度至可燃物着火点以下。
11. 人体内的一些液体正常pH范围如下,其中呈酸性的是
A. 血浆7.35-7.45 B. 胆汁7.1-7.3
C. 胃液0.9-1.5 D. 胰液7.5-8.0
【答案】C
【解析】
pH>7溶液呈碱性,pH<7溶液呈酸性,pH=7溶液呈中性。其中呈酸性的是胃液。故选C。
12. 分类是一种重要的研究方法。以下对常见物质的分类正确的是
A. 氧化物:水、生石灰、五氧化二磷 B. 碱:火碱、熟石灰、纯碱C. 混合物:煤、食盐水、冰水混合物 D. 合成材料:羊毛、塑料、合成橡胶
【答案】A
【解析】
【分析】
氧化物是由两种元素组成,其中一种元素是氧元素的化合物,混合物是由不同种物质组成,合成材料包括合
成纤维、合成橡胶、塑料,碱是指在水溶液中电离出的阴离子全部都是氢氧根离子的物质,盐是指一类金
属离子或铵根离子与酸根离子或非金属离子结合的化合物。
【详解】A、水、生石灰、五氧化二磷都是氧化物,故A正确;
B、火碱、熟石灰是碱,纯碱是盐,故B不正确;
C、煤、食盐水是混合物,冰水混合物是由水分子构成的纯净物,故C不正确;
D、塑料、合成橡胶是合成材料,羊毛是天然纤维D不正确。故选A。
13. 两瓶标签损毁的溶液分别是稀盐酸、稀硫酸,下列试剂中能够用来区分两种溶液的是.
A. 锌粒 B. 氯化钡溶液 C. 紫色石蕊溶液 D. 氢氧化钠溶液
【答案】B
【解析】
【详解】A、锌粒和稀盐酸、稀硫酸都能反应,放出氢气,不能区分,故A不正确;
B、氯化钡溶液和稀盐酸不反应,氯化钡溶液和稀硫酸反应生成硫酸钡沉淀和盐酸,可以区分,故B正确;
C、稀盐酸、稀硫酸都能使紫色石蕊溶液变红色,不能区分,故C不正确;
D、氢氧化钠溶液能和稀盐酸、稀硫酸都发生反应,无明显现象,不能区分,故D不正确。故选B。
14. 推理是一种重要的思维方法。下列推理正确的是
A. 分子是构成物质的微粒,所以物质都是由分子构成
B. 氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素
C. 溶液是均一、稳定的混合物,所以均一、稳定的物质就是溶液
D. 化合物由多种元素组成,所以由多种元素组成的物质就是化合物
【答案】B
【解析】
【详解】A、分子是构成物质的微粒,物质可以由分子、原子、离子构成,故A不正确;
B、氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素,故B正确;
C、溶液是均一、稳定的混合物,均一、稳定的物质不一定是溶液,如水,故C不正确;
D、化合物由多种元素组成,由多种元素组成的物质不一定是化合物,可以是混合物,故D不正确。故选
B。
15. 下列实验方案不能达到实验目 的的是实验目的 实验方案
A 鉴别木炭粉和铁粉 分别加入到足量稀硫酸中
B 鉴别棉线和合成纤维 点燃,闻气味、看灰烬
C 除去氯化亚铁溶液中少量的氯化铜 加人足量锌粉
D 除去氧气中的二氧化碳 将气体通入足量的氢氧化钠溶液
A. A B. B C. C D. D
【答案】C
【解析】
【分析】
除杂要求:不引入新的杂质,加入的物质不和原物质反应。
【详解】A、鉴别木炭粉和铁粉,分别加入到足量稀硫酸中,铁粉和稀硫酸反应生成硫酸亚铁,溶液变为
浅绿色,木炭粉不和稀硫酸反应,可以鉴别,故A正确;
B、鉴别棉线和合成纤维,棉线吸水性强燃烧时散发刺鼻气味燃烧的灰烬分散颜色发白,合成纤维结实、
吸水性弱、燃烧时散发焦肉气味、燃烧的灰烬成团颜色发黑并且未燃烧完全的会变的和硬塑料似的,可以
鉴别,故B正确;
C、除去氯化亚铁溶液中少量的氯化铜,加人足量锌粉,锌粉和氯化亚铁、氯化铜均能反应,除杂的时候
可能除去氯化亚铁,故C不正确;
D、除去氧气中的二氧化碳,将气体通入足量的氢氧化钠溶液,二氧化碳和氢氧化钠反应,氧气不和氢氧
化钠反应,可以除去二氧化碳,故D正确。故选C。
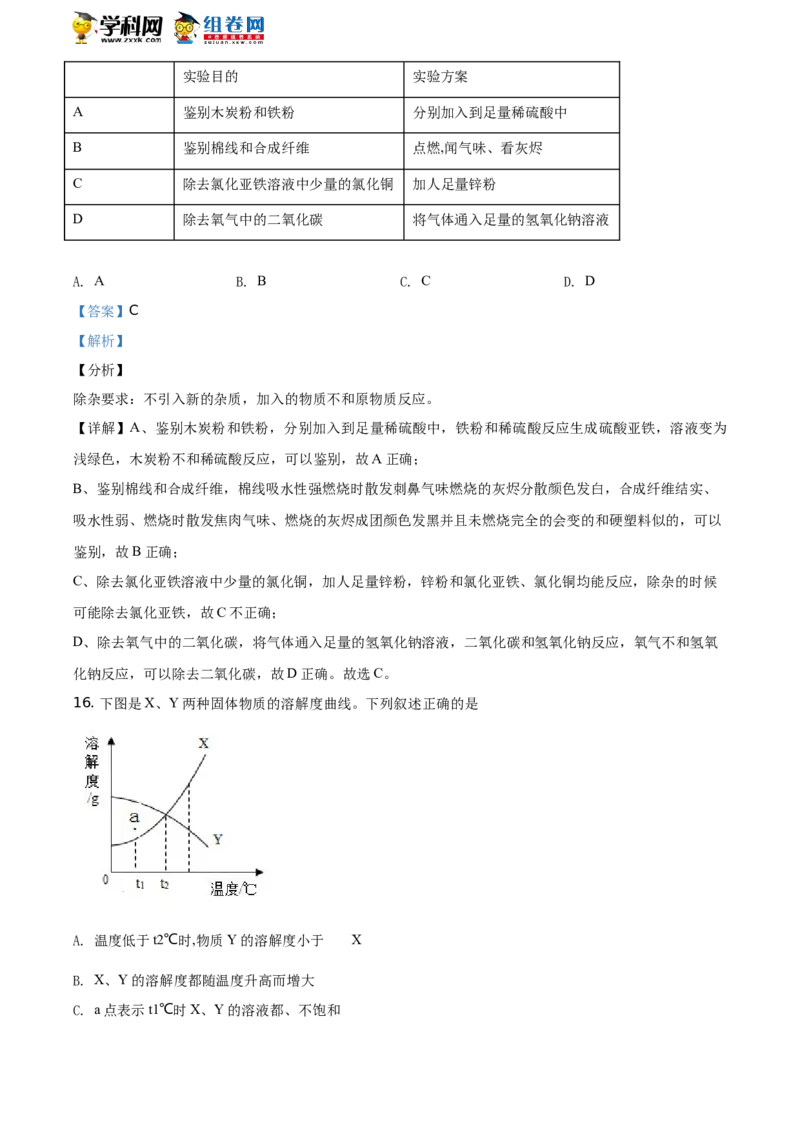
16. 下图是X、Y两种固体物质的溶解度曲线。下列叙述正确的是
A. 温度低于t2℃时,物质Y的溶解度小于 X
B. X、Y的溶解度都随温度升高而增大
C. a点表示t1℃时X、Y的溶液都、不饱和D. Y的饱和溶液降低温度后,溶质质量分数不变
【答案】D
【解析】
【分析】
由X、Y两种固体物质的溶解度曲线图可知,X的溶解度随温度的增加而增大,Y的溶解度随温度的增加
而减小,交点表示在t℃时,X、Y两种固体物质的溶解度相同。
2
【详解】A、温度低于t℃时,物质Y的溶解度大于X,故A不正确;
2
B、X的溶解度随温度的增加而增大,Y的溶解度随温度的增加而减小,故B不正确;
C、 a点表示t℃时X的溶液饱和,Y的溶液不饱和,故C不正确;
1
D、Y的饱和溶液降低温度后,溶质质量和溶剂质量都没变,则溶质质量分数不变,故D正确。故选D。
【点睛】物质的溶解度随温度的增加而减小,饱和溶液降低温度后,溶质质量分数不变。
二、理解与应用(本大题包括5个小题,共30分)
17. 化学与生活息息相关。请回答下列问题:
(1)大枣含有蛋白质、糖类及维生素等营养素,其中能起到调节人体新陈代谢,预防疾病作用的是
_____________________。
(2)净化水时放入活性炭除去色素、异味,这是利用了活性炭的______________性。
(3)家庭中常用洁厕灵(有效成分为盐酸)去除尿垢(其中含有碳酸钙)。写出盐酸与碳酸钙反应的化学方程式
______________________________________________________。
【答案】 (1). 维生素 (2). 吸附 (3).
【解析】
【分析】
盐酸与碳酸钙反应生成氯化钙和水和二氧化碳。
【详解】(1)大枣含有蛋白质、糖类及维生素等营养素,其中能起到调节人体新陈代谢,预防疾病作用的是维
生素。
(2)净化水时放入活性炭除去色素、异味,这是利用了活性炭的吸附性。
(3)家庭中常用洁厕灵(有效成分为盐酸)去除尿垢(其中含有碳酸钙)。盐酸与碳酸钙反应生成氯化钙和水和
二氧化碳,化学方程式为 。
18. “化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门
科学的认识解答以下问题:
(1)通过电解水的实验,可以推断水是由________________(填元素符号)元素组成。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是_____________________________________________。
(3)以下物质用途主要是由其物理性质决定的是________(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体 ③天然气作燃料 ④用铜制作导线
(4)以下符合化学方程式书写原则的是__________________(填序号)。
①C+O =CO ②A1+HCl=AICl +H ↑ ③Ca(OH) +Na CO=CaCO ↓+2NaOH
2 2 3 2 2 2 3 3
【答案】 (1). (2). 碳原子的排列方式不同 (3). ①②④ (4). ③
【解析】
【分析】
电解水的实验说明水是由氢元素和氧元素组成;物理性质是不通过化学变化就表现出的性质。
【详解】(1)通过电解水的实验,可以推断水是由氢元素和氧元素组成,化学式为 。
(2)金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是碳原子的排列方式不同。
(3) ①氢气填充探空气球,利用氢气密度小,属于物理性质,故①正确;
②氢氧化钠干燥气体,利用吸水性,属于物理性质,故②正确;
③天然气作燃料,利用其可燃性,属于化学性质,故③不正确;
④用铜制作导线,利用其导电性,故④正确。故选①②④。
(4) ①C+O =CO 没有反应条件,故①不正确;
2 2
②A1+HCl=AICl +H ↑,未配平,故②不正确;
3 2
③Ca(OH) +Na CO=CaCO ↓+2NaOH,配平正确,故③正确。故选③。
2 2 3 3
【点睛】化学方程式要标明反应物、生成物和反应条件。
19. 含氮元素的物质与人类生产,生活关系密切。请你回答有关问题:
(1)N 、NH 、HNO 等都是常见的含氮物质,其中氮元素化合价最低的物质是___________。
2 3 3
(2)氮气具有广泛的用途.如超导材料在液氮的低温环境下能显示超导性能。从微观角度分析:制取液氮时,在
氮气液化过程中发生变化的是______________(填序号).
①分子的大小 ②分子的质量 ③分子间的间隔 ④分子的数目
(3)将空气中的氮气转化为含氮化合物的过程称为固氮(“氮"指氮元素)。某些生物(如大豆根系中的根瘤菌)就
具有固氮作用。经田间试验测定,一亩大豆可固氮8kg,相当于施用____________kg(保留整数)尿素[化学式为
CO(NH)]。
2 2
(4)下面是在汽车尾气治理过程中有关化学反应的微观示意图。图中所示反应的化学方程式为
_______________________________________。【答案】 (1). (或氨气) (2). ③ (3). 17 (4).
【解析】
【分析】
根据质量守恒定律,化学反应前后原子种类和个数都不变,汽车尾气治理过程中有关化学反应的微观示意
图可知,化学方程式为 。
【详解】(1)N 、NH 、HNO 等都是常见的含氮物质,氮气中氮的化合价为0,氨气中氮元素的化合价为-3
2 3 3
价,硝酸中氮元素的化合价为+5价,其中氮元素化合价最低的物质是 (或氨气)。
(2)氮气具有广泛的用途.如超导材料在液氮的低温环境下能显示超导性能。微观角度分析:制取液氮时,在氮
气液化过程中发生变化的是分子间的间隔,故选③。
(3)将空气中的氮气转化为含氮化合物的过程称为固氮(“氮"指氮元素)。某些生物(如大豆根系中的根瘤菌)
就具有固氮作用。经田间试验测定,一亩大豆可固氮8kg,相当于施用
(4)在汽车尾气治理过程中有关化学反应的微观示意图。反应的化学方程式为
。
20. 依据对初中所学四种反应类型(化合反应、分解反应、置换反应、复分解反应)概念的理解,结合下列
化学方程式,比较反应前后元素化合价的变化情况:(1)一定有变化的是_______(填反应类型.下同);(2)不一定
有变化的是____;(3)一定没有变化的是______。
①CO+H O=HCO ②Cu+2AgNO =Cu(NO)+2Ag
2 2 2 3 3 3 2
③ ④⑤NaOH+HCl=NaCl+H O ⑥
2
【答案】 (1). 置换反应 (2). 化合反应、分解反应 (3). 复分解反应
【解析】
【详解】① 化合价没变化,属于化合反应;
② 有单质参加反应和有单质生成,化合价发生变化,属于置换反应;
③ 有单质参加,则化合价发生变化,属于化合反应;
④ 有单质生成,化合价发生变化,属于分解反应。
(1)一定有变化的是置换反应。
(2)不一定有变化的是化合反应、分解反应。
(3)一定没有变化的是复分解反应。
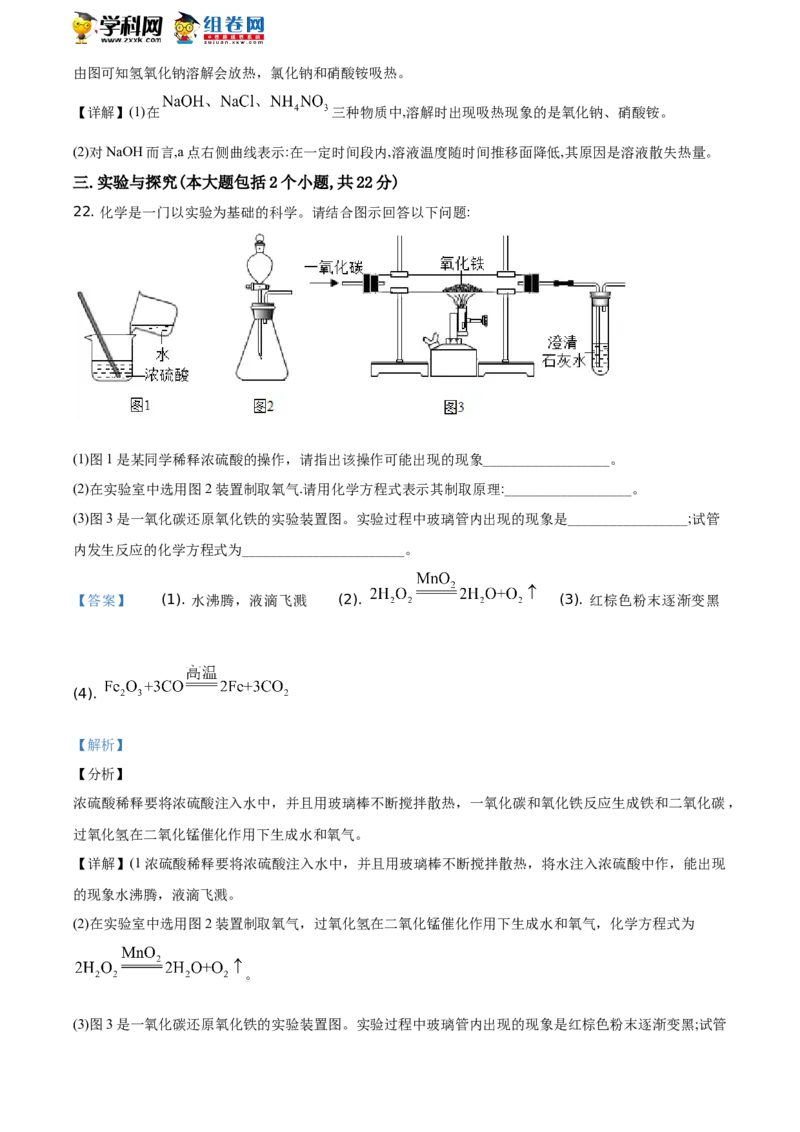
21. 将NaOH、NaCl、NH NO 固体各10g分别放入盛有100mL水 的烧杯中充分溶解。在不同时间测量溶
4 3
液的温度,绘制成如下图像:
分析图像,回答问题:
(1)在NaOH、NaCl、NH NO 三种物质中,溶解时出现吸热现象的是______________(写名称);
4 3
(2)对NaOH而言,a点右侧曲线表示:在一定时间段内,溶液温度随时间推移面___________(填“升高”或“降
低”),其原因是___________________________。
【答案】 (1). 氧化钠、硝酸铵 (2). 降低 (3). 溶液散失热量
【解析】
【分析】由图可知氢氧化钠溶解会放热,氯化钠和硝酸铵吸热。
【详解】(1)在 三种物质中,溶解时出现吸热现象的是氧化钠、硝酸铵。
(2)对NaOH而言,a点右侧曲线表示:在一定时间段内,溶液温度随时间推移面降低,其原因是溶液散失热量。
三.实验与探究(本大题包括2个小题,共22分)
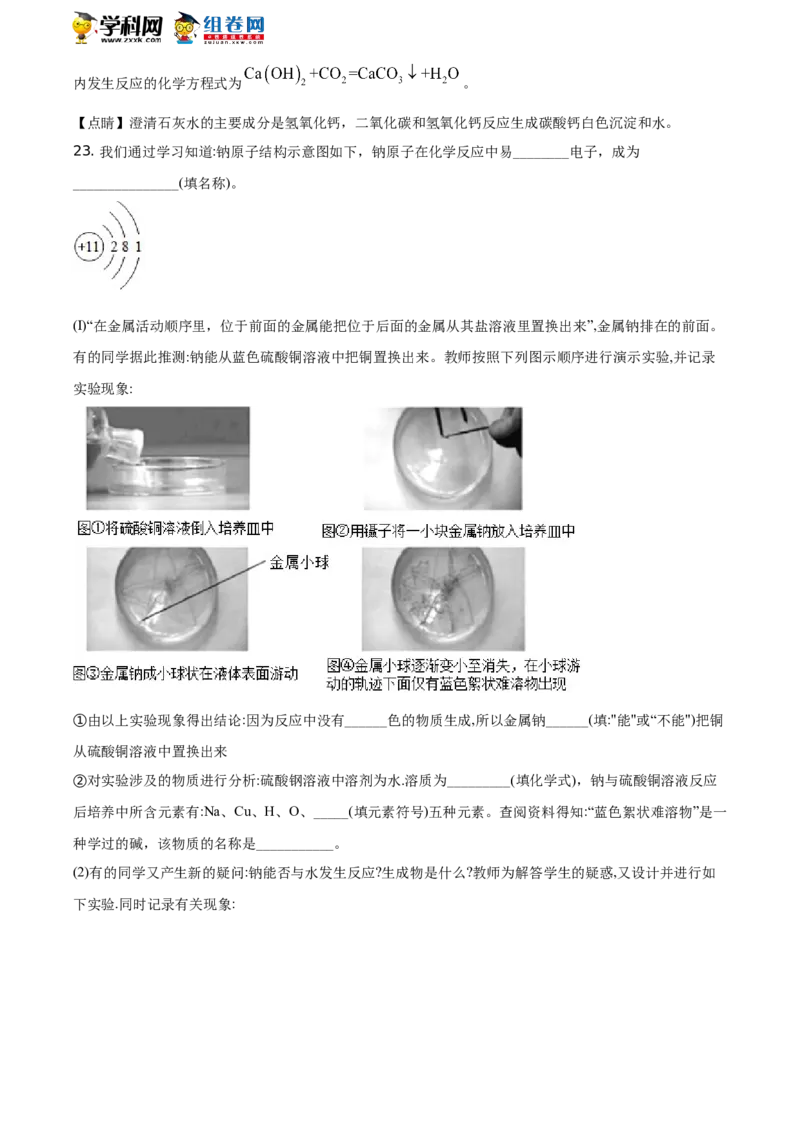
22. 化学是一门以实验为基础的科学。请结合图示回答以下问题:
(1)图1是某同学稀释浓硫酸的操作,请指出该操作可能出现的现象__________________。
(2)在实验室中选用图2装置制取氧气.请用化学方程式表示其制取原理:__________________。
(3)图3是一氧化碳还原氧化铁的实验装置图。实验过程中玻璃管内出现的现象是_________________;试管
内发生反应的化学方程式为_______________________。
【答案】 (1). 水沸腾,液滴飞溅 (2). (3). 红棕色粉末逐渐变黑
(4).
【解析】
【分析】
浓硫酸稀释要将浓硫酸注入水中,并且用玻璃棒不断搅拌散热,一氧化碳和氧化铁反应生成铁和二氧化碳,
过氧化氢在二氧化锰催化作用下生成水和氧气。
【详解】(1浓硫酸稀释要将浓硫酸注入水中,并且用玻璃棒不断搅拌散热,将水注入浓硫酸中作,能出现
的现象水沸腾,液滴飞溅。
(2)在实验室中选用图2装置制取氧气,过氧化氢在二氧化锰催化作用下生成水和氧气,化学方程式为
。
(3)图3是一氧化碳还原氧化铁的实验装置图。实验过程中玻璃管内出现的现象是红棕色粉末逐渐变黑;试管内发生反应的化学方程式为 。
【点睛】澄清石灰水的主要成分是氢氧化钙,二氧化碳和氢氧化钙反应生成碳酸钙白色沉淀和水。
23. 我们通过学习知道:钠原子结构示意图如下,钠原子在化学反应中易________电子,成为
_______________(填名称)。
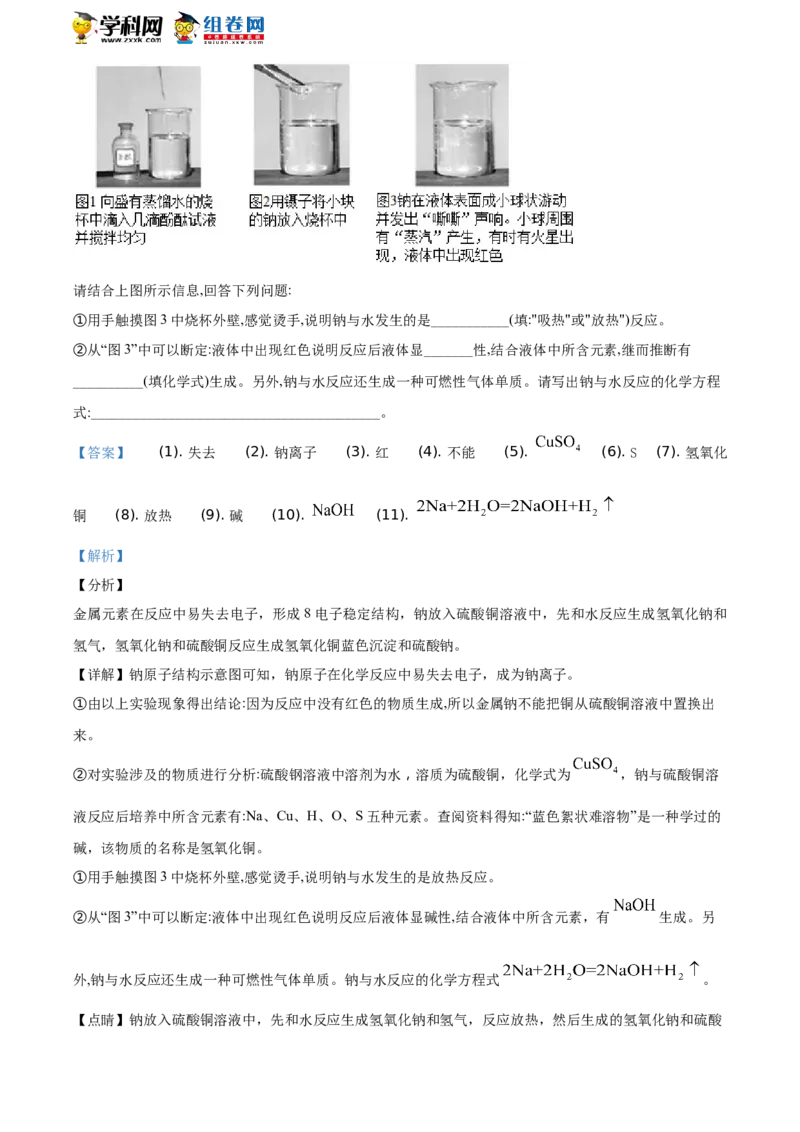
(I)“在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在的前面。
有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。教师按照下列图示顺序进行演示实验,并记录
实验现象:
①由以上实验现象得出结论:因为反应中没有______色的物质生成,所以金属钠______(填:"能"或“不能")把铜
从硫酸铜溶液中置换出来
②对实验涉及的物质进行分析:硫酸钢溶液中溶剂为水.溶质为_________(填化学式),钠与硫酸铜溶液反应
后培养中所含元素有:Na、Cu、H、O、_____(填元素符号)五种元素。查阅资料得知:“蓝色絮状难溶物”是一
种学过的碱,该物质的名称是___________。
(2)有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?教师为解答学生的疑惑,又设计并进行如
下实验.同时记录有关现象:请结合上图所示信息,回答下列问题:
①用手触摸图3中烧杯外壁,感觉烫手,说明钠与水发生的是___________(填:"吸热"或"放热")反应。
②从“图3”中可以断定:液体中出现红色说明反应后液体显_______性,结合液体中所含元素,继而推断有
__________(填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程
式:_________________________________________。
【答案】 (1). 失去 (2). 钠离子 (3). 红 (4). 不能 (5). (6). S (7). 氢氧化
铜 (8). 放热 (9). 碱 (10). (11).
【解析】
【分析】
金属元素在反应中易失去电子,形成8电子稳定结构,钠放入硫酸铜溶液中,先和水反应生成氢氧化钠和
氢气,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠。
【详解】钠原子结构示意图可知,钠原子在化学反应中易失去电子,成为钠离子。
①由以上实验现象得出结论:因为反应中没有红色的物质生成,所以金属钠不能把铜从硫酸铜溶液中置换出
来。
②对实验涉及的物质进行分析:硫酸钢溶液中溶剂为水,溶质为硫酸铜,化学式为 ,钠与硫酸铜溶
液反应后培养中所含元素有:Na、Cu、H、O、S五种元素。查阅资料得知:“蓝色絮状难溶物”是一种学过的
碱,该物质的名称是氢氧化铜。
①用手触摸图3中烧杯外壁,感觉烫手,说明钠与水发生的是放热反应。
②从“图3”中可以断定:液体中出现红色说明反应后液体显碱性,结合液体中所含元素,有 生成。另
外,钠与水反应还生成一种可燃性气体单质。钠与水反应的化学方程式 。
【点睛】钠放入硫酸铜溶液中,先和水反应生成氢氧化钠和氢气,反应放热,然后生成的氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀和硫酸钠。
四、计算题(本大题包括2个小题,共12分)
24. 甲醇是一种无色、有特殊香味、易挥发的液体,可用于制造甲醛和农药等。已知:甲醇由碳、氢、氧三
种元素组成,其中氢元素的质量分数为12.5%,氧元素的质量分数为50%;一个甲醇分子中含有4个氢原子。
请通过计算回答下列问题:
(1)甲醇的相对分子质量是__________;
(2)一个甲醇分子中含氧原子的个数是__________。
【答案】(1)甲醇由碳、氢、氧三种元素组成,氢元素的质量分数为12.5%,一个甲醇分子中含有4个氢原子,
则甲醇的相对分子质量为
(2) 甲醇由碳、氢、氧三种元素组成,氢元素的质量分数为12.5%,一个甲醇分子中含有4个氢原子,则甲
醇的相对分子质量为 ,氧元素的质量分数为50%,则氧元素的质量为 ,氧原
子个数为 ,碳元素的质量分数为 , 碳元素的质量为 ,碳
原子个数为 ,故甲醇的化学式为 。故一个甲醇分子中含氧原子的个数是1。
【解析】
【分析】
甲醇由碳、氢、氧三种元素组成,氢元素的质量分数为12.5%,一个甲醇分子中含有4个氢原子,则甲醇的
相对分子质量为 ,氧元素的质量分数为50%,则氧元素的质量为 ,氧原子个
数为 ,碳元素的质量分数为 ,
碳元素的质量为 ,碳原子个数为 ,故甲醇的化学式为
【详解】见答案。
【点睛】
25. 在进行“实验活动1氧气的实验室制取与性质”前,化学老师预计本次实验共需要收集45瓶氧气,通过计
算得知:这些氧气的总质量约是16g。请计算要想制取足够的氧气,至少需要准备多少克高锰酸钾?
_________。
【答案】158g
【解析】
【分析】高锰酸钾加热生成锰酸钾和二氧化锰和氧气。
【详解】设反应消耗的锰酸钾的质量为x
答:至少需要准备158g高锰酸钾。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635