文档内容
专题 05 实验探究题
1.如图是实验室常用的实验装置,请回答下列问题。
(1)仪器①的名称___ __。
(2)用A装置制取氧气的文字表达式_______________。C和D都可以收集O,选择D装置的优点_____。
2
(3)E装置中水的作用_____。
【答案】(1)长颈漏斗;(2)高锰酸钾=====锰酸钾+二氧化锰+氧气; 收集的气体较为纯净 ;(3)
防止生成物熔化溅落下来使瓶底炸裂
【解析】解:(1)仪器①的名称是长颈漏斗;(2)装置A属于固体加热型,试管口放有一团棉花,采用
的加热高锰酸钾的方法,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是高锰
酸钾=====锰酸钾+二氧化锰+氧气。C和D都可以收集O,D装置是排水法,选择D装置的优点是收集
2
的气体较为纯净;(3)铁丝在氧气中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气瓶的底部应
放少量的水或铺一层细沙,E装置中水的作用是防止生成物熔化溅落下来使瓶底炸裂。故答案为:(1)长
颈漏斗;(2)高锰酸钾=====锰酸钾+二氧化锰+氧气;收集的气体较为纯净;(3)防止生成物熔化溅
落下来使瓶底炸裂。
2.氧气是人类无法离开的物质。
(1)工业上常采用分离液态空气的方法获取O。能说明空气中存在氧气的事例有_______(写一点即可)。
2
(2)实验室用双氧水和二氧化锰制取并收集氧气,可选择的装置组合是_________,该反应的文字表达式
为___________。(3)某些空气净化剂含超氧化钾,其净化原理为: 。该方法一般不用于
实验室制取氧气的原因是________(写一点即可)。
【答案】(1)动物可在空气中呼吸(或食物在空气中腐败等;合理即可);(2)BC或BE; 过氧化氢
=====水+氧气 ;(3)酒精灯;9. 9 ;(4)气体不纯
【解析】(1)人和动物可在空气中呼吸、食物在空气中腐败都说明空气中有氧气,故填:动物可在空气
中呼吸(或食物在空气中腐败等;合理即可)。(2)实验室用双氧水和二氧化锰制取并收集氧气,文字表达
式为:过氧化氢=====水+氧气,该反应不需要加热发生装置选B,氧气不易溶于水,密度比空气大,可
用排水法或向上排空气法收集,收集装置选C或E,故选:BC或BE;过氧化氢=====水+氧气。(3)某
些空气净化剂含超氧化钾,其净化原理为: 。该方法一般不用于实验室
制取氧气的原因是氧气不纯会含有一些二氧化碳,故填:气体不纯。
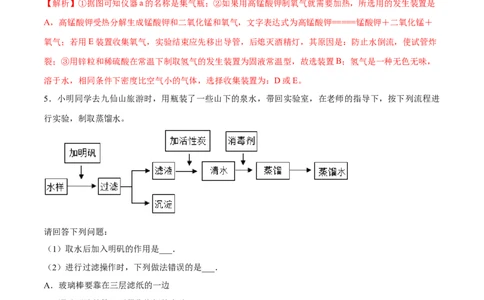
3.(2020广东广州)大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是______。
(2)研究表明氧化铜可催化过氧化氢分解。
①用如图所示装置和药品制取氧气,反应的化学方程式为_________。
②上图中收集氧气的方法是向______排空气法。为了检验氧气是否收集满,将_____放在集气瓶口。
③反应结束后,弃去试管中的上层清液,再向试管中加入过量稀硫酸,充分振荡,可观察到的现象
_______。
④为了制取较大量氧气,并便于多次添加过氧化氢溶液,请从下图中选择合适的仪器或装置,重组一套制
取装置,需要用到的是________(填标号)。
(3)下列设想有可能通过找到合适的催化剂来实现的是______(填标号)。
A 利用太阳光将水分解生产H
2B 将空气中的He分解生产H
2
C 常温下Cu从硫酸镁溶液中置换出Mg
D 使一定质量CH 完全燃烧放出的热量变多
4
【答案】(1)改变反应的速率(或提高生产效率);(2)① ;上;②带火星的
木条;③黑色固体消失,溶液变蓝色;④ACFG ;(3)A
【解析】根据在化学反应里能改变其它物质的化学反应速率,而本身的质量和化学性质在反应前后都没有
发生变化的物质叫做催化剂(又叫触媒);催化剂的特点可以概括为“一变二不变”,一变是能够改变化
学反应速率,二不变是指质量和化学性质在化学反应前后保持不变;发生装置、收集装置的选择依据;进
行分析作答。(1)催化剂的特点是改变反应的速率,速率的改变也会提高生成效率,所以化工生产使用
催化剂的目的是改变反应的速率或提高生产效率;(2)①如图所示装置和药品是过氧化氢在氧化铜的催
化作用下分解制取氧气,反应的化学方程式为 ;②图中收集氧气的方法是向上排
空气法,因为氧气的密度比空气略大;为了检验氧气是否收集满,将带火星的木条放在集气瓶口;③反应
结束后,氧化铜的质量和化学性质不变,向试管中加入过量稀硫酸,氧化铜和稀硫酸反应生成硫酸铜和水,
可观察到的现象是黑色固体消失,溶液变蓝色;④为了制取较大量氧气,并便于多次添加过氧化氢溶液,
发生装置应选择的仪器是锥形瓶、带导管的双孔塞和长颈漏斗,氧气不易溶于水,可用排水法收集,仪器
标号是:ACFG;(3)A、水能分解产生氢气,利用太阳光和催化剂将水分解生产H, 符合题意;B、根
2
据质量守恒定律,化学反应前后元素的种类不变,空气中的He不能分解生产H,不符合题意;C、金属的
2
活动性是:Mg大于Cu,所以常温下Cu不能从硫酸镁溶液中置换出Mg,反应不能发生,不符合题意;
D、催化剂的特点是改变反应的速率,不能改变反应进行的程度,使一定质量CH 完全燃烧放出的热量变
4
多不能实现,不符合题意。故选A。
4.化学是一门以实验为基础的科学。根据下列图示回答问题。①仪器a的名称是_________。
②实验室用高锰酸钾制取氧气的文字表达式为_______。所选用的发生装置是______(填序号)。若用E
装置收集氧气,实验完毕后,先将导管从水槽中移出,再熄灭酒精灯的目的是_________。
③氢气是一种清洁能源。实验室常用锌粒和稀硫酸来制取氢气,应选择的发生装置是_____(填序号,下
同),收集装置除选E外,还可以选_________。
【答案】(1)集气瓶;(2)高锰酸钾=====锰酸钾+二氧化锰+氧气;A;防止水倒流,使试管炸裂 ;
(3)B ;D
【解析】①据图可知仪器a的名称是集气瓶;②如果用高锰酸钾制氧气就需要加热,所选用的发生装置是
A,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,文字表达式为高锰酸钾=====锰酸钾+二氧化锰+
氧气;若用E装置收集氧气,实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸
裂;③用锌粒和稀硫酸在常温下制取氢气的发生装置为固液常温型,故选装置B;氢气是一种无色无味,
溶于水,相同条件下密度比空气小的气体,选择收集装置为:D或E。
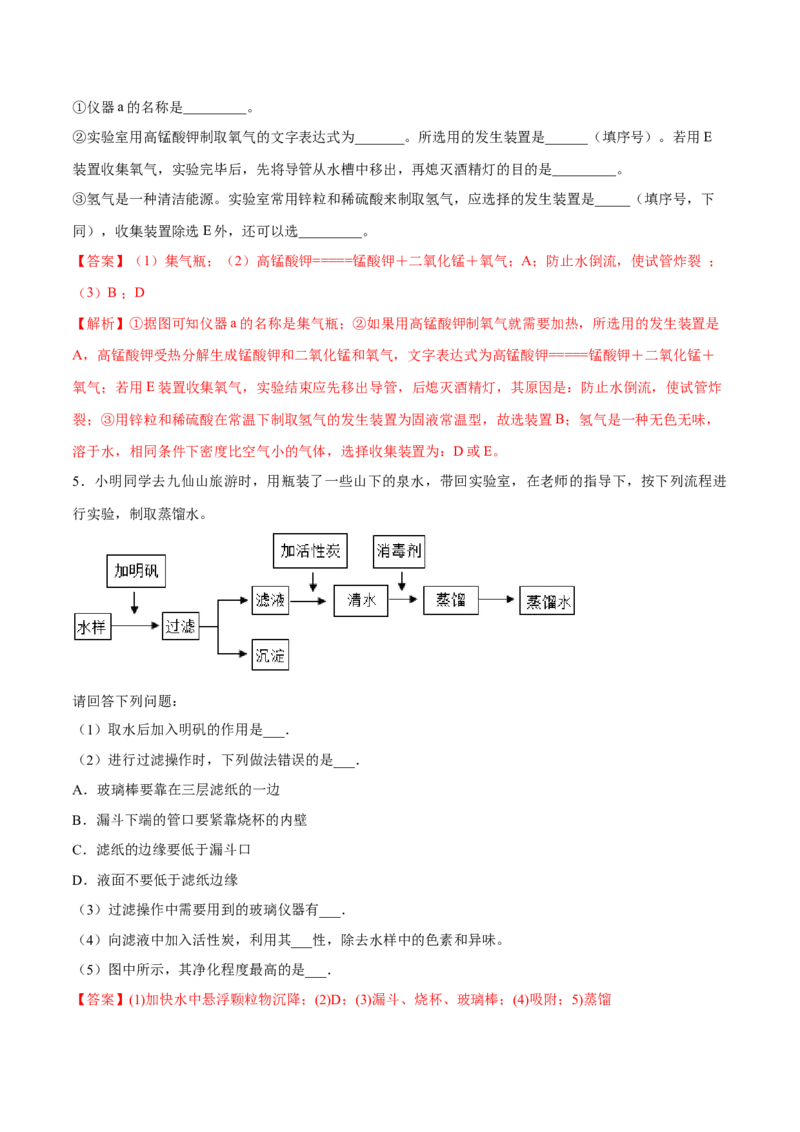
5.小明同学去九仙山旅游时,用瓶装了一些山下的泉水,带回实验室,在老师的指导下,按下列流程进
行实验,制取蒸馏水。
请回答下列问题:
(1)取水后加入明矾的作用是___.
(2)进行过滤操作时,下列做法错误的是___.
A.玻璃棒要靠在三层滤纸的一边
B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口
D.液面不要低于滤纸边缘
(3)过滤操作中需要用到的玻璃仪器有___.
(4)向滤液中加入活性炭,利用其___性,除去水样中的色素和异味。
(5)图中所示,其净化程度最高的是___.
【答案】(1)加快水中悬浮颗粒物沉降;(2)D;(3)漏斗、烧杯、玻璃棒;(4)吸附;5)蒸馏【解析】(1)明矾溶于水形成的胶体能吸附水中的悬浮杂质,使杂质沉降来达到净水的目的;(2)A、
玻璃棒要靠在三层滤纸的一边,操作正确;B、漏斗下端的管口要紧靠烧杯的内壁,操作正确;C、滤纸的
边缘要低于漏斗口,操作正确;D、液面不要低于滤纸边缘,液体会从滤纸和漏斗间流下,操作不正确;
(3)过滤操作中需要用到的玻璃仪器有漏斗、烧杯、玻璃棒;(4)向滤液中加入活性炭,利用其吸附性,
除去水样中的色素和异味。(5)由图示可知,用到的净化水的方法有吸附、过滤、蒸馏、消毒。其中蒸馏得
到的水是纯净物,是净化程度最高的方法。故答为:(1)加快水中悬浮颗粒物沉降;(2)D;(3)漏斗、烧杯、
玻璃棒;(4)吸附;(5)蒸馏。
6.过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水。分液漏斗可以通过调节活塞控制
液体滴加速度。甲、乙两位同学要选用下图所示装置,用过氧化氢溶液和二氧化锰制取氧气。试回答下列
问题:
(1)分液漏斗中应放入的物质是_ __,锥形瓶中应放入的物质是__ _,发生反应的化学方程式为
__ ;
(2)乙两位同学在制取氧气时,都选择A装置作为气体的发生装置,但它们收集气体的装置不同,实验后对比
知道。甲收集的气体纯度比乙高,则甲选择__ _装置收集氧气,乙选择__ _装置收集氧气(填字母)
(3)甲同学选择该装置收集氧气的依据是 ;
(4)乙同学选择该装置收集氧气的依据是 ;
(5)装置A中反应剧烈,据此提出实验安全性注意事项是__ _填(序号)
A.控制液体的滴加速度
B.用体积小的锥形瓶
C.加热反应物。
【答案】(1)过氧化氢溶液;二氧化锰;2HO 2HO+O↑;(2)D、B;(3)氧气不易溶于水;
2 2 2 2
(4)氧气的密度比空气大;(5)A
【解析】(1)分液漏斗中加入的是液体,所以加入的是过氧化氢溶液,锥形瓶中加入的是固体,是二氧化锰;过氧化氢溶液在二氧化锰催化作用下生成水和氧气,故化学方程式为:2HO 2HO+O↑;
2 2 2 2
(2)氧气不易溶于水且密度比空气大,所以可用排水法或向上排空气法收集,利用排水法收集的气体比
排空气法收集的气体纯净,甲收集的氧气比乙纯说明甲用的是排水法,乙用的是向上排空气法收集;
(3)甲同学选择D装置收集氧气的依据是氧气不易溶于水;当集气瓶口有大气泡逸出时说明集气瓶已满;
(4)乙同学选用B收集装置的依据是氧气的密度比空气大;证明氧气已集满的方法是把带火星的木条放
在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了;(5)A、装置A中反应
剧烈,产生大量的氧气,可能会引起爆炸,为了控制反应,可通过控制液体的滴加速度达到控制二者的接
触的目的;故A正确;B、用体积小的锥形瓶,会因产生大量的氧气散发不出去引起爆炸;故 B错误;
C、加热反应物会使反应更加剧烈,更加不易控制,故 C错误;故答案为:(1)过氧化氢溶液;二氧化锰;
2HO 2HO+O↑;(2)D、B;(3)氧气不易溶于水;(4)氧气的密度比空气大;(5)A。
2 2 2 2
7.在二氧化锰的催化作用下,过氧化氢可以迅速分解。除催化剂外还有哪些因素还影响着过氧化氢分解
的速率?课外活动小组结些进行了更深入的探究:
( 1 ) 请 写 出 在 二 氧 化 锰 的 催 化 作 用 下 , 过 氧 化 氢 分 解 的 文 字 表 达 式
。
(2)探究实验一:浓度对化学反应速率的影响
实验步骤 现 象 结 论
取一支试管加入3 5mL5%的过氧化氢溶液,然后加入少量二氧 缓慢有少量气泡
化锰。 冒出
∼
另取一支试管加入3 5mL15%的过氧化氢溶液,然后加入少量二 迅速有大量气泡
氧化锰。 冒出
∼
(3)请你设计:实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
现
实验步骤 结 论
象
温度越高,过氧化氢分解的速率越大
【答案】(1)过氧化氢 水+氧气;(2)温度越高,过氧化氢分解的速率越大;(3)
实验步骤 现 象 结 论
取一支试管加入3~5mL5%的过氧化氢溶液,加入少 缓慢有少量气泡 温度越高,过氧化氢分解的速
量二氧化锰,然后放入冷水中. 冒出 率越大另取一支试管加入3~5mL5%的过氧化氢溶液,加入 迅速有大量气泡
少量二氧化锰,然后放入热水中 冒出
【解析】
(1)过氧化氢在二氧化锰催化剂作用下,分解生成水和氧气,反应的文字表达式为:过氧化氢 水
+氧气,故填:过氧化氢 水+氧气;(2)探究实验一:根据实验现象可以看出,过氧化氢溶液的浓
度越大,在放入二氧化锰时反应越迅速,说明浓度越大,过氧化氢分解的速率越快;故填:浓度越大,过
氧化氢分解越快;(3)探究实验二:要探究温度对化学反应速率的影响,由固定变量可知,该实验操作
是用试管取一定体积和一定浓度的过氧化氢溶液,分别放入盛放冷水和热水的烧杯中观察发生的现象,放
入冷水中的过氧化氢反应不剧烈,而放入热水中的过氧化氢反应剧烈,有大量气泡出现.所以.实验如下:
实验步骤 现 象 结 论
取一支试管加入3~5mL5%的过氧化氢溶液,加入少 缓慢有少量气泡冒
量二氧化锰,然后放入冷水中. 出
温度越高,过氧化氢分解的速
率越大
另取一支试管加入3~5mL5%的过氧化氢溶液,加入 迅速有大量气泡冒
少量二氧化锰,然后放入热水中 出
故答案为:
实验步骤 现 象 结 论
取一支试管加入3~5mL5%的过氧化氢溶液,加入少 缓慢有少量气泡
量二氧化锰,然后放入冷水中. 冒出
温度越高,过氧化氢分解的速
率越大
另取一支试管加入3~5mL5%的过氧化氢溶液,加入 迅速有大量气泡
少量二氧化锰,然后放入热水中 冒出
8.(2020甘肃金昌)实验室常用下列装置制取气体,请你根据所学知识回答有关问题。
(1)写出图中标有序号的仪器名称:①____________;②____________;
(2)实验室用装置A来制取氧气,但装置A有明显错误,请你指出错误___________,若按该装置操作的
后果是______________。
(3)实验室常用装置B来制取氧气,其反应的化学方程式为_________________,收集装置选__________。
实验室选用装置B或装置C还可以制取CO,其反应药品是____________,与装置B相比,装置C的一个
2突出优点是______________。
【答案】(1)①试管;②锥形瓶;(2)试管口高于试管底部 ;冷凝水倒流,试管炸裂;(3)2HO
2 2
2HO+O↑ E或F ;石灰石或大理石和稀盐酸; 可控制反应的发生和停止
2 2
【解析】(1)由图可知①为试管;②为锥形瓶,故填:试管;锥形瓶。(2)试管口需低于试管底部,否
则容易造成冷凝水倒流试管炸裂,故填:试管口高于试管底部;冷凝水倒流,试管炸裂。(3)过氧化氢
制氧气,不需要加热,可用B做发生装置,过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学
方程式为2HO 2HO+O↑,氧气密度比空气大,不易溶于水,可用排水法或向上排空气法收集,故
2 2 2 2
收集装置选E或F;实验室用石灰石或大理石和稀盐酸制取二氧化碳,在装置C中,固体药品放在多孔隔
板上,液体药品从长颈漏斗中加入。反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入
长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固
体混合,反应进行。实验室常用装置C代替装置B制取气体,装置C的优点是可以随时控制反应的发生与
停止,故填:2HO 2HO+O↑;E或F;石灰石或大理石和稀盐酸;可控制反应的发生和停止。
2 2 2 2
9.(2020辽宁锦州)实验可以培养学生的化学核心素养。根据下图回答问题:
(1)仪器a的名称是_____________。
(2)若实验室制取氧气的发生装置选用A装置,反应的化学方程式为_____________。用C装置进行氧气
性质实验时,水的作用是__________。
(3)实验室制取二氧化碳应选择的发生装置是________(填字母序号),将制得的二氧化碳通入到D装
置中,发生反应的化学方程式为__________。
(4)若用E装置收集一瓶干燥的气体,则该气体可能是___________(填字母序号)。A、H B、CO C、O
2 2 2
【答案】(1)长颈漏斗;(2)2KMnO =====KMnO +MnO +O↑ ;防止高温熔化物溅落下来,炸裂瓶
4 2 4 2 2
底等合理表述;(3)B ; CO +Ca(OH) =CaCO↓+H O;(4)A
2 2 3 2
【解析】(1)仪器a的名称是:长颈漏斗;(2)A装置适用于固体加热制取氧气,且试管口有棉花,适
用于高锰酸钾加热制取氧气,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式为:
2KMnO =====KMnO +MnO +O↑;铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成的高温熔
4 2 4 2 2
融物溅落,容易炸裂瓶底,故水的作用是:防止高温熔化物溅落下来,炸裂瓶底;(3)实验室通常用石
灰石和稀盐酸反应制取二氧化碳,该反应属于固液不加热反应,发生装置应选B;将制得的二氧化碳通入
到D装置中,二氧化碳与氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:CO +Ca(OH)
2 2
=CaCO ↓+H O;(4)若用E装置收集一瓶干燥的气体,该气体不与浓硫酸反应,且密度比空气小(收集
3 2
时,从短管进入)。故选A。
10.(2020内蒙古鄂尔多斯)走进化学实验室会给你带来无限乐趣。现有如下装置,结合装置图回答问题:
(1)写出图中带标号①的仪器名称 ________ 。
(2)连接装置 A 和 D ,可制取一种熟悉的气体,反应的化学方程式是 _________ 。要干燥制得的气体,
可将气体通入 F 装置,F 装置中应该装入的试剂名称是 _______ 。
(3)实验室制取气体发生装置的选择依据是 __________ 。选择装置 B 制取二氧化碳时,虽然操作简单,
但无法控制反应速率。将该装置进行简单改进后就可达到控制反应速率的目的,改进措施是 __________ 。
【答案】(1)锥形瓶;(2)2KMnO K MnO + MnO + O ↑ ;浓硫酸(填符号不得分);(3)反
4 2 4 2 2
应条件和反应物的状态(二者缺一不得分);B 装置中再安装一个注射器(或改用装有分液漏斗的双孔塞
等合理答案均可)
【解析】(1)图中带标号①的仪器名称锥形瓶;(2)A装置是固体加热型,且有棉花,则是高锰酸钾制
取氧气,装置D是排水法收集氧气,因为氧气不易溶于水,则反应的化学方程式是2KMnO K MnO
4 2 4+ MnO + O ↑。要干燥制得的气体,可将气体通入 F 装置,F装置中应该装入的试剂名称是浓硫酸;因为
2 2
浓硫酸是液体,有吸水性;(3)实验室制取气体发生装置的选择依据是反应条件和反应物的状态。选择
装置 B 制取二氧化碳时,虽然操作简单,但无法控制反应速率。将该装置进行简单改进后就可达到控制反
应速率的目的,改进措施是B装置中再安装一个注射器(或改用装有分液漏斗的双孔塞等合理答案均可)。
11.根据如图回答问题。
(1)反应原理
①加热高锰酸钾、分解过氧化氢溶液或加热氯酸钾均可产生氧气,其中分解过氧化氢溶液和加热氯酸钾时,
加入二氧化锰在反应中起的作用是___________。三种方法中,写出其中一个反应的化学方程式_______。
②石灰石和稀盐酸反应产生二氧化碳的化学方程式为___________。
(2)制取O 和CO。连接如图的装置完成实验。
2 2
装置(填“甲”或
反应物 物质 B作用 C作用
“乙”)|
_______ _______ 水 _______ 接水
石灰石和稀盐酸 乙 _______ 干燥CO _______
2
【答案】(1)催化作用 ; (或 ;
) ; ;(2)HO 溶液和二氧化锰 ;
2 2
甲 ;收集O;浓HSO ;收集二氧化碳
2 2 4
【解析】(1)①分解过氧化氢溶液和加热氯酸钾时,二氧化锰是催化剂,故加入二氧化锰在反应中起的
作用是:催化作用;过氧化氢在二氧化锰的催化下受热分解为水和氧气,该反应的化学方程式为:
;高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式为:;氯酸钾在二氧化锰的催化下受热分解为氯化钾和氧气,该反应的化
学方程式为: ;②石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯
化钙、二氧化碳和水,该反应的化学方程式为: ;(2)该装置是
固液不加热反应制取氧气,适用于过氧化氢与二氧化锰制取氧气,故反应物是:HO 溶液和二氧化锰;所
2 2
连接装置内所加的物质是水,故应连接甲装置,氧气的密度比水小,从 a端进入,是排水法收集氧气,故
填:HO 溶液和二氧化锰;甲;收集氧气;制取二氧化碳,反应物是:石灰石和稀盐酸,连接装置乙,长
2 2
进短出,故是洗气,可在装置乙中加浓硫酸,浓硫酸具有吸水性,且不与二氧化碳反应,可用于干燥二氧
化碳,二氧化碳的密度比空气大,可用向上排空气法收集,故 C的作用是收集二氧化碳,故填:浓硫酸;
收集二氧化碳。
12.根据下图回答问题:
(1)写出仪器①的名称:_________________。
(2)实验室若用装置A制取较纯净的氧气,反应的文字表达式为______________,可以选
______________(填装置序号)作收集装置。
(3)实验室制取CO,应选择的发生和收集装置的组合是_____________(填装置序号)。在装入药品前,
2
必须要进行的实验操作是______________。
【答案】(1)集气瓶 ;高锰酸钾=====锰酸钾+二氧化锰+氧气;E ;(3)BC;检查装置的气密性
【解析】(1)由图可知,仪器①的名称是:集气瓶;(2)装置A适用于固体加热反应制取气体,且试管
口有一团棉花,适用于加热高锰酸钾制取氧气,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的
文字表达式为:高锰酸钾=====锰酸钾+二氧化锰+氧气; 氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,排水法收集的氧气比较纯净,故收集装置选E;(3)实验室通常用石灰石和稀盐酸
反应制取二氧化碳,该反应属于固液不加热反应,发生装置应选B,二氧化碳溶于水,且密度比空气大,
应用向上排空气法收集,收集装置应选C,故应选择的发生和收集装置的组合是BC;在装入药品前,必须
要进行的实验操作是:检查装置的气密性,防止收集不到气体。
13.(2020内蒙古呼伦贝尔)实验室制取气体时需要的一些装置如下图所示,请回答下列问题。
(1)写出仪器①的名称__________________。
(2)实验室用A装置制取并收集干燥的氧气,所选装置的连接顺序为:A→________→________(填装置
代号),写出A装置中使用催化剂制取氧气的化学方程式:________________________。若用C装置收集
氧气,导管口开始有气泡放出时,不宜立即收集,应在________________时,开始收集气体。
(3)某兴趣小组的同学在实验室连接B、G装置进行实验。若实验时,在G装置中放置一个燃着的蜡烛,
实验过程中蜡烛熄灭,说明生成的气体具有_________________的化学性质,则B装置中反应的化学方程
式为________________________;若将G装置中的蜡烛取出来,改用G装置收集此气体时,验满的方法是
_____________________。
【答案】(1)铁架台;(2)F;E ; ;导管口气泡连续均匀冒出;(3)
不可燃、不助燃 ;CaCO +2HCl=CaCl +H O+CO↑;将燃着的木条放在b管口处,若木条火焰熄灭,则集
3 2 2 2
满二氧化碳
【解析】(1)根据图示,仪器①的名称是:铁架台;(2)实验室用A装置制取并收集干燥的氧气,制取
后,应先用盛有浓硫酸的F装置干燥,再用向上排空气法收集,所选装置的连接顺序为:A→F→E;A装
置中使用催化剂制取氧气,对应的是利用氯酸钾和二氧化锰的混合物加热制取氧气,化学方程式是:
。若用C装置收集氧气,导管口开始有气泡放出时,不宜立即收集,因为开
始排出的气体是装置中原有的空气,所以应在导管口气泡连续均匀冒出时,开始收集气体。(3)在实验室连接B、G装置进行实验。若实验时,在G装置中放置一个燃着的蜡烛,实验过程中蜡烛熄灭,说明B
装置中生成的气体具有不可燃、不助燃的化学性质;在初中阶段利用B装置生成的不可燃、不助燃的气体
是二氧化碳,反应物是大理石和稀盐酸,大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成二氧化碳、
水、氯化钙,反应的化学方程式为:CaCO +2HCl=CaCl +H O+CO↑;若将G装置中的蜡烛取出来,改用
3 2 2 2
G装置收集二氧化碳,由于二氧化碳的密度比空气的大,气体应从a管进入,瓶内的空气从b管排出,验
满的方法是:将燃着的木条放在管口b处,若木条火焰熄灭,则集满二氧化碳。
14.下图是实验室中常见装置。回答下列问题。
(1)装置A中仪器m的名称是________。
(2)用过氧化氢溶液制取氧气的化学方程式为_________,发生装置是_________(填字母序号)。
(3)用装置C收集CO 气体时,气体应从________(填“a”或“b”)端通入。
2
(4)下列气体中,只能用装置D而不能用装置C收集的是________(填数字序号)。
①H ②N ③O
2 2 2
【答案】(1)酒精灯;(2)2HO=====2HO+O↑ ; B;(3)a;(4)②
2 2 2 2
【解析】(1)装置A中仪器m的名称是:酒精灯;(2)过氧化氢在二氧化锰的催化下分解为水和氧气,
该反应的化学方程式为:2HO=====2HO+O↑;该反应属于固液不加热反应,发生装置应选B;(3)二
2 2 2 2
氧化碳的密度比空气大,用装置C收集CO 气体时,气体应从a端通入;(4)①H 难溶于水,可以排水
2 2
法收集,故可用装置D收集,氢气的密度比空气小,用装置C收集,可从b端进入,不符合题意;②N 的
2
密度与空气相差不大,不能用排空气法收集,故不能用装置 C收集,氮气不易溶于水,可用排水法收集,
即可用装置D收集,符合题意;③O 的密度比空气大,用装置C收集时,气体应从a端通入,氧气不易溶
2
于水,可用排水法收集,即可用装置D收集,不符合题意。故选②。
15.在实验室里可采用多种方法制取氧气。(1)写出用如图装置制氧气的化学方程式____________。(写出一个即可)
(2)收集氧气可以采用排水法,这是利用了氧气的什么性质____________?
【答案】(1) ;(2)不溶于水且不与水发生化学反应
【解析】(1)如图装置制氧气是固体加热型,试管口没有一团棉花,其反应原理是氯酸钾在二氧化锰催
化加热的条件下生成氯化钾和氧气,其化学方程式 。(2)收集氧气可以采
用排水法,这是利用了氧气的不溶于水且不与水发生化学反应。
16.化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。
(1)图中标有序号①的仪器名称是________。
(2)实验室用A装置制取氧气,发生反应的化学方程式是________,在试管口放棉花团的作用是
________。
(3)用双氧水制取氧气,探究石蜡燃烧的产物,应选择装置B与________、________(填字母)组合。
收集过程中,检验氧气集满的方法是_________。
【答案】(1)集气瓶;(2)2KMnO =====KMnO +MnO +O↑;防止加热时,高锰酸钾粉末进入导管;
4 2 4 2 2
(3)E ;F;将带火星的木条放在集气瓶口,木条复燃,说明已经集满
【解析】(1)图中标有序号①的仪器名称是:集气瓶;(2)A装置适用于固体加热反应制取氧气,且试管口有一团棉花,故适用于高锰酸钾加热制取氧气,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反
应的化学方程式为:2KMnO =====KMnO +MnO +O↑;在试管口放棉花团的作用是:防止加热时,高
4 2 4 2 2
锰酸钾粉末进入导管;(3)氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,石蜡燃
烧生成二氧化碳和水,为了不影响对石蜡燃烧产物的干扰,收集的氧气应干燥,浓硫酸具有吸水性,且不
与氧气反应,可用浓硫酸进行干燥,为了得到干燥的氧气,应用向上排空气法收集,故应选择B与F、E;
氧气验满:将带火星的木条放在集气瓶口,木条复燃,说明已经集满。
17.(2020黑龙江龙东)结合下列化学实验装置,回答有关问题。
(1)写出图中标有字母的仪器名称:a__________。
(2)实验室用氯酸钾和二氧化锰制取氧气时应选择_________(填代号)作为发生装置,此反应的化学方
程式为_____________。常温下,下列收集氧气的方法不可行的是_____________(填字母序号)。
a.向上排空气法 b.向下排空气法 c.排水法
(3)实验室制取二氧化碳的化学反应方程式为_____,用装置D收集二氧化碳,气体应从__________(填
①或②)端进入。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是_________。
【答案】(1)锥形瓶;(2)A; ;b ;(3)
① ;可以控制反应的发生和停止
【解析】(1)仪器a的名称是:锥形瓶;(2)实验室用氯酸钾和二氧化锰制取氧气,属于固体加热反应,
发生装置应选A;氯酸钾在二氧化锰的催化下受热分解为氯化钾和氧气,该反应的化学方程式为:
;氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集。
故选b;(3)实验室通常用石灰石和稀盐酸反应制取二氧化碳,石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为: ;
二氧化碳的密度比空气大,用装置D收集二氧化碳,气体应从①端进入;(4)实验室常用装置C代替装
置B制取气体,装置C的优点是:可以控制反应的发生和停止,将石灰石置于多孔隔板上,关闭止水夹,
通过长颈漏斗添加稀盐酸,使固液接触,反应发生,生成二氧化碳气体,装置内压强增大,将稀盐酸压入
长颈漏斗中,固液分离,反应停止,打开止水夹,固液接触,反应发生。
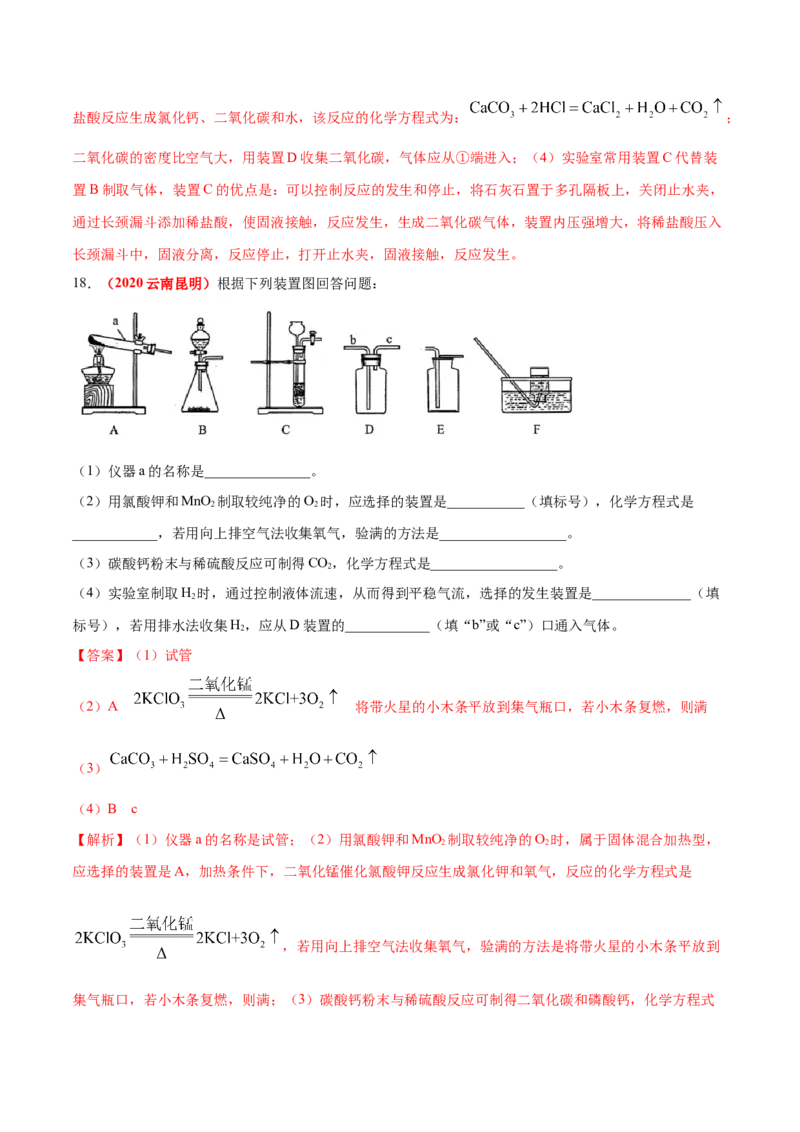
18.(2020云南昆明)根据下列装置图回答问题:
(1)仪器a的名称是_______________。
(2)用氯酸钾和MnO 制取较纯净的O 时,应选择的装置是___________(填标号),化学方程式是
2 2
____________,若用向上排空气法收集氧气,验满的方法是__________________。
(3)碳酸钙粉末与稀硫酸反应可制得CO,化学方程式是__________________。
2
(4)实验室制取H 时,通过控制液体流速,从而得到平稳气流,选择的发生装置是______________(填
2
标号),若用排水法收集H,应从D装置的____________(填“b”或“c”)口通入气体。
2
【答案】(1)试管
(2)A 将带火星的小木条平放到集气瓶口,若小木条复燃,则满
(3)
(4)B c
【解析】(1)仪器a的名称是试管;(2)用氯酸钾和MnO 制取较纯净的O 时,属于固体混合加热型,
2 2
应选择的装置是A,加热条件下,二氧化锰催化氯酸钾反应生成氯化钾和氧气,反应的化学方程式是
,若用向上排空气法收集氧气,验满的方法是将带火星的小木条平放到
集气瓶口,若小木条复燃,则满;(3)碳酸钙粉末与稀硫酸反应可制得二氧化碳和磷酸钙,化学方程式是 ;(4)实验室制取氢气时,通过控制液体流速,从而得到
平稳气流,选择的发生装置是B,通过分液漏斗控制液体的添加量,可得到稳定的气流,若用排水法收集
氢气,应从D装置的c口通入气体,将水从b口排出。
19.(2020四川内江)利用下列装置进行气体的制取实验,请问答下列问题:
(1)写出仪器的名称:①____________②______________。
(2)实验室用过氧化氯溶液制取氧气时,若要制取一瓶干燥的氧气,必须使气体通过__________(填字母,
下同)装置,选用装置___________收集,验满的方法是____________。
(3)实验室用加热高锰酸钾固体的方法制取较纯净的氧气,选用发生装置____________和收集装置G组
合,检查该装置气密性的方法是:连接好仪器,把导管的一端浸入水中,_____________,证明装置连接
完好、不漏气。
(4)实验室用电石固体与饱和食盐水常温下反应制取乙炔(C H)气体,同时有糊状 Ca(OH) 生成,
2 2 2
发生装置选用C而不选用B的原因是_____________;乙炔充分燃烧的化学方程式为____________。
【答案】(1)①铁架台;②分液漏斗;(2)D ; F;用带火星的木条靠近集气瓶口,若木条复燃,则已
经充满 ;(3)A;手紧握试管,如果导管口有气泡冒出 ;(4) 可以控制滴加液体速率和防止糊状Ca
(OH) 堵塞长颈漏斗的下端;
2
【解析】(1)由图可知,仪器①的名称是:铁架台;仪器②的名称是:分液漏斗;(2)浓硫酸具有吸水
性,且浓硫酸与氧气不反应,可用浓硫酸干燥氧气,故若要制取一瓶干燥的氧气,必须使气体通过D装置;
氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,要想得到干燥的氧气,应用向上排空
气法收集,故收集装置选F;氧气具有助燃性,氧气验满:用带火星的木条靠近集气瓶口,若木条复燃,
则已经充满;(3)高锰酸钾加热制取氧气,属于固体加热反应,发生装置应选A;检查该装置气密性的方
法是:连接好仪器,把导管的一端浸入水中,手紧握试管,如果导管口有气泡冒出,证明装置连接完好、不漏气;(4)发生装置选用C而不选用B,因为C装置可通过分液漏斗控制药品的滴加速率,从而控制
反应速率,同时分液漏斗下端无需浸入液面以下,糊状Ca(OH) 不会堵塞漏斗的下端,故填:可以控制
2
滴加液体速率和防止糊状Ca(OH) 堵塞长颈漏斗的下端;乙炔充分燃烧生成二氧化碳和水,该反应的化
2
学方程式为: 。
20.根据下列实验装置回答问题。
(1)仪器a的名称是__________。
(2)用加热高锰酸钾的方法制取氧气,反应的化学方程式为__________。若用排水法收集氧气,停止加
热时,应__________(填序号)。
①先熄灭酒精灯,再把导管移出水面
②先把导管移出水面,再熄灭酒精灯
(3)用大理石和稀盐酸制取并收集二氧化碳,应选用的装置为__________(填序号),反应的化学方程
式为__________。
【 答 案 】 ( 1 ) 铁 架 台 ; ( 2 ) 2KMnO =====KMnO + MnO + O↑ ; ② ; ( 3 ) BD ;
4 2 4 2 2
CaCO +2HCl=CaCl +H O+CO↑
3 2 2 2
【解析】(1)仪器a的名称是铁架台;(2)用加热高锰酸钾的方法制取氧气,反应的原理是高锰酸钾在
加热条件下生成锰酸钾、氧气、二氧化锰,化学方程式为2KMnO =====KMnO +MnO +O↑。若用排水
4 2 4 2 2
法收集氧气,停止加热时,应先把导管移出水面,再熄灭酒精灯,否则易导致水到流入试管内,使试管炸
裂,故选②;(3)用大理石和稀盐酸制取二氧化碳,应选择固-液常温型发生装置B,收集二氧化碳,应
选用的装置为D,因二氧化碳的密度比空气的大,能溶于水并和水反应,只能用向上排空气法收集,反应
的化学方程式为CaCO +2HCl=CaCl +H O+CO↑。
3 2 2 2