文档内容
第一讲 金属的化学性质
知识讲解
(考什么,学什么,轻松提成绩!)
知识点一 金属与氧气的反应
反应条件 金属 现象 化学方程式
常温下反应 镁 ①打磨过的镁条在空气中逐渐变暗; ①常温下:
2Mg+O =2MgO
2
铝 ①打磨过的铝条在空气中逐渐变暗,生成一层致 ①常温下:
密的氧化膜;
4Al+3O =2AlO
2 2 3
点燃或加热 铁 ①常温下,在干燥空气中铁很难与氧气反应;
时反应 ②点燃时:3Fe+2O Fe O
②点燃后,在氧气中剧烈反应。 2 3 4
铜 加热后,表面会生成黑色物质。
②加热时:2Cu+O 2CuO
2
高温不反应 金 在空气中加热不变色 无
归纳总结
1.反应条件分为三种:①常温、②加热(或点燃)、③高温。反应条件越容易,说明金属越活泼。
2.铝制品和金制品都能耐腐蚀,但原理不同。
①铝原理:铝与氧气反应形成一层致密的氧化膜,能阻止铝进一步腐蚀。此是一个化学反应过程。
②金原理:金的化学性质稳定,不与氧气反应。
知识点二 金属与酸的反应
1.镁、锌、铁、铜与盐酸、硫酸反应
金属 现象 化学方程式反应程度 溶液颜色及现象 稀盐酸 稀硫酸
镁 剧烈反应, 溶液仍为无色,有大量气泡。 Mg+2HCl=MgCl +H ↑ Mg+H SO =MgSO +H ↑
2 2 2 4 4 2
生成的气体能燃烧并产生淡蓝
色火焰
锌 较剧烈反应 溶液仍未无色,有大量气泡
铁 反应缓慢 溶液由无色逐渐变为浅绿色。
铜 无任何现象 不反应 不反应
模仿镁与盐酸与硫酸的反应方程式,书写Zn、Fe、的方程式:
锌:Zn+2HCl=ZnCl +H ↑;Zn+H SO =ZnSO +H ↑
2 2 2 4 4 2
铁:Fe+2HCl=FeCl +H ↑;Fe+H SO =FeSO+H ↑
2 2 2 4 4 2
归纳总结
1.四种金属的活动性由强到弱的顺序:Mg>Zn>Fe>Cu。
2.酸最好选择稀硫酸。因为浓硫酸具有氧化性,与活泼金属反应生成SO ,不生成H。
2 2
3.常见有颜色的盐溶液:Cu2+:蓝色;Fe2+:浅绿色;Fe3+:黄色;
练1 下列实验现象的描述正确的是( )
A.铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,溶液由蓝色变为浅绿色
B.一氧化碳在空气中燃烧:火焰淡黄色,放出大量的热
C.将生锈的铁钉放入稀硫酸中:开始时溶液由无色变为浅绿色
D.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热
【答案】A
【解析】
A、铁和硫酸铜反应生成硫酸亚铁和铜,所以铁钉放在硫酸铜溶液中:银白色固体表面有紫红色固体析出,
溶液由蓝色变为浅绿色,故说法正确;
B、一氧化碳在空气中燃烧,火焰淡蓝色,放出大量的热,故说法错误;
C、将生锈的铁钉放入稀硫酸中,开始时铁锈的主要成分氧化铁与稀硫酸反应,生成硫酸铁和水,溶液由
无色变为黄色,故说法错误;
D、生石灰中加入一定量的水,生石灰与水反应生成氢氧化钙,生成的氢氧化钙微溶于水,白色固体变成
白色浆液,反应放出大量的热,故说法错误。故选A。
2.置换反应
Mg + 2HCl = MgCl + H ↑
2 2Zn + 2HCl = ZnCl + H ↑
2 2
Fe + 2HCl = FeCl + H ↑
2 2
单质 化合物 化合物 单质
1.定义:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应叫置换反应。
2.特点:A+BC AC+B
化合反应、分解反应、置换反应的比较
反应类型 特点 举例 简单表示
化合反应 多变一 A+B+……→C
2H+O 2HO
2 2 2
分解反应 一变多 A→C+B+……
2HO 2HO+O↑
2 2 2 2
置换反应 一换一 HSO +Zn ZnSO+H↑ A+BC→B+AC
2 4 4 2
归纳总结
1.由于置换反应是单质与化合物反应生成新的单质和新的化合物,单质中元素的化合价为0,化合物中元
素的化合价不为0,因此置换反应中一定有元素化合价发生变化。
2.置换反应中的单质不一定是金属单质。
3.金属与酸反应后金属质量减少,溶液质量增加。
练1 下列化学反应中不属于置换反应的是
A. Fe+H SO =FeSO +H ↑
2 4 4 2
B. C+2CuO 2Cu+CO
2
C. Cl+2NaI=2NaCl +I
2 2
D. Fe + CuSO =FeSO+ Cu
4 4
【答案】B
练2 下列属于置换反应的是
A.2HO 2H↑+O ↑ B.S+O SO
2 2 2 2 2
C.NaOH+HCl NaCl+H O D.2Al+6HCl 2AlCl +3H ↑
2 3 2【答案】D
知识点三 金属活动性顺序
1.金属活动性顺序的内容
(1)规律
钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。(嫁给那美女)
(2)意义
在金属活动性顺序表中:
①金属的位置越靠前,它的活动性就越_____________。
②位于氢前面的金属能置换出盐酸、稀硫酸(不可以用浓硫酸和硝酸)中的______。
③位于前面的金属(钾、钙、钠除外)能把位于后面的金属从它们化合物的溶液里__________出来。当金
属与两种以上盐溶液反应时,优先置换出__________的金属。即:前置后,盐可溶,钾、钙、钠除外,不
活泼金属的盐溶液优先。
①强 ②氢 ③置换 最不活泼
练1 下列金属中,金属活动性最强的是( )
A.铝 B.铁 C.铜 D.金
【答案】A
练2 金属X在溶液中的活动性是AgY>Z B.Z>X>Y C.X>Z>Y D.Y>X>Z
【答案】B
【解析】
在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的
活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。X、Y、Z三种金属片,分别
放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,说明X、Z在氢前,Y在氢后,X放入ZCln溶液,没
有明显现象,说明X在Z后,三种金属的活动性由强到弱的顺序是Z>X>Y。故选B。
练2 某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的是
( )
A. 将Fe、Cu分别加入AgNO 溶液中
3
B. 将Fe、Cu、Ag分别加入稀盐酸中
C. 将Fe分别加入CuSO 、AgNO 溶液中
4 3
D. 将Fe、Ag分别加入CuSO 溶液中
4
【答案】D
【解析】A、铁、铜都能与AgNO 溶液反应,证明铁、铜的活动性比银强,但不能比较铁、铜的活动性的
3
强弱,故该方案不能达到目的;
B、铁和稀盐酸反应,铜、银和稀盐酸不反应,而则得出:铁>铜、银,但不能比较铜、银的活动性的强
弱,故该方案不能达到目的;
C、铁与CuSO 、AgNO 溶液反应,说明了活动性铁>铜、银,但不能比较铜、银的活动性的强弱,故该
4 3
方案不能达到目的;
D、铁与CuSO 溶液反应置换出铜,说明了活动性铁>铜;银与CuSO 溶液不反应,说明了活动性铜>银,
4 4
由此可得的三种金属活动性铁>铜>银,故该方案能达到目的。
3.金属与金属化合物溶液反应后滤液、滤渣成分的判断
1.活动性强的金属优先置换出活动性最弱的金属,再置换出活动性较弱的金属。
2.多种活泼金属单质与一种不活泼金属化合物溶液反应时,活动性最强的金属优先反应,然后是活动性较弱的金属反应。
3.根据反应物量的不同,反应分三种情况:部分反应、恰好完全反应、过量,据此分析滤液和滤渣的成
分。
练1 在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,滤渣中所含物
质不可能的情况是( )
A.可能有银和铜,没有锌 B.可能只有银,没有铜和锌
C.一定有银,可能有铜和锌 D.一定有银、没有锌,可能有铜
【答案】C
【解析】
在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,说明仍有硫酸铜,锌
比铜和银都活泼,铜比银活泼。A、滤渣中可能有银和铜,没有锌,锌为不足量,故A正确;B、可能只
有银,没有铜和锌,锌比铜和银都活泼,铜比银活泼,故B正确;C、一定有银,可能有铜,一定没有锌,
故C错误;D、 一定有银、没有锌,可能有铜,故D正确。
知识点四 流程题——金属回收利用问题
练1 某校化学社团—“拉瓦锡实验室”的活动丰富多彩。他们在实验室废液桶中收集了含有大量
FeSO 、CuSO 的废水,为防止废水直接排放到下水道造成重金属污染和浪费,设计了如图所示
4 4
(1)整个实验过程中多次采用过滤,该操作用到的玻璃仪器有烧杯、________和玻璃棒。
(2)所加物质X是________________________(填名称),其加入废水后发生反应的化学方程式为
____________________________________。溶液Y是____________(填名称);固体A中含有的物质是
____________(填化学式)。
(3)该小组的同学又收集到一些含硝酸银、硝酸铜的混合废液,同学们向其中加入一定量锌粉,反应停
止后过滤,滤液仍为蓝色。则下列有关判断正确的是____________(填字母)。A 滤渣中一定有银,没有铜和锌
B 滤渣中一定有银和锌,可能有铜
C 滤液中一定有硝酸锌、硝酸铜、硝酸银
D 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
【答案】漏斗 铁 Fe+CuSO=FeSO+Cu 稀硫酸 Cu、Fe D
4 4
【分析】
最终产物为Cu和FeSO ,因此第一步需将溶液中的Cu2+和Fe2+分离,故应加入过量的铁,将Cu2+转化为
4
Cu,固体中含有置换出的Cu和过量的Fe,Fe可通过加入稀硫酸转化为FeSO ,与第一步的滤液混合。
4
【详解】
(1)过滤涉及到的玻璃仪器有烧杯、漏斗和玻璃棒。
(2)通过上述分析,X为铁,铁与CuSO 的产物为Cu和FeSO ,化学方程式Fe+CuSO=FeSO+Cu。溶液
4 4 4 4
Y为稀硫酸;固体A是含有Cu、Fe。
(3)向AgNO 和Cu(NO ) 的混合溶液中加入Zn,Zn会先与AgNO 反应,当AgNO 被反应完后,再与
3 3 2 3 3
Cu(NO ) 反应。此实验中,滤液呈蓝色,说明溶液中一定有Cu(NO ) ,但不能确定AgNO 是否被反应完,
3 2 3 2 3
溶液中一定有 Zn(NO ) 。Zn 会先置换出 Ag,再置换出 Cu,因此滤渣中一定有 Ag,根据溶液中有
3 2
Cu(NO ) 可知,Zn无剩余,Cu可能有。故选D。
3 2
知识点五 金属与酸反应的图像
1.Zn、Mg、Fe与盐酸反应图像
1.等质氢图
思考与交流
1、过量的Al、Fe与少量且等质量的稀盐酸反应,哪个金属率先反应完酸?
Al。活泼性:Al>Fe,所以Al的先反应完
2、产生的氢气由金属还是稀盐酸决定?反应完全后,氢气的质量相等吗?
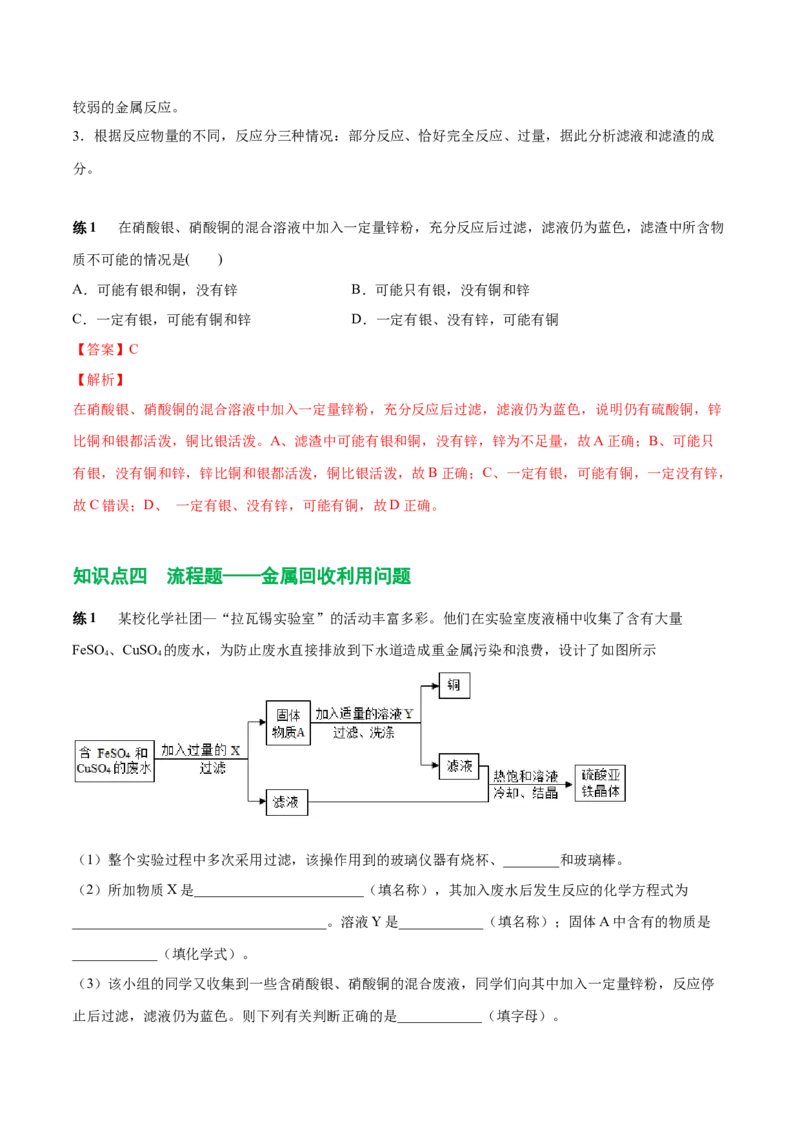
稀盐酸;相等。两种金属反应产生的氢气质量相同,此图反映了两种情况:
(1)酸不足,金属过量,产生的氢气质量由酸的质量决定。
(2)酸足量,产生的氢气质量由金属的质量决定,产生氢气的质量相同。如18 g铝和56 g铁分别投入足
量的稀硫酸中反应产生的氢气质量相同。
2.等质等价金属图
思考与交流
1、计算均为1g的Mg、Zn、Fe与足量的稀盐酸反应,得到多少g的H ?并做个比较。
2
Mg+2HCl=MgCl +H Zn+2HCl=ZnCl +H Fe+2HCl=FeCl +H
2 2 2 2 2 2
24 2 65 2 56 2
1g xg 1g xg 1g xg
x=2/24 x=2/65 x=2/56
2、思考金属的相对原子质量与m(H )的关系?
2
相对原子质量越小,产生氢气越多。
3、尝试根据Mg、Zn、Fe的活泼性、产物H 的质量,绘制反应时间(t)—氢气质量(m(H ))的图像。
2 2
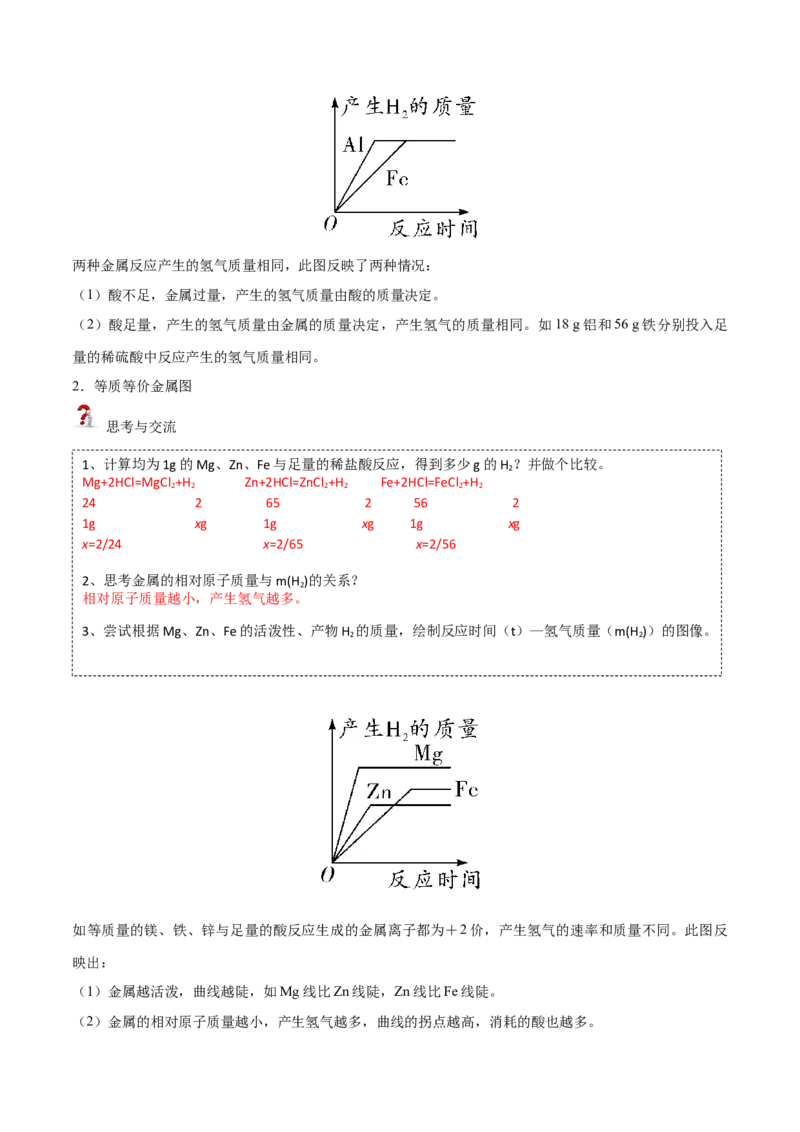
如等质量的镁、铁、锌与足量的酸反应生成的金属离子都为+2价,产生氢气的速率和质量不同。此图反
映出:
(1)金属越活泼,曲线越陡,如Mg线比Zn线陡,Zn线比Fe线陡。
(2)金属的相对原子质量越小,产生氢气越多,曲线的拐点越高,消耗的酸也越多。可简单概况为“越陡越活,越高越小”。
练1 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2
价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
A.M、N两种金属中较活泼的是N
B.生成H 的质量M<N
2
C.相对原子质量较小的是M
D.产生H 的速率N>M
2
【答案】C
【解析】
A、由图中信息可知,M与稀盐酸反应的速率快,说明M比N活泼,此选项错误;
B、由图中信息可知,M与稀盐酸反应生成氢气的质量大,此选项错误;
C、设M、N的质量都是z,相对原子质量分别为x、y,生成氢气的质量为m、n,
,解得x= ,
,解得y= ,
因为m>n,所以x<y,即N的相对原子质量大于M的相对原子质量,此选项正确;
D、由图中信息可知,M与稀盐酸反应生成氢气的速率快于N和稀盐酸反应生成氢气的速率,此选项错误。
故选C。练2 等质量的下列金属,分别与足量稀盐酸反应,生成氢气最多的是( )
A.Ag B.Mg C.Fe D.Zn
【答案】B
【解析】银不能与稀盐酸反应,不能生成氢气.
Mg的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成 克氢气.
铁的相对原子质量56,56g铁可反应生成2g氢气,即1g铁生成 g氢气.
Zn的相对原子质量为65,65g锌可反应生成2g氢气,即1g锌生成 克氢气.
所以镁放出的氢气最多.
故选B.
练3 将质量相等的A、B、C三种金属,分别放入三份质量分数相同且足量的稀盐酸中,反应生成H 的
2
质量与反应时间的关系如图所示,根据图中所提供的信息,得到的结论正确的是( )
(已知:A、B、C在生成物中均为+2价)
A.反应速率最大的是A
B.放出H 的质量是A>B>C
2
C.相对原子质量是A>B>C
D.金属活动性顺序是A>B>C
【答案】B
【解析】
根据化学反应图像可知,B与酸的化学反应速率最快,活动性最强,A次之,C的活动性最弱。由于A、
B、C在生成物中均为+2价,它们与酸反应的质量比即为相对分子质量之比,相对原子质量越大,生成的
氢气的质量越小,故相对原子质量是C>B>A。根据图像可知,放出H 的质量是A>B>C,B正确。
2
故选B。
练4 在托盘天平两边各放一只烧杯并注入相同的足量稀盐酸,调节至平衡,然后向左、右两边烧杯中分
别投入等质量的镁和铝,则天平指针的偏转情况是( )A.先偏向右,最后偏向左 B.先偏向右,最后平衡
C.先偏向左,最后偏向右 D.先偏向左,最后平衡
【答案】A
【详解】
解:镁、铝和稀盐酸反应的化学方程式及其反应物、生成物之间的质量关系为:
, 根据反应物和生成物的质量关系可知,等质量
的镁和铝和足量稀盐酸反应时,铝和稀盐酸反应生成的氢气多,因此天平指针最后偏向左;因为镁比铝活
泼,与稀盐酸反应时,镁和稀盐酸反应的速率比铝和稀盐酸反应的速率快,因此开始时镁和稀盐酸反应生
成的氢气速率快,天平指针偏向右,因此向左、右两边烧杯中分别投入等质量的镁和铝,则天平指针的偏
转情况是先偏向右,最后偏向左。故选A。
课后作业
1.现有甲、乙、丙三种金属,甲在常温下就能与氧气反应,乙、丙在常温下几乎不与氧气反应;如果将
乙、丙分别放入硫酸铜溶液中,过一会儿,在丙的表面有红色固体析出,而乙表面没有变化,则甲、乙、
丙三种金属的活动性由弱到强的顺序是( )
A.甲乙丙 B.乙甲丙 C.乙丙甲 D.甲丙乙
【答案】C
【详解】
有甲、乙、丙三种金属,甲在常温下就能与氧气反应,乙、丙在常温下几乎不与氧气反应,说明甲的活动
性最强,乙、丙的活动性较弱,即金属活动性甲>乙、丙;把乙和丙分别放入硫酸铜溶液中,过一会儿,
在丙的表面有红色固体析出,说明丙的金属活动性比铜强,即丙>铜;而乙表面没有变化,说明乙的金属
活动性比铜弱,即铜>乙;则甲、乙、丙三种金属的活动性由强到弱的顺序是甲>丙>乙。因此由弱到强的
顺序是:乙<丙<甲。
故选C2.某溶液中有Cu(NO ) 和Fe(NO ),加入一定量的Zn粉末充分反应后过滤,在滤渣中滴加稀盐酸,有气
3 2 3 2
泡产生。下列关于滤液的判断正确的是( )
A.一定不会是无色 B.一定不会是蓝色
C.一定不会是浅绿色 D.以上判断皆不正确
【答案】B
【解析】
在金属活动性顺序中,Zn>Fe>H>Cu,向溶液中有Cu(NO ) 和Fe(NO ),加入一定量的Zn粉,锌
3 2 3 2
优先与Cu(NO ) 反应,再与Fe(NO ) 反应。在滤渣中滴加稀HCl,有气泡产生,说明了滤渣中有活
3 2 3 2
动性大于氢的金属存在,一定有铁,可能有锌。A、当锌的量过量,能把铁全部置换出来时,溶液呈无色,
错误;B、由于有活动性大于氢的金属存在,溶液中的铜全部被置换出来,所以溶液一定不会是蓝色,正
确;C、当锌的量不足时,不能把铁全部置换出来,溶液可能呈浅绿色,错误;D、以上判读中B正确,D
错误。故选B。
3.(双选)为了验证铁、镁、铜的活动性顺序,最适宜的试剂组是( )
A.镁、铁、氯化铜溶液
B.铁、铜、硫酸镁溶液
C.铜、硫酸镁溶液、氯化亚铁溶液
D.铁、氯化镁溶液、硫酸铜溶液
【答案】AD
【详解】
A、将活动性比铜强的铁放入氯化铜溶液,根据置换出的铜检验铁的活动性比铜强;然后将镁放入反应得
到的氯化亚铁溶液中,通过置换出铁检验镁的活动性比铁强;试剂适宜;
B、由于铁、铜均不能与硫酸镁溶液发生反应,使用该组试剂不能完成三种金属活动性的验证;试剂不适
宜;
C、铜既不能与硫酸镁溶液反应也不能与氯化亚铁溶液反应,使用该组试剂不能完成三种金属活动性的验
证;试剂不适宜;
D、铁能置换出硫酸铜中的铜而不能与氯化镁发生反应,可说明铁的活动性比铜强而比镁弱,使用该组试
剂可验证三种金属活动性强弱;试剂适宜;
故选:AD。
4.将等质量的镁、铁、锌三种金属分別放入三份溶质质量分数相等的稀盐酸中.生成H 的质量与反应时
2间的关系如图所示.金属X是__(填化学式,下同),反应后可能已经反应完的金属是__,一定有剩余的
金属是__.
【答案】Mg Zn、Fe Mg
【详解】
解:Mg+2HCl=MgCl +H ↑;Fe+2HCl=FeCl +H ↑;Zn+2HCl=ZnCl +H ↑
2 2 2 2 2 2
由化学方程式可知,24份质量的镁会生成2份质量的氢气,56份质量的铁会生成2份质量的氢气,65份质
量的锌会生成2份质量的氢气,通过分析图象可知,镁的金属活动性最强,金属X是Mg,由质量关系可
知,反应后可能已经反应完的金属是Zn、Fe,一定有剩余的金属是Mg。观察图像可知,三种金属反应的
速率X>Y>Z,判断出三种金属的活动性顺序为X>Y>Z,从而得知X为镁,Y为锌,Z为铁。相同质量的
三种金属完全参加反应,应该是镁消耗的酸最多,铁次之,锌最少,但图中铁产生氢气最多,即消耗稀盐
酸最多;镁锌产生氢气一样多,即消耗稀盐酸一样多,故镁过量,但锌无法确定。故选C。
5.小明同学家新换了水龙头,从说明书上了解到该水龙头是钢质镀铬。好奇的小明想探究铬(Cr)与常
见金属铁、铜的活动性强弱,邀请你一同参加。
(1)(作出猜想)
小明根据金属活动顺序: K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au,作出猜想:
猜想1. Cr>Fe>Cu;猜想2. Fe>Cu>Cr;猜想 3.你的猜想是_____。
(2)(查阅资料)
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(GrSO ) 溶液。
4
(3)(设计与实验)
小明同学取大小相等的三种金属片,用砂纸打磨光亮,再分别放入三支试管中,然后分别加入等量的同种
稀硫酸,观察现象并得出了猜想1正确的结论,请你根据猜想1正确的结论完成表格:
实验 试管1 试管2 试管3实验
操作
实验 铜片表面没有气产生,溶液
①_____,_____。 ②_____,_____。
现象 颜色无明显变化
(4)(结论与解释)
①实验前用砂纸打磨金属片的目的是_____。
②请你写出铬与稀硫酸反应的化学方程式_____。
【答案】Fe>Cr>Cu 铁片表面有气泡产生而且较慢 溶液由无色变浅绿色 铬片表面有气泡产生而
且较快 溶液由无色变蓝色 除去金属表面的氧化膜 Cr+H SO =CrSO+H ↑
2 4 4 2
【详解】
(1)作出猜想:由于铁、铜的活动性顺序为Fe>Cu,则金属Cr可放在前、后、中间位置;故答案为:
Fe>Cr>Cu;
(3)观察现象并得出了猜想1正确的结论,所以三种金属的活动性顺序是Cr>Fe>Cu;
铁与硫酸反应生成硫酸亚铁和氢气,试管1中的实验现象是铁片表面有气泡产生而且较慢,溶液由无色变
浅绿色;
铬的活动性大于铁,硫酸亚铬(GrSO ) 溶液呈蓝色,试管2中的实验现象是铬片表面有气泡产生而且较
4
快,溶液由无色变蓝色;
(4)(结论与解释)
①实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜;
②铬与稀硫酸反应生成硫酸铬和氢气,反应的化学方程式:Cr+H SO =CrSO+H ↑。
2 4 4 2