文档内容
第八单元 课题1 金属材料
1.金属材料分类:包括纯金属和合金。
2.人类利用金属的先后顺序是铜、铁、铝。
3.金属的物理性质及用途
(1)物理共性:具有金属光泽→制成装饰品
良好的导电性→制电线、电缆
良好的导热性→制作炊具
良好的延展性→拉成细丝、压成薄片
(2)物理特性:颜色:大多数金属都呈银白色,但铜呈紫红色,金呈黄色。
状态:常温下,大多数金属都是固体,但汞是液体。
4.金属之最
生活中应用最广泛的金属是铁,导电、导热性最好的金属是铜,
地壳中含量最高的金属元素是铝,人体中含量最高的金属是钙,
熔点最高的金属是钨,熔点最低的金属是汞。
5.合金
(1)定义:在金属中加热熔合某些金属或非金属,制得的具有金属特性的混合物。
(2)特性:与组成合金的纯金属相比,硬度更大、熔点更低、抗腐蚀性更强。
(3)铁合金:
生铁和钢性能不同的原因是 含碳量 不同 ,其在生铁中的含量为2%~4.3%,在钢中的含量为0.03%~2%。
(4)钛和钛合金:
被认为是21世纪的重要金属材料,钛合金与人体具有良好的“相容性”,可用来造人造骨。
钛和钛合金的优点:①熔点高、密度小; ②可塑性好、易于加工、机械性能好; ③抗腐蚀性能好。
第八单元 课题2 金属的化学性质
1.金属+氧气→金属氧化物
(1)3Fe+2O
点燃
Fe O(火星四射,生成黑色固体);
2 3 4
(2)4Al+3O===2Al O(表面光泽变暗,致密保护膜);
2 2 3
(3)2Cu+O ∆ 2CuO(铜表面变黑或红色固体变黑);
2
(4) “真金不怕火炼”:金 在 高温下也不与氧气反应 。
2.金属(氢前)+酸(稀盐酸、稀硫酸)→ 盐 + 氢气
(1)Mg+2HCl==MgCl +H ↑;Mg+HSO ==MgSO +H ↑;
2 2 2 4 4 2(2)Fe+2HCl==FeCl +H ↑;Fe+HSO ==FeSO + H ↑;(溶液由无色变为浅绿色)
2 2 2 4 4 2
(3)2Al+6HCl==2AlCl + 3H ↑;2Al+3HSO ==Al (SO ) + 3H ↑。
3 2 2 4 2 4 3 2
3.金属+盐溶液→ 新金属 + 新盐
(1)Fe+CuSO ==FeSO + C u(铁表面覆盖红色固体,溶液由蓝色逐渐变 浅 绿 色);
4 4
(2)Cu+2AgNO== 2Ag + Cu(NO ) (铜表面覆盖银白色固体,溶液由无色逐渐变蓝色);
3 3 2
(3)2Al+3CuSO == 3Cu + Al (SO ) (铝表面覆盖红色固体,溶液由蓝色逐渐变无色)。
4 2 4 3
4.金属活动性
(1)金属活动性顺序:
K Ca Na (Mg)(Al)(Zn)(Fe)Sn Pb (H)(Cu)(Hg)(Ag)Pt Au
(2)应用:
①金属的位置越靠前,金属的活动性就越强。
②位于氢前面的金属可以与稀盐酸、稀硫酸反应,且位置越靠前,反应越剧烈。
③位于前面的金属能把位于后面的金属从它们的盐溶液里置换出来。
注意:涉及金属的有关反应不涉 及 K 、 C a 、 N a 三种金属,酸不涉及 浓 H SO 和硝酸,涉铁的置换反应不涉
2 4
及 +3 价铁 的化合物。
第八单元 课题3 金属资源的利用和保护
1.常见的金属矿石
赤铁矿(主要成分是Fe O )、磁铁矿(主要成分是Fe O )菱铁矿(主要成分是FeCO )、铝土矿(主要
2 3 3 4 3
成分是Al O)。
2 3
2.铁的冶炼
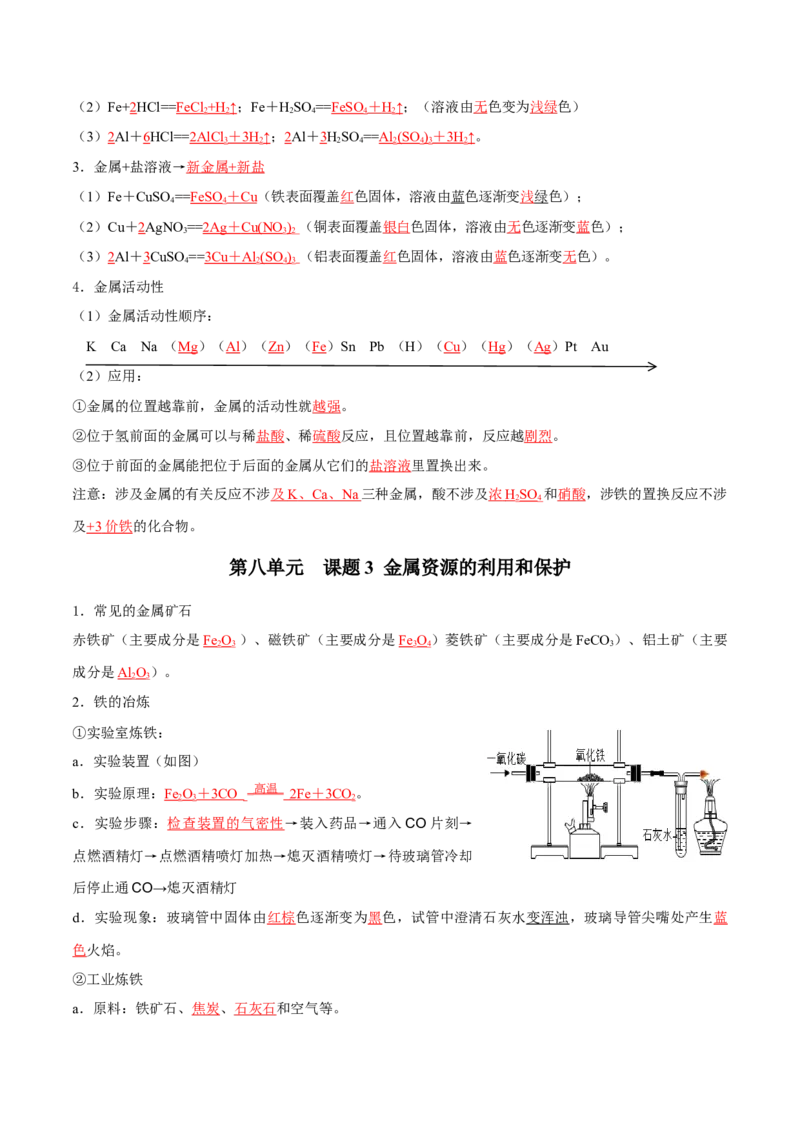
①实验室炼铁:
a.实验装置(如图)
b.实验原理:Fe O + 3CO
高温
2F e + 3CO 。
2 3 2
c.实验步骤:检查装置的气密性→装入药品→通入CO片刻→
点燃酒精灯→点燃酒精喷灯加热→熄灭酒精喷灯→待玻璃管冷却
后停止通CO→熄灭酒精灯
d.实验现象:玻璃管中固体由红棕色逐渐变为黑色,试管中澄清石灰水变浑浊,玻璃导管尖嘴处产生蓝
色火焰。
②工业炼铁
a.原料:铁矿石、焦炭、石灰石和空气等。b.主要设备:高炉。
c.发生的化学反应:
主要反应(以赤铁矿为原料)Fe O + 3CO
高温
2F e + 3CO 。
2 3 2
焦炭的作用:燃烧提供热量(C+ O
高温
CO)、制取CO(C+CO
高温
2CO) 。
2 2 2
石灰石的作用:将矿石中的二氧化硅转变为炉渣。
高温
拓展:百炼成钢的主要化学反应是C+ O CO。
2 2
3.金属资源的保护
(1)金属的腐蚀和防护
①铁制品锈蚀条件的探究
实验装置
经过一段时间后,试管A中铁钉表面出现红色铁锈,试管B和C中铁钉表面无明显现
实验现象
象。
对比试管A和B中的现象可知,铁生锈需要氧气。
实验结论 对比试管A和C中的现象可知,铁生锈需要水。 铁锈是主要成分是Fe O。
2 3
铁生锈的条件是与氧气和水同时接触。
试管中是经煮沸迅速冷却的蒸馏水,煮沸的目的是除去水中溶解的氧气,迅速冷却的目的
是 防止空气中氧气溶解到水中 。
实验拓展 试管B中植物油的作用是隔绝空气。
试管C中干燥剂的作用是隔绝水。
在高温、酸、食盐溶液等环境中铁生锈的速率会加快。
②防止铁制品生锈的原理及措施
防锈原理:破坏铁生锈的两个必备条件之一即可。隔绝氧气或隔绝水。
防锈措施:保持铁制品表面洁净干燥;在铁制品表面覆盖保护层,如涂油、刷漆、烤蓝、镀其他金属等;
改变金属的内部结构,如制成不锈钢等。
(2)金属资源的保护
①有效途径:防止金属腐蚀;回收利用废旧金属;有计划、合理地开采矿物;寻找金属的替代品。②回收利用废旧金属的优点:节约金属资源和能源、 保护环境。