文档内容
高三化学解析
一.选择题
1.【答案】C
【解析】A.植物油中含有不饱和键,和H 发生加成反应变成饱和高级脂肪酸甘油酯,延迟保质期,A正确;
2
B.葡萄糖是多羟基醛,属于单糖,含有羟基,能够和硝酸发生酯化反应,B正确;
C.N 因其键能较大,性质较稳定,一般不用做火箭推进剂的助燃剂,C错误;
2
D.甲壳素、壳聚糖是膳食纤维,属于纤维素的一种,(不知道的可以翻书),D正确。
2.【答案】A
【解析】A,OF 的价层电子对为4,其中有2对孤对电子,故A正确;
2
B,HBrO的结构式应为:H-O-Br,其中O有2个单电子,成二价键,故O原子排在中间,故B错误;
C,NaH属于离子化合物,故C错误;
D,HCl分子中的共价键是s-p头碰头形成σ,其中s能级电子云形状为球形,故D错误。
3.【答案】B
【解析】A.1mol冰中平均含2mol氢键,A正确;
B.因为存在2NO 2N
2
O
4
反应,NO
2
相对于H
2
的密度大于23,B错误;
C.即使存在2NO 2N
2
O
4
反应,但NO
2
微粒数不变,1.5molNO
2
微粒发生反应:3NO
2
+H
2
O=2HNO
3
+NO
转移的电子数为N ,C正确;
A
D.发生的反应为2NO +2OH-=NO+NO+H O,D正确。
2 2 3 2
4.【答案】C
【解析】A项,向足量的Na SO 溶液中通入少量的Cl :Cl +3SO2+H O=SO2+2Cl-+2HSO -,故A错误;
2 3 2 2 3 2 4 3
B项,H O 使酸性KMnO 溶液褪色:2MnO+5H O +6H+=2Mn2++5O ↑+8H O,故B错误;
2 2 4 4 2 2 2 2
C项,邻羟甲基苯酚分子间脱水缩合制酚醛树脂: ,
发生分子间脱水,故C正确;
D项,向0.1molFeBr 溶液中通入标况下2.24L的Cl :2Fe2++2Br-+2Cl =2Fe3++Br +4Cl-,故D错误。
2 2 2 2
5.【答案】B
【解析】A.分子式应为C H O NF,A错误;
8 8 2
B.羰基C以sp2杂化,与所连的N/C共平面,N连在苯环上,可通过旋转苯环C-N键实现所有CN共平面,
B正确;
C.因为有-OH,所以红外光谱会出现O-H键的伸缩振动吸收峰,C错误;
D.-F处水解,最多可消耗2molNaOH,所以1mol氟代对乙酰氨基酚最多可消耗4molNaOH,D错误。
化学解析(共 8 页)第 1 页6.【答案】D
【解析】A.蒸馏时一般选用直形冷凝管,球形冷凝管会在球部有液体残留,A错误;
B.蒸发结晶一般选用蒸发皿,B错误;
C.酸性高锰酸钾溶液盛装在酸式滴定管中,C错误;
D.盛装NaOH溶液的试剂瓶需选用橡胶塞,D正确。
7.【答案】B
【解析】根据题意,可知A为Na S或Na S O ,B为H SO ,C为S,D为Na SO ,E为SO ,F为SO ,
2 2 2 3 2 4 2 4 2 3
M/N为Na S或Na SO 。
2 2 3
A.浓硫酸常温下有强氧化性,能够使Fe和Al钝化,故可以用铁制品或铝制品来贮存,A正确;
B.S和O 一步反应只能得到SO ,不能得到SO ,B错误;
2 2 3
C.SO 催化氧化得到SO ,原料气中含有砷、硒化合物等杂质,会让钒催化剂永久中毒失去活性,C正确;
2 3
D.Na S和Na SO 都有较强的还原性,可以被强氧化剂氧化成Na SO (Na S一般被氧化成S,但是在被过
2 2 3 2 4 2
量的强氧化剂条件下,可以逐步被氧化成Na SO ),D正确。
2 4
8.【答案】D
【解析】A.已知KrF 是直线形分子,则其正负电荷中心重合,属于非极性分子,A正确。
2
197x 67.47% x 1
B.设B的化学式为Au F ,B中Au、F的质量分数分别为67.47%、32.53%,则 , ,故
x y
19y 32.53% y 5
△
B的化学式为AuF ,加热A分解生成B的化学方程式为KrAuF AuF +Kr↑+F ↑,B正确;
5 7 5 2
C.Au最高价为+5价,易和F-形成一种稳定的八面体构型的配离子,即[AuF ]-,(参考选择性必修2SF 的
6 6
结构),A为强电解质,则A的电离方程式为KrAuF =[KrF]++[AuF ]-,C正确;
7 6
D.电离不是分解,不考虑KrF 在HF中以Kr和F 的形式存在,且稀有气体也很难以单独的离子(Kr2+)存
2 2
在,再结合核磁共振谱表明溶于液态HF的KrF 的两个氟原子是等同的,说明KrF 未电离,即以分子的形
2 2
式存在,D错误。
9.【答案】A
A.金刚石、石墨、C 由不同数目的碳原子构成,物理性质差异较大的原因是C的排列方式不同,并非碳原
60
子数目不同导致的,A错误。
B.分子晶体:分子间作用力;离子晶体:离子键;共价晶体:共价键,物理性质差异显著是因为静电作用
的强度不同,B正确。
C.NaCl:离子键;HCl:共价键,熔融状态下离子键断裂但是共价键不能断裂,熔融状态下二者导电和不导
电相互矛盾,也可以作为离子化合物和共价化合物区别的依据。
D.化学平衡状态特点:逆等动定变,平衡只是一种表观静止状态,属于动态平衡,并未停止,故D正确。
10.【答案】B
【解析】【分析】现有W、X、Y、Z、A、B、R七种前四周期常见元素,原子序数依次递增,其中,W核
外只有一个电子,所以W是H元素,X是植物生长三要素之一,应为N、P、K某一种,Y是地壳中含量
最多的元素,所以Y是O,X是N元素,且Y与A的最外层电子数相同,则A可能是S、Se元素;Z、R
化学解析(共 8 页)第 2 页是金属元素,其中Z的原子半径是短周期中最大的,Z是Na元素,能与B形成离子化合物NaB,所以B
可能是Cl、Br元素,含R的金属是用量最大的金属材料,其合金被称为“黑色金属”,R是Fe元素,所以A
是S元素,B是Cl元素。
5114
【详解】A.XW为NH,中心原子N的孤电子对为 =0,价层电子对为0+4=4,与4个H形成
4 4 2
6113
4个σ键,无孤电子对,为正四面体结构,W Y+为H O+,中心原子O的孤电子对为 =1,价层电
3 3
2
子对为1+3=4,H O+为三角锥形;孤电子对对成键电子对的排斥作用大于对成键电子对间的排斥作用,使
3
键角减小,因此NH的键角大于H O+,A正确;
4 3
B.X、Y、Z三种元素分别为N、O、Na,对应原子半径Na>N>O,B错误;
C.Z、A、B、R四种元素分别为Na、S、Cl、Fe,一般情况下:金属性越强,第一电离能越小,非金属性
越强,第一电离能越大,一般非金属的第一电离能大于金属的第一电离能,则第一电离能有Cl>S>Fe>Na,
C正确;
6224
D.AY2、BY分别为SO2、ClO,SO2中心原子S的孤电子对为 =0,价层电子对为0+4=4,
4 4 4 4 4 2
VSEPR模型为正四面体形,S与4个O形成4个σ键,无孤电子对,空间构型为正四面体形,ClO中心原
4
7124
子Cl的孤电子对为 =0,价层电子对为0+4=4,VSEPR模型为正四面体形,Cl与4个O形成4
2
个σ键,无孤电子对,空间构型为正四面体形,则SO2、ClO的VSEPR模型与实际空间构型均相同,D正
4 4
确。
11.【答案】A
【解析】A,上述过程①的反应类型是取代反应,故A错误;
B,Na+半径204pm,Cs+半径334pm,与18-冠-6空腔直径范围为260-320pm不匹配,不可以与Na+、Cs+
形成稳定的超分子,故B正确;
C,K+@18-冠-6中存在O对K+的吸引,故C正确;
D,超分子是由两种或两种以上的广义上的分子通过分子间相互作用形成的分子聚集体,故D正确;
12. 【答案】C
【解析】该晶胞为CuCl的晶胞,Cl填充在部分由Cu原子围成的四面体空隙中,
A.Cl的配位数为4,所以Cu的配位数也为4,A正确;
B.由均摊法易算得,B正确。
3
C.最近Cu与Cl的距离为体对角线的四分之一,应为 anm,C错误。
4
D.在晶胞中Cu原子围成的四面体空隙有8个,其中只有4个空隙填充了Cl原子,故Cl原子填充在Cu原
子围成的四面体空隙中,填充率为50%,D正确。
13.【答案】C
【解析】A.选修一教材实验,略过量的NaOH能保证HCl完全反应,此时测出的中和热更准确,A评价错误;
化学解析(共 8 页)第 3 页B.酚酞变色范围为8.4-10.0,肼为弱碱,强酸滴定弱碱,若选用酚酞作为指示剂,会提前变色判定终点,导
致测出肼的浓度偏低,B评价错误;
C.存在HCl挥发,干扰碳酸和硅酸酸性强弱判断,不能根据实验操作验证碳的金属性强于硅,C评价正确。
D.该实验是验证水晶柱的各向异性,D评价错误。
14.【答案】C
【解析】分析装置可知,左侧装置为原电池装置,b为负极,a为正极;右侧装置为电解池,c、d分别为阴
极和阳极。
A.III 室 发 生 的 电 极 反 应 为 : 2CN--10e-+4H
2
O=2CO
2
↑+N
2
↑+8H+ , I 室 电 极 反 应 为
CrO2
4
+3e-+4H
2
O=Cr(OH)
3
+5OH-,H+、OH-分别移向II室,生成H
2
O,导致NaCl溶液浓度降低,A正确;
B.c极电极反应为2H O+2e-=H ↑+2OH-,每转移10mol电子,b极产生3mol气体,c极产生5mol气体,
2 2
B正确;
C.电子只能在导线中传递,不能在电解质溶液中迁移,C错误;
D.d极首先发生H
2
O-e-=·OH+H+,进而发生·OH氧化CN-的反应,1molCN-被氧化会转移5mol电子,消
耗5mol·OH,所以当线路中转移5mol电子时,b极和d极分别可处理1molCN-,D正确。
15.【答案】D
【解析】
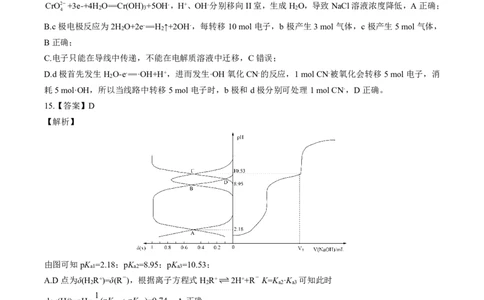
由图可知pK =2.18;pK =8.95;pK =10.53;
a1 a2 a3
A.D点为δ(H R+)=δ(R-),根据离子方程式H R+2H++R- K=K ·K 可知此时
2 2 a2 a3
1
-lgc(H+)=pH= (pK pK )=9.74,A正确;
2 a2 a3
B.B点为δ(HR)=δ(H R+),根据电荷守恒:c(Na+)+2c(H R2+)+c(H R+)+c(H+)=c(OH-)+c(Cl-)+c(R-)
2 3 2
在滴定H RCl 过程中始终存在物料守恒:2c(H R2+)+2c(H R+)+2c(HR)+2c(R-)=c(Cl-),两个守恒方程联立可
3 2 3 2
得:c(Na+)+c(H+)=c(OH-)+c(H R+)+2c(HR)+3c(R-)=c(OH-)+3c(H R+)+3c(R-),因为B点pH=8.95,所以c(H+)
2 2
<c(OH-),故c(Na+)>3c(H R+)+3c(R-),B正确;
2
K
C.反应HR+H
3
R2+2H
2
R+的平衡常数K
K
a1 106.77,数量级为106,C正确;
a2
D.V =30mL 时,此时溶质为NaCl∶NaR=2∶1,存在c(Na+)=3c(H R2+)+3c(H R+)+3c(HR)+3c(R-),但是C
3 3 2
点不对应V =30mL,因为C点δ(HR)=δ(R-),然而NaR溶液中δ(HR)<δ(R-),D错误。
3
化学解析(共 8 页)第 4 页二、非选择题
16.【答案】
(1)三颈烧瓶
(2)除去NO气体中混有NO ;
2
△
(3)2NO+CaO Ca(NO )
2 2 2
(4)防止装置Ⅵ中的水蒸气进入Ⅳ中,引起亚硝酸钙潮解,降低产品的纯度
(5)CrO2+2NO+6H+=2NO+2Cr3++3H O
2 7 3 2
(6)①当滴加半滴酸性KMnO 溶液,溶液颜色由无色变为浅红色,且半分钟内不褪色,则达到滴定终点。
4
②88.0%
【分析】用CaO 与NO制备亚硝酸钙,实验开始前先通氮气是为了排除装置内的空气,在装置Ⅰ中由铜和稀
2
硝酸反应制取一氧化氮,产生的气体中混有少量的HNO 蒸汽,可用Ⅱ装置进行除杂,则Ⅱ装置中盛放的试
3
剂为蒸馏水,发生反应的化学方程式为:3NO +H O=2HNO +NO,装置Ⅲ为干燥装置,通过Ⅳ中与过氧化
2 2 3
钙反应生成亚硝酸钙,装置Ⅴ为防止尾气处理装置中的水蒸气进入装置Ⅳ中,装置Ⅵ为尾气吸收装置。
【详解】(1)根据装置图,盛装铜片的仪器为三颈烧瓶;
(2)制出的NO中可能混有HNO 和NO ,故装置I的作用是除去NO气体中混有的HNO 蒸汽,同时将
3 2 3
NO气体中混有的NO 除去;
2
△
(3)NO与CaO 发生氧化还原反应:2NO+CaO Ca(NO )
2 2 2 2
(4)由题干信息可知,亚硝酸钙易潮解,故若缺少装置Ⅴ,产生的影响是装置Ⅵ中的水蒸气进入Ⅳ中,引
起亚硝酸钙潮解,减低产品的纯度。装置Ⅵ中的水蒸气进入Ⅳ中,引起亚硝酸钙潮解,降低产品的纯度
(5)装置Ⅵ中氮元素被氧化成5价,即NO被氧化成NO,Cr O2被还原为Cr3+,根据得失电子守恒,
3 2 7
该反应的离子方程式为CrO2+2NO+6H+=2NO+2Cr3++3H O
2 7 3 2
(6)①反应终点的判断,当滴加半滴酸性KMnO 溶液,溶液颜色由无色变为浅红色,且半分钟内不褪色,
4
则达到滴定终点。
②5Ca(NO ) ~4KMnO 由关系式法求出250mL溶液中对应Ca(NO ) 的质量m[Ca(NO ) ]=26.4g,故ω=88.0%
2 2 4 2 2 2 2
17.【答案】
(1) (1分)
(2)提高氧气浓度,加快反应速率
(3)Fe(OH) ZnO(不完整扣1分)
3
(4)Ga O +6H+=2Ga3++3H O
2 3 2
(5)不可以,Ga(OH) 和Cu(OH) 均会溶于过量氨水,不能将Cu和Ga元素分离(结论和理由各1分)
3 2
(6)阴极
化学解析(共 8 页)第 5 页(7)冷却结晶(或70℃以下冷却结晶)(1分) 过滤(1分)
【解析】
(1)Ga为第四周期IIIA族元素,其价层电子排布图为:
(2)增大压强可以提高O 的溶解度,增大O 浓度,可加快反应速率,提高浸取率。
2 2
(3)利用过量ZnO调pH除铁,铁会转化为Fe(OH) ,滤渣中还有剩余的ZnO,所以滤渣的主要成分为Fe(OH) 、
3 3
ZnO。
(4)Ga O 与酸反应的离子方程式为:Ga O +6H+=2Ga3++3H O。
2 3 2 3 2
(5)因为Cu(OH) 会溶于过量的氨水,Ga(OH) 也会溶,不能将Cu和Ga元素分离。
2 3
(6)镓在化合物中必以正价存在,电解得其单质,必须发生还原反应,所以电解可在阴极得到单质镓。
(7)从图中可以看出在低于70℃时,ZnSO •7H O的溶解度随着温度的升高而升高,为了结晶得到更多的
4 2
ZnSO •7H O晶体,一般浓缩ZnSO 溶液,再控制温度低于70℃冷却结晶,随后过滤分离出ZnSO •7H O晶
4 2 4 4 2
体,用稀硫酸和蒸馏水洗涤晶体之后,干燥即得ZnSO •7H O晶体。
4 2
18.【答案】
(1)(c-a)kJ/mol (未带单位扣1分,见错不给分)
(2)汽车行驶过程中,空气中的N 和O 在发动机燃烧室的高温高压下发生化合反应生成NO
2 2
(3)①α >80%(1分)【α 较大也可】,反应放热,绝热条件下随着反应进行,体系温度升高,反应正向
1 1
进行的程度小于恒温条件的反应进行程度,(1分)故恒温条件下平衡转化率大于80%。② 4
低温
(4)①
6NO+3O 8NH 7N 12H O
(未写条件扣1分)
2 3 2 2
②高温条件下,过量的O 可能会把NH 氧化成N O等氮氧化物,使脱硝率降低
2 3 2
③2NO+4e-+2H O=N +4OH-
2 2
【详解】(1)根据盖斯定律,反应④=反应③-反应①,则ΔH =ΔH -ΔH =(c-a)kJ/mol,故答案为(c-a)kJ/mol。
4 3 1
(2)汽车尾气中的氮氧化物的来源不是汽油的不充分燃烧,汽油中含有一定的含氮化合物,但是不会燃烧
生成氮氧化物,主要来源是在汽车行驶过程中,发动机舱燃烧室是一个高温高压条件,而进入的空气中含
有的氮气会在高温高压条件下和空气中的氧气反应生成NO,故答案为:汽车行驶过程中,空气中的N 和
2
O 在发动机燃烧室的高温高压下发生化合反应生成NO;
2
(3)①由图可知,绝热条件下,反应2NO(g)+C(s)N
2
(g)+CO
2
(g) ΔΗ=-34kJ·mol-1的平衡转化率为80%,
又因为该反应放热,所以在绝热体系中,随着反应的进行,体系的温度会不断升高,温度升高后,对于放
热反应而言反应进行的程度会变小,故绝热体系下的平衡转化率会比恒温体系下的平衡转化率低。(可以简
单的看成在恒温体系下达到平衡后升高温度,平衡逆向移动,转化率降低)故答案为:α >80%,反应放热,
1
绝热条件下随着反应进行,体系温度升高,反应正向进行的程度小于恒温条件的反应进行程度,故恒温条
件下平衡转化率大于80%。
(4)①题目中限定了NO∶O =2∶1,根据反应机理,可知脱硝反应可分为两步:第一步:2NO+O =2NO ,
2 2 2
化学解析(共 8 页)第 6 页第二步:NO 在催化剂的作用下和NH 发生反应生成N 和H O,反应方程式为6NO +8NH =7N +12H O,
2 3 2 2 2 3 2 2
低 温
实现脱硝,故总反应方程式为:6NO+3O +8NH 7N +12H O。
2 3 催 化 剂 2 2
②高温条件下的脱硝过程看反应历程2,不难发现,在加入氨气时,氨气会有两个反应过程,其一是和
反应生成N 实现脱硝,其二是和氧气反应生成N O和水,但是生成新的氮氧化物这一步就会使得整个反应
2 2
的脱硝效果降低,故答案为:高温条件下,过量的O 可能会把NH 氧化成N O等氮氧化物,使脱硝率降低。
2 3 2
③观察原电池装置,在碱性条件下,N极通入NO后生成N ,故电极反应式为:2NO+4e-+2H O=N +
2 2 2
4OH-。
19.【答案】
(1)碳碳双键、酰胺基(每个1分,漏写扣1分,字写错不给分)
(2)
(漏写条件、等号连接扣1分,见错不给分)
(3)
(4)15
(5)5
(6)消耗反应生成的HCl,促进反应正向进行,提高转化率
(7) (见错不给分)
【详解】(1)由A的结构简式可知,A中官能团的名称为:碳碳双键、酰胺基
(2)A生成B是A在酸性条件下和甲醇发生醇解(类比酰胺的水解),故反应方程式为:(注意写条件并用
箭头连接)
(3)注意已知信息,Boc O的结构简式已知,B生成C其实是B中的氨基和Boc O酸酐发生取代反应,生
2 2
化学解析(共 8 页)第 7 页成酰胺,再结合D的结构简式,可知C的结构简式为:
(4)根据B的结构简式得出B的不饱和度为3,有一个六元碳环(不饱和度占1)又能发生银镜反应和水
解反应,应该含有甲酸某酯(不饱和度占1),含有两个取代基,则分别为-NH 和-OOCH,则还有一个
2
不饱和度在六元环中,即环己烯上不同的碳连接-NH 和-OOCH,根据定一移一法,可知同分异构体数目
2
一共有3×5=15种。
(5)E中手性碳位置如图 ,总共5个手性碳原子
(6)F生成G的化学反应方程式为
;由此可知,加入NaOH会消耗生成的
HCl,促进反应正向进行,提高产率,故答案为:消耗反应生成的HCl,促进反应正向进行,提高转化率。
(7)依据以上合成路线可知,首先,用 和 在NaClO作用下进行反应
成环,得到M,其次在NaBH 和NiCl 条件下开环得到目标产物,注意,此时不再需要D生成E的第二步
4 2
条件,Ac O,TEA,DCM,是为了和在开环之后生成的-NH 反应生成酰胺,而目标产物中不需要这一步,
2 2
不要弄错。具体合成路线为
所以中间体M为 。
化学解析(共 8 页)第 8 页