文档内容
2024 级高一下 3 月月考化学试题
出题人:何会梅 审题人:王晓洪
你可能会用到的相对原子质量H1 O16 S32 Cu64 Fe56
一、单选题
1.化学与生活、科技密切相关。下列说法错误的是
A.葡萄酒中加适量SO 可起到杀菌、抗氧化的作用
2
B.碳酸氢铵、碳酸氢钠均可用作食品膨松剂
C.砖瓦、有色玻璃、水晶饰物都是硅酸盐制品
D.医疗上将BaSO 用作消化系统X射线检查的内服药剂--“钡餐”
4
2.下列变化中,属于吸热反应的是
A.过氧化钠和水的反应 B.干冰升华
C.盐酸和氢氧化钠的反应 D.灼热的木炭与CO 的反应
2
3.下列化学用语或图示表达不正确的是
A.H O的结构式: B.NH Cl的电子式为
2 4
C.中子数为8的氮原子:15N D.CO 的结构式为O=C=O
7 2
4.N 代表阿伏加德罗常数的值,下列说法中正确的是
A
A.20gD O中含有的电子数目为9N
2 A
B.标准状况下,11.2LSO 含有分子数目为0.5N
3 A
C.1molN 与足量的H 充分反应,转移的电子数目少于6N
2 2 A
D.16.8gFe与足量的硫蒸气完全反应转移的电子数目为0.9N
A
5.常温下,下列各组离子在溶液中一定能大量共存的是
A.澄清透明的溶液中:Cl—、Na+、SO2、Cu2+
4
B.紫色石蕊呈红色的溶液:NO
3
—、Cl、Fe2+、SCN-
C.BaCl 溶液中:NH、Na、SO2、Mg2
2 4 4
D.与铝粉反应放出氢气的溶液中:S2—、NH +、Ca2+、K+
4
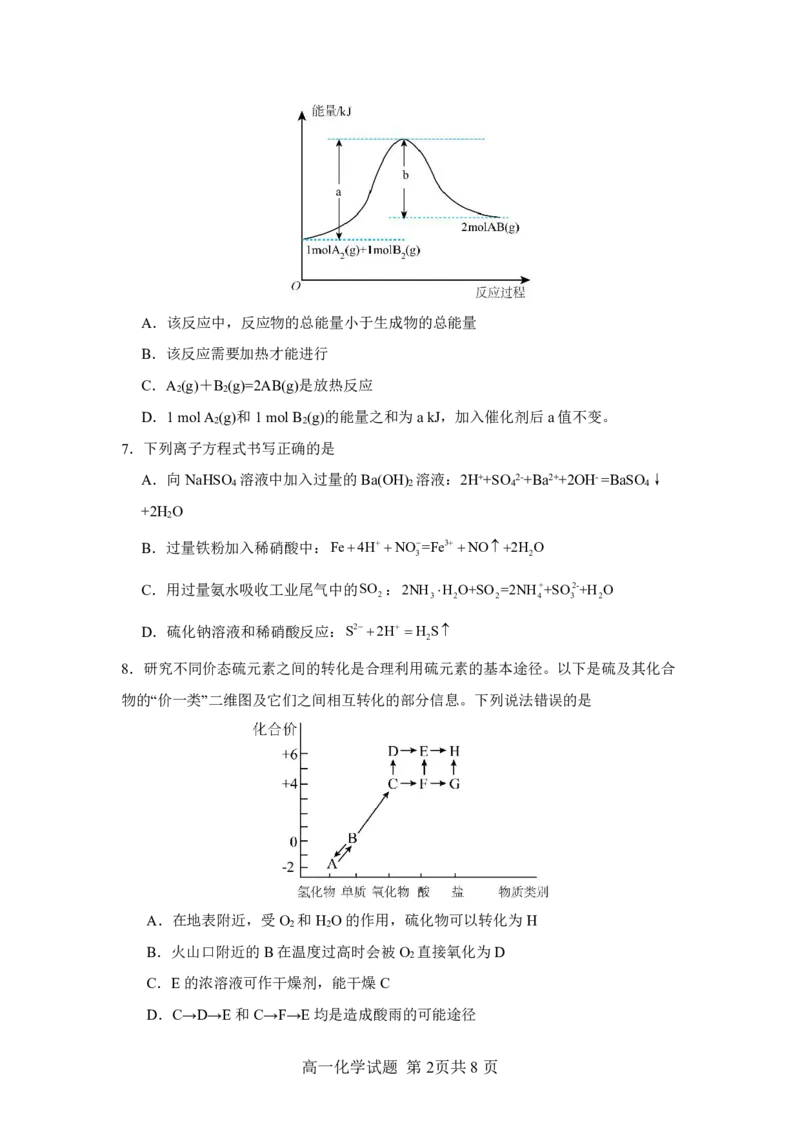
6.“能量-反应过程”图是表示反应过程中物质能量变化的示意图,如图为某反应的“能量
-反应过程”图,下列有关说法正确的是
高一化学试题 第1页共8页A.该反应中,反应物的总能量小于生成物的总能量
B.该反应需要加热才能进行
C.A (g)+B (g)=2AB(g)是放热反应
2 2
D.1molA (g)和1molB (g)的能量之和为akJ,加入催化剂后a值不变。
2 2
7.下列离子方程式书写正确的是
A.向NaHSO 溶液中加入过量的Ba(OH) 溶液:2H++SO 2-+Ba2++2OH-=BaSO ↓
4 2 4 4
+2H O
2
B.过量铁粉加入稀硝酸中:Fe4HNO=Fe3NO2H O
3 2
C.用过量氨水吸收工业尾气中的SO :2NH H O+SO =2NH++SO2-+H O
2 3 2 2 4 3 2
D.硫化钠溶液和稀硝酸反应:S22H H S
2
8.研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。以下是硫及其化合
物的“价一类”二维图及它们之间相互转化的部分信息。下列说法错误的是
A.在地表附近,受O 和H O的作用,硫化物可以转化为H
2 2
B.火山口附近的B在温度过高时会被O 直接氧化为D
2
C.E的浓溶液可作干燥剂,能干燥C
D.C→D→E和C→F→E均是造成酸雨的可能途径
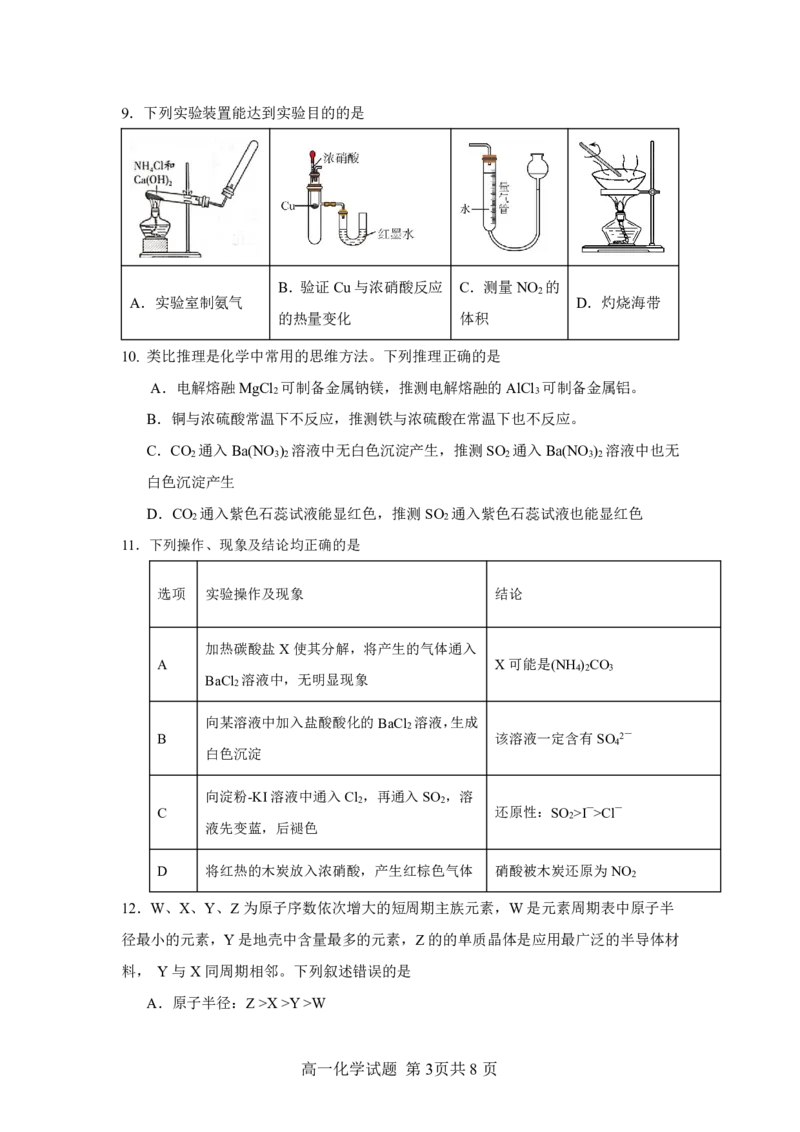
高一化学试题 第2页共8页9.下列实验装置能达到实验目的的是
B.验证Cu与浓硝酸反应 C.测量NO 的
2
A.实验室制氨气 D.灼烧海带
的热量变化 体积
10. 类比推理是化学中常用的思维方法。下列推理正确的是
A.电解熔融MgCl 可制备金属钠镁,推测电解熔融的AlCl 可制备金属铝。
2 3
B.铜与浓硫酸常温下不反应,推测铁与浓硫酸在常温下也不反应。
C.CO 通入Ba(NO ) 溶液中无白色沉淀产生,推测SO 通入Ba(NO ) 溶液中也无
2 3 2 2 3 2
白色沉淀产生
D.CO 通入紫色石蕊试液能显红色,推测SO 通入紫色石蕊试液也能显红色
2 2
11.下列操作、现象及结论均正确的是
选项 实验操作及现象 结论
加热碳酸盐X使其分解,将产生的气体通入
A X可能是(NH ) CO
4 2 3
BaCl 溶液中,无明显现象
2
向某溶液中加入盐酸酸化的BaCl 溶液,生成
2
B 该溶液一定含有SO 2—
4
白色沉淀
向淀粉-KI溶液中通入Cl ,再通入SO ,溶
2 2
C 还原性:SO >I—>Cl—
2
液先变蓝,后褪色
D 将红热的木炭放入浓硝酸,产生红棕色气体 硝酸被木炭还原为NO
2
12.W、X、Y、Z为原子序数依次增大的短周期主族元素,W是元素周期表中原子半
径最小的元素,Y是地壳中含量最多的元素,Z的的单质晶体是应用最广泛的半导体材
料, Y与X同周期相邻。下列叙述错误的是
A.原子半径:Z>X>Y>W
高一化学试题 第3页共8页B.Z的氧化物是酸性氧化物,不能与酸反应
C.W、X和Y可形成既含有离子键也含有共价键的化合物
D.W与X形成的二元化合物可以使湿润的红色石蕊试纸变蓝
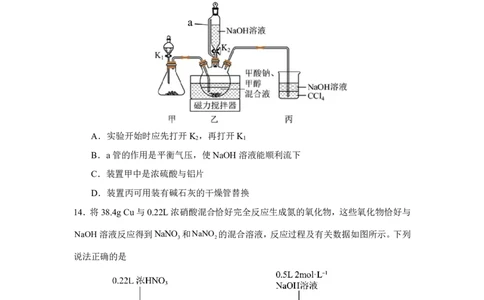
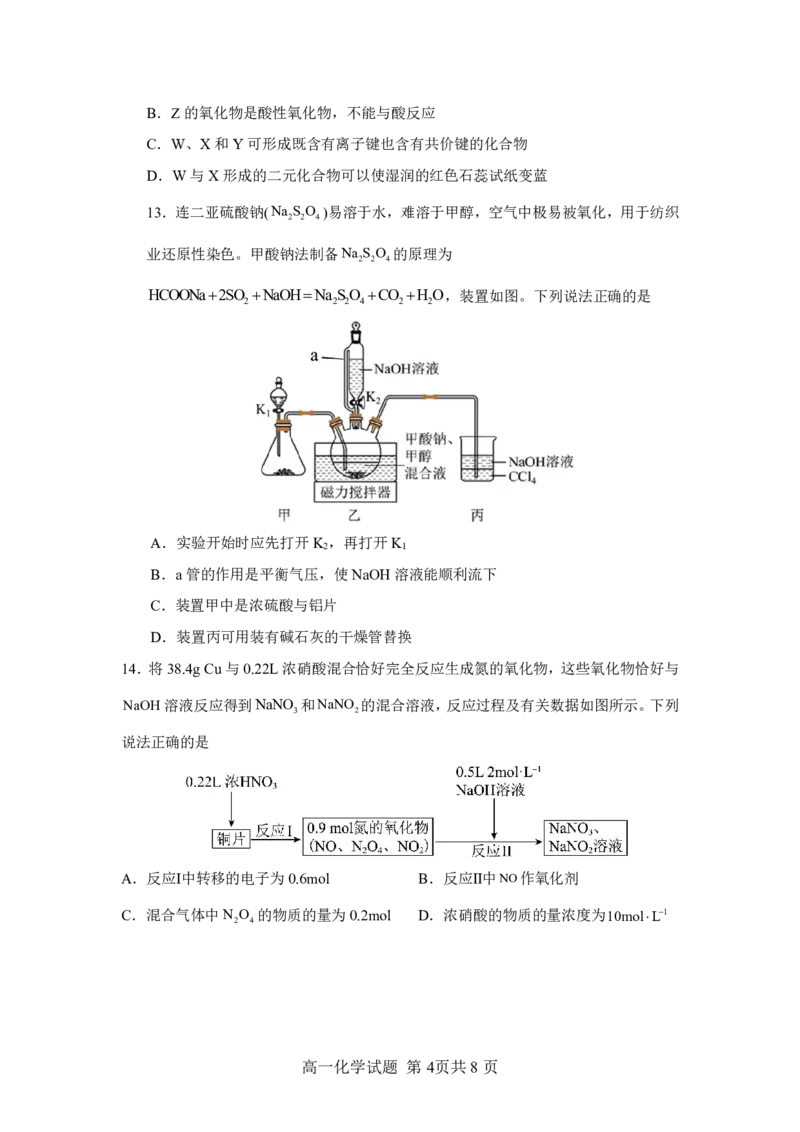
13.连二亚硫酸钠(Na S O )易溶于水,难溶于甲醇,空气中极易被氧化,用于纺织
2 2 4
业还原性染色。甲酸钠法制备Na S O 的原理为
2 2 4
HCOONa2SO NaOHNa SO CO H O,装置如图。下列说法正确的是
2 2 2 4 2 2
A.实验开始时应先打开K ,再打开K
2 1
B.a管的作用是平衡气压,使NaOH溶液能顺利流下
C.装置甲中是浓硫酸与铝片
D.装置丙可用装有碱石灰的干燥管替换
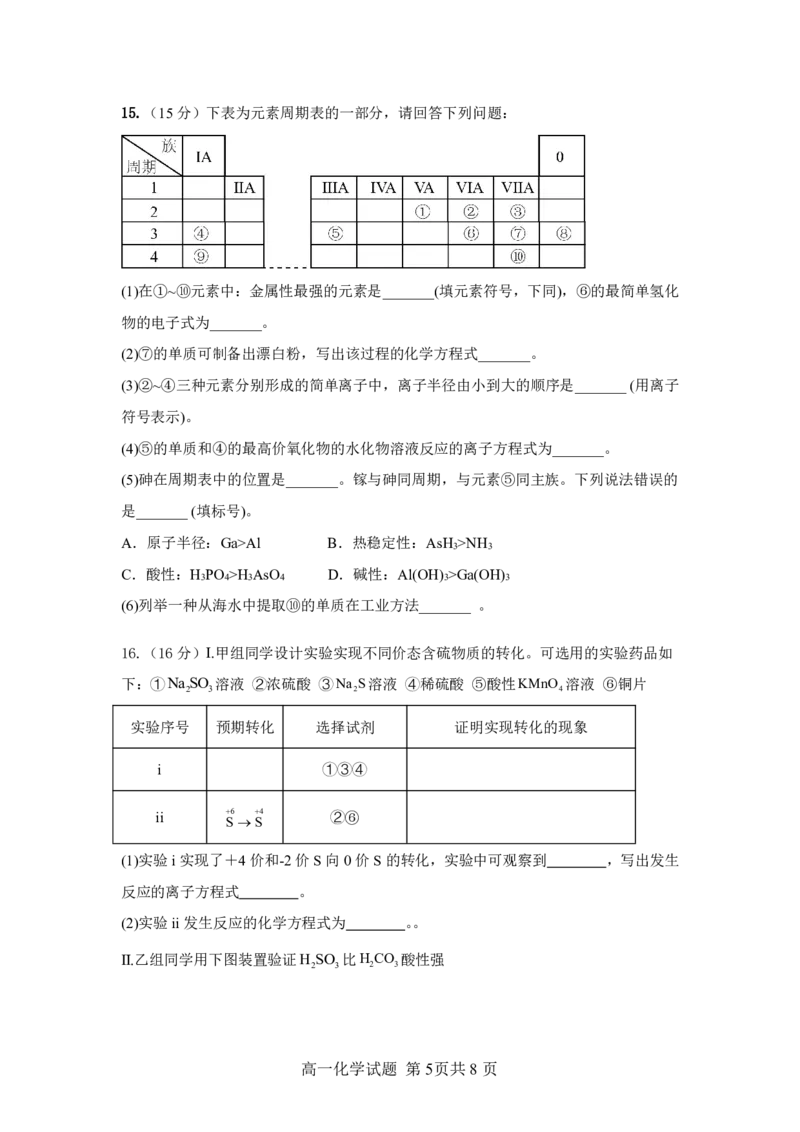
14.将38.4gCu与0.22L浓硝酸混合恰好完全反应生成氮的氧化物,这些氧化物恰好与
NaOH溶液反应得到NaNO 和NaNO 的混合溶液,反应过程及有关数据如图所示。下列
3 2
说法正确的是
A.反应Ⅰ中转移的电子为0.6mol B.反应Ⅱ中NO作氧化剂
C.混合气体中N O 的物质的量为0.2mol D.浓硝酸的物质的量浓度为10molL1
2 4
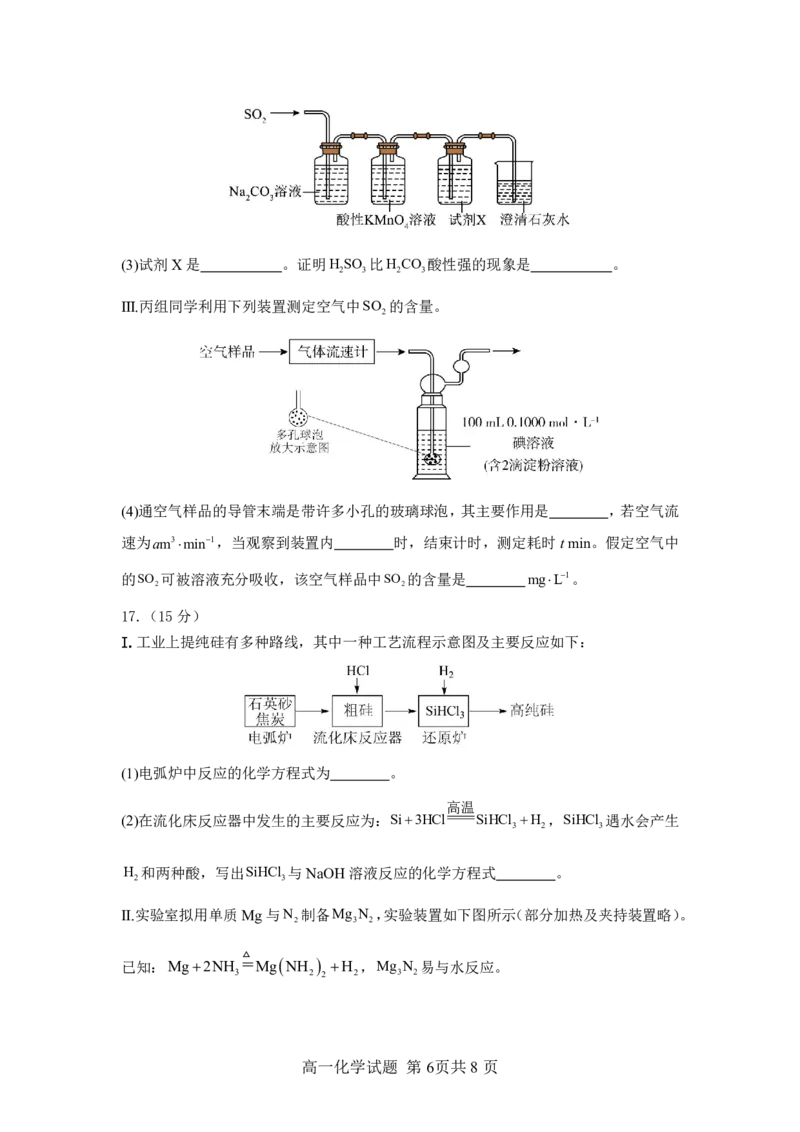
高一化学试题 第4页共8页15.(15分)下表为元素周期表的一部分,请回答下列问题:
(1)在①~⑩元素中:金属性最强的元素是_______(填元素符号,下同),⑥的最简单氢化
物的电子式为_______。
(2)⑦的单质可制备出漂白粉,写出该过程的化学方程式_______。
(3)②~④三种元素分别形成的简单离子中,离子半径由小到大的顺序是_______(用离子
符号表示)。
(4)⑤的单质和④的最高价氧化物的水化物溶液反应的离子方程式为_______。
(5)砷在周期表中的位置是_______。镓与砷同周期,与元素⑤同主族。下列说法错误的
是_______(填标号)。
A.原子半径:Ga>Al B.热稳定性:AsH >NH
3 3
C.酸性:H PO >H AsO D.碱性:Al(OH) >Ga(OH)
3 4 3 4 3 3
(6)列举一种从海水中提取⑩的单质在工业方法_______ 。
16.(16分)Ⅰ.甲组同学设计实验实现不同价态含硫物质的转化。可选用的实验药品如
下:①Na SO 溶液 ②浓硫酸 ③Na S溶液 ④稀硫酸 ⑤酸性KMnO 溶液 ⑥铜片
2 3 2 4
实验序号 预期转化 选择试剂 证明实现转化的现象
i ①③④
ii S 6 S 4 ②⑥
(1)实验i实现了+4价和-2价S向0价S的转化,实验中可观察到 ,写出发生
反应的离子方程式 。
(2)实验ii发生反应的化学方程式为 。。
Ⅱ.乙组同学用下图装置验证H SO 比H CO 酸性强
2 3 2 3
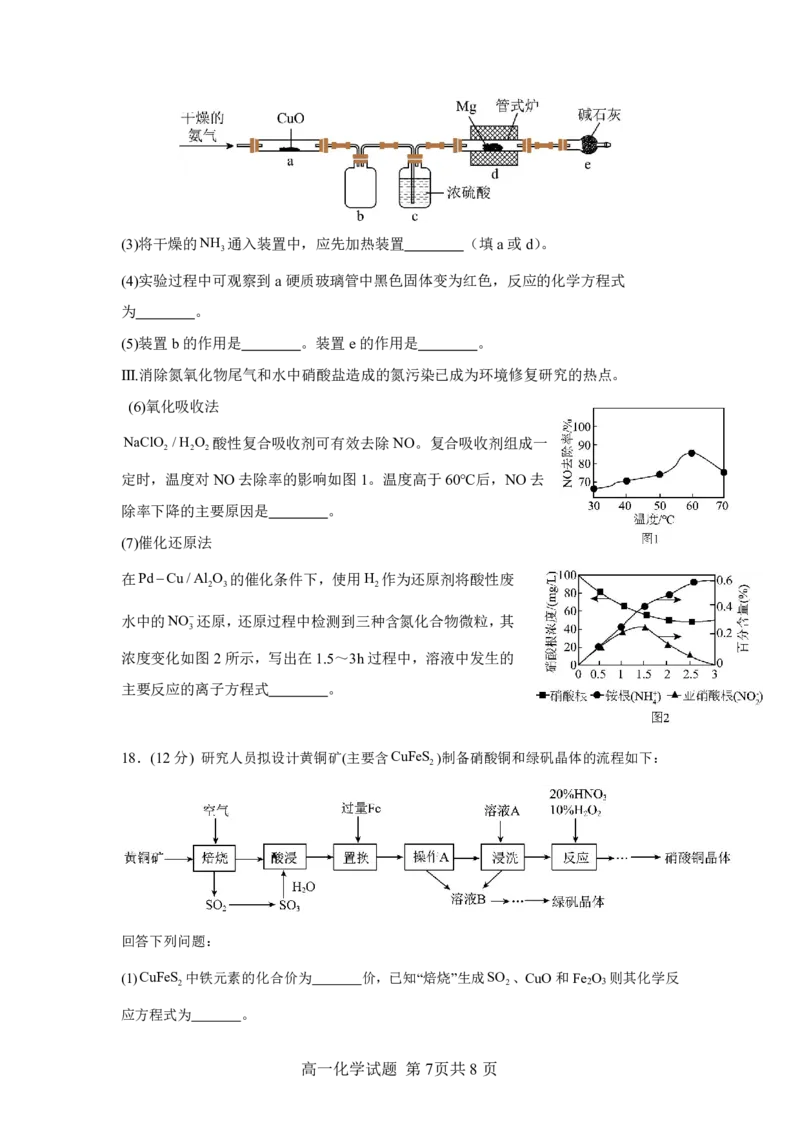
高一化学试题 第5页共8页(3)试剂X是 。证明H SO 比H CO 酸性强的现象是 。
2 3 2 3
Ⅲ.丙组同学利用下列装置测定空气中SO 的含量。
2
(4)通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是 ,若空气流
速为am3min1,当观察到装置内 时,结束计时,测定耗时tmin。假定空气中
的SO 可被溶液充分吸收,该空气样品中SO 的含量是 mgL1。
2 2
17.(15分)
I.工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
(1)电弧炉中反应的化学方程式为 。
高温
(2)在流化床反应器中发生的主要反应为:Si3HCl SiHCl H ,SiHCl 遇水会产生
3 2 3
H 和两种酸,写出SiHCl 与NaOH溶液反应的化学方程式 。
2 3
II.实验室拟用单质Mg与N 制备Mg N ,实验装置如下图所示(部分加热及夹持装置略)。
2 3 2
已知:Mg2NH Mg NH H ,Mg N 易与水反应。
3 2 2 2 3 2
高一化学试题 第6页共8页(3)将干燥的NH 通入装置中,应先加热装置 (填a或d)。
3
(4)实验过程中可观察到a硬质玻璃管中黑色固体变为红色,反应的化学方程式
为 。
(5)装置b的作用是 。装置e的作用是 。
Ⅲ.消除氮氧化物尾气和水中硝酸盐造成的氮污染已成为环境修复研究的热点。
(6)氧化吸收法
NaClO /H O 酸性复合吸收剂可有效去除NO。复合吸收剂组成一
2 2 2
定时,温度对NO去除率的影响如图1。温度高于60℃后,NO去
除率下降的主要原因是 。
(7)催化还原法
在PdCu/Al O 的催化条件下,使用H 作为还原剂将酸性废
2 3 2
水中的NO还原,还原过程中检测到三种含氮化合物微粒,其
3
浓度变化如图2所示,写出在1.5~3h过程中,溶液中发生的
主要反应的离子方程式 。
18.(12分) 研究人员拟设计黄铜矿(主要含CuFeS )制备硝酸铜和绿矾晶体的流程如下:
2
回答下列问题:
(1)CuFeS 中铁元素的化合价为 价,已知“焙烧”生成SO 、CuO和Fe O 则其化学反
2 2 2 3
应方程式为 。
高一化学试题 第7页共8页(2)“置换”步骤中发生的所有反应的离子方程式有Fe+Cu2+ Fe2++Cu
Fe+2H+ Fe2++H 、 。
2
(3)流程中“操作A”所需的玻璃仪器有烧杯、玻璃棒、 。
(4)“浸洗”步骤中加入用于分离Cu、Fe的溶液A是 (填“稀H SO ”或“稀HNO ”)。
2 4 3
(5)“反应”步骤中,10%H O 为氧化剂,20%HNO 提供H,可以避免污染性气体的产生,
2 2 3
写出该“反应”的离子方程式: 。
(6)绿矾晶体(FeSO 7H O)在空气中极易变质;验证绿矾晶体已变质的实验方案为 。
4 2
高一化学试题 第8页共8页