文档内容
化学试题
相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 A1-27 S-32
Cu-64
一、选择题(本大题共17题,共20分)1~14每题只有1个正确选项,每题1分,共14分。
1.空气中体积分数最大的气体是( )
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
2.我国大力推广使用脱硫煤,以减少SO 对空气的污染。SO 中硫元素的化合价为( )
2 2
A.-2 B.0 C.+4 D.+6
3.化学式书写错误的是( )
A.硝酸铜:Cu(NO ) B.碳酸钾:KCO
3 2 2 3
C.氯化铁:FeCl D.氧化铝:Al O
2 2 3
4.“手撕钢”的厚度仅为0.015mm,这体现了钢具有( )
A.密度小 B.导电性 C.导热性 D.延展性
5.净水机中加入活性炭,主要是利用活性炭的( )
A.吸附性 B.稳定性 C.还原性 D.难溶于水
6.下列果汗或饮料中,呈碱性的是( )
A.苹果汁(pH≈3) B.番茄汁(pH≈4) C.西瓜汁(pH≈6) D.苏打水
(pH≈9)
7.自来水生产过程中无需进行的操作是( )
A.降温结晶 B.絮凝沉降 C.杀菌消毒 D.细沙滤水
8.变瘪的乒乓球放入热水中,会鼓起来恢复原样。说明乒乓球内的气体分子( )
A.间隔增大 B.质量增大 C.种类增多 D.数目增多
9.石墨烯是由碳元素组成的单质,下列物质与石墨烯互为同素异形体的是( )
A.白磷 B.干冰 C.臭氧 D.金刚石
10.下列物质的用途错误的是( )
A.一氧化碳:作燃料 B.氯气:保存食品
C.金刚石:切割玻璃 D.氦气:充填飞艇
11.有关电解水的实验,说法错误的是( )
A.检验正极相连的管内生成的气体可选用带火星的小木条
B.与负极相连的管内生成的气体为氢气
C.负极产生的气体体积小于正极端产生的气体体积
D.该实验的结论是:水是由氢元素和氧元素组成的
12.某反应为 ,有关分析正确的是( )
A.物质X是单质 B.1gCO 与3gH 恰好能完全反应
2 2
C.n一定为1 D.H元素的存在形态没有发生改变
13.为了便于贮存和运输过氧化氢,工业上常将其转化为过碳酸钠晶体(2NaCO·3H O),该晶体具有
2 3 2 2
NaCO 和HO 的双重性质。过碳酸钠晶体与下列物质接触不会失效的是( )
2 3 2 2A.二氧化锰 B.氯化钠 C.盐酸 D.石灰水
14.一定温度下,向12g蒸馏水加入无水硫酸铜粉末,充分溶解,过滤得蓝色晶体和4.2g滤液,若此温度下
无水硫酸铜的溶解度为40g/100g水,则加入的无水硫酸铜质量是( )
A.6.6g B.9g C.15.6g D.17.2g
15~17每题有12个正确选项,每题2分,共6分。有2个正确选项的,选对1个得1分,多选
或错选得0分。
15.关于提纯物质分析正确的是( )
A.一定发生了化学变化 B.一定要进行过滤
C.一定利用了各物质的不同性质 D.一定加入了另外的试剂
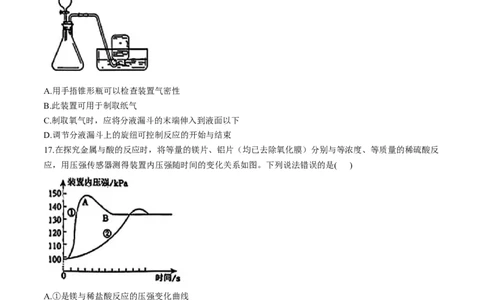
16.有关右图的实验装置,说法正确的是( )
A.用手捂锥形瓶可以检查装置气密性
B.此装置可用于制取纸气
C.制取氧气时,应将分液漏斗的末端伸入到液面以下
D.调节分液漏斗上的旋纽可控制反应的开始与结束
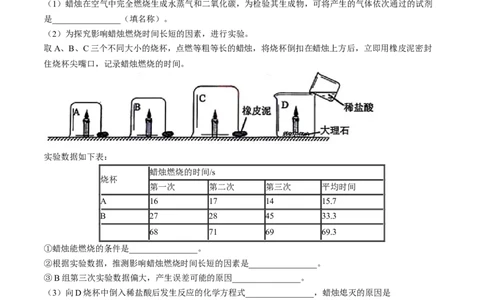
17.在探究金属与酸的反应时,将等量的镁片、铝片(均已去除氧化膜)分别与等浓度、等质量的稀硫酸反
应,用压强传感器测得装置内压强随时间的变化关系如图。下列说法错误的是( )
A.①是镁与稀盐酸反应的压强变化曲线
B.①上升得高,说明产生氢气的量多
C.AB段下除可能是反应结束不再产生热量导致的
D.反应后镁片一定有剩余
六、简答题(共30分。第18题7分,第19题8分,第20题6分,第21题9分)
18.《齐民要术》记载“粟米曲作酢”,“酢”即醋酸(CHCOOH)。
3
(1)古法酿醋是用粮食经过发酵而成,粮食酿醋属于______________(选填“物理”或“化学”)变化。
(2)醋酸由种元素组成,其中碳元素与氯元素的质量比为___________________。
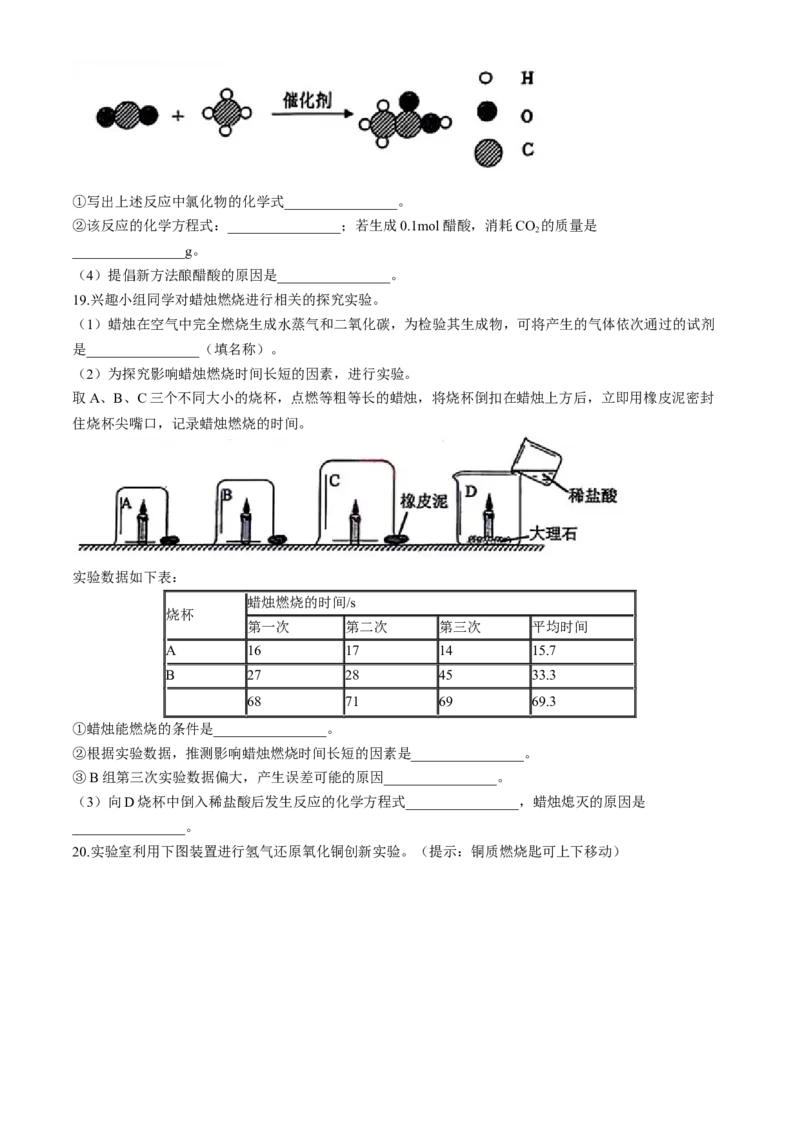
(3)我国科研人员研究出制取醋酸的新方法。新方法的反应微观示意图如下:①写出上述反应中氯化物的化学式________________。
②该反应的化学方程式:________________;若生成0.1mol醋酸,消耗CO 的质量是
2
________________g。
(4)提倡新方法酿醋酸的原因是________________。
19.兴趣小组同学对蜡烛燃烧进行相关的探究实验。
(1)蜡烛在空气中完全燃烧生成水蒸气和二氧化碳,为检验其生成物,可将产生的气体依次通过的试剂
是________________(填名称)。
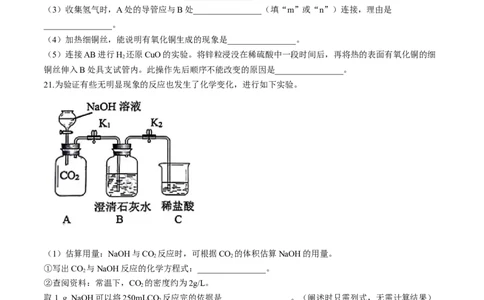
(2)为探究影响蜡烛燃烧时间长短的因素,进行实验。
取A、B、C三个不同大小的烧杯,点燃等粗等长的蜡烛,将烧杯倒扣在蜡烛上方后,立即用橡皮泥密封
住烧杯尖嘴口,记录蜡烛燃烧的时间。
实验数据如下表:
蜡烛燃烧的时间/s
烧杯
第一次 第二次 第三次 平均时间
A 16 17 14 15.7
B 27 28 45 33.3
68 71 69 69.3
①蜡烛能燃烧的条件是________________。
②根据实验数据,推测影响蜡烛燃烧时间长短的因素是________________。
③B组第三次实验数据偏大,产生误差可能的原因________________。
(3)向D烧杯中倒入稀盐酸后发生反应的化学方程式________________,蜡烛熄灭的原因是
________________。
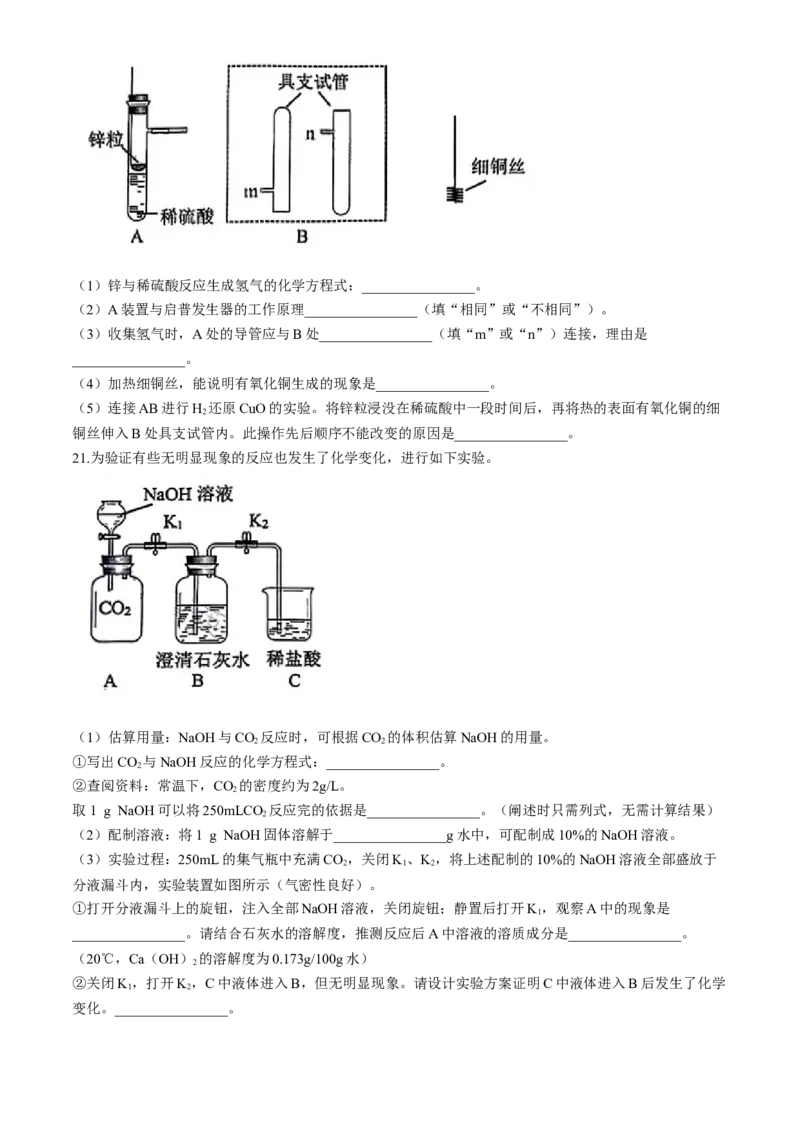
20.实验室利用下图装置进行氢气还原氧化铜创新实验。(提示:铜质燃烧匙可上下移动)(1)锌与稀硫酸反应生成氢气的化学方程式:________________。
(2)A装置与启普发生器的工作原理________________(填“相同”或“不相同”)。
(3)收集氢气时,A处的导管应与B处________________(填“m”或“n”)连接,理由是
________________。
(4)加热细铜丝,能说明有氧化铜生成的现象是________________。
(5)连接AB进行H 还原CuO的实验。将锌粒浸没在稀硫酸中一段时间后,再将热的表面有氧化铜的细
2
铜丝伸入B处具支试管内。此操作先后顺序不能改变的原因是________________。
21.为验证有些无明显现象的反应也发生了化学变化,进行如下实验。
(1)估算用量:NaOH与CO 反应时,可根据CO 的体积估算NaOH的用量。
2 2
①写出CO 与NaOH反应的化学方程式:________________。
2
②查阅资料:常温下,CO 的密度约为2g/L。
2
取1 g NaOH可以将250mLCO 反应完的依据是________________。(阐述时只需列式,无需计算结果)
2
(2)配制溶液:将1 g NaOH固体溶解于________________g水中,可配制成10%的NaOH溶液。
(3)实验过程:250mL的集气瓶中充满CO,关闭K、K,将上述配制的10%的NaOH溶液全部盛放于
2 1 2
分液漏斗内,实验装置如图所示(气密性良好)。
①打开分液漏斗上的旋钮,注入全部NaOH溶液,关闭旋钮;静置后打开K,观察A中的现象是
1
________________。请结合石灰水的溶解度,推测反应后A中溶液的溶质成分是________________。
(20℃,Ca(OH) 的溶解度为0.173g/100g水)
2
②关闭K,打开K,C中液体进入B,但无明显现象。请设计实验方案证明C中液体进入B后发生了化学
1 2
变化。________________。(4)实验结论:本实验通过证明________________,验证了无明显现象的反应也发生了化学变化。
(5)反思总结:本实验还体现了碱的化学性质有________________(填字母序号)。
a.能与指示剂反应 b.能与酸反应
c.能与酸性氧化物反应 d.能与某些盐反应