文档内容
微信公众号:上海通优教案资料中心
化学部分
202604
可能用到的相对原子质量:H-1 C-12 O-16 Fe-56
一、食品膨松剂——泡打粉(18分)
泡打粉是一种常见的食品膨松剂,常用于烘焙、面点制作,其中碳酸氢钠是产生气体的核心成分。下
表为三种不同品牌泡打粉的成分表:
1. XX牌泡打粉 2. XX牌泡打粉 3. XX牌双效泡打粉
焦磷酸二氢二钠、碳酸 碳酸氢钠、固体酒石酸、 磷酸二氢二钠、碳酸氢钠、淀粉、
主要成分
氢钠、磷酸二氢钙等 玉米淀粉、维生素C等 柠檬酸、碳酸钙、酒石酸氢钾等
主要作用 产生气体,使面包松软
1. 这三种泡打粉均属于______(选填 “纯净物” 或 “混合物”),泡打粉的作用主要是遇酸反应,产生了
______(填写化学式)气体。
2. 上表中属于有机物的是______(任写表中一种物质名称),属于盐的是______(任写表中一种物质名称)。
3. 第三种品牌中碳酸氢钠(NaHCO₃)与碳酸钙,他们化学性质有相似的原因是__________________。
4. 品牌1中磷酸二氢钙的化学式是Ca(H₂PO₃)₂。
(1)该物质由______种元素组成;该物质溶于水,测得 pH 约为5,该溶液为______(选填 “酸性” 或 “碱
性”)。
(2)农业上该物质可以作为______。
A. 氮肥 B. 磷肥 C. 钾肥 D. 复合肥
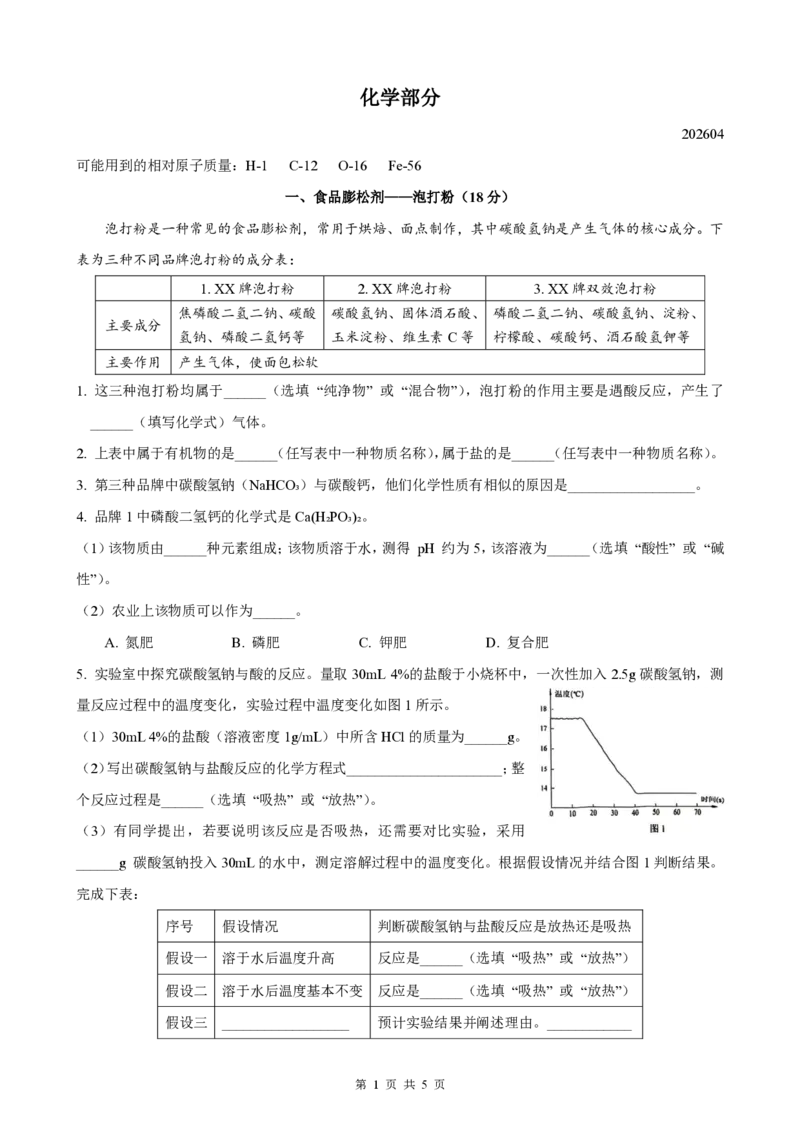
5. 实验室中探究碳酸氢钠与酸的反应。量取30mL 4%的盐酸于小烧杯中,一次性加入2.5g碳酸氢钠,测
量反应过程中的温度变化,实验过程中温度变化如图1所示。
(1)30mL 4%的盐酸(溶液密度1g/mL)中所含HCl的质量为______g。
(2)写出碳酸氢钠与盐酸反应的化学方程式______________________;整
个反应过程是______(选填 “吸热” 或 “放热”)。
(3)有同学提出,若要说明该反应是否吸热,还需要对比实验,采用
______g 碳酸氢钠投入30mL的水中,测定溶解过程中的温度变化。根据假设情况并结合图1判断结果。
完成下表:
序号 假设情况 判断碳酸氢钠与盐酸反应是放热还是吸热
假设一 溶于水后温度升高 反应是______(选填 “吸热” 或 “放热”)
假设二 溶于水后温度基本不变 反应是______(选填 “吸热” 或 “放热”)
假设三 __________________ 预计实验结果并阐述理由。____________
第 1 页 共 5 页微信公众号:上海通优教案资料中心
二、高铁中的材料化学(17分)
从“追赶”到“领跑”,中国高铁已成为一张闪亮的国家名片。飞驰的列车背后,是无数材料科学与
化学工程的智慧结晶。
6. 高铁列车上的常见物质,其中属于金属材料制成的是______。
A. 车厢内塑料餐桌 B. 不锈钢饮水台面
C. 高强度挡风玻璃 D. 一次性可降解餐盒
7. 高铁生产中常用到铝、铁、铜,这三者中金属活动性最强的是______;将铁片浸入到硫酸铜溶液中,发
生的化学方程式是________________________。
8. 高铁列车依靠车顶的受电弓滑板由石墨制造,这一应用与石墨的下列性质有关的是______(不定项)。
A. 滑腻感 B. 熔点高 C. 导电性 D. 化学性质稳定
高铁列车车顶的受电弓滑板与接触网供电线路(如图2所示)接触受电。供电线路采用
折线而不是直线的原因是__________________________________________。
9. 为适应提速并运行平稳,需把短轨焊接连成长轨。焊接使用的熔融的铁,采用的反应:
高温
2Al + Fe₂O₃ Al₂O₃ + 2Fe
(1)该反应发生时,放出高温得到熔融的铁。该反应属于______。
A. 分解反应 B. 化合反应 C. 复分解反应 D. 置换反应
(2)焊接若需要56kg的铁,则需要Fe₂O₃多少kg(根据化学方程式列式计算)?至少需要携带多少kg铁
红(含90%Fe O 的粉末)?
2 3
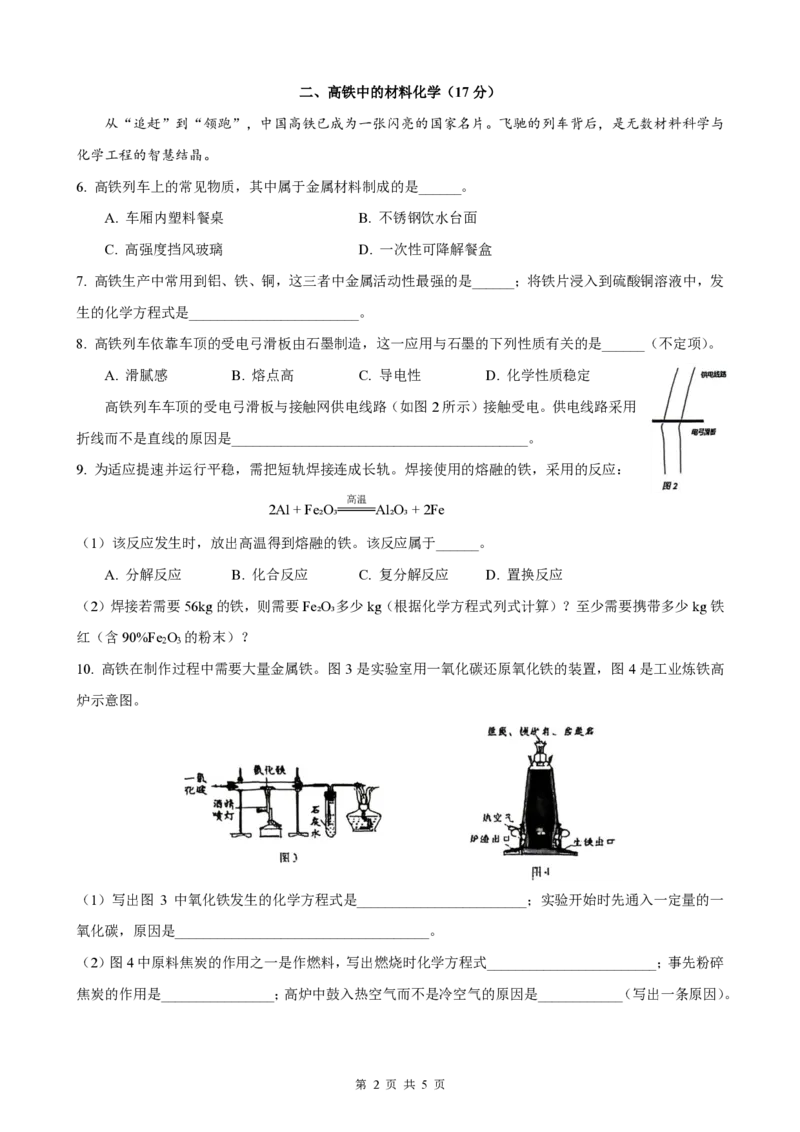
10. 高铁在制作过程中需要大量金属铁。图3是实验室用一氧化碳还原氧化铁的装置,图4是工业炼铁高
炉示意图。
(1)写出图 3 中氧化铁发生的化学方程式是________________________;实验开始时先通入一定量的一
氧化碳,原因是____________________________________。
(2)图4中原料焦炭的作用之一是作燃料,写出燃烧时化学方程式________________________;事先粉碎
焦炭的作用是________________;高炉中鼓入热空气而不是冷空气的原因是____________(写出一条原因)。
第 2 页 共 5 页微信公众号:上海通优教案资料中心
三、浮法玻璃工艺(7分)
浮法玻璃工艺制取的成品玻璃平整度高,是主流平板玻璃工艺。在玻璃熔窑中,原料纯碱和石灰石分
别与石英砂在高温下发生反应,生成硅酸钠和硅酸钙,同时产生二氧化碳。锡(Sn)的熔点为232°C,高
温下易被氧化为二氧化锡。锡槽内依靠玻璃液带入的热量形成高温液态锡。因锡密度远大于玻璃液,玻璃
液浮在锡面,故称为 “浮法”。下图5为生产的主要流程。
11. 玻璃主要成分是SiO₂,SiO₂属于______(不定项)。
A. 单质 B. 化合物 C. 盐 D. 氧化物
12. “切裁玻璃” 发生的是____________(选填 “物理变化”“化学变化”)。
13. 产生的二氧化碳过多排入大气,会造成不良的环境影响是__________________;“物尽其用” 才是正确
的物质观,请写出二氧化碳的一种用途______________________________。
14. “锡槽成型” 过程中,相关说法正确的是______(多项)
A. 锡槽内面要不断地加热 B. 通入氮气,可以防止锡在高温下被氧化
C. 锡槽中的温度控制在1200°C D. 熔融的锡起到一个 “水平面” 的作用
四、海水晒盐(8分)
海水中溶解盐类总含量约为3.5%,是海水晒盐的基础原料。其中氯化钠占总盐类的78%左右,是晒盐
的目标产物,其余为氯化镁、硫酸镁、硫酸钙等杂质。随着海水蒸发浓缩,溶液密度逐渐升高,不同盐类
会依次析出。
下表为常温常压下海水在不同密度时析出的主要成分表。
海水密度 硫酸钙析出量 氯化钠析出量 氯化镁析出量 硫酸镁析出量
(g/mL) (g/L) (g/L) (g/L) (g/L)
<1.13 0 0 0 0
1.13 0.56 0 0 0
1.20 0.91 0 0 0
1.21 0.05 3.26 0.004 0.008
1.22 0.015 9.65 0.01 0.04
1.26 0.01 2.64 0.02 0.02
1.31 0 1.40 0.54 0.03
第 3 页 共 5 页微信公众号:上海通优教案资料中心
15. 氯化钠、氯化镁、硫酸镁、硫酸钙按照酸根可以分为盐酸盐和______;他们都是由金属正离子与酸根
负离子形成的,其中钠离子的化学符号是______。
16. 上表中溶解度最小物质是______。
A. 氯化钠 B. 氯化镁 C. 硫酸镁 D. 硫酸钙
17.(1)海水密度为1.21g/mL时,海水中的氯化钠为______(选填 “不饱和” 或 “饱和”)溶液。常温下(此
时,氯化钠溶解度是36g)进行海水晒盐得到氯化钠3600g,若溶解这些食盐至少需要水的质量是______g。
(2)海水晒盐,最有利氯化钠析出的海水密度范围是____________。
18. 晒盐得到氯化钠,剩余的溶液中溶质质量最多的是______。
A. 氯化钠 B. 氯化镁 C. 硫酸镁 D. 硫酸钙
第 4 页 共 5 页微信公众号:上海通优教案资料中心
参考答案
一、
1. 混合物;CO₂
2. 玉米淀粉(或维生素C、酒石酸、柠檬酸);碳酸氢钠(或磷酸二氢钙、碳酸钙、酒石酸氢钾)
3. 都属于碳酸盐
4.(1)4;酸性 (2)B
5.(1)1.2
(2)NaHCO₃+HCl=NaCl+H₂O+CO₂↑;吸热
(3)2.5;吸热;吸热;溶于水后温度降低;无法直接判断,若测得反应后降温幅度比单纯溶解更大,则
反应吸热;若降温幅度比单纯溶解更小,则反应放热
二、
6. B
7. 铝;Fe+CuSO₄=FeSO₄+Cu
8. ABCD;为了让受电弓滑板的不同位置与接触网导线均匀接触,避免某一点长期摩擦造成过度磨损,从
而延长受电弓和接触网的使用寿命,同时也能改善散热条件,防止局部过热
9.(1)D (2)80 kg;88.9 kg
高温
10.(1)3CO+Fe₂O₃ 2Fe+3CO ;排尽装置内空气,防止加热爆炸
2
点燃
(2)C+O CO₂;增大接触面积,使燃烧更充分;提高炉内温度/加快反应速率
2
三、
11. BD
12. 物理变化
13. 温室效应;灭火(或作气体肥料、制碳酸饮料等)
14. ABD
四、
15. 硫酸盐;Na⁺
16. D
17.(1)饱和;10000 (2)1.21~1.22 g/mL
18. B
第 5 页 共 5 页