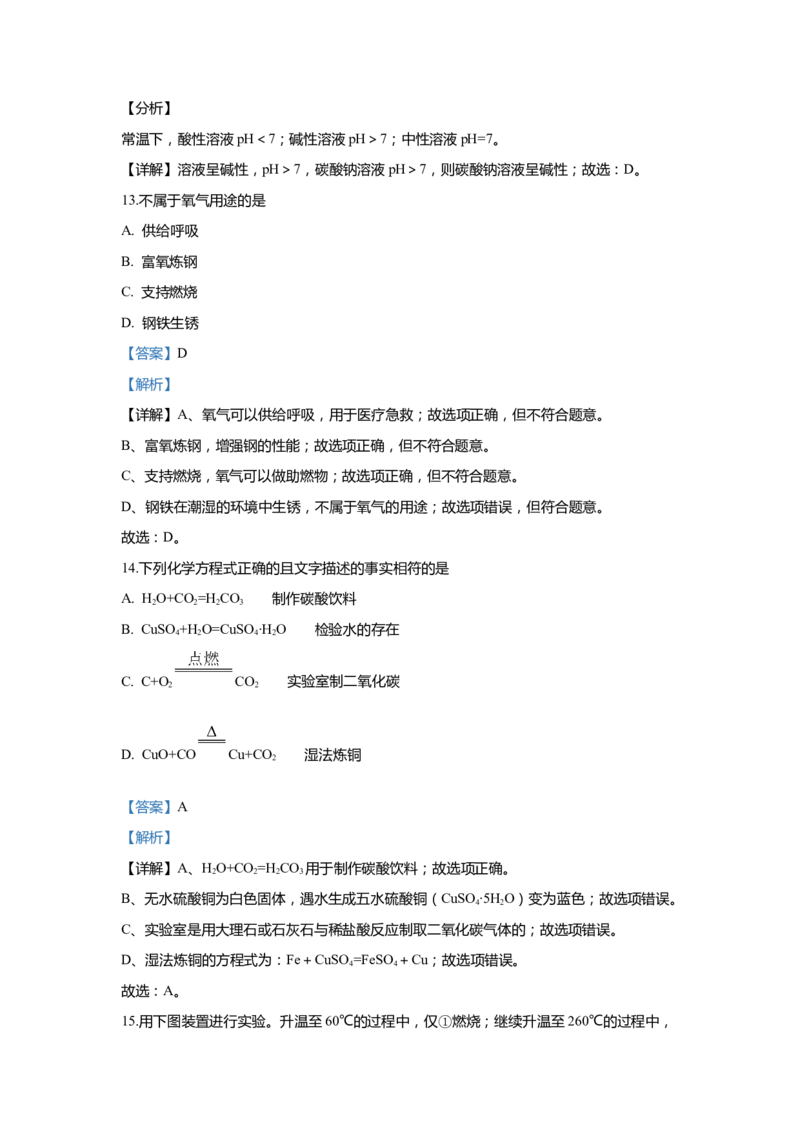文档内容
嘉定区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)答案解析版
2020.1
六、单项选择题(共 20 分)
1.空气中体积分数约为78%的物质是
A. O B. N C. CO D. HO
2 2 2 2
【答案】B
【解析】
A、空气中各成分体积分数分别为:氮气-78%、氧气-21%、稀有气体-0.94%、二氧化
碳-0.03%、其他-0.03%。综上,选B。
2.属于化学变化的是
A. 香水气味充满整个房间 B. 自行车长期使用后,车身金属部
分氧化
C. 干冰用于人工降雨 D. 从冰箱拿出的干燥玻璃杯,过一
会表面有很多水珠
【答案】B
【解析】
【详解】A、香水气味充满整个房间属于分子扩撒,没有新物质产生;属于物理变化;故
选项错误。
B、自行车长期使用后,车身金属部分容易生锈被氧化,有新物质产生,属于化学变化;
故选项正确。
C、干冰用于人工降雨,干冰升华吸热,是水蒸气预冷凝结成小水珠,形成降雨,没有新
物质产生,属于物理变化;故选项错误。
D、从冰箱拿出的干燥玻璃杯,过一会表面有很多水珠,水蒸气冷凝形成水珠,没有新物
质产生,属于物理变化;故选项错误。
故选:B。
3.属于混合物的是
A. 碳酸钙 B. 干冰 C. 冰水 D. 木炭
【答案】D【解析】
【详解】A、碳酸钙中只含有一种物质成分,属于纯净物;故选项错误。
B、干冰是固体二氧化碳,只含有一种物质成分,属于纯净物;故选项错误。
C、冰水中只含有水分子,属于纯净物;故选项错误。
D、木炭中含有碳以及少量杂质,属于混合物;故选项正确。
故选:D。
【点睛】纯净物与混合物的区别:是否含有单一成分,或者有唯一的化学式。
4.属于化合反应的是
A. CH+2O CO+2H O B. 2HO 2H↑+O ↑
4 2 2 2 2 2 2
C. 2Na+Cl 2NaCl D. C+2CuO CO↑+2Cu
2 2
【答案】C
【解析】
【详解】A、CH+2O CO+2H O,不符合“多变一”,不属于化合反应;故选项
4 2 2 2
错误。
B. 2HO 2H↑+O ↑,符合“一变多”属于分解反应;故选项错误。
2 2 2
C. 2Na+Cl 2NaCl,符合“多变一”属于化合反应;故选项正确。
2
D. C+2CuO CO↑+2Cu符合“单质+化合物=新单质+新化合物”属于置换反应;
2
故选项错误。
故选:C。
5.84消毒液中有效成分为次氯酸钠NaClO,其中氯元素的化合价为
A. 0 B. -1 C. +1 D. +2
【答案】C【解析】
【详解】设氯元素化合价为x,则(+1)+x+(-2)=0,则x=+1;故选:C。
6.与石墨互称同素异形体的是
A. 活性炭 B. 木炭 C. 一氧化碳 D. 金刚石
【答案】D
【解析】
【分析】
由同种元素组成的性质不同的单质,互称同素异形体。
【详解】A、活性炭中含有杂质,不属于单质;故选项错误。
B、木炭中含有杂质,不属于单质;故选项错误。
C、一氧化碳中含有碳、氧两种元素,不属于单质;故选项错误。
D、金刚石中只含有碳元素,属于单质;故选项正确。
故选:D。
7.化学反应常常伴随发光、变色、产生沉淀等现象,下列反应现象描述错误的是
A. 镁带在空气中燃烧,发出耀眼白光 B. 硫在氧气中燃烧,发出蓝紫色火
焰
C. 铁丝在氧气中燃烧,生成四氧化三铁 D. 红磷在空气中燃烧,产生大量白
烟
【答案】C
【解析】
【详解】A、镁带在空气中燃烧,发出耀眼白光;故选项正确,但不符合题意。
B、硫在氧气中燃烧,发出蓝紫色火焰;故选项正确,但不符合题意。
C、铁丝在氧气中燃烧,生成黑色固体;故选项错误,但符合题意。
D、红磷在空气中燃烧,产生大量白烟;故选项正确,但不符合题意。
故选:C。
【点睛】注意区分:实验现象与实验结论
8.表示两个氢分子的是
A. 2H B. 2H C. H D. H
2 2
【答案】B
【解析】A. 2H:表示两个氢原子 B. 2H 表示两个氢分子 C. H 宏观表示氢元素,微观表示
2
一个氢原子 D. H 宏观表示氢气,微观表示一个氢分子。故选B
2
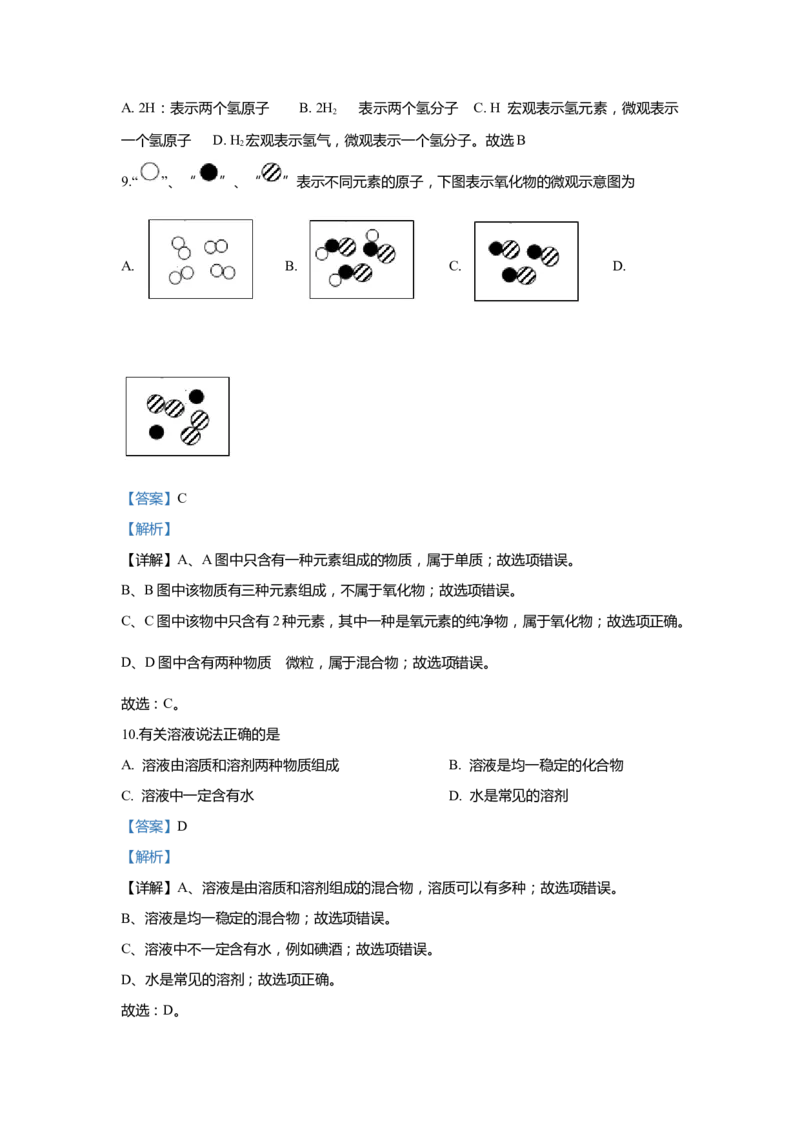
9.“ ”、“ ”、“ ”表示不同元素的原子,下图表示氧化物的微观示意图为
A. B. C. D.
【答案】C
【解析】
【详解】A、A图中只含有一种元素组成的物质,属于单质;故选项错误。
B、B图中该物质有三种元素组成,不属于氧化物;故选项错误。
C、C图中该物中只含有2种元素,其中一种是氧元素的纯净物,属于氧化物;故选项正确。
D、D图中含有两种物质 的微粒,属于混合物;故选项错误。
故选:C。
10.有关溶液说法正确的是
A. 溶液由溶质和溶剂两种物质组成 B. 溶液是均一稳定的化合物
C. 溶液中一定含有水 D. 水是常见的溶剂
【答案】D
【解析】
【详解】A、溶液是由溶质和溶剂组成的混合物,溶质可以有多种;故选项错误。
B、溶液是均一稳定的混合物;故选项错误。
C、溶液中不一定含有水,例如碘酒;故选项错误。
D、水是常见的溶剂;故选项正确。
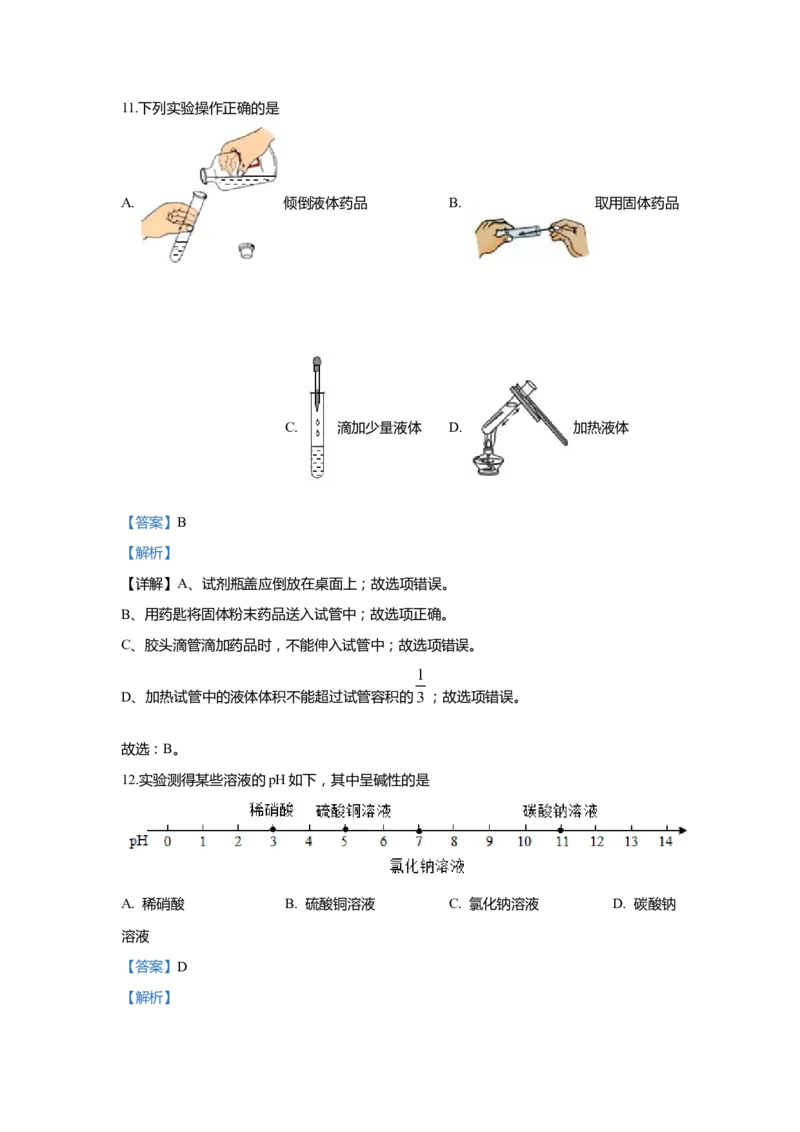
故选:D。11.下列实验操作正确的是
A. 倾倒液体药品 B. 取用固体药品
C. 滴加少量液体 D. 加热液体
【答案】B
【解析】
【详解】A、试剂瓶盖应倒放在桌面上;故选项错误。
B、用药匙将固体粉末药品送入试管中;故选项正确。
C、胶头滴管滴加药品时,不能伸入试管中;故选项错误。
D、加热试管中的液体体积不能超过试管容积的 ;故选项错误。
故选:B。
12.实验测得某些溶液的pH如下,其中呈碱性的是
A. 稀硝酸 B. 硫酸铜溶液 C. 氯化钠溶液 D. 碳酸钠
溶液
【答案】D
【解析】【分析】
常温下,酸性溶液pH<7;碱性溶液pH>7;中性溶液pH=7。
【详解】溶液呈碱性,pH>7,碳酸钠溶液pH>7,则碳酸钠溶液呈碱性;故选:D。
13.不属于氧气用途的是
A. 供给呼吸
B. 富氧炼钢
C. 支持燃烧
D. 钢铁生锈
【答案】D
【解析】
【详解】A、氧气可以供给呼吸,用于医疗急救;故选项正确,但不符合题意。
B、富氧炼钢,增强钢的性能;故选项正确,但不符合题意。
C、支持燃烧,氧气可以做助燃物;故选项正确,但不符合题意。
D、钢铁在潮湿的环境中生锈,不属于氧气的用途;故选项错误,但符合题意。
故选:D。
14.下列化学方程式正确的且文字描述的事实相符的是
A. HO+CO=H CO 制作碳酸饮料
2 2 2 3
B. CuSO +H O=CuSO ∙H O 检验水的存在
4 2 4 2
C. C+O CO 实验室制二氧化碳
2 2
D. CuO+CO Cu+CO 湿法炼铜
2
【答案】A
【解析】
【详解】A、HO+CO=H CO 用于制作碳酸饮料;故选项正确。
2 2 2 3
B、无水硫酸铜为白色固体,遇水生成五水硫酸铜(CuSO ∙5H O)变为蓝色;故选项错误。
4 2
C、实验室是用大理石或石灰石与稀盐酸反应制取二氧化碳气体的;故选项错误。
D、湿法炼铜的方程式为:Fe+CuSO =FeSO+Cu;故选项错误。
4 4
故选:A。
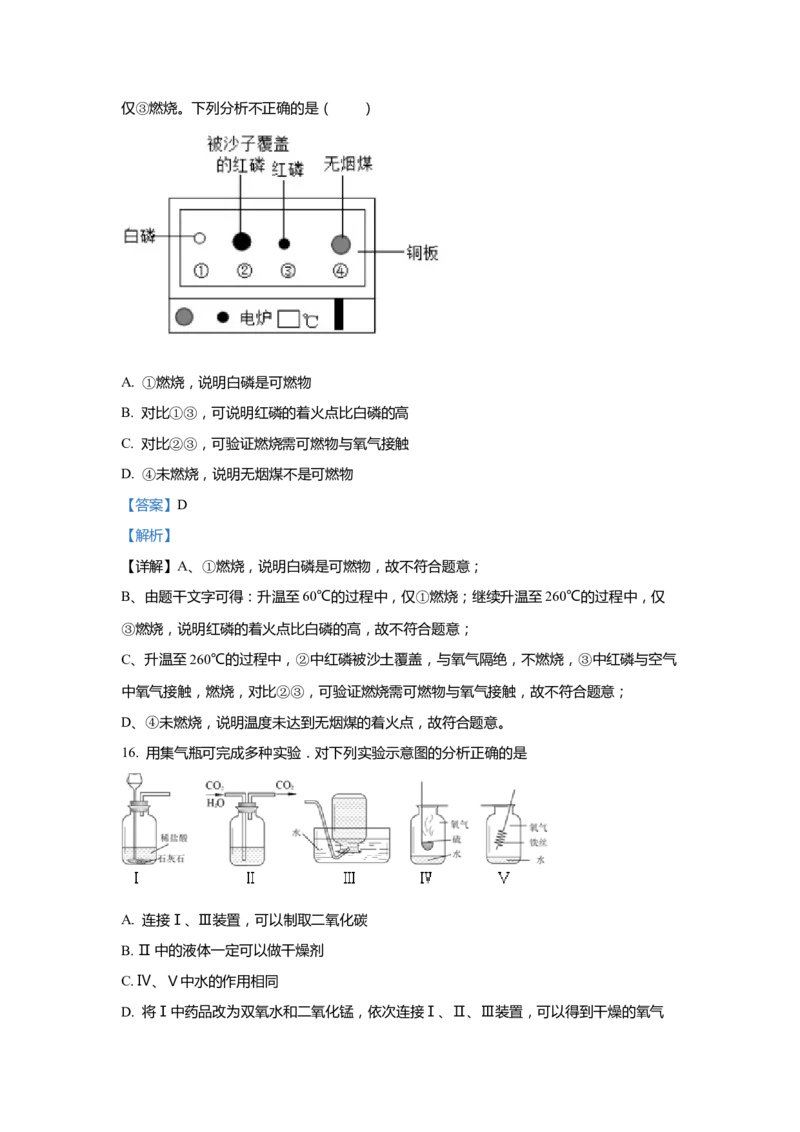
15.用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( )
A. ①燃烧,说明白磷是可燃物
B. 对比①③,可说明红磷的着火点比白磷的高
C. 对比②③,可验证燃烧需可燃物与氧气接触
D. ④未燃烧,说明无烟煤不是可燃物
【答案】D
【解析】
【详解】A、①燃烧,说明白磷是可燃物,故不符合题意;
B、由题干文字可得:升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅
③燃烧,说明红磷的着火点比白磷的高,故不符合题意;
C、升温至260℃的过程中,②中红磷被沙土覆盖,与氧气隔绝,不燃烧,③中红磷与空气
中氧气接触,燃烧,对比②③,可验证燃烧需可燃物与氧气接触,故不符合题意;
D、④未燃烧,说明温度未达到无烟煤的着火点,故符合题意。
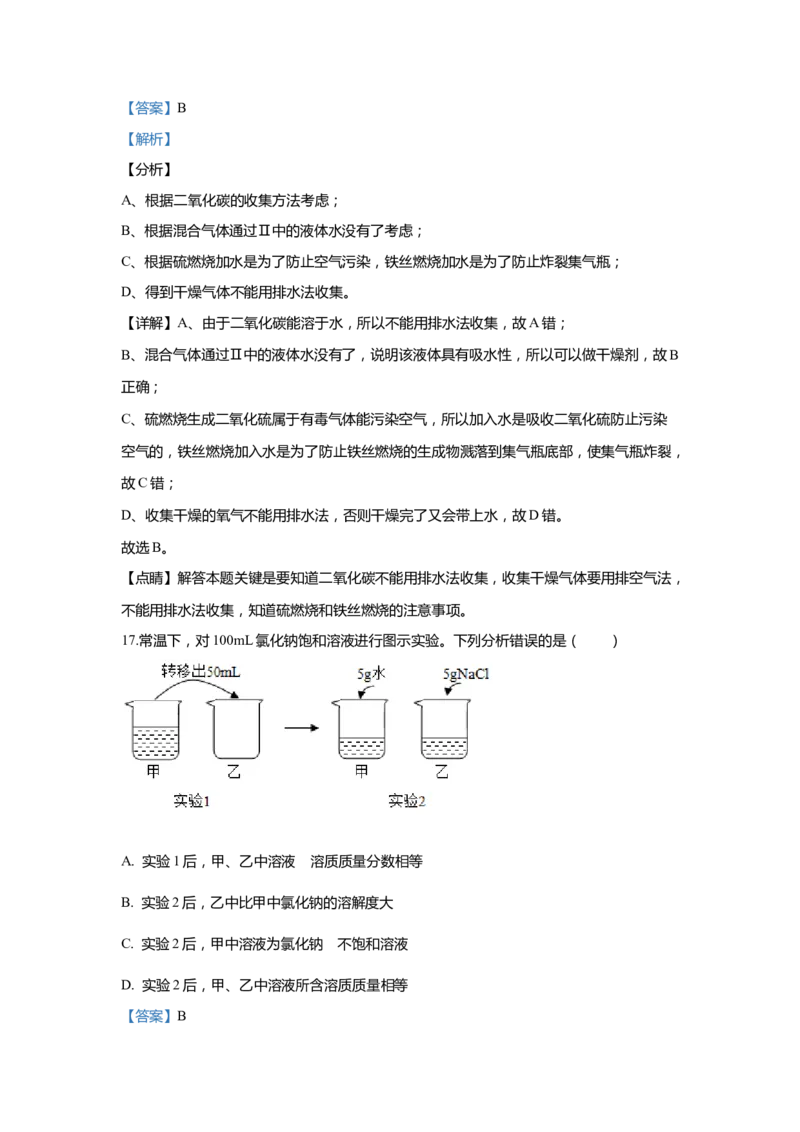
16. 用集气瓶可完成多种实验.对下列实验示意图的分析正确的是
A. 连接Ⅰ、Ⅲ装置,可以制取二氧化碳
B. Ⅱ中的液体一定可以做干燥剂
C. Ⅳ、Ⅴ中水的作用相同
D. 将Ⅰ中药品改为双氧水和二氧化锰,依次连接Ⅰ、Ⅱ、Ⅲ装置,可以得到干燥的氧气【答案】B
【解析】
【分析】
A、根据二氧化碳的收集方法考虑;
B、根据混合气体通过Ⅱ中的液体水没有了考虑;
C、根据硫燃烧加水是为了防止空气污染,铁丝燃烧加水是为了防止炸裂集气瓶;
D、得到干燥气体不能用排水法收集。
【详解】A、由于二氧化碳能溶于水,所以不能用排水法收集,故A错;
B、混合气体通过Ⅱ中的液体水没有了,说明该液体具有吸水性,所以可以做干燥剂,故B
正确;
C、硫燃烧生成二氧化硫属于有毒气体能污染空气,所以加入水是吸收二氧化硫防止污染
空气的,铁丝燃烧加入水是为了防止铁丝燃烧的生成物溅落到集气瓶底部,使集气瓶炸裂,
故C错;
D、收集干燥的氧气不能用排水法,否则干燥完了又会带上水,故D错。
故选B。
【点睛】解答本题关键是要知道二氧化碳不能用排水法收集,收集干燥气体要用排空气法,
不能用排水法收集,知道硫燃烧和铁丝燃烧的注意事项。
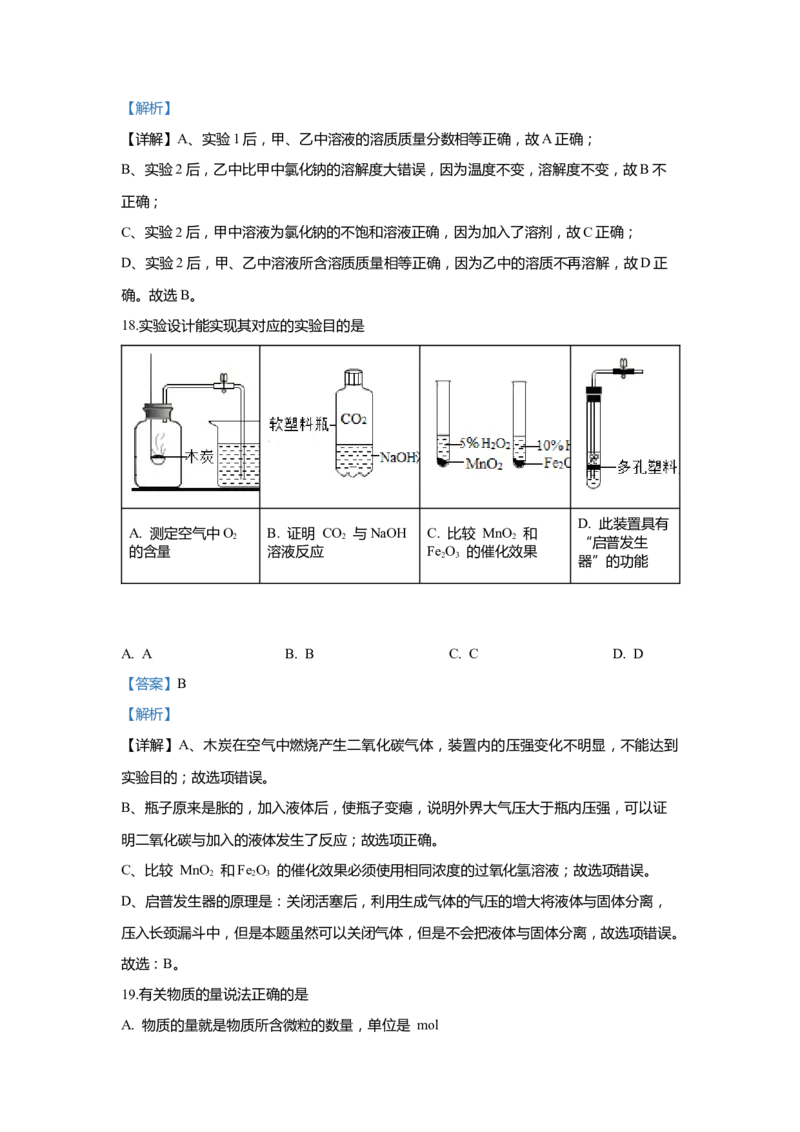
17.常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )
A. 实验1后,甲、乙中溶液 的溶质质量分数相等
B. 实验2后,乙中比甲中氯化钠的溶解度大
C. 实验2后,甲中溶液为氯化钠 不的饱和溶液
D. 实验2后,甲、乙中溶液所含溶质质量相等
【答案】B【解析】
【详解】A、实验1后,甲、乙中溶液的溶质质量分数相等正确,故A正确;
B、实验2后,乙中比甲中氯化钠的溶解度大错误,因为温度不变,溶解度不变,故B不
正确;
C、实验2后,甲中溶液为氯化钠的不饱和溶液正确,因为加入了溶剂,故C正确;
D、实验2后,甲、乙中溶液所含溶质质量相等正确,因为乙中的溶质不再溶解,故D正
确。故选B。
18.实验设计能实现其对应的实验目的是
D. 此装置具有
A. 测定空气中O B. 证明 CO 与NaOH C. 比较 MnO 和
2 2 2
“启普发生
的含量 溶液反应 Fe O 的催化效果
2 3
器”的功能
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、木炭在空气中燃烧产生二氧化碳气体,装置内的压强变化不明显,不能达到
实验目的;故选项错误。
B、瓶子原来是胀的,加入液体后,使瓶子变瘪,说明外界大气压大于瓶内压强,可以证
明二氧化碳与加入的液体发生了反应;故选项正确。
C、比较 MnO 和Fe O 的催化效果必须使用相同浓度的过氧化氢溶液;故选项错误。
2 2 3
D、启普发生器的原理是:关闭活塞后,利用生成气体的气压的增大将液体与固体分离,
压入长颈漏斗中,但是本题虽然可以关闭气体,但是不会把液体与固体分离,故选项错误。
故选:B。
19.有关物质的量说法正确的是
A. 物质的量就是物质所含微粒的数量,单位是 molB. 物质的量就是 1mol 物质的质量
C. 物质的量越大,表示该物质的分子越大
D. 物质的量是国际单位制中的一个物理量,用符号“n”表示
【答案】D
【解析】
【详解】A、物质的量:具有一定数目粒子的集合体;故选项错误。
B、物质的量不是物质的质量;故选项错误。
C、物质的量越大,表示该物质的分子越多;故选项错误。
D、物质的量是国际单位制中的一个物理量,用符号“n”表示;故选项正确。
故选:D。
20.t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH >7。关于溶液变
浑浊的原因,同学们有两种观点:①Ca(OH) 的溶解度随温度升高而减小;②Ca
2
(OH) 与空气中 CO 反应。他们设计以下方案进行探究,其中没有意义的是
2 2
A. 将装有浊液的烧杯,用冰水冷却,恢复到 t℃,观察浑浊是否消失
B. 取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C. 取适量浊液,过滤,往滤液中加入酚酞,观察是否变红色
D. 其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
【答案】C
【解析】
【详解】A、将装有浊液的烧杯,用冰水冷却,恢复到 t℃,温度降低,氢氧化钙溶解度增
大,观察浑浊是否消失;故选项正确,但不符合题意。
B、取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生,来判断溶液中是否有
碳酸钙;故选项正确,但不符合题意。
C、取适量浊液,过滤,往滤液中加入酚酞,观察是否变红色,此时不需要判断溶液的酸
碱性;故选项错误,但符合题意。
D、其他条件不变,隔绝空气,再做一个加热石灰水的对比实验,验证石灰水是否与空气
中的二氧化碳反应;故选项正确,但不符合题意。
故选:C。
七、填空题
21.化学就在我们身边,人类的生活离不开化学,请用化学符号填空:(1)地壳中含量最多的金属元素是_____;
(2)自来水生产中,用作消毒剂的是_____;
(3)三大化石燃料中属于气态燃料的是_____;
(4)“钻石恒久远”这句广告词体现了_____的化学性质在常温下非常稳定。
【答案】 (1). Al (2). Cl (3). CH (4). C
2 4
【解析】
【详解】(1)地壳中含量前四的元素是氧、硅、铝、铁,含量最多的金属元素是Al;
(2)氯气有强氧化性,能用来自来水生产中消毒,消毒剂是Cl;
2
(3)三大化石燃料包括:煤(固态)、石油(液态)、天然气(气态),中属于气态燃料
的是CH;
4
(4)“钻石恒久远”这句广告词体现了碳的化学性质在常温下非常稳定。
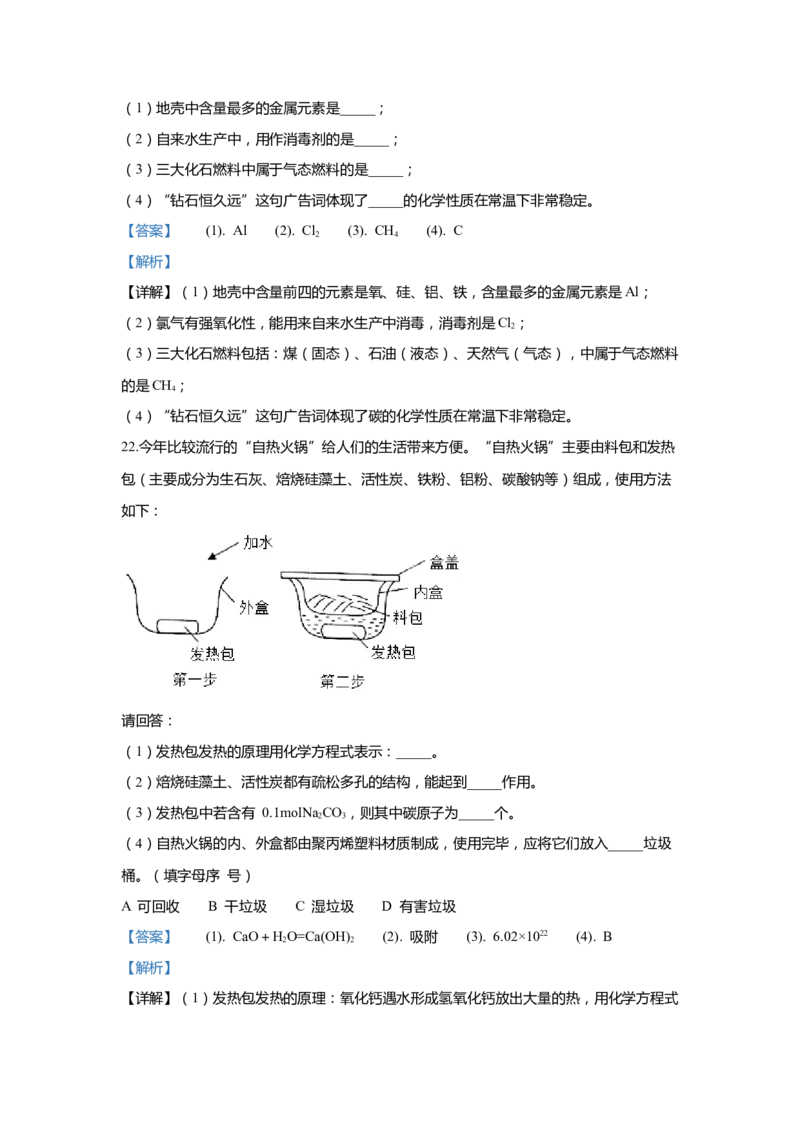
22.今年比较流行的“自热火锅”给人们的生活带来方便。“自热火锅”主要由料包和发热
包(主要成分为生石灰、焙烧硅藻土、活性炭、铁粉、铝粉、碳酸钠等)组成,使用方法
如下:
请回答:
(1)发热包发热的原理用化学方程式表示:_____。
(2)焙烧硅藻土、活性炭都有疏松多孔的结构,能起到_____作用。
(3)发热包中若含有 0.1molNa CO,则其中碳原子为_____个。
2 3
(4)自热火锅的内、外盒都由聚丙烯塑料材质制成,使用完毕,应将它们放入_____垃圾
桶。(填字母序 号)
A 可回收 B 干垃圾 C 湿垃圾 D 有害垃圾
【答案】 (1). CaO+HO=Ca(OH) (2). 吸附 (3). 6.02×1022 (4). B
2 2
【解析】
【详解】(1)发热包发热的原理:氧化钙遇水形成氢氧化钙放出大量的热,用化学方程式表示:CaO+HO=Ca(OH) 。
2 2
(2)焙烧硅藻土、活性炭都有疏松多孔的结构,能起到吸附作用。
(3)发热包中若含有 0.1molNa CO,则其中碳原子为n=0.1×6.02× 。
2 3
(4)自热火锅的内、外盒都由聚丙烯塑料材质制成,使用完毕,应将它们放入有害垃圾桶。
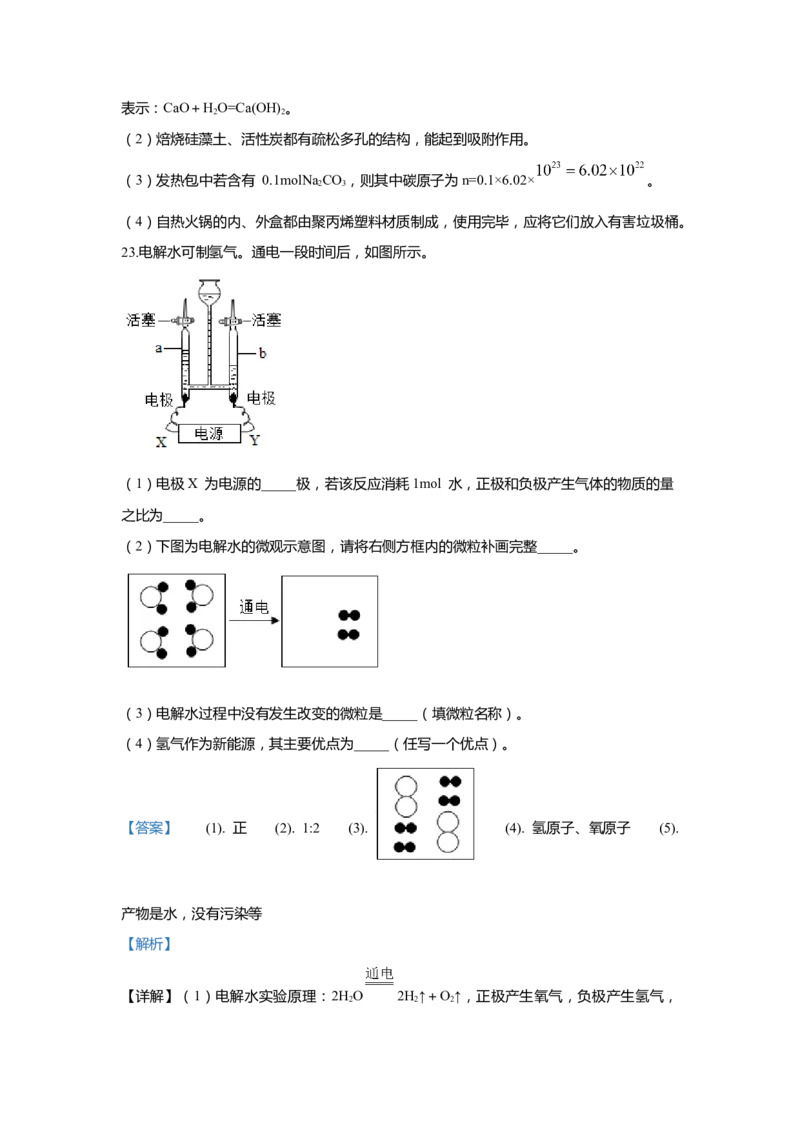
23.电解水可制氢气。通电一段时间后,如图所示。
(1)电极X 为电源的_____极,若该反应消耗1mol 水,正极和负极产生气体的物质的量
之比为_____。
(2)下图为电解水的微观示意图,请将右侧方框内的微粒补画完整_____。
(3)电解水过程中没有发生改变的微粒是_____(填微粒名称)。
(4)氢气作为新能源,其主要优点为_____(任写一个优点)。
【答案】 (1). 正 (2). 1:2 (3). (4). 氢原子、氧原子 (5).
产物是水,没有污染等
【解析】
【详解】(1)电解水实验原理:2HO 2H↑+O↑,正极产生氧气,负极产生氢气,
2 2 2氧气与氢气的体积比为1:2;电极X端产生的气体是氧气, 为电源的正极,若该反应消耗
1mol 水,正极和负极产生气体的物质的量之比=分子个数比=化学方程式计量数之比=1:2。
(2)下图为电解水的微观示意图,请将右侧方框内的微粒补画完整: 。
(3)原子是化学变化中的最小粒子,电解水过程中没有发生改变的微粒是氢原子、氧原子。
(4)氢气作为新能源,其主要优点为:产物是水,没有污染等。
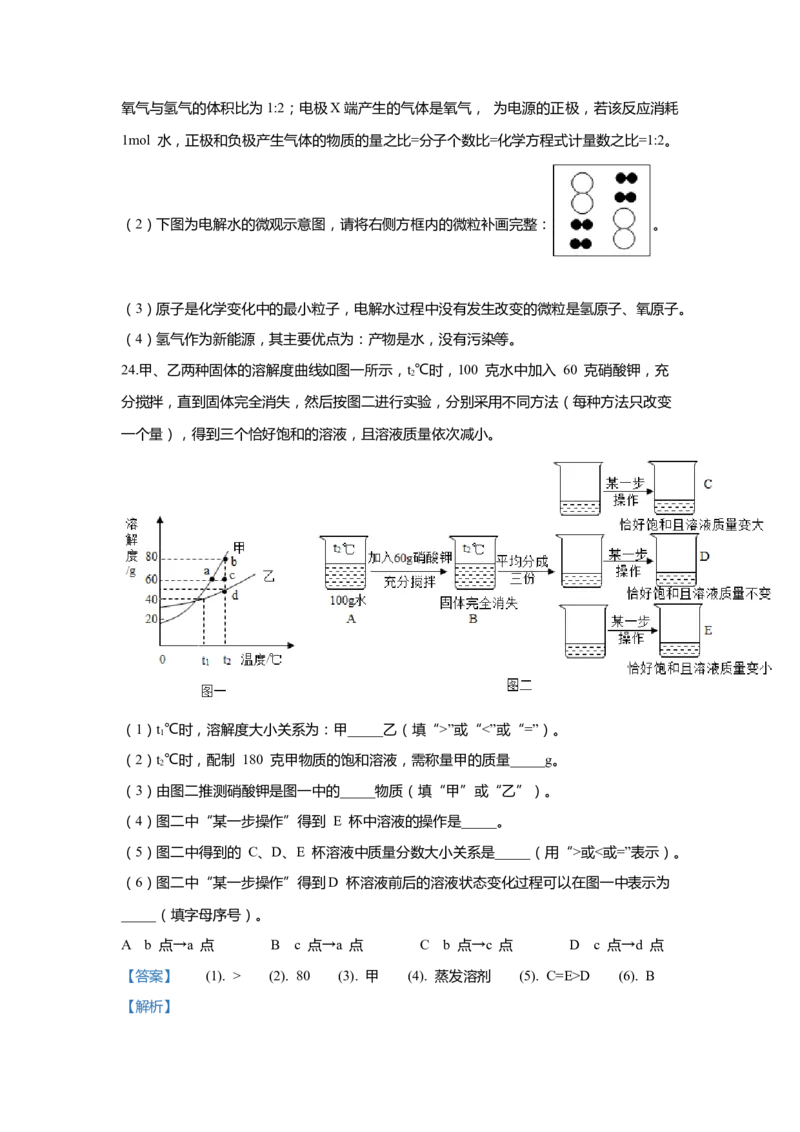
24.甲、乙两种固体的溶解度曲线如图一所示,t℃时,100 克水中加入 60 克硝酸钾,充
2
分搅拌,直到固体完全消失,然后按图二进行实验,分别采用不同方法(每种方法只改变
一个量),得到三个恰好饱和的溶液,且溶液质量依次减小。
(1)t℃时,溶解度大小关系为:甲_____乙(填“>”或“<”或“=”)。
1
(2)t℃时,配制 180 克甲物质的饱和溶液,需称量甲的质量_____g。
2
(3)由图二推测硝酸钾是图一中的_____物质(填“甲”或“乙”)。
(4)图二中“某一步操作”得到 E 杯中溶液的操作是_____。
(5)图二中得到的 C、D、E 杯溶液中质量分数大小关系是_____(用“>或<或=”表示)。
(6)图二中“某一步操作”得到D 杯溶液前后的溶液状态变化过程可以在图一中表示为
_____(填字母序号)。
A b 点→a 点 B c 点→a 点 C b 点→c 点 D c 点→d 点
【答案】 (1). > (2). 80 (3). 甲 (4). 蒸发溶剂 (5). C=E>D (6). B
【解析】【详解】(1)由溶解度图像可知:t℃时,溶解度大小关系为:甲>乙。
1
(2)t℃时,甲物质的溶解度为80g,说明:100g水中最多溶解80g甲物质,配制 180 克
2
甲物质的饱和溶液,需要水的质量为100g,称量甲的质量80g。
(3)由图二可知:t℃时,100g水中加入60g硝酸钾,升温至t℃后,固体全部溶解,变
1 2
为不饱和溶液,则硝酸钾在t℃的溶解度大于60g,推测硝酸钾是图一中的甲物质。
2
(4)图二中“某一步操作”得到E杯中溶液的操作是蒸发溶剂,使溶液质量变少,同时变
为饱和溶液。
(5)图二中得到的 C和E都是t℃时的饱和溶液,D是降温后得到的饱和溶液,D烧杯
2
温度低,溶液中质量分数大小关系是:C=E>D。
(6)图二中“某一步操作”得到D 杯溶液前后的溶液状态变化过程可以在图一中表示为
t℃的不饱和溶液降温后,变为t℃的饱和溶液;故选:B ,c 点→a 点。
2 1
八、简答题
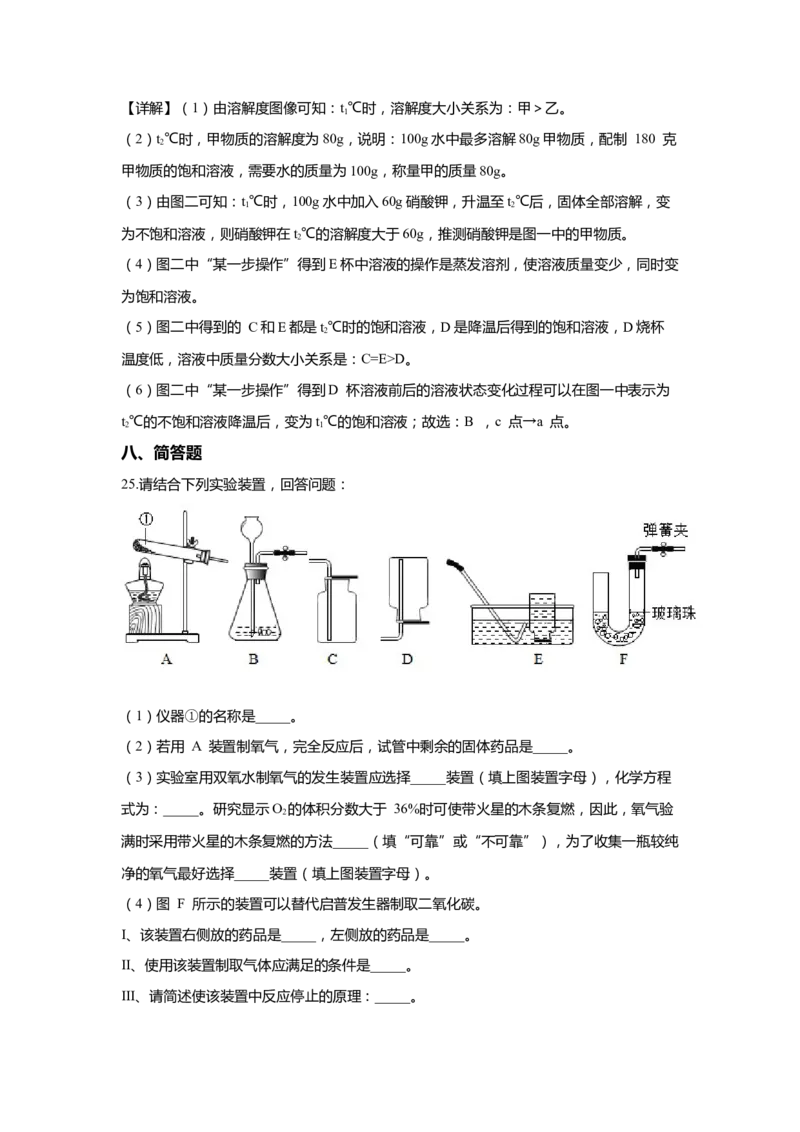
25.请结合下列实验装置,回答问题:
(1)仪器①的名称是_____。
(2)若用 A 装置制氧气,完全反应后,试管中剩余的固体药品是_____。
(3)实验室用双氧水制氧气的发生装置应选择_____装置(填上图装置字母),化学方程
式为:_____。研究显示O 的体积分数大于 36%时可使带火星的木条复燃,因此,氧气验
2
满时采用带火星的木条复燃的方法_____(填“可靠”或“不可靠”),为了收集一瓶较纯
净的氧气最好选择_____装置(填上图装置字母)。
(4)图 F 所示的装置可以替代启普发生器制取二氧化碳。
I、该装置右侧放的药品是_____,左侧放的药品是_____。
II、使用该装置制取气体应满足的条件是_____。
III、请简述使该装置中反应停止的原理:_____。(5)实验室用 100g 的大理石与足量的稀盐酸制取二氧化碳,充分反应后生成 0.5mol 二
氧化碳气体,请问参加反应的碳酸钙质量为多少克?_____(根据化学方程式列式计算)
【答案】 (1). 试管 (2). KCl、MnO (3). B (4). 2HO 2HO+O↑
2 2 2 2 2
(5). 不可靠 (6). E (7). 块状大理石 (8). 稀盐酸 (9). 块状固体与液体反应,
不加热 (10). 夹紧弹簧夹,继续反应生成的气体使右侧压强增大将液体压入左侧,右侧
固液分离,反应停止 (11). 50g
【解析】
【详解】(1)仪器①的名称是:试管。
(2)若用 A 装置氯酸钾和二氧化锰混合物固体制氧气,完全反应后,试管中剩余的固体
药品是:KCl和MnO 。
2
(3)实验室用双氧水制氧气的发生装置应选择固-液发生装置B,化学方程式为:2HO
2 2
2HO+O↑;研究显示 O 的体积分数大于 36%时可使带火星的木条复燃,因此,
2 2 2
氧气验满时采用带火星的木条复燃的方法不可靠,为了收集一瓶较纯净的氧气最好选择排
水法收集装置E。
(4)图 F 所示的装置可以替代启普发生器制取二氧化碳:
I、该装置右侧放的药品是块状石灰石,左侧放的药品是稀盐酸;
II、使用该装置制取气体应满足的条件是:块状固体与液体反应,不需要加热条件;
III、该装置中反应停止 的原理:夹紧弹簧夹,继续反应生成的气体使右侧压强增大将液体
压入左侧,右侧固液分离,反应停止;
(5)实验室用 100g 的大理石与足量的稀盐酸制取二氧化碳,充分反应后生成 0.5mol 二
氧化碳气体,
设碳酸钙的物质的量为n,n=0.5mol
参加反应的碳酸钙质量为m=n×M=0.5mol×100g/mol=50g。
26.资料:1. 实验室常用甲酸(HCO)和浓硫酸混合加热制备一氧化碳,化学方程式为
2 2
HCO HO+CO↑。2. 浓硫酸具有吸水性。3. 氢氧化钠溶液可以吸收二氧化碳、
2 2 2
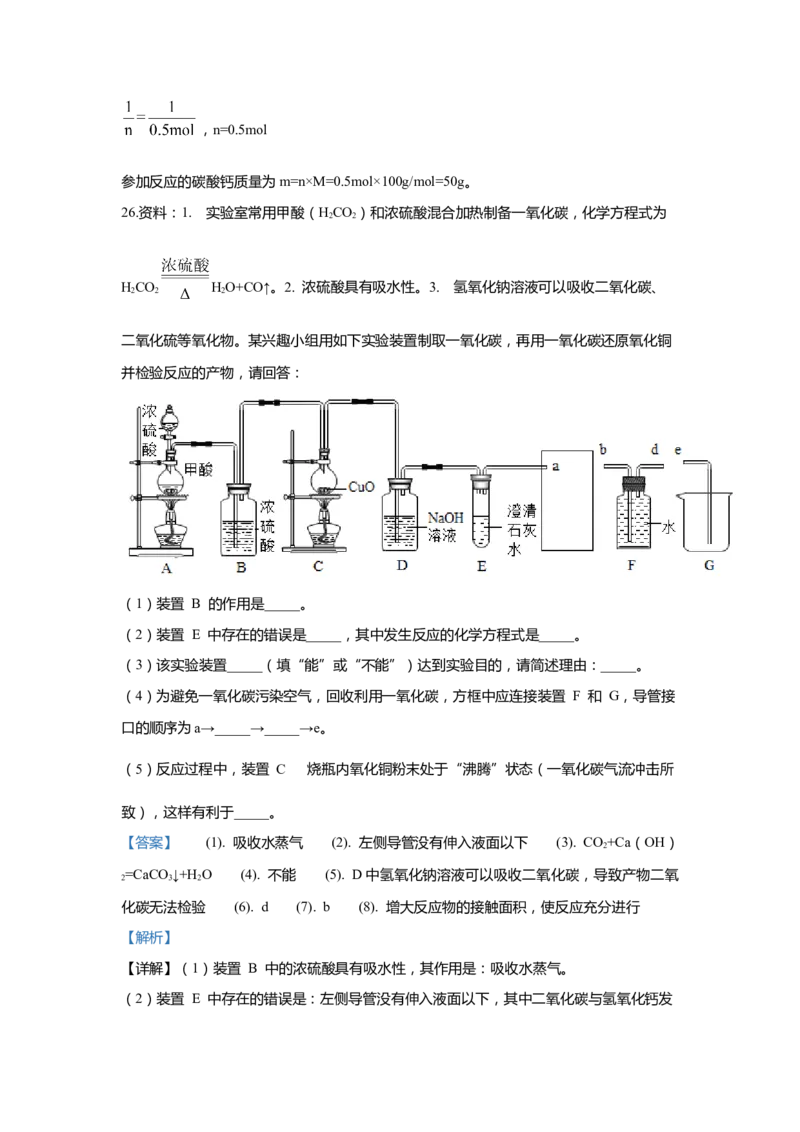
二氧化硫等氧化物。某兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜
并检验反应的产物,请回答:
(1)装置 B 的作用是_____。
(2)装置 E 中存在的错误是_____,其中发生反应的化学方程式是_____。
(3)该实验装置_____(填“能”或“不能”)达到实验目的,请简述理由:_____。
(4)为避免一氧化碳污染空气,回收利用一氧化碳,方框中应连接装置 F 和 G,导管接
口的顺序为a→_____→_____→e。
(5)反应过程中,装置 C 烧的瓶内氧化铜粉末处于“沸腾”状态(一氧化碳气流冲击所
致),这样有利于_____。
【答案】 (1). 吸收水蒸气 (2). 左侧导管没有伸入液面以下 (3). CO+Ca(OH)
2
=CaCO ↓+H O (4). 不能 (5). D中氢氧化钠溶液可以吸收二氧化碳,导致产物二氧
2 3 2
化碳无法检验 (6). d (7). b (8). 增大反应物的接触面积,使反应充分进行
【解析】
【详解】(1)装置 B 中的浓硫酸具有吸水性,其作用是:吸收水蒸气。
(2)装置 E 中存在的错误是:左侧导管没有伸入液面以下,其中二氧化碳与氢氧化钙发生反应的化学方程式是:CO+Ca(OH) =CaCO ↓+HO。
2 2 3 2
(3)该实验装置不能达到实验目的,理由是:D中氢氧化钠溶液可以吸收二氧化碳,导致
产物二氧化碳无法检验。
(4)为避免一氧化碳污染空气,回收利用一氧化碳,方框中应连接装置 F 和 G,用排水
法收集一氧化碳气体,导管接口的顺序为a→d→b→e。
(5)反应过程中,装置 C 的烧瓶内氧化铜粉末处于“沸腾”状态,这样有利于:增大反
应物的接触面积,使反应充分进行。