文档内容
雅安中学 2024-2025 学年下期 3 月考试高一年级
化学试题
注意事项:
1.答题前,考生务必将自己的姓名、座位号和准考证号填写在答题卡相应位置上。
2.第 I 卷的答案用 2B 铅笔填涂到答题卡上,第Ⅱ卷必须将答案填写在答题卡规定位置。回答
非选择题时,将答案写在答题卡上,写在试卷上无效。
3.考试结束,将答题卡交回。
4.本试卷分第 I 卷选择题和第Ⅱ卷非选择题,满分 100 分,考试时间 75 分钟。
可能用到的相对原子质量:Cu:64 Al:27
第 I 卷(单项选择题 共 45 分)
一、选择题(本题共 15 小题,每小题给出的四个选项中,只有一个选项是符合题意的,每题 3
分)
1. 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙黏土而为之”“凡坯既成,干燥之后,则堆积窖
中燃薪举火”“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是( )
A. “燃薪举火”使黏土发生了复杂的物理化学变化 B. 沙子和黏土的主要成分为硅酸盐
C. 烧制后自然冷却成红瓦,浇水冷却成青瓦 D. 黏土是制作砖瓦和陶瓷的主要原料
2. 下列关于 SO 的说法正确的是
2
A. 将 SO 通入滴有酚酞的 NaOH 溶液,溶液褪色,说明 SO 具有漂白性
2 2
B. 将 SO 通入 HS 的水溶液中,溶液出现黄色浑浊,体现了 SO 的还原性
2 2 2
C. SO 具有漂白性,将 SO 的水溶液滴到蓝色石蕊试纸上,试纸先变红后褪色
2 2
D. SO 通入足量 Ba(NO ) 溶液中可生成不溶于盐酸的白色沉淀
2 3 2
3. 以下有关氨气叙述中正确的是
A. 氨的喷泉实验体现了氨气是一种弱碱,氨水显碱性
B. 实验室常用加热固体氯化铵的方式制取氨气
C. 将蘸有浓氨水和浓硫酸的两根玻璃棒相互靠近,会看到有白烟生成。
D. 氨具有还原性,在一定条件下可与 NO 或 NO 反应转化为无毒气体。
2
4. N 为阿伏加徳罗常数的值,下列说法正确的是
A
A. 50 mL、18.4 mol/L 浓硫酸与足量铜加热反应,生成 SO 分子的数目为 0.46N
2 A
B. 12.8 g Cu 和 0.2 mol S 充分反应转移电子数为 0.2N
A
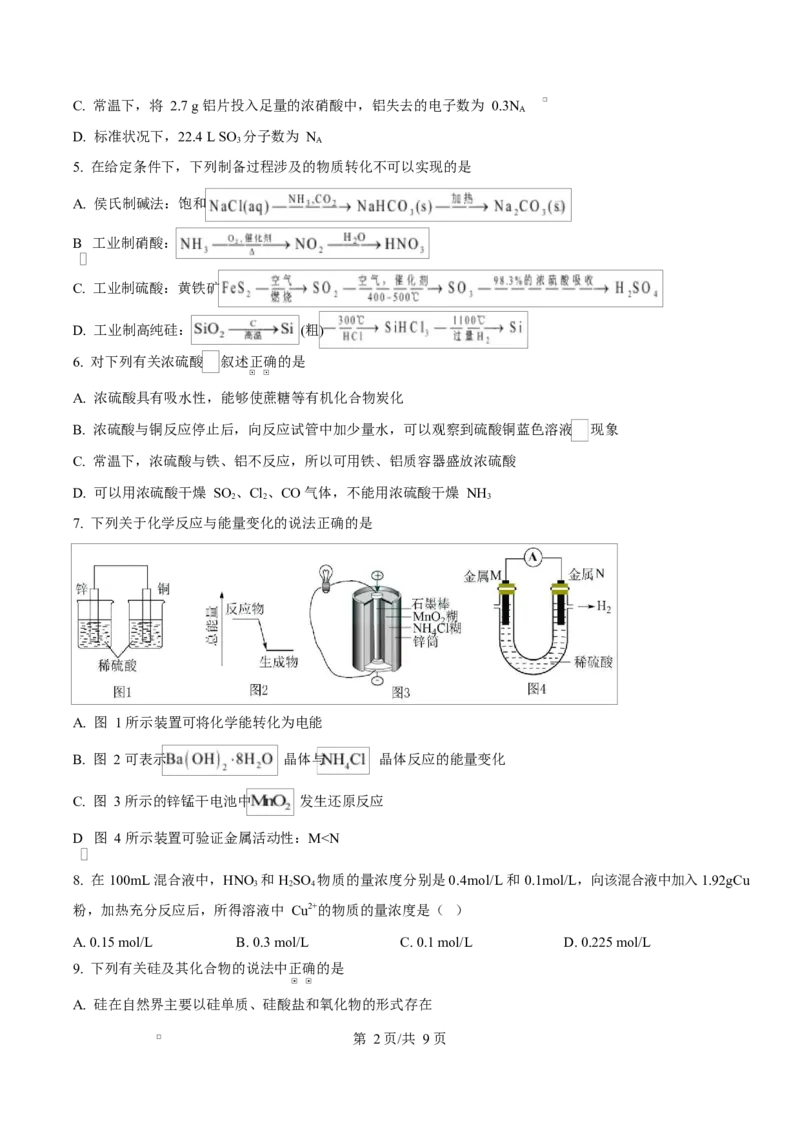
第 1页/共 9页C. 常温下,将 2.7 g 铝片投入足量的浓硝酸中,铝失去的电子数为 0.3N
A
D. 标准状况下,22.4 L SO 分子数为 N
3 A
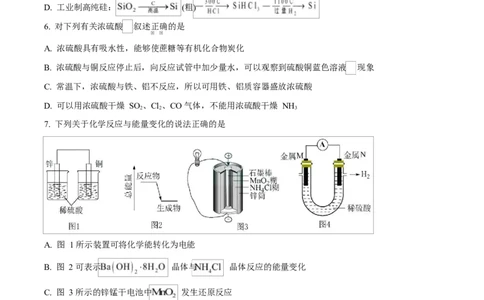
5. 在给定条件下,下列制备过程涉及的物质转化不可以实现的是
A. 侯氏制碱法:饱和
B 工业制硝酸:
C. 工业制硫酸:黄铁矿
D. 工业制高纯硅: (粗)
6. 对下列有关浓硫酸 叙述正确的是
A. 浓硫酸具有吸水性,能够使蔗糖等有机化合物炭化
B. 浓硫酸与铜反应停止后,向反应试管中加少量水,可以观察到硫酸铜蓝色溶液 现象
C. 常温下,浓硫酸与铁、铝不反应,所以可用铁、铝质容器盛放浓硫酸
D. 可以用浓硫酸干燥 SO 、Cl、CO 气体,不能用浓硫酸干燥 NH
2 2 3
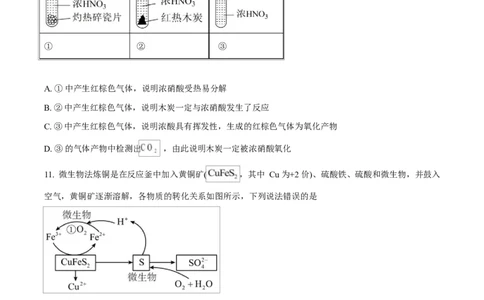
7. 下列关于化学反应与能量变化的说法正确的是
A. 图 1 所示装置可将化学能转化为电能
B. 图 2 可表示 晶体与 晶体反应的能量变化
C. 图 3 所示的锌锰干电池中 发生还原反应
D 图 4 所示装置可验证金属活动性:MH SiO
2 3
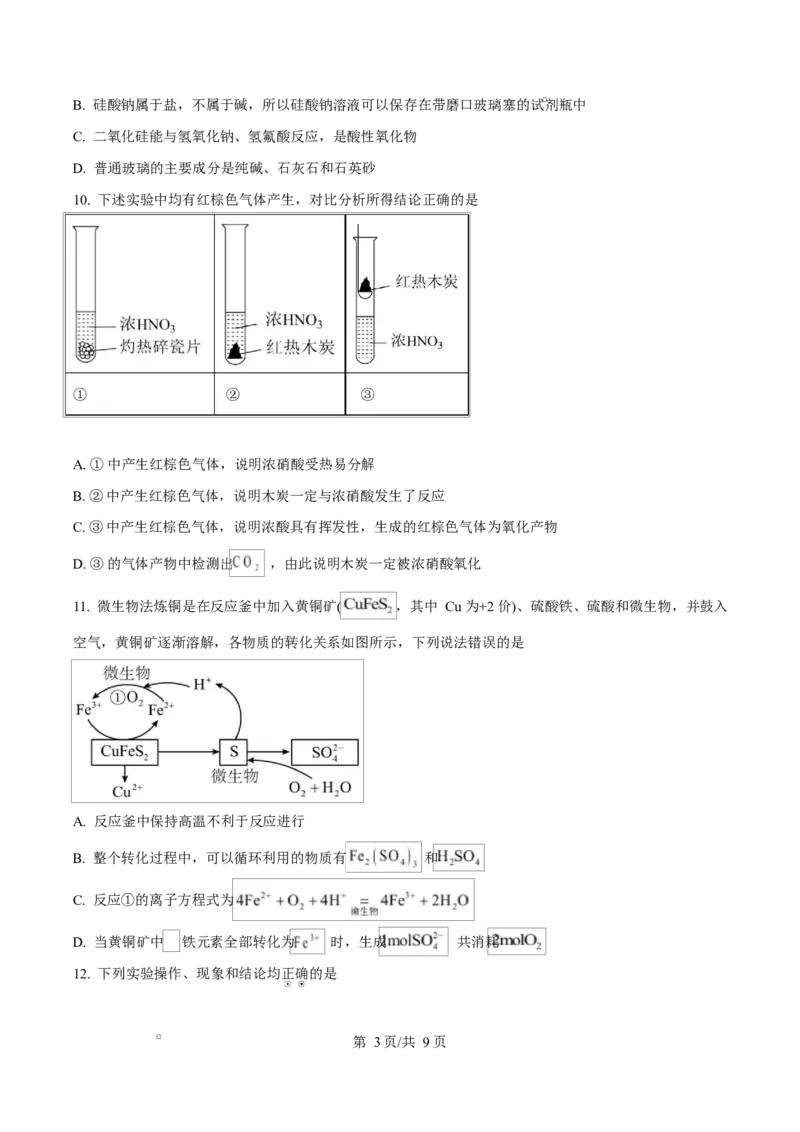
A. A B. B C. C D. D
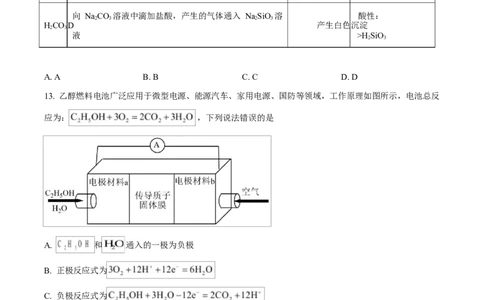
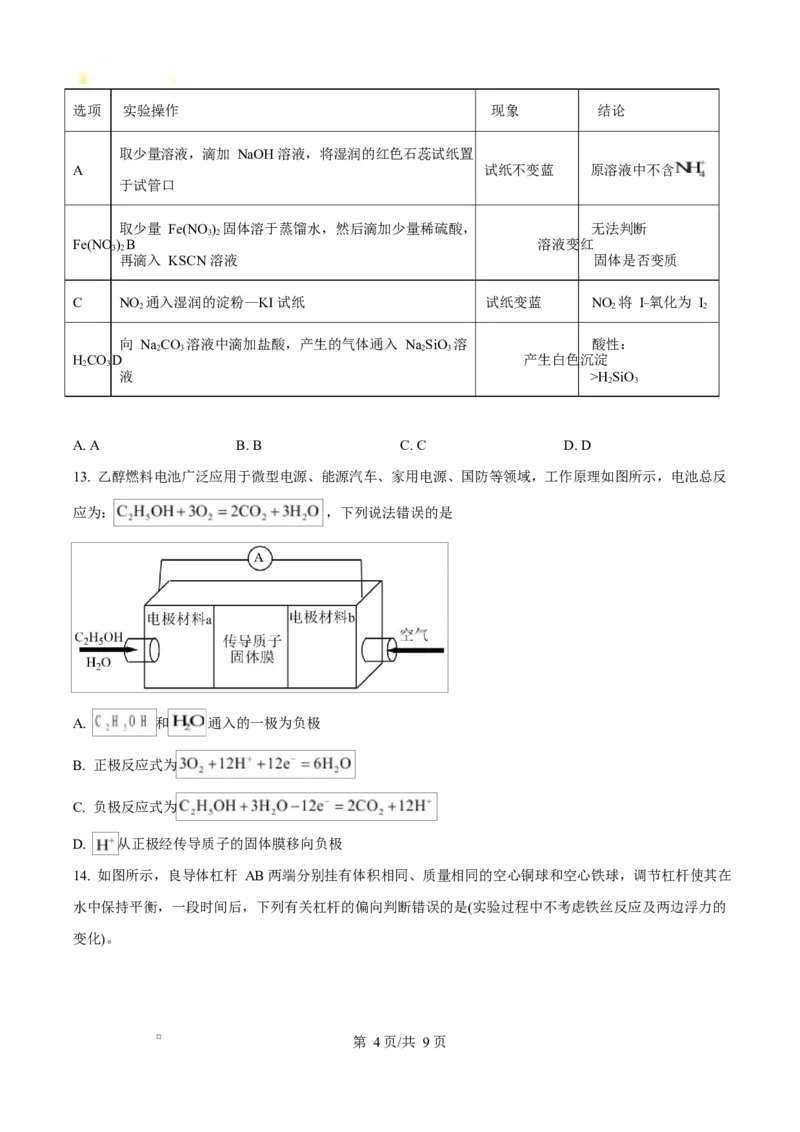
13. 乙醇燃料电池广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,电池总反
应为: ,下列说法错误的是
A. 和 通入的一极为负极
B. 正极反应式为
C. 负极反应式为
D. 从正极经传导质子的固体膜移向负极
14. 如图所示,良导体杠杆 AB 两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在
水中保持平衡,一段时间后,下列有关杠杆的偏向判断错误的是(实验过程中不考虑铁丝反应及两边浮力的
变化)。
第 4页/共 9页A. 若烧杯中为 溶液,则 A 端低 B 端高
B. 若烧杯中为 溶液,则 A 端低 B 端高
C. 若烧杯中为浓硝酸溶液,则 A 端低 B 端高
D. 若烧杯中为 溶液,铜球换成等质量等体积铝球,则 A 端高 B 端低
15. 计算机模拟催化剂表面水煤气产氢反应[ ]过程中能量的变化如
图所示。下列说法错误的是
A. 过程 I、Ⅱ均表示断键的吸收能量过程
B. 由图可知 比 CO 稳定
C. 过程Ⅲ既有共价键断裂,又有共价键形成
D. 该反应为放热反应
第 II 卷(非选择题 共 55 分)
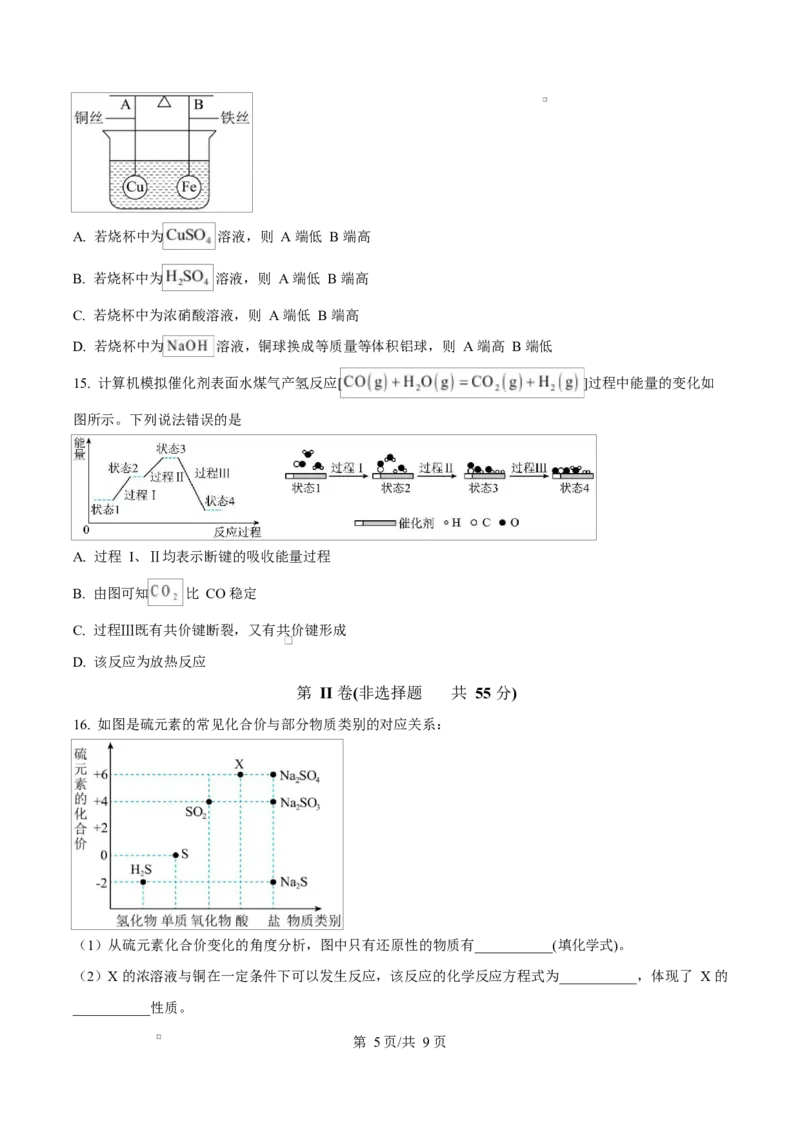
16. 如图是硫元素的常见化合价与部分物质类别的对应关系:
(1)从硫元素化合价变化的角度分析,图中只有还原性的物质有___________(填化学式)。
(2)X 的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为___________,体现了 X 的
___________性质。
第 5页/共 9页(3)某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取 SO 并完成相关性质探
2
究(不考虑水蒸气)。
①有同学认为制得的 SO 中可能混有杂质,其化学式为___________。
2
②为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
为验证并吸收 SO ,装置 B 中加入的试剂为___________;装置 C 中品红溶液的作用是___________;装置
2
H 的作用为___________。
(4)兴趣小组设计如图装置验证二氧化硫的化学性质。
为验证 SO 的还原性,取试管 b 中充分反应后的溶液分成三份,分别进行如下实验:
2
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入 BaCl 溶液,产生白色沉淀;
2
方案Ⅲ:向第三份溶液中加入 AgNO 溶液,有白色沉淀生成。
3
上述方案中合理的是___________(填Ⅰ、Ⅱ或Ⅲ);试管 b 中发生反应的离子方程式为___________。
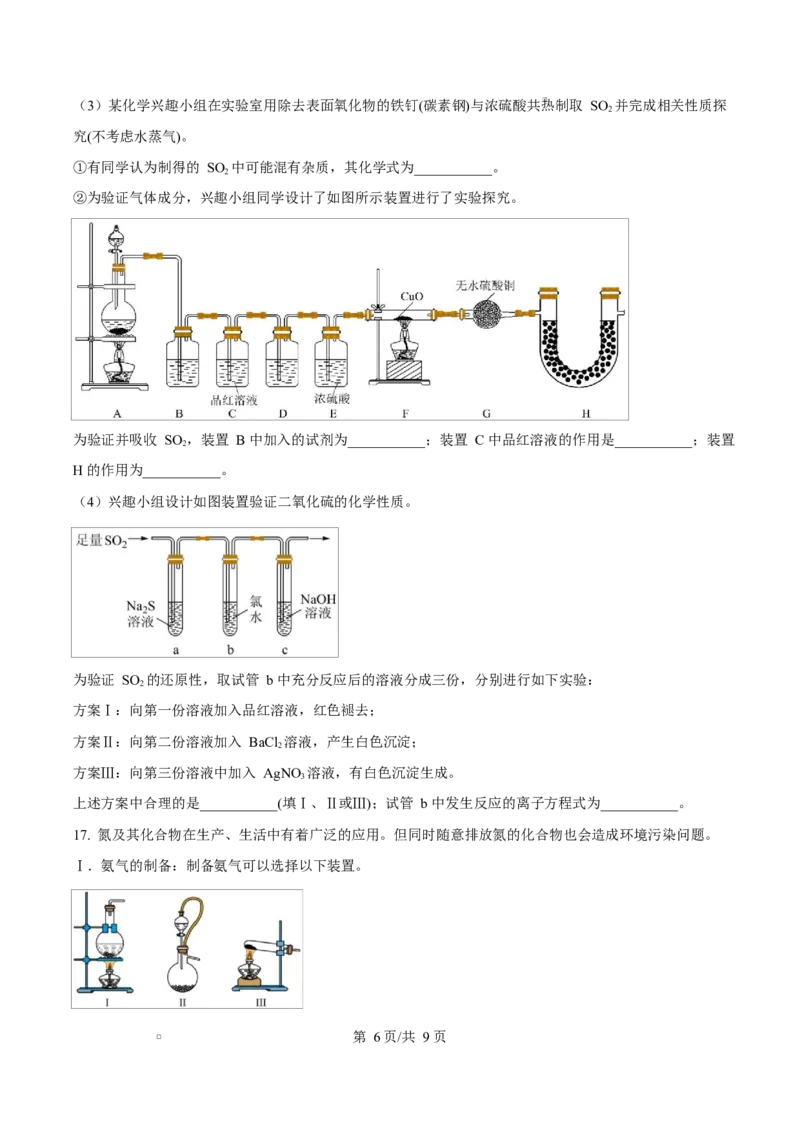
17. 氮及其化合物在生产、生活中有着广泛的应用。但同时随意排放氮的化合物也会造成环境污染问题。
Ⅰ.氨气的制备:制备氨气可以选择以下装置。
第 6页/共 9页(1)若选浓氨水与生石灰反应制备少量氨气,应选择装置___________(填序号)。
(2)若选择装置Ⅲ制备氨气,该反应的化学方程式:___________。
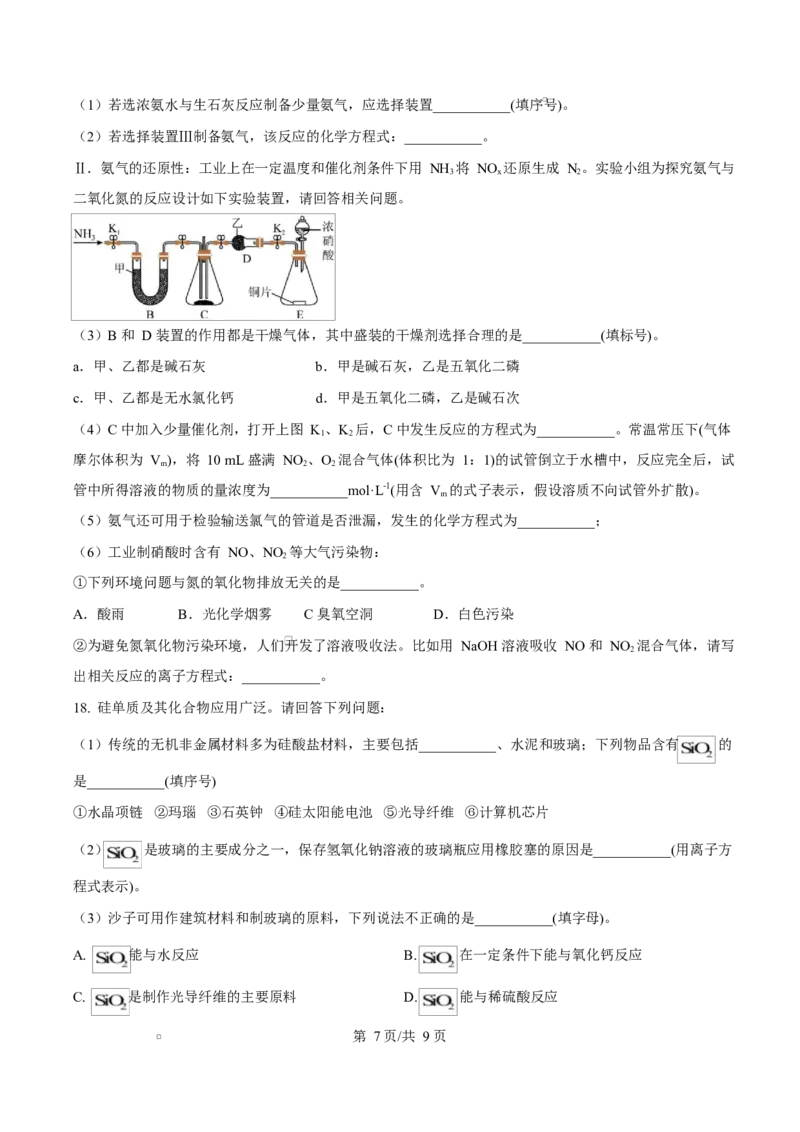
Ⅱ.氨气的还原性:工业上在一定温度和催化剂条件下用 NH 将 NO 还原生成 N。实验小组为探究氨气与
3 x 2
二氧化氮的反应设计如下实验装置,请回答相关问题。
(3)B 和 D 装置的作用都是干燥气体,其中盛装的干燥剂选择合理的是___________(填标号)。
a.甲、乙都是碱石灰 b.甲是碱石灰,乙是五氧化二磷
c.甲、乙都是无水氯化钙 d.甲是五氧化二磷,乙是碱石次
(4)C 中加入少量催化剂,打开上图 K、K 后,C 中发生反应的方程式为___________。常温常压下(气体
1 2
摩尔体积为 V ),将 10 mL 盛满 NO 、O 混合气体(体积比为 1:1)的试管倒立于水槽中,反应完全后,试
m 2 2
管中所得溶液的物质的量浓度为___________mol·L-1(用含 V 的式子表示,假设溶质不向试管外扩散)。
m
(5)氨气还可用于检验输送氯气的管道是否泄漏,发生的化学方程式为___________;
(6)工业制硝酸时含有 NO、NO 等大气污染物:
2
①下列环境问题与氮的氧化物排放无关的是___________。
A.酸雨 B.光化学烟雾 C 臭氧空洞 D.白色污染
②为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用 NaOH 溶液吸收 NO 和 NO 混合气体,请写
2
出相关反应的离子方程式:___________。
18. 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________、水泥和玻璃;下列物品含有 的
是___________(填序号)
①水晶项链 ②玛瑙 ③石英钟 ④硅太阳能电池 ⑤光导纤维 ⑥计算机芯片
(2) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是___________(用离子方
程式表示)。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是___________(填字母)。
A. 能与水反应 B. 在一定条件下能与氧化钙反应
C. 是制作光导纤维的主要原料 D. 能与稀硫酸反应
第 7页/共 9页(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl )还原法是当前制备高纯硅的主要方法,生产过程如
3
图:
①写出制粗硅的化学方程式___________。
②整个制备过程必须严格控制无水无氧。SiHCl 遇水剧烈反应生成 、HCl 和一种气体单质,写出发
3
生反应的化学方程式___________;在制备高纯硅的过程中若混入 ,可能引起的后果是___________。
19. 现代社会中,人类的一切活动都离不开能量,而许多能量的利用与化学反应中的能量变化密切相关。
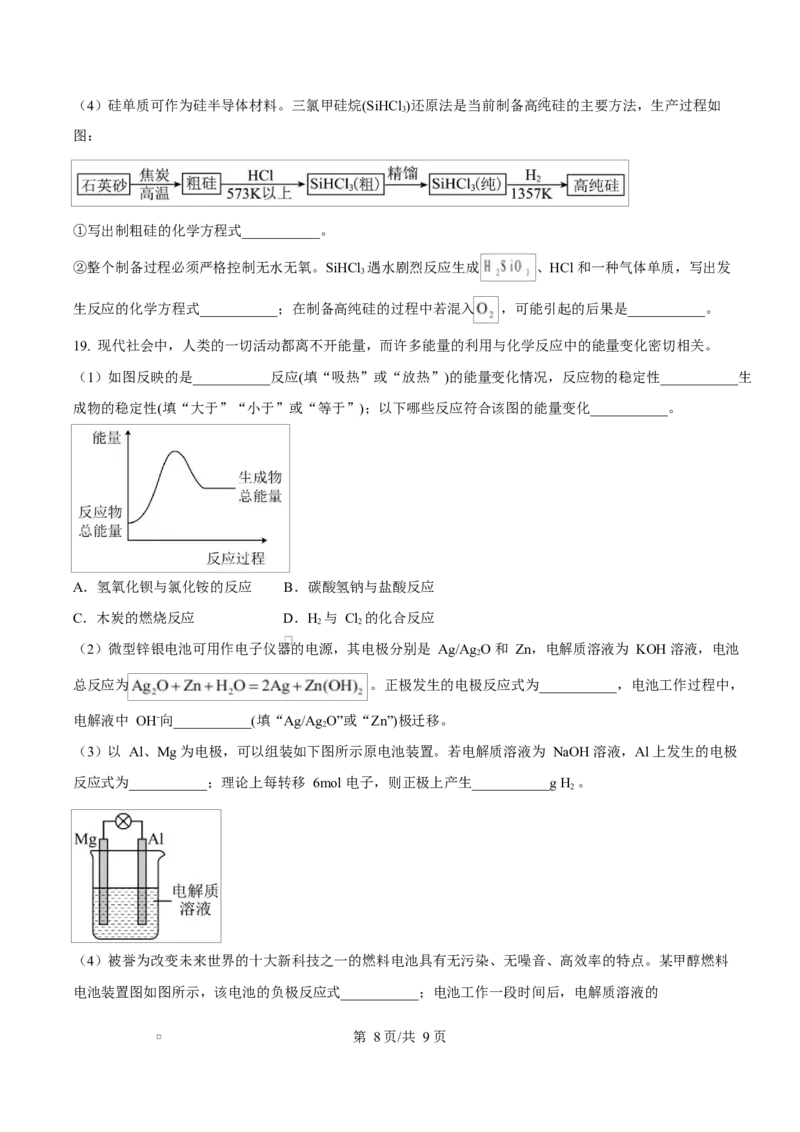
(1)如图反映的是___________反应(填“吸热”或“放热”)的能量变化情况,反应物的稳定性___________生
成物的稳定性(填“大于”“小于”或“等于”);以下哪些反应符合该图的能量变化___________。
A.氢氧化钡与氯化铵的反应 B.碳酸氢钠与盐酸反应
C.木炭的燃烧反应 D.H 与 Cl 的化合反应
2 2
(2)微型锌银电池可用作电子仪器的电源,其电极分别是 Ag/Ag O 和 Zn,电解质溶液为 KOH 溶液,电池
2
总反应为 。正极发生的电极反应式为___________,电池工作过程中,
电解液中 OH-向___________(填“Ag/Ag O”或“Zn”)极迁移。
2
(3)以 Al、Mg 为电极,可以组装如下图所示原电池装置。若电解质溶液为 NaOH 溶液,Al 上发生的电极
反应式为___________;理论上每转移 6mol 电子,则正极上产生___________g H 。
2
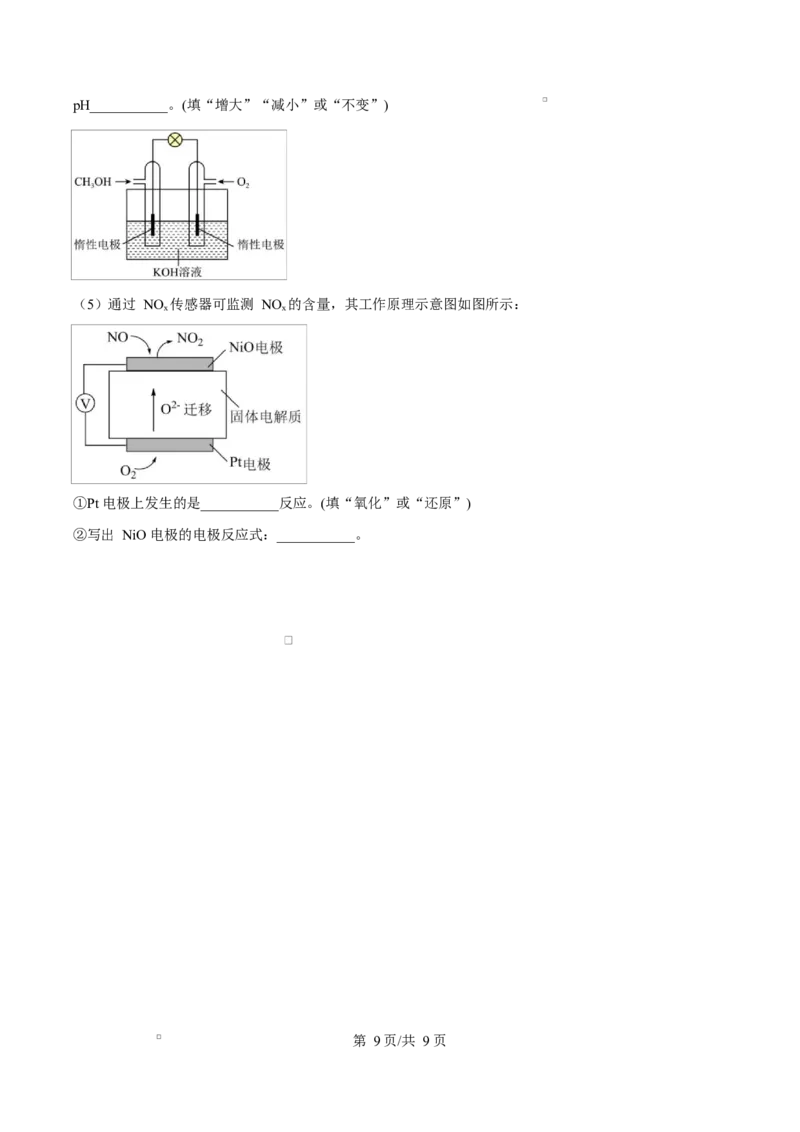
(4)被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。某甲醇燃料
电池装置图如图所示,该电池的负极反应式___________;电池工作一段时间后,电解质溶液的
第 8页/共 9页pH___________。(填“增大”“减小”或“不变”)
(5)通过 NO 传感器可监测 NO 的含量,其工作原理示意图如图所示:
x x
①Pt 电极上发生的是___________反应。(填“氧化”或“还原”)
②写出 NiO 电极的电极反应式:___________。
第 9页/共 9页