文档内容
虹口区 2020~2021 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2022. 1
相对原子质量: H-1 N-14 O-16 C-35. 5 K-39
五、选择题(共20 分)
请将正确选项的代号用2B铅笔填涂在答题纸相应位置上,更改答案时,用橡皮擦去,重
新填涂.
21~34题均只有一个正确选项
21. 常见的液体中属于纯净物的是
A. 汽水 B. 河水 C. 湖水 D. 蒸馏水
22. 空气中含量最多的气体是
A. 氩气 B. 水蒸气 C. 氧气 D. 氮气
23. 在水中能形成溶液的是
A. 硫酸铜 B. 大理石 C. 花生油 D. 木炭粉
24. 实验测得一些液体室温时的pH,其中酸性最强的是
A. 84消毒液: 10 B. 某洗发水: 7 C. 柔顺剂: 6 D. 洁厕剂: 1
25. SO 中S的化合价是
3
A. -6 B. -3 C. +3 D. +6
26. 自来水生产中,通入氯气的作用是
A. 杀菌消毒 B. 吸附异味 C. 促进沉降 D. 凝聚小颗粒
27. 属于化学变化的是
A. 矿石粉碎 B. 蔗糖溶解 C. 燃气燃烧 D. 酒精挥发
28. 硫在氧气中燃烧的现象是
A. 发出白光 B. 产生蓝紫色火焰 C. 产生白雾 D. 生成无气味气体
29. 属于氧化物的是
A. O B. N O C. C H OH D. K CO
2 2 5 2 5 2 3
30. 关于氦气的说法正确的是
A. 化学式: He B. 元素存在形态:游离态
2
C. 化学性质:密度小 D. 用途:助燃
31. 用“C” 和“●”分别表示两种不同的原子,则根据分子模型“ ”,分析正确的是
A. 该分子构成的物质由两种元素组成
B. “ ”是保持该物质性质的微粒
C. 该物质的一个分子由两个原子构成
1D. 该物质的化学式可能是2HO
32. 对事实或现象的微观解释正确的是
A. 氧气液化:分子种类变化
B. 水变成冰体积变大:水分子变大
C. 圧缩气体:微粒间隙变小
D. 气态二氧化碳变成干冰:微粒不再运动
33. 化学方程式书写正确的是
A. 4Fe+3O 二2Fe O B. 2Mg+O 2MgO
2 2 3 2
C. 2P+50 == P O D. H CO -二CO +H O
2 5 2 3 2 2
34. 物质与其性质、用途对应正确的是
物质 性质 用途
A 金刚石 无色、透明 用于切割玻璃
B 石墨 软 制作电极
C 石灰石 高温分解 生产生石灰
D 碳 常温下性质稳定 燃料
35 -37题每题均有1~2 个正确选项
35. 关于同素异形体的相关分析正确的是
A. 红磷和白磷互为同素异形体
B. 石墨和活性炭互为同素异形体
C. 互为同素异形体的物质,若物质的量相等则质量相等
D. 互为同素异形体的物质,元素组成相同但结构不同
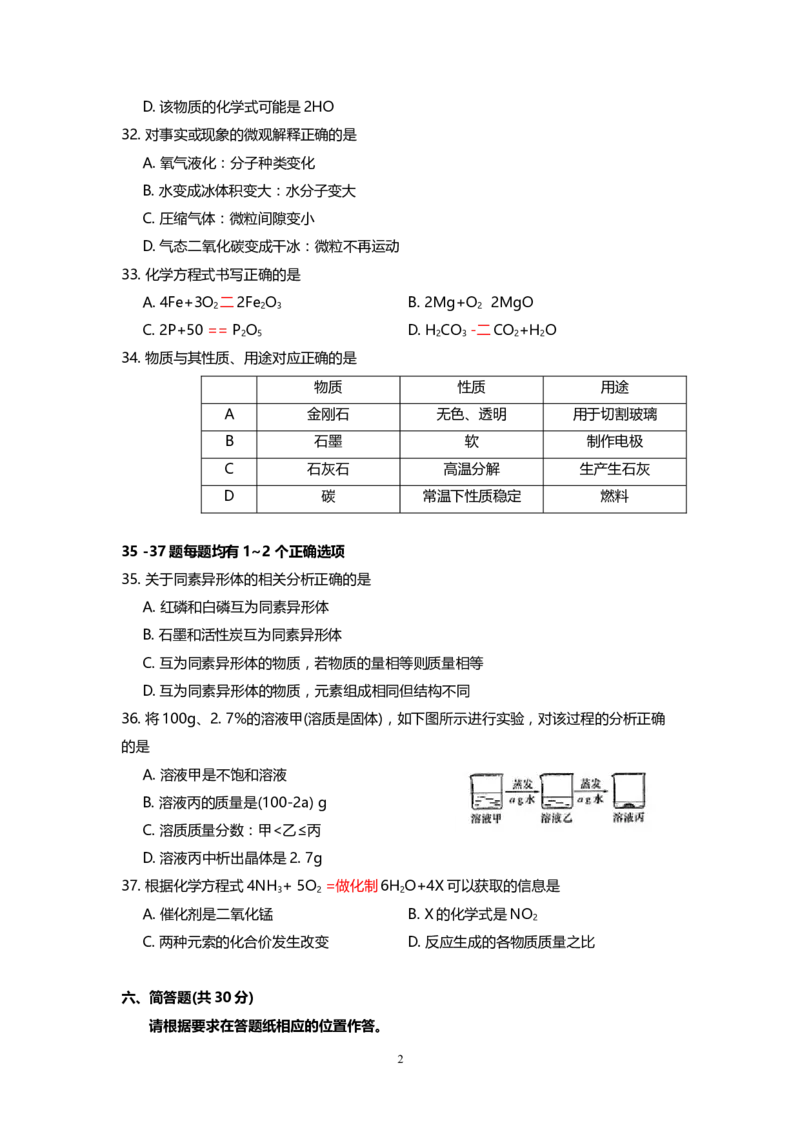
36. 将100g、2. 7%的溶液甲(溶质是固体),如下图所示进行实验,对该过程的分析正确
的是
A. 溶液甲是不饱和溶液
B. 溶液丙的质量是(100-2a) g
C. 溶质质量分数:甲<乙≤丙
D. 溶液丙中析出晶体是2. 7g
37. 根据化学方程式4NH + 5O =做化制6H O+4X可以获取的信息是
3 2 2
A. 催化剂是二氧化锰 B. X的化学式是NO
2
C. 两种元索的化合价发生改变 D. 反应生成的各物质质量之比
六、简答题(共30分)
请根据要求在答题纸相应的位置作答。
238. 中国航天事业自创建以来取得了辉煌成就。
①偏二甲肼(C H N )是长征二号F火箭的推进剂之一,0. 5 mol C H N 中约含有
2 8 2 2 8 2
_________个N原子。
②我国新一代运载火箭广泛采用液氢、液氧、煤油作为推进剂。
I 氢气在氧气中燃烧的化学方程式是_________;该反应属于
_________(选填“化合反应”或“分解反应”)。
II 煤油与氧气反应的生成物是H O和CO ,说明煤油中一定含有的
2 2
元素是_________元素(填元素名称)。
III 水通电分解可以产生氢气和氧气。如右图所示的电解水实验中,a处玻璵管内的气体是
_________,检验生成氧气的方法是_________。
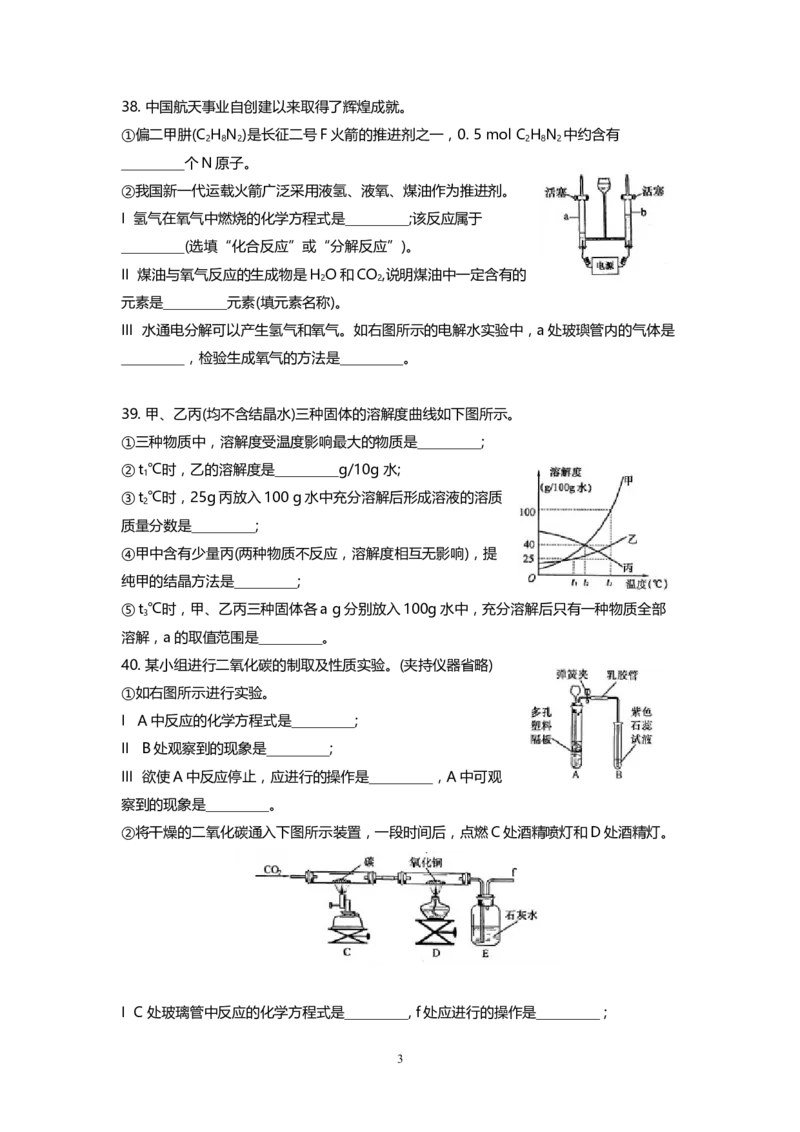
39. 甲、乙丙(均不含结晶水)三种固体的溶解度曲线如下图所示。
①三种物质中,溶解度受温度影响最大的物质是_________;
②t ℃时,乙的溶解度是_________g/10g 水;
1
③t ℃时,25g丙放入100 g水中充分溶解后形成溶液的溶质
2
质量分数是_________;
④甲中含有少量丙(两种物质不反应,溶解度相互无影响),提
纯甲的结晶方法是_________;
⑤t ℃时,甲、乙丙三种固体各a g分别放入100g水中,充分溶解后只有一种物质全部
3
溶解,a的取值范围是_________。
40. 某小组进行二氧化碳的制取及性质实验。(夹持仪器省略)
①如右图所示进行实验。
I A中反应的化学方程式是_________;
II B处观察到的现象是_________;
III 欲使A中反应停止,应进行的操作是_________,A中可观
察到的现象是_________。
②将干燥的二氧化碳通入下图所示装置,一段时间后,点燃C处酒精喷灯和D处酒精灯。
I C 处玻璃管中反应的化学方程式是_________, f处应进行的操作是_________ ;
3II D处玻璃管中的现象是_________;
III E处石灰水变浑浊,说明进入E的气体中含有_________;请分析该气体的来源
_________。
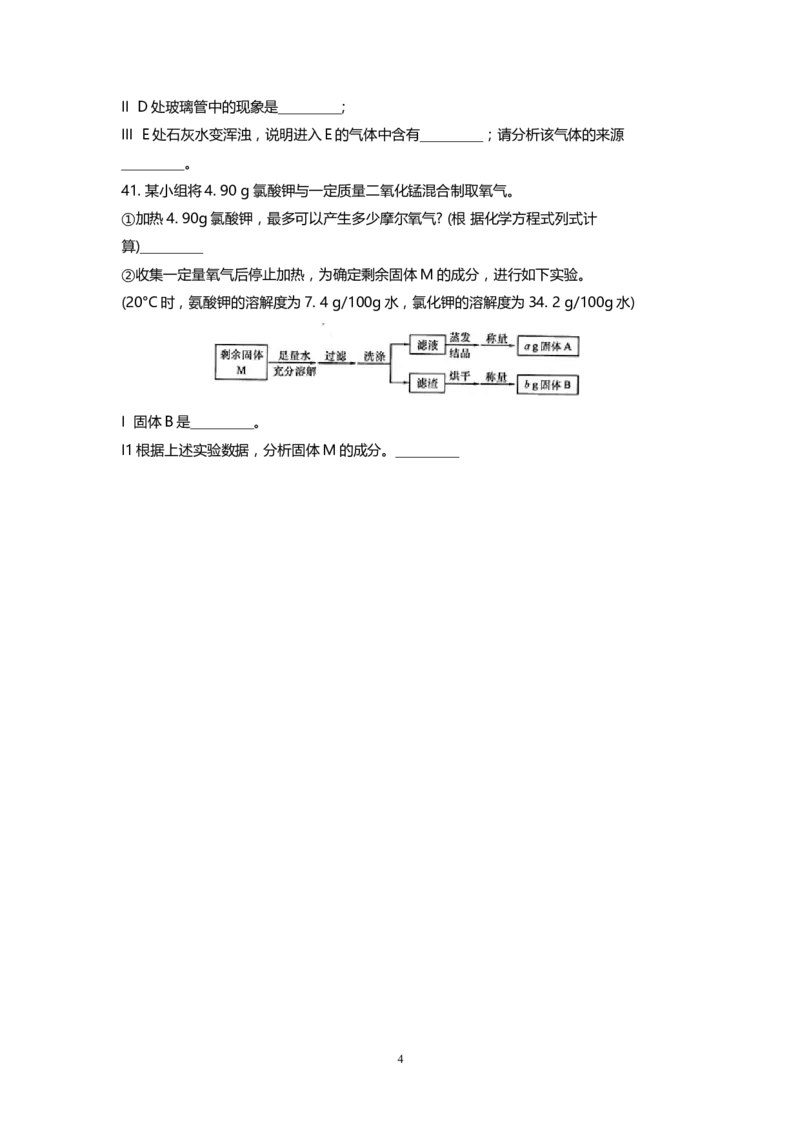
41. 某小组将4. 90 g氯酸钾与一定质量二氧化锰混合制取氧气。
①加热4. 90g氯酸钾,最多可以产生多少摩尔氧气? (根 据化学方程式列式计
算)_________
②收集一定量氧气后停止加热,为确定剩余固体M的成分,进行如下实验。
(20°C时,氨酸钾的溶解度为7. 4 g/100g水,氯化钾的溶解度为34. 2 g/100g水)
I 固体B是_________。
I1根据上述实验数据,分析固体M的成分。_________
4