文档内容
长宁区 2020~2021 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2022.1
相对原子质量:H-1 O-16 C-12
五、选择题(共 20 分)21~34 题每题均只有 1 个正确选项
21. 不能改善空气质量的措施是
A. 推广清洁能源 B. 汽车尾气净化 C. 控制工地扬尘 D. 使用空气香薰
22. 氢元素符号书写正确的是
A. N B. Ne C. H D. He
23. 空气中含量最多的成分是
A. 氧气 B. 氮气 C. 氖气 D. 二氧化碳
24. SO 中硫元素的化合价是
2
A. +1 B. +2 C. +3 D. +4
25. 属于碳的化学性质的是
A. 还原性 B. 导电性 C. 导热性 D. 吸附性
26. 自来水生产中,能起到杀菌消毒作用的试剂是
A. 活性炭 B. 氯气 C. 砂石 D. 明矾
27. NaCO 中原子团的名称是
2 3
A. 三氧化碳 B. 碳酸 C. 碳酸根 D. 碳氧根
28. 属于分解反应的是
A. 煅烧大理石 B. 硫的燃烧
C. 向生石灰中滴加水 D. 加热木炭与氧化铜的混合物
29. 一定能增大二氧化碳在水中溶解度的操作是
A. 边升温边加压 B. 边降温边加压 C. 边升温边减压 D. 边降温边减压
30. 室温下,将 pH 为 12 的澄清石灰水敞口放置一段时间后,溶液的 pH 变化可能是
A. 变小为 10 B. 变小为 2 C. 基本不变 D. 变大为 13
31. 为了使酒精充分燃烧,做法错误的是
A. 用纯氧替代空气 B. 使用固体酒精
C. 将酒精加热为酒精蒸气 D. 将酒精喷成雾状
32. 由一种分子构成的物质不可能是
A. 单质 B. 化合物 C. 混合物 D. 氧化物
33. 关于实验室制取氧气的操作,描述正确的是
A. 分别取等量的氯酸钾和二氧化锰,依次加入到试管底部并混合均匀
B. 由上至下,从右向左组装仪器C. 集气瓶装满水,倒放在水槽中,并将导管伸入集气瓶中
D. 反应停止后,先将导管从水槽中取出,再熄灭酒精灯
34. 关于相对原子质量说法正确的是
A. 相对原子质量的单位是 kg
B. 相对原子质量是一个比值,单位是 g
C. 某原子的相对原子质量在数值上是该原子的实际质量的 12 倍
D. 相对原子质量越大,原子的实际质量也越大
35~37 每题均有 1~2 个正确选项
35. 对金刚石和石墨描述正确的是
A. 碳元素都以游离态存在
B. 碳元素都以化合态存在
C. 化学性质相同是由于碳原子排列结构相似
D. 物理性质不同是由于碳原子排列结构不同
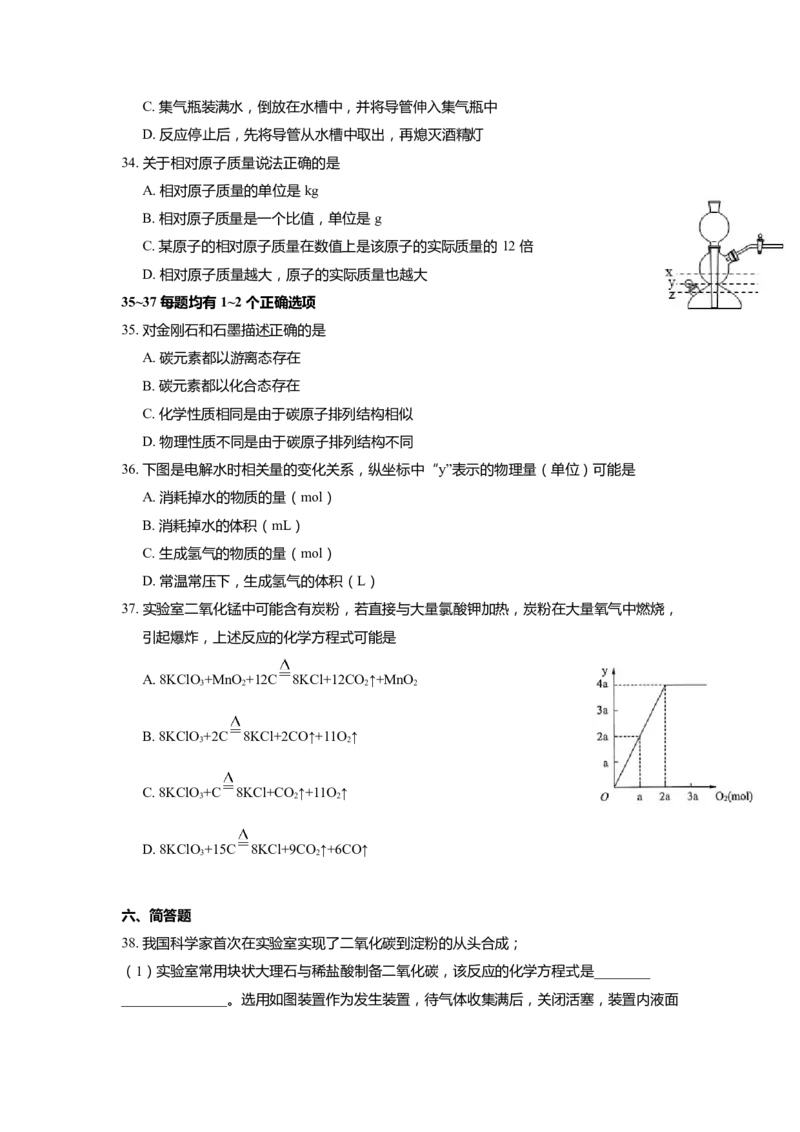
36. 下图是电解水时相关量的变化关系,纵坐标中“y”表示的物理量(单位)可能是
A. 消耗掉水的物质的量(mol)
B. 消耗掉水的体积(mL)
C. 生成氢气的物质的量(mol)
D. 常温常压下,生成氢气的体积(L)
37. 实验室二氧化锰中可能含有炭粉,若直接与大量氯酸钾加热,炭粉在大量氧气中燃烧,
引起爆炸,上述反应的化学方程式可能是
A. 8KClO+MnO+12C 8KCl+12CO ↑+MnO
3 2 2 2
B. 8KClO+2C 8KCl+2CO↑+11O ↑
3 2
C. 8KClO+C 8KCl+CO ↑+11O ↑
3 2 2
D. 8KClO+15C 8KCl+9CO ↑+6CO↑
3 2
六、简答题
38. 我国科学家首次在实验室实现了二氧化碳到淀粉的从头合成;
(1)实验室常用块状大理石与稀盐酸制备二氧化碳,该反应的化学方程式是________
_______________。选用如图装置作为发生装置,待气体收集满后,关闭活塞,装置内液面将由 x 降至___________处(选填“y”或“z”),此时装置内气体压强_____________外界
大气压(选填“大于”、“等于”或“小于”)。
(2)该合成中的第一步是先将二氧化碳转换成甲醇(化学式为 CHO),这属于
4
____________(选填“物理”或“化学”)变化,甲醇是由___________种元素组成,摩尔
质量为____________,1mol 甲醇中约含有____________个碳原子。
(3)该合成的最后一步是将碳六化合物合成为淀粉,该人工合成淀粉中一定含有氢元素、
氧元素和_____________元素。
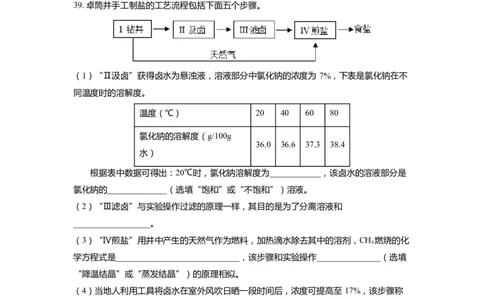
39. 卓筒井手工制盐的工艺流程包括下面五个步骤。
(1)“Ⅱ汲卤”获得卤水为悬浊液,溶液部分中氯化钠的浓度为 7%,下表是氯化钠在不
同温度时的溶解度。
温度(℃) 20 40 60 80
氯化钠的溶解度(g/100g
36.0 36.6 37.3 38.4
水)
根据表中数据可得出:20℃时,氯化钠溶解度为____________,该卤水的溶液部分是
氯化钠的______________(选填“饱和”或“不饱和”)溶液。
(2)“Ⅲ滤卤”与实验操作过滤的原理一样,其目的是为了分离溶液和
__________________。
(3)“Ⅳ煎盐”用井中产生的天然气作为燃料,加热滴水除去其中的溶剂,CH 燃烧的化
4
学方程式是_____________________________,该步骤和实验操作_______________(选填
“降温结晶”或“蒸发结晶”)的原理相似。
(4)当地人利用工具将卤水在室外风吹日晒一段时间后,浓度可提高至 17%,该步骤称
为“晒卤”,应位于步骤_______________(选填“Ⅱ”、“Ⅲ”或“Ⅳ”)之后,请比较
卓筒井手工制盐中“晒卤”和“煎盐”,两者的原理有何相似之处和不同之处
___________________________
______________________________________________________________________________
。
40. 实验室利用 6.4g 铜网制氧化铜,探究一氧化碳的还原性。实验装置如下(装置气密性
良好,夹持仪器省略)。(1)关闭弹簧夹k,点燃酒精灯,铜网与装置内的氧气反应生成氧化铜,该反应的化学方
程式是______________。
(2)打开弹簧夹k,打开装置A 中分液漏斗并控制蒸馏水流速平缓,目的是
_______________
_______________, 一段时间后,B 中铜网表面的现象是__________________________,
说明一氧化碳具有还原性,此时C 中的现象是____________________________,产生此现
象的化学方程式是______________________________。
(3)装置 D 的作用是_________________________________________________________。
(4)为了能重复使用铜网,有人建议将铜网取出并称量,若质量_______________6.4g
(选填“大于”、“等于”或““小于”),说明铜网表面残留氧化铜,需完全除去后才
能重复使用,你是否同意该方案,并阐述你的理由
_________________________________________________
______________________________________________________________________________
。
41. 实验室常用 3%的过氧化氢溶液制备氧气。
(1)欲配置 100g 3%的过氧化氢溶液,需取用 10%的过氧化氢溶液____________mL。
(2)含 0.04mol 溶质的过氧化氢溶液完全反应,能产生多少克的氧气___________?(根据
化学方程式列式计算)(3)反应结束后,发生装置内剩余气体的主要成分为氧气,请设计实验方案,收集该剩余
气体___________________________________________________________________________
______________________________________________________________________________
。