文档内容
黄浦区 2020~2021 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2022. 1
相对原子质量: H-1 C-12 N-14 O-16 Mg-24 S-32 Ca-40
五、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦
去,重新填涂。
21~34每题均只有一个正确选项
21. 硅的元素符号是
A. Ag B. Si C. Ar D. Li
22. 天然气的主要成分是
A. 甲烧 B. 一氧化碳 C. 氢气 D. 乙炔
23. 四个氮原子的符号书写正确的是
A. N B. 2N C. 4N D. 4N
2 4
24. 二氧化氯(CIO )中,氯元素的化合价为
2
A. -1 B. -2 C. +2 D. +4
25. 工业上分离空气得到氧气,是利用各组分具有不同的
A. 沸点 B. 密度 C. 溶解性 D. 熔点
26. 辉铜矿是炼铜的原料,各地的辉铜矿样品含铜量各不相同。由此推测,辉铜
矿属于
A. 化合物 B. 混合物 C. 氧化物 D. 单质
27. 右图是硫酸铵中各元素质量分数的示意图,其中“区域4”表示的元素是
A. 氮 B. 氢 C. 硫 D. 氧
28. 铁丝在氧气中燃烧,生成固体的颜色为
A. 蓝色 B. 红色 C. 黑色 D. 白色
29. 25℃时,测得某种溶液的pH=8,有关该溶液的说法正确的是
A. 溶质属于酸 B. 溶液呈碱性
C. 加入水,pH增大 D. 能使石蕊试液变红
30. 关于氢气在氧气中燃烧的实验,说法错误的是
A. 产生淡蓝色火焰 B. 产物能使无水硫酸铜变蓝
C. 该实验能证明水的元素组成 D. 变化中的最小微粒是氢分子
31. 室温下,将1 g葡萄糖(C H O ) 放入一定最水中,充分搅拌后,配制成溶液。在此过
6 12 6
程中,葡萄糖分子发生改变的是
1A. 分子的大小 B. 分子间的问隔
C. 分子的总数 D. 分子中的原子个数
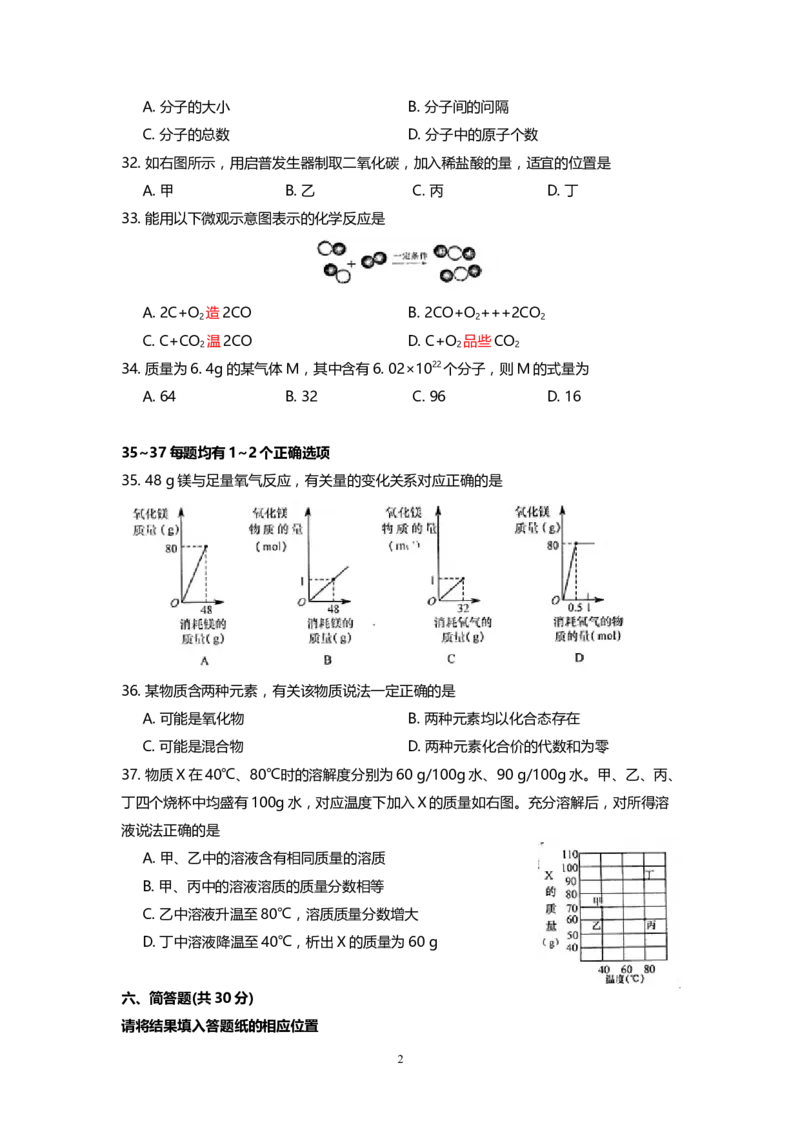
32. 如右图所示,用启普发生器制取二氧化碳,加入稀盐酸的量,适宜的位置是
A. 甲 B. 乙 C. 丙 D. 丁
33. 能用以下微观示意图表示的化学反应是
A. 2C+O 造2CO B. 2CO+O +++2CO
2 2 2
C. C+CO 温2CO D. C+O 品些CO
2 2 2
34. 质量为6. 4g的某气体M,其中含有6. 02×1022个分子,则M的式量为
A. 64 B. 32 C. 96 D. 16
35~37每题均有1~2个正确选项
35. 48 g镁与足量氧气反应,有关量的变化关系对应正确的是
36. 某物质含两种元素,有关该物质说法一定正确的是
A. 可能是氧化物 B. 两种元素均以化合态存在
C. 可能是混合物 D. 两种元素化合价的代数和为零
37. 物质X在40℃、80℃时的溶解度分别为60 g/100g水、90 g/100g水。甲、乙、丙、
丁四个烧杯中均盛有100g水,对应温度下加入X的质量如右图。充分溶解后,对所得溶
液说法正确的是
A. 甲、乙中的溶液含有相同质量的溶质
B. 甲、丙中的溶液溶质的质量分数相等
C. 乙中溶液升温至80℃,溶质质量分数增大
D. 丁中溶液降温至40℃,析出X的质量为60 g
六、简答题(共30分)
请将结果填入答题纸的相应位置
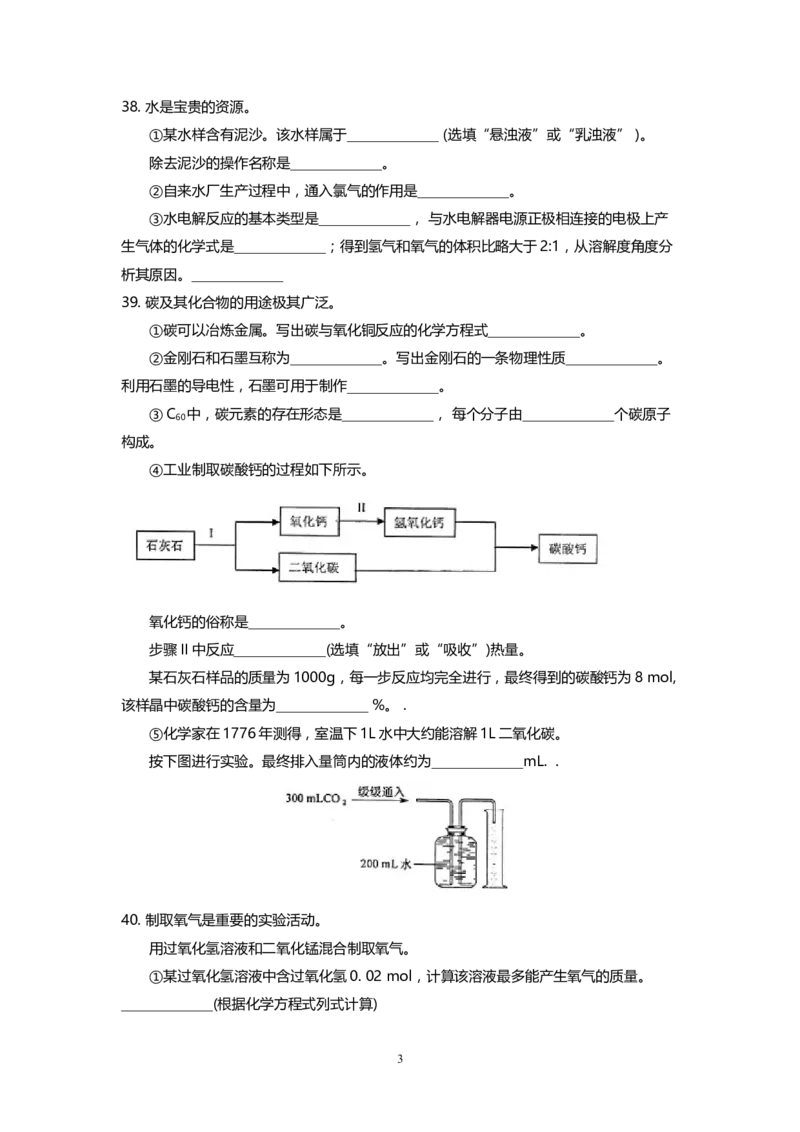
238. 水是宝贵的资源。
①某水样含有泥沙。该水样属于_____________ (选填“悬浊液”或“乳浊液” )。
除去泥沙的操作名称是_____________。
②自来水厂生产过程中,通入氯气的作用是_____________。
③水电解反应的基本类型是_____________, 与水电解器电源正极相连接的电极上产
生气体的化学式是_____________;得到氢气和氧气的体积比略大于2:1,从溶解度角度分
析其原因。_____________
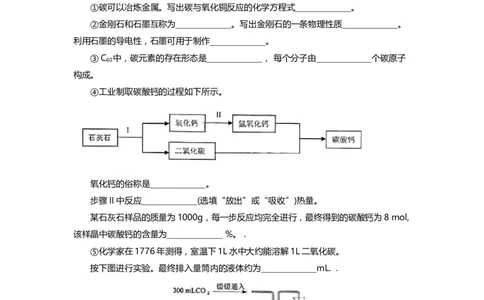
39. 碳及其化合物的用途极其广泛。
①碳可以冶炼金属。写出碳与氧化铜反应的化学方程式_____________。
②金刚石和石墨互称为_____________。写出金刚石的一条物理性质_____________。
利用石墨的导电性,石墨可用于制作_____________。
③C 中,碳元素的存在形态是_____________, 每个分子由_____________个碳原子
60
构成。
④工业制取碳酸钙的过程如下所示。
氧化钙的俗称是_____________。
步骤II中反应_____________(选填“放出”或“吸收”)热量。
某石灰石样品的质量为1000g,每一步反应均完全进行,最终得到的碳酸钙为8 mol,
该样晶中碳酸钙的含量为_____________ %。 .
⑤化学家在1776年测得,室温下1L水中大约能溶解1L二氧化碳。
按下图进行实验。最终排入量筒内的液体约为_____________mL. .
40. 制取氧气是重要的实验活动。
用过氧化氢溶液和二氧化锰混合制取氧气。
①某过氧化氢溶液中含过氧化氢0. 02 mol,计算该溶液最多能产生氧气的质量。
_____________(根据化学方程式列式计算)
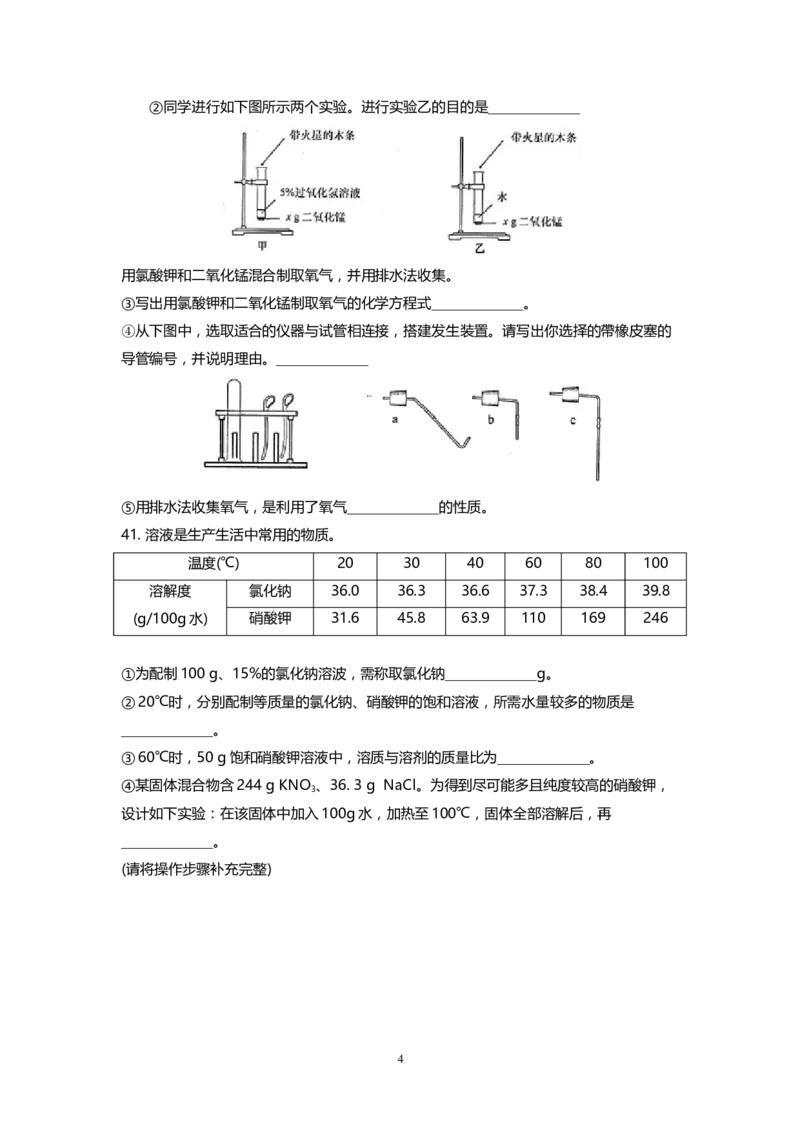
3②同学进行如下图所示两个实验。进行实验乙的目的是_____________
用氯酸钾和二氧化锰混合制取氧气,并用排水法收集。
③写出用氯酸钾和二氧化锰制取氧气的化学方程式_____________。
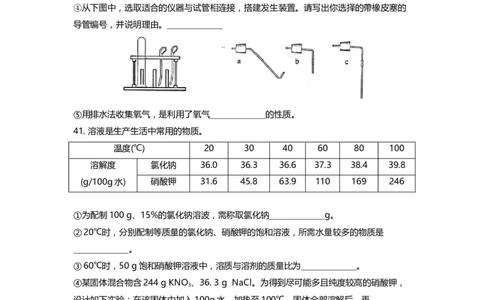
④从下图中,选取适合的仪器与试管相连接,搭建发生装置。请写出你选择的帶橡皮塞的
导管编号,并说明理由。_____________
⑤用排水法收集氧气,是利用了氧气_____________的性质。
41. 溶液是生产生活中常用的物质。
温度(℃) 20 30 40 60 80 100
溶解度 氯化钠 36.0 36.3 36.6 37.3 38.4 39.8
(g/100g水) 硝酸钾 31.6 45.8 63.9 110 169 246
①为配制100 g、15%的氯化钠溶波,需称取氯化钠_____________g。
②20℃时,分别配制等质量的氯化钠、硝酸钾的饱和溶液,所需水量较多的物质是
_____________。
③60℃时,50 g饱和硝酸钾溶液中,溶质与溶剂的质量比为_____________。
④某固体混合物含244 g KNO 、36. 3 g NaCl。为得到尽可能多且纯度较高的硝酸钾,
3
设计如下实验:在该固体中加入100g水,加热至100℃,固体全部溶解后,再
_____________。
(请将操作步骤补充完整)
4