文档内容
黄浦区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)答案解析版
2020.1
一、选择题
1.地壳中含量最多的金属元素是( )
A. Al B. O C. Si D. Fe
【答案】A
【解析】
【详解】地壳中元素含量居前四位的分别是氧、硅、铝、铁,氧元素和硅元素属于非金属
元素,氯元素和铁元素属于金属元素,所以地壳中含量最多的金属元素是铝元素,故选
A。
2.有新物质产生的物质变化是( )
A. 粮食发酵 B. 切割玻璃 C. 湿衣晒干 D. 粉碎废
纸
【答案】A
【解析】
【详解】A、粮食发酵有酒精等新的物质产生,正确;
B、切割玻璃只是改变了玻璃的形状,没有新的物质产生,错误;
C、湿衣晒干只是液态水转变为气态水,水的状态发生改变,没有新的物质产生,错误;
D、粉粹废纸只是改变了纸的形状,没有新的物质产生,错误。
故选A。
3.物质名称与化学式都正确的是( )
A. 氧化二氮:NO B. 碳酸:CO C. 碳酸氢铵:NH HCO D. 氯化钾:
2 3 4 3
KCl
2
【答案】C
【解析】
【详解】A、NO的名称是一氧化二氮,错误;
2
B、碳酸的化学式是HCO,错误;
2 3
C、碳酸氢铵的化学式是NH HCO ,正确;
4 3D、氯化钾的化学式是KCl,错误。
故选C。
4.液态水变成气态时体积膨胀,此过程中水分子发生的变化是( )
A. 体积增大 B. 质量增大 C. 个数最多 D. 间距增
大
【答案】D
【解析】
【详解】液态水变成气态时体积膨胀是因为温度升高,分子的间距增大,故选D。
5.按目前上海市生活垃圾分类标准,废弃的电器属于( )
A. 湿垃圾 B. 有害垃圾 C. 可回收物 D. 干垃圾
【答案】C
【解析】
【详解】废气的电器中的塑料外壳,金属配件等都是可回收物品,故废弃的电器属于可回
收物。
6.表示两个氢分子的符号是( )
A. 2HCl B. 2H C. H D. 2H
2 2
【答案】D
【解析】
【详解】A、2HCl表示两个氯化氢分子;
B、2H表示两个氢原子;
C、H 表示一个氢分子或者氢气;
2
D、2H 表示两个氢分子。故选D。
2
7.能在氧气中燃烧并生成黑色固体的物质是( )
A. 红磷 B. 木炭 C. 氢气 D. 铁丝
【答案】D
【解析】
【详解】A、红磷在氧气中燃烧生成五氧化二磷,五氧化二磷是白色固体,错误;
B、木炭在氧气中燃烧生成二氧化碳气体,错误;
C、氢气在氧气中燃烧生成水,错误;
D、铁丝在氧气中燃烧生成四氧化三铁黑色固体,正确。故选D。
8.干冰的用途是利用其化学性质的是( )
A. 人工降雨 B. 无水灭火 C. 保存食物 D. 舞台
“雾气缭绕”
【答案】B
【解析】
【详解】A、人工降雨是利用干冰升华吸热的原理,利用的是物理性质,错误;
B、干冰是固态二氧化碳,二氧化碳不支持燃烧,故干冰能灭火是利用了其不支持燃烧的
化学性质,正确;
C、干冰能保存食物是利用其升华吸收大量的热,使温度降低,用于保存食物,利用的是
物理性质,错误;
D、舞台“雾气缭绕”是利用干冰升华吸热导致周边空气冷凝成水蒸气形成雾气,利用的
是物理性质,错误。
故选B。
9.“火上浇油”可以使燃烧更剧烈,其主要原理是( )
A. 增加易燃物 B. 增大氧气浓度
C. 提高可燃物的着火点 D. 增大物质的接触面积
【答案】A
【解析】
【详解】油是易燃物,火上浇油增加了易燃物,使其燃烧的更剧烈,故选A。
【点睛】着火点是物质的特性,基本上不会改变。
10.在常温下,向 pH=3 的苹果汁中不断地加水,则该苹果汁的 pH 变化情况正确的是
( )
A. 不断变小 B. 一直变大 C. 可能等于 6 D. 可能等
于 8
【答案】C
【解析】
【详解】向 pH=3 的苹果汁中不断地加水,氢离子的浓度不断减小,pH不断增大,但是苹
果汁还是酸性的,不可能超过7成为碱性,故pH可能等于6。故选C。11.放入水中不能形成溶液 的物质是( )
A. 面粉 B. 味精 C. 蔗糖 D. 酒精
【答案】A
【解析】
【详解】A、面粉放入水中形成不均一、不稳定的悬浊液,符合题意;
B、味精溶于水能形成均一、稳定的溶液,不符合题意;
C、蔗糖溶于水能形成均一、稳定的溶液,不符合题意;
D、酒精溶于水能形成均一、稳定的溶液,不符合题意。
故选A 。
12.镁带在氧气中燃烧化学方程式书写正确的是( )
A. Mg+O MgO B. 2Mg+CO 2MgO+C
2 2 2
C. 2Mg+O↑ 2MgO D. 2Mg+O 2MgO
2 2
【答案】D
【解析】
【分析】
镁带在氧气中燃烧生成氧化镁:MgO。
【详解】A、氧化镁的化学式是MgO,不是MgO ,书写错误;
2
B、镁带在氧气中燃烧生成氧化镁,没有C,书写错误;
C、氧气在反应物中,不能带气体符号,书写错误;
D、镁条在氧气中燃烧生成氧化镁,书写正确。
故选D。
13.根据化学方程式 S+O SO ,无法获得的信息是( )
2 2
A. 反应前后反应物和生成物的种类 B. 参加反应硫和二氧化硫的质量比
C. 化学反应速率的快慢程度 D. 反应发生所需要的条件
【答案】C
【解析】【详解】A、根据化学方程式可以获知反应物为硫和氧气,生成物为二氧化硫,不符合题
意;
B、根据化学方程式可以获知参加反应的硫和二氧化硫的质量比为1:2,不符合题意;
C、根据化学方程式不可以获知化学反应速率的快慢程度,符合题意;
D、根据化学方程式可以获知参加反应的条件是点燃,不符合题意。
故选C。
14.对“混合物”理解错误的是( )
A. 一定由多种物质组成 B. 一定有多种分子组成
C. 可能由一种元素组成 D. 可能由多种原子组成
【答案】B
【解析】
【详解】A、由多种物质组成的物质称为混合物,故混合物一定由多种物质组成,正确;
B、混合物可能由分子组成,也可能由原子组成等等,不一定由多种分子组成,错误;
C、混合物可能由一种元素组成,例如金刚石和石墨组成的混合物只有碳元素,正确;
D、混合物可能由多种原子组成,例如金刚石和晶体硅的混合物,正确。
故选B。
15.检验一瓶二氧化碳气体中是否混有少量一氧化碳,正确操作方法是( )
A. 点燃气体,观察气体是否燃烧
B. 通入灼热的氧化铜,观察固体颜色是否变化
C. 闻气体的气味,是否闻到有特殊气味
D. 倒入少量澄清的石灰水,观察溶液是否变浑浊
【答案】B
【解析】
【详解】A、二氧化碳不支持燃烧,故只含有少量一氧化碳的二氧化碳气体是无法燃烧的,
无法鉴别,错误;
B、通入灼热的氧化铜,如果混有一氧化碳,黑色的氧化铜会被还原成红色的铜,故可以
鉴别,正确;
C、二氧化碳和一氧化碳都是无色无味的气体,无法鉴别,况且一氧化碳有毒,最好别闻,
错误;
D、二氧化碳可以和澄清石灰水反应,一氧化碳不能和澄清石灰水反应,故无法确定是否有一氧化碳,错误。
故选B。
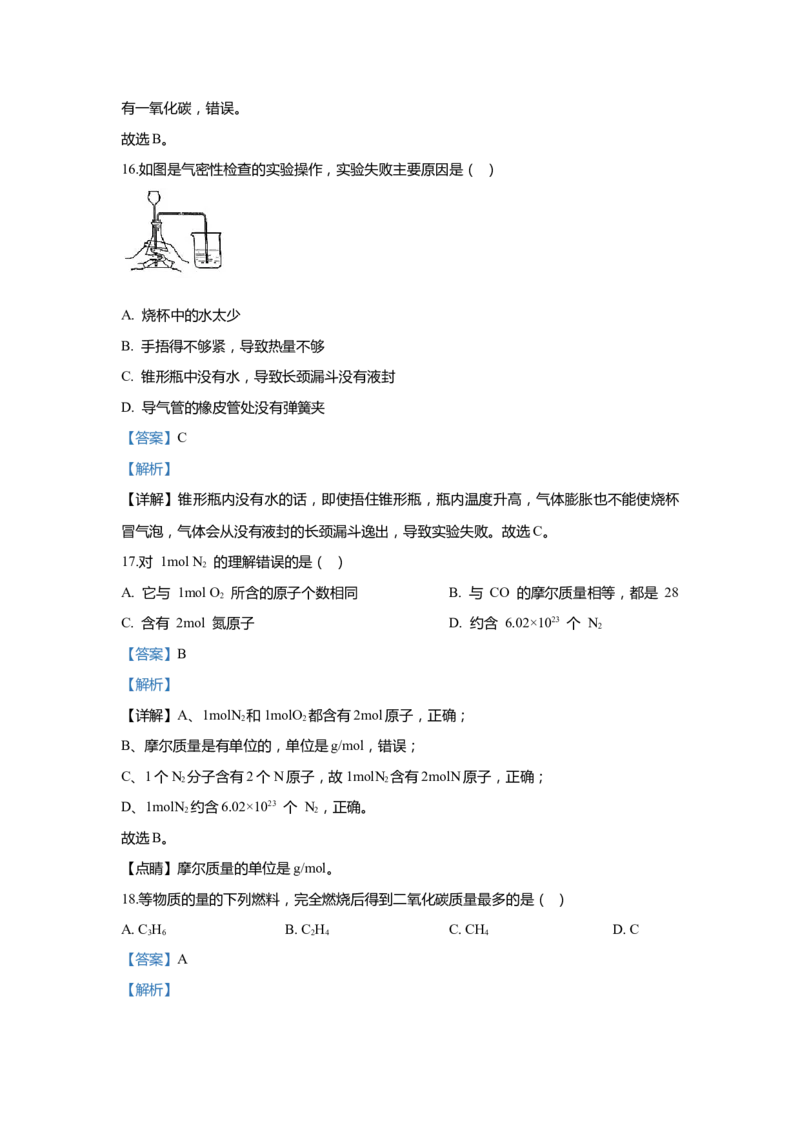
16.如图是气密性检查的实验操作,实验失败主要原因是( )
A. 烧杯中的水太少
B. 手捂得不够紧,导致热量不够
C. 锥形瓶中没有水,导致长颈漏斗没有液封
D. 导气管的橡皮管处没有弹簧夹
【答案】C
【解析】
【详解】锥形瓶内没有水的话,即使捂住锥形瓶,瓶内温度升高,气体膨胀也不能使烧杯
冒气泡,气体会从没有液封的长颈漏斗逸出,导致实验失败。故选C。
17.对 1mol N 的理解错误的是( )
2
A. 它与 1mol O 所含的原子个数相同 B. 与 CO 的摩尔质量相等,都是 28
2
C. 含有 2mol 氮原子 D. 约含 6.02×1023 个 N
2
【答案】B
【解析】
【详解】A、1molN 和1molO 都含有2mol原子,正确;
2 2
B、摩尔质量是有单位的,单位是g/mol,错误;
C、1个N 分子含有2个N原子,故1molN 含有2molN原子,正确;
2 2
D、1molN 约含6.02×1023 个 N,正确。
2 2
故选B。
【点睛】摩尔质量的单位是g/mol。
18.等物质的量的下列燃料,完全燃烧后得到二氧化碳质量最多的是( )
A. C H B. C H C. CH D. C
3 6 2 4 4
【答案】A
【解析】【详解】A、C H 燃烧的化学方程式为 ;C H 与CO 的关
3 6 3 6 2
系式为1:3,即1mol C H 生成3mol CO;
3 6 2
B、同理C H 与CO 的关系式为1:2,即1mol C H 生成2mol CO;
2 4 2 2 4 2
C、同理CH 与CO 的关系式为1:1,即1molCH 生成1molCO ;
4 2 4 2
D、同理C与CO 的关系式为1:1,即1molC生成1molCO 。
2 2
故C H 燃烧生成的CO 质量最大,故选A。
3 6 2
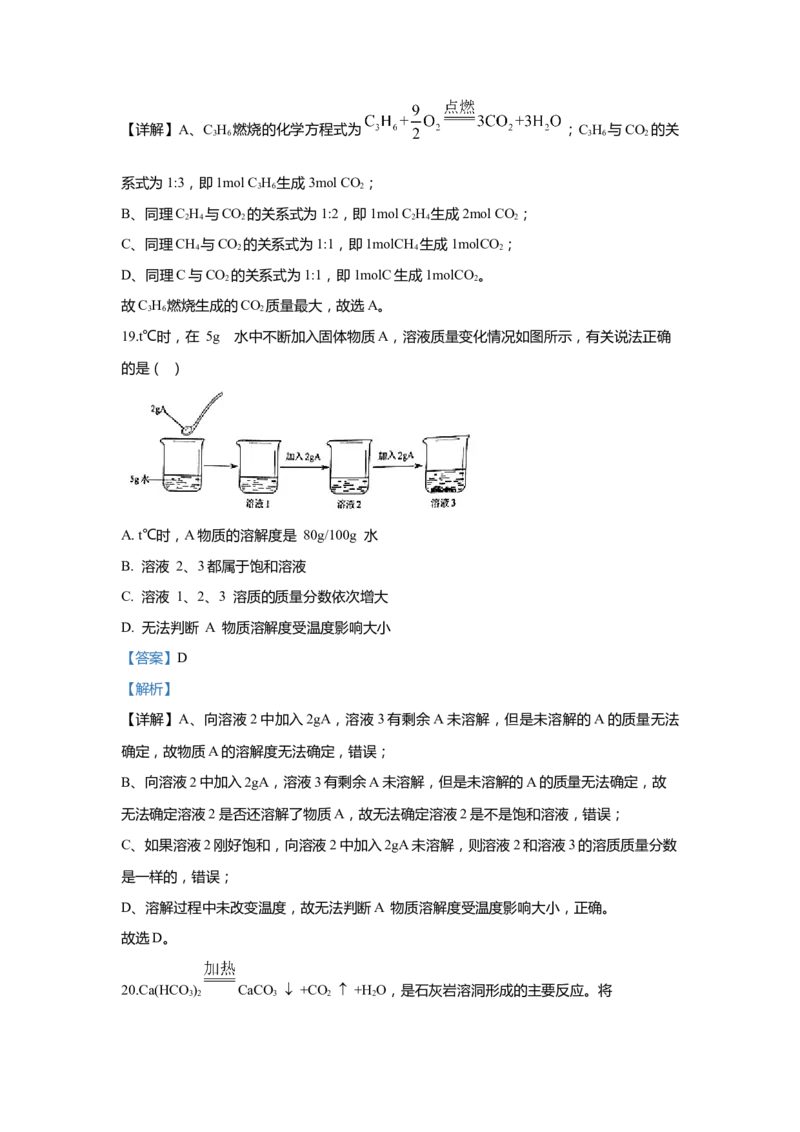
19.t℃时,在 5g 水中不断加入固体物质A,溶液质量变化情况如图所示,有关说法正确
的是( )
A. t℃时,A物质的溶解度是 80g/100g 水
B. 溶液 2、3都属于饱和溶液
C. 溶液 1、2、3 溶质的质量分数依次增大
D. 无法判断 A 物质溶解度受温度影响大小
【答案】D
【解析】
【详解】A、向溶液2中加入2gA,溶液3有剩余A未溶解,但是未溶解的A的质量无法
确定,故物质A的溶解度无法确定,错误;
B、向溶液2中加入2gA,溶液3有剩余A未溶解,但是未溶解的A的质量无法确定,故
无法确定溶液2是否还溶解了物质A,故无法确定溶液2是不是饱和溶液,错误;
C、如果溶液2刚好饱和,向溶液2中加入2gA未溶解,则溶液2和溶液3的溶质质量分数
是一样的,错误;
D、溶解过程中未改变温度,故无法判断A 物质溶解度受温度影响大小,正确。
故选D。
20.Ca(HCO ) CaCO +CO +H O,是石灰岩溶洞形成的主要反应。将
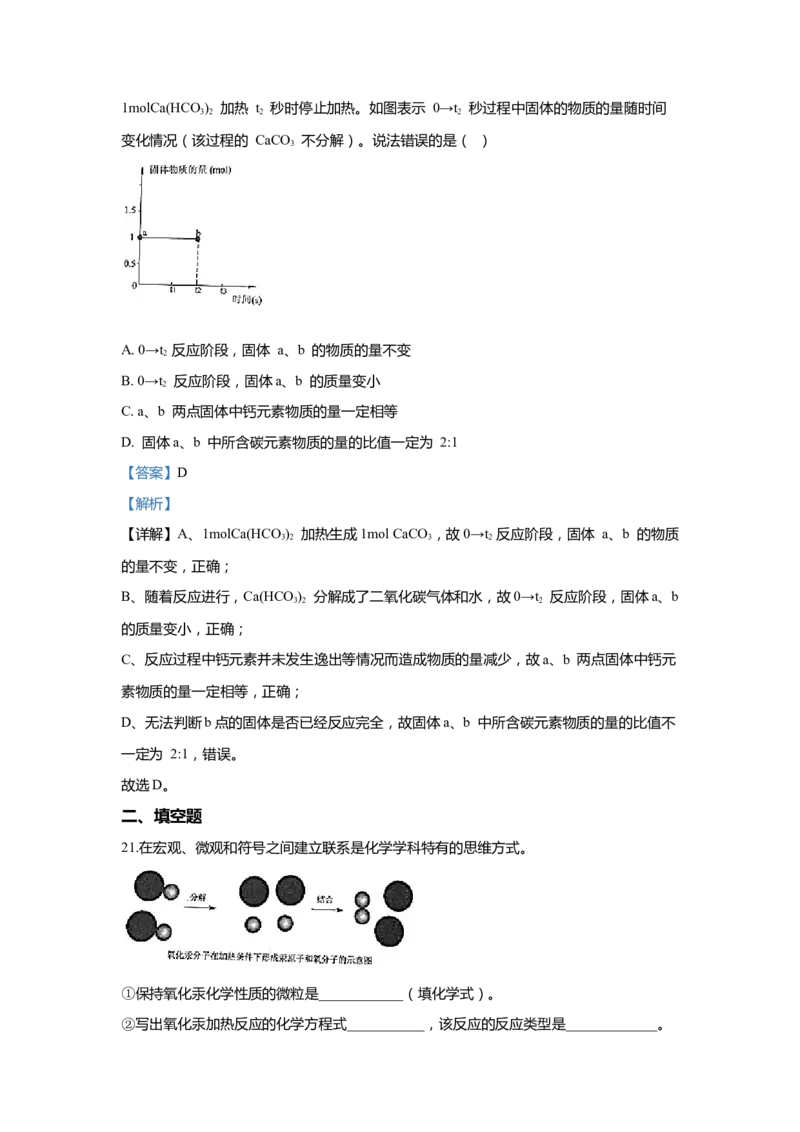
3 2 3 2 21molCa(HCO ) 加热 t 秒时停止加热。如图表示 0→t 秒过程中固体的物质的量随时间
3 2 2 2
变化情况(该过程的 CaCO 不分解)。说法错误的是( )
3
A. 0→t 反应阶段,固体 a、b 的物质的量不变
2
B. 0→t 反应阶段,固体a、b 的质量变小
2
C. a、b 两点固体中钙元素物质的量一定相等
D. 固体a、b 中所含碳元素物质的量的比值一定为 2:1
【答案】D
【解析】
【详解】A、1molCa(HCO ) 加热生成1mol CaCO ,故0→t 反应阶段,固体 a、b 的物质
3 2 3 2
的量不变,正确;
B、随着反应进行,Ca(HCO ) 分解成了二氧化碳气体和水,故0→t 反应阶段,固体a、b
3 2 2
的质量变小,正确;
C、反应过程中钙元素并未发生逸出等情况而造成物质的量减少,故a、b 两点固体中钙元
素物质的量一定相等,正确;
D、无法判断b点的固体是否已经反应完全,故固体a、b 中所含碳元素物质的量的比值不
一定为 2:1,错误。
故选D。
二、填空题
21.在宏观、微观和符号之间建立联系是化学学科特有的思维方式。
①保持氧化汞化学性质的微粒是____________(填化学式)。
②写出氧化汞加热反应的化学方程式___________,该反应的反应类型是_____________。③对微粒示意图的理解错误的是________________。
A 每二个氧原子可以构成一个氧分子
B 原子可以直接构成物质
C 反应前后氧、汞元素存在形态都发生变化
D 反应过程中氧元素的化合价降低为 0 价
E 反应前后分子种类不变
【答案】 (1). HgO (2). 2HgO Hg+O (3). 分解反应 (4). DE
2
【解析】
【详解】①保持氧化汞化学性质的微粒是氧化汞分子,化学式为HgO;
②氧化汞加热生成汞单质和氧气,反应的化学方程式2HgO Hg+O ;
2
该反应符合“一变多”的特征,属于分解反应;
③A、每二个氧原子可以构成一个氧分子,正确;
B、原子可以直接构成物质,例如石墨是由C原子构成的,正确;
C、反应前后氧、汞元素存在形态都发生变化,正确;
D、反应过程中氧元素的化合价升高为 0 价,错误;
E、反应前只有氧化汞分子,反应后只有氧分子,分子种类发生变化,错误。
故选D、E。
22.果糖(C H O)大量存在于水果中。每个 C H O 是由________个原子构成。它在体
6 12 6 6 12 6
内代谢的化学方程式为:C H O+6O 6X+6HO,该反应生成物 X表示的物质是
6 12 6 2 2
_______。1mol 果糖分子中碳原子的质量与______________g 蔗糖(C H O )中碳原子
12 22 11
质量相同。
【答案】 (1). 24 (2). 二氧化碳(CO) (3). 171
2
【解析】
【详解】每个 C H O 是由6+12+6=24个原子构成的;
6 12 6果糖在体内代谢的化学方程式为:C H O+6O 6X+6HO,根据质量守恒定律,反应前
6 12 6 2 2
有6个C原子,12个H原子和18个O原子,反应后有12个H原子和6个O原子和6X,
故6X中含有6个C原子和12个O原子,故一个X中含有1个C原子和2个O原子,故X
表示CO;
2
1mol 果糖分子中含有6molC原子,1mol蔗糖(C H O )分子中含有12molC原子,故
12 22 11
1mol中C原子 的质量与0.5mol蔗糖中C原子质量相同,故蔗糖的质量为
0.5mol×(12×12g/mol+22×1 g/mol +11×16 g/mol)=171g。
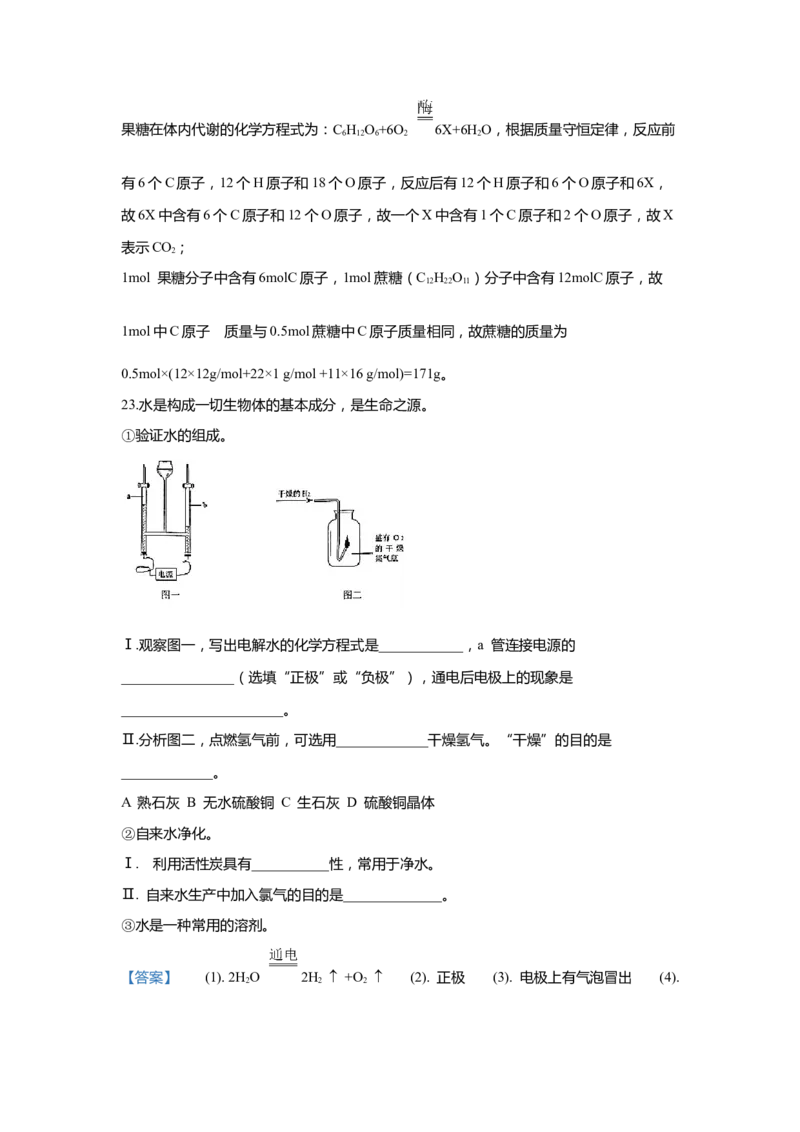
23.水是构成一切生物体的基本成分,是生命之源。
①验证水的组成。
Ⅰ.观察图一,写出电解水的化学方程式是____________,a 管连接电源的
________________(选填“正极”或“负极”),通电后电极上的现象是
_______________________。
Ⅱ.分析图二,点燃氢气前,可选用_____________干燥氢气。“干燥”的目的是
_____________。
A 熟石灰 B 无水硫酸铜 C 生石灰 D 硫酸铜晶体
②自来水净化。
Ⅰ. 利用活性炭具有___________性,常用于净水。
Ⅱ. 自来水生产中加入氯气的目的是______________。
③水是一种常用的溶剂。
【答案】 (1). 2H O 2H +O (2). 正极 (3). 电极上有气泡冒出 (4).
2 2 2BC (5). 除去氢气中的水,防止对氢气燃烧后的产物水的干扰 (6). 吸附 (7). 杀
菌消毒
【解析】
【详解】①水电解产生氢气和氧气,反应的化学方程式为2HO 2H +O ;
2 2 2
A管产生的是氧气,故a管连接电源的正极;
通电后电极上的现象是电极上有气泡冒出;
点燃氢气前,可选用无水硫酸铜和生石灰作为氢气的干燥剂,故选BC;
“干燥”的目的是除去氢气中的水,防止对氢气燃烧后的产物水的干扰;
②活性炭常用于净水是利用活性炭的吸附性;
自来水生产中加入氯气的目的是利用氯气与水反应生成次氯酸,有着杀菌消毒的作用。
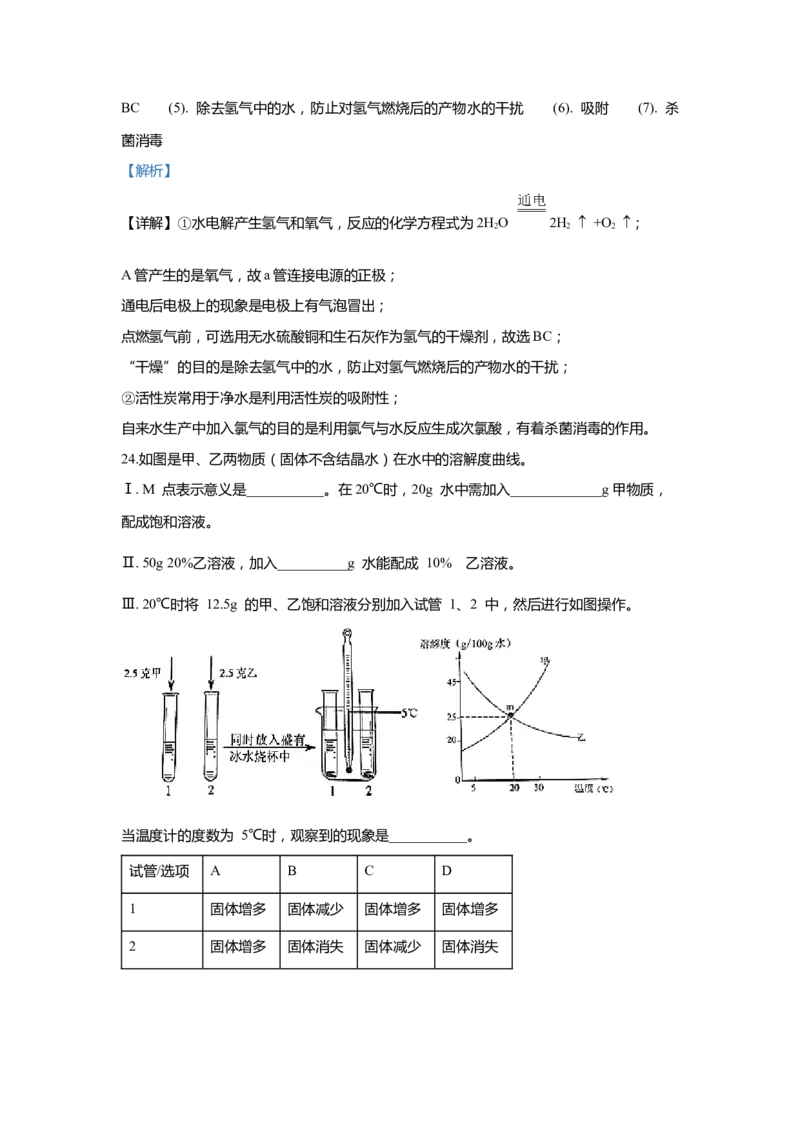
24.如图是甲、乙两物质(固体不含结晶水)在水中的溶解度曲线。
Ⅰ. M 点表示意义是___________。在20℃时,20g 水中需加入_____________g甲物质,
配成饱和溶液。
Ⅱ. 50g 20%乙溶液,加入__________g 水能配成 10% 的乙溶液。
Ⅲ. 20℃时将 12.5g 的甲、乙饱和溶液分别加入试管 1、2 中,然后进行如图操作。
当温度计的度数为 5℃时,观察到的现象是___________。
试管/选项 A B C D
1 固体增多 固体减少 固体增多 固体增多
2 固体增多 固体消失 固体减少 固体消失【答案】 (1). 20℃时,甲和乙的溶解度相等,均为 25g/100g 水 (2). 5 (3). 50
(4). C
【解析】
【详解】Ⅰ、m点是甲乙两条溶解度曲线的交点,表示20℃时,甲和乙的溶解度相等,均
为 25g/100g 水;
20℃时,甲物质的溶解度为25g/100g 水,故20g水中需要加入 甲物质才能配成饱
和溶液;
Ⅱ、设需加入水的质量为xg,计算过程如下: ,解得x=50g,
故需加入50g水;
Ⅲ、当温度计的度数为 5℃时,甲的溶解度减小,乙的溶解度增大,故试管1固体增多,
试管2固体减少,故选C。
三、简答题
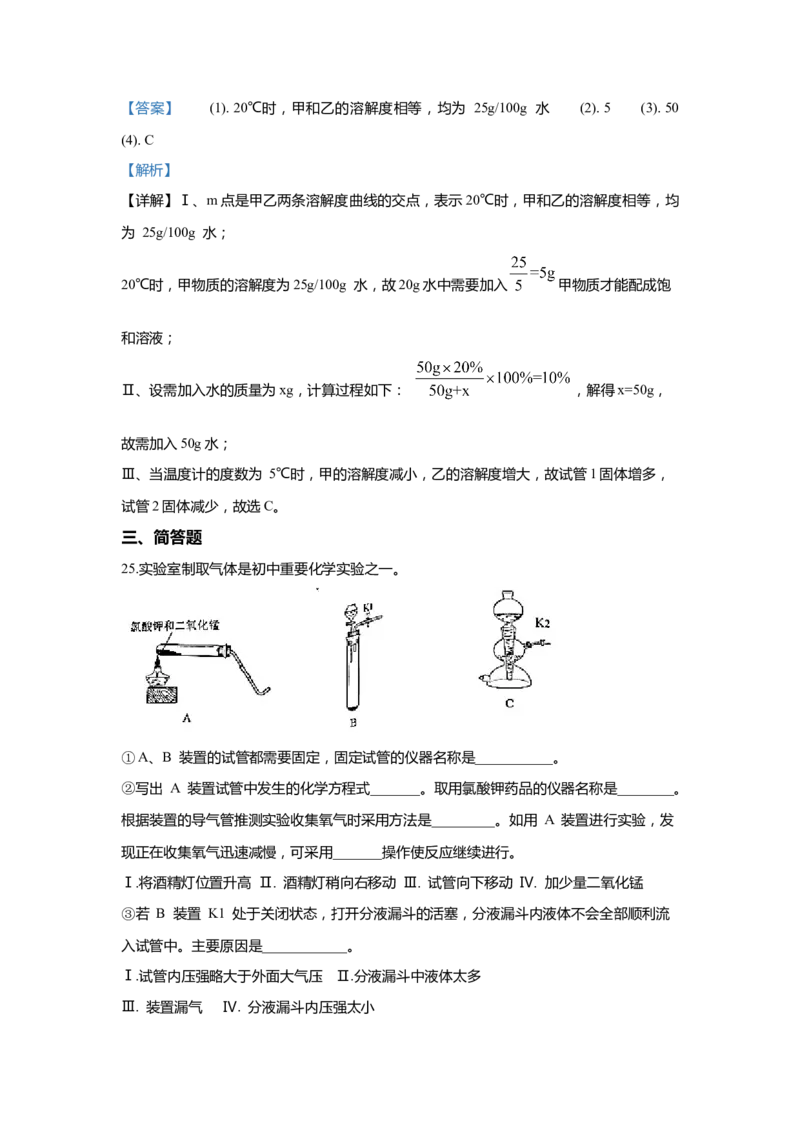
25.实验室制取气体是初中重要化学实验之一。
①A、B 装置的试管都需要固定,固定试管的仪器名称是___________。
②写出 A 装置试管中发生的化学方程式_______。取用氯酸钾药品的仪器名称是________。
根据装置的导气管推测实验收集氧气时采用方法是_________。如用 A 装置进行实验,发
现正在收集氧气迅速减慢,可采用_______操作使反应继续进行。
Ⅰ.将酒精灯位置升高 Ⅱ. 酒精灯稍向右移动 Ⅲ. 试管向下移动 Ⅳ. 加少量二氧化锰
③若 B 装置 K1 处于关闭状态,打开分液漏斗的活塞,分液漏斗内液体不会全部顺利流
入试管中。主要原因是____________。
Ⅰ.试管内压强略大于外面大气压 Ⅱ.分液漏斗中液体太多
Ⅲ. 装置漏气 Ⅳ. 分液漏斗内压强太小④B、C 装置都可用于实验室制二氧化碳,理由是_______。观察 C 装置,判断该装置正
处于_________反应(选填“正在”或“停止”)。使用 C 装置制取气体的优点是
________。
⑤把 2g 含 80%碳酸钙的大理石放入 14.6g 过量的盐酸中完全反应,理论上可生成
__________mol 二氧化碳(根据化学方程式列式计算)。
【答案】 (1). 铁架台 (2). 2KClO 2KCl+3O (3). 药匙(纸槽)
3 2
(4). 排水法 (5). Ⅱ (6). Ⅰ (7). 都适用于固体和液体在常温下发生反应制取气体
(8). 停止 (9). 随开随用,随关随停(或随时控制反应的发生和停止) (10). 0.016
【解析】
【详解】①固定试管的仪器名称是铁架台;
②氯酸钾在二氧化锰催化下加热生成氯化钾和氧气,反应的化学方程式为2KClO
3
2KCl+3O ;
2
取用氯酸钾药品 的仪器名称是药匙(纸槽);
根据装置的导气管推测实验收集氧气时采用方法是排水法;
如用 A 装置进行实验,发现正在收集氧气迅速减慢,可采用将酒精灯向右移的操作使反
应继续进行,故选Ⅱ;
③若 B 装置 K1 处于关闭状态,打开分液漏斗的活塞,分液漏斗内液体不会全部顺利流
入试管中。主要原因是随着反应的进行,产生的气体越来越多,当试管内压强略大于外面
大气压时,分液漏斗内液体就不会下流,故选Ⅰ;
④B、C 装置都可用于实验室制二氧化碳,理由是都适用于固体和液体在常温下发生反应
制取气体;
观察 C 装置,判断该装置正处于停止状态;
使用 C 装置制取气体的优点是随开随用,随关随停(或随时控制反应的发生和停止);
⑤把 2g 含 80%碳酸钙的大理石放入 14.6g 过量的盐酸中完全反应,设产生的二氧化碳
质量为xg,计算过程如下:,解得x=0.704g,
CO 的摩尔质量为44g/mol,故生成的CO 的物质的量为 。
2 2
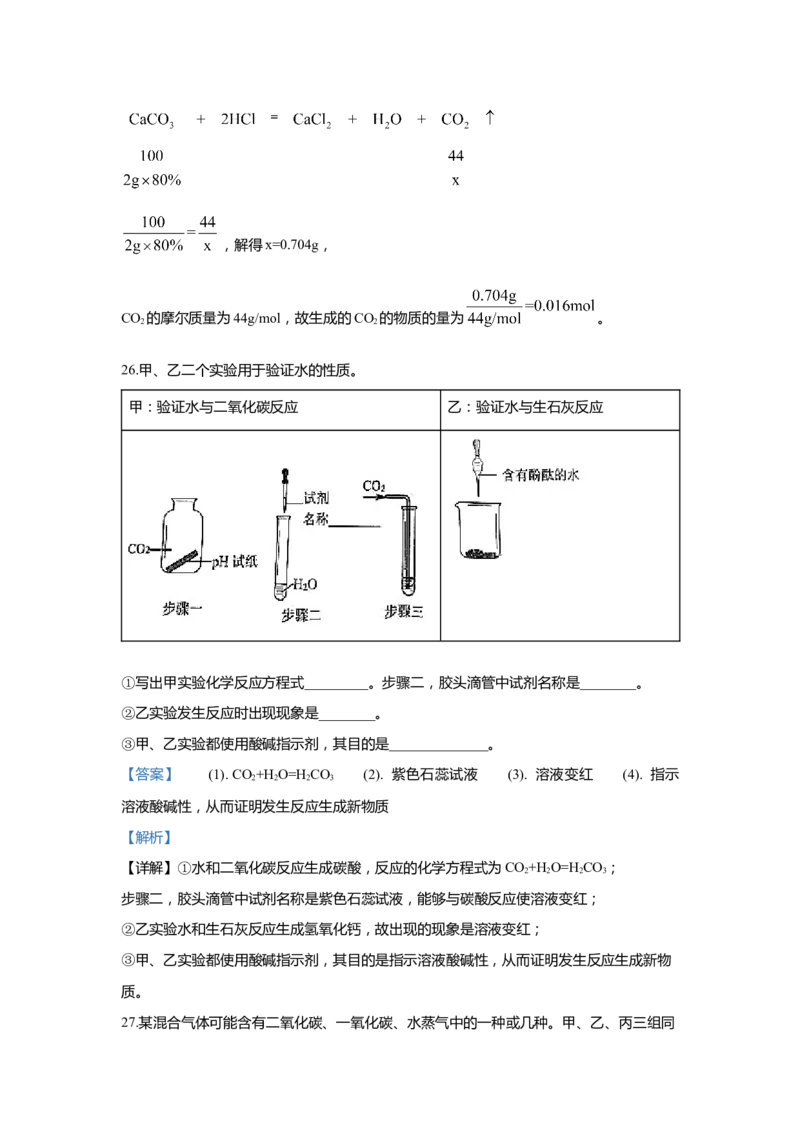
26.甲、乙二个实验用于验证水的性质。
甲:验证水与二氧化碳反应 乙:验证水与生石灰反应
①写出甲实验化学反应方程式_________。步骤二,胶头滴管中试剂名称是________。
②乙实验发生反应时出现现象是________。
③甲、乙实验都使用酸碱指示剂,其目的是______________。
【答案】 (1). CO +H O=HCO (2). 紫色石蕊试液 (3). 溶液变红 (4). 指示
2 2 2 3
溶液酸碱性,从而证明发生反应生成新物质
【解析】
【详解】①水和二氧化碳反应生成碳酸,反应的化学方程式为CO+H O=HCO;
2 2 2 3
步骤二,胶头滴管中试剂名称是紫色石蕊试液,能够与碳酸反应使溶液变红;
②乙实验水和生石灰反应生成氢氧化钙,故出现的现象是溶液变红;
③甲、乙实验都使用酸碱指示剂,其目的是指示溶液酸碱性,从而证明发生反应生成新物
质。
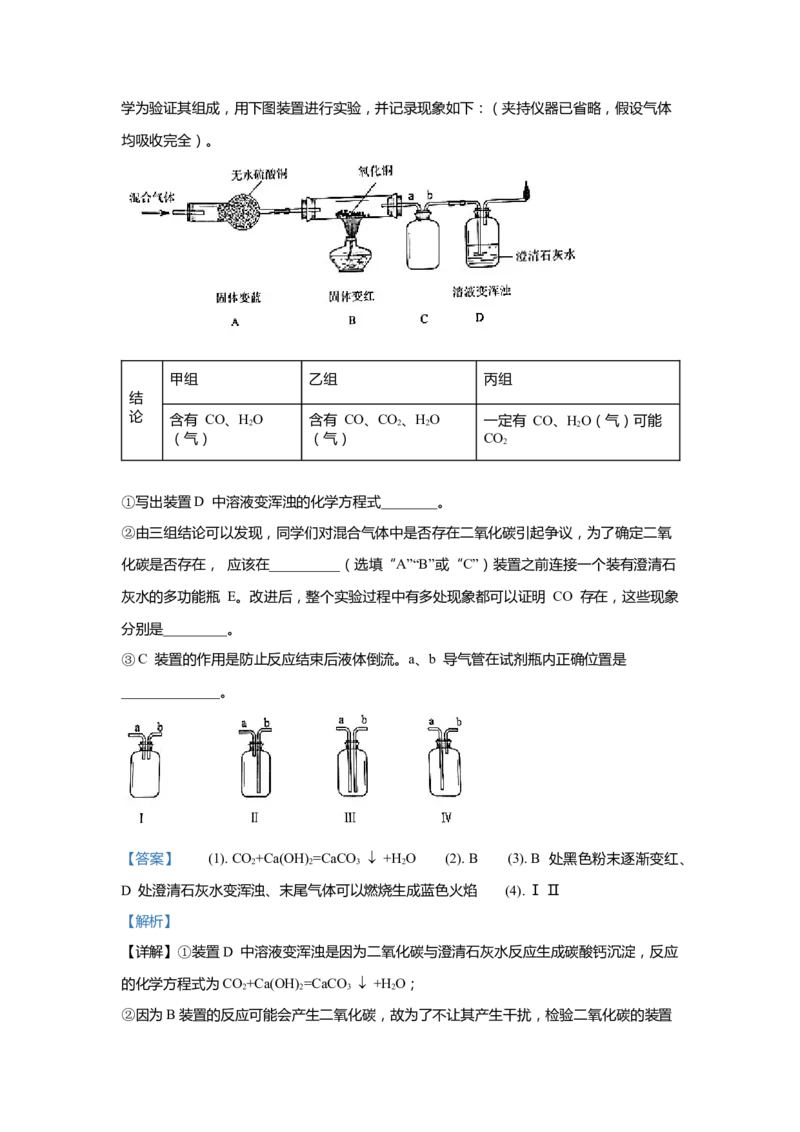
27.某混合气体可能含有二氧化碳、一氧化碳、水蒸气中的一种或几种。甲、乙、丙三组同学为验证其组成,用下图装置进行实验,并记录现象如下:(夹持仪器已省略,假设气体
均吸收完全)。
甲组 乙组 丙组
结
论 含有 CO、H 2 O 含有 CO、CO 2 、H 2 O 一定有 CO、H 2 O(气)可能
(气) (气) CO
2
①写出装置D 中溶液变浑浊的化学方程式________。
②由三组结论可以发现,同学们对混合气体中是否存在二氧化碳引起争议,为了确定二氧
化碳是否存在, 应该在__________(选填“A”“B”或“C”)装置之前连接一个装有澄清石
灰水的多功能瓶 E。改进后,整个实验过程中有多处现象都可以证明 CO 存在,这些现象
分别是_________。
③C 装置的作用是防止反应结束后液体倒流。a、b 导气管在试剂瓶内正确位置是
______________。
【答案】 (1). CO +Ca(OH) =CaCO +H O (2). B (3). B 处黑色粉末逐渐变红、
2 2 3 2
D 处澄清石灰水变浑浊、末尾气体可以燃烧生成蓝色火焰 (4). Ⅰ Ⅱ
【解析】
【详解】①装置D 中溶液变浑浊是因为二氧化碳与澄清石灰水反应生成碳酸钙沉淀,反应
的化学方程式为CO+Ca(OH) =CaCO +H O;
2 2 3 2
②因为B装置的反应可能会产生二氧化碳,故为了不让其产生干扰,检验二氧化碳的装置应该放在B装置之前;
改进后,整个实验过程中有多处现象都可以证明 CO 存在,这些现象分别是B 处黑色粉
末逐渐变红、D 处澄清石灰水变浑浊、末尾气体可以燃烧生成蓝色火焰;
③C 装置的作用是防止反应结束后液体倒流,则a导气管必须短一点,b导气管可短可长,
故选Ⅰ 、Ⅱ。