文档内容
九年级化学学科练习
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40 Cu-64
一、选择题(共35分)1-25题只有一个正确选项
1. 氯元素的符号是
A. cl B. CL C. Cl D. cL
【答案】C
【解析】
【详解】由两个字母表示的元素符号,第二个字母必须小写,所以氯元素的符号是:Cl,故选C。
2. NO中氮元素的化合价是( )
A. +4 B. +1 C. +3 D. +2
【答案】D
【解析】
【详解】氧元素一般显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+
(-2)=0,则x=+2价。
故选D。
3. 属于氧气化学性质的是
A. 能变成液氧 B. 能支持燃烧
C. 密度比空气大 D. 常温常压下是无色气体
【答案】B
【解析】
【详解】A、氧气能变成液氧,这是氧气的物理性质,不需要发生化学反应就能变现出来,故A不符合题
意;
B、氧气能支持燃烧,需要通过化学变化表现出来,故B符合题意;
C、氧气密度比空气大,这是氧气的物理性质,不需要发生化学反应就能变现出来,故C不符合题意;
D、氧气常温常压下是无色气体,这是氧气的物理性质,不需要发生化学反应就能变现出来,故D不符合
题意;
故应选B。
4. 空气中体积分数最大的气体是
A. 氮气 B. 氧气 C. 二氧化碳 D. 氦气
【答案】A
【解析】
【详解】空气中体积分数最大的气体是氮气,占空气总体积的78%,其次是氧气为21%,二氧化碳为
第1页/共19页
学科网(北京)股份有限公司0.03%,稀有气体为0.94%。
故选A。
5. 物质在氧气中燃烧产生白烟的是
A. 硫 B. 木炭 C. 铁丝 D. 红磷
【答案】D
【解析】
【详解】A、硫在氧气中燃烧,产生蓝紫色火焰,生成有刺激性气味的气体,不符合题意;
B、木炭在氧气中燃烧,发出白光,产生能使澄清石灰水变浑浊的气体,不符合题意;
C、铁丝在氧气中燃烧,火星四射,生成黑色固体,不符合题意;
D、红磷在空气中燃烧,产生大量白烟,符合题意;
故选D。
6. 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指( )
A. 原子 B. 分子 C. 元素 D. 单质
【答案】C
【解析】
【详解】豆类、动物肝脏中含有丰富的“铁和锌”不是以单质、分子、原子等形式存在,这里所指的“铁
和锌”是强调存在的元素,与具体形态无关。故选C。
7. 物质的用途错误的是
A. 稀有气体制作电光源 B. 二氧化碳制作碳酸饮料
C. 氢气作燃料 D. 碳酸钙作干燥剂
【答案】D
【解析】
【详解】A、稀有气体通电时能发出不同颜色的光,则可制作电光源,该选项用途正确;
B、二氧化碳能与水反应生成碳酸,则可制作碳酸饮料,该选项用途正确;
C、氢气具有可燃性,可作燃料,该选项用途正确;
D、碳酸钙含有钙元素可用于补钙剂,但不具有吸水性不能作干燥剂,该选项用途不正确。
故选D。
8. 水果散发出诱人的香味,你能闻到香味的原因是( )
A. 分子的体积很小
B. 分子在不断运动
C. 分子之间有间隔
D. 分子的质量很小
【答案】B
第2页/共19页
学科网(北京)股份有限公司【解析】
【详解】由于分子是运动的,水果香味的分子通过运动能分散到周围的空气中,所以能闻到水果散发出诱
人的香味。与分子体积、质量的大小,分子间的间隔等无关。故选B。
9. 以下化学方程式书写正确的是
A. B.
C. D.
【答案】D
【解析】
【详解】硫在氧气中燃烧生成二氧化硫,反应的化学方程式为 ;
故选D。
10. 与酸雨形成有关的气体是( )
A. 二氧化硫 B. 一氧化碳 C. 二氧化碳 D. 氢气
【答案】A
【解析】
【详解】A、二氧化硫是形成酸雨的主要气体,二氧化硫与雨水、氧气反应生成硫酸,符合题意;
B、一氧化碳难溶于水,不能形成酸雨,不符合题意;
C、二氧化碳溶于水生成碳酸,为弱酸,不形成酸雨,不符合题意;
D、氢气难溶于水,不能形成酸雨,不符合题意。
故选:A。
11. 表示化合物的是
A. 蒸馏水 B. 氢气 C. 稀有气体 D. C
60
【答案】A
【解析】
【详解】A、蒸馏水只含一种物质水,是纯净物,由氢、氧元素组成,是化合物;
B、氢气是一种物质,是纯净物,只含有氢元素,是单质;
C、稀有气体是氦氖氩氪氙氡等气体的统称,含多种物质,是混合物;
D、C 是一种物质,是纯净物,只含碳元素,是单质;
60
故选A。
12. 不属于同素异形体的一组物质是
第3页/共19页
学科网(北京)股份有限公司A. 一氧化碳与二氧化碳 B. 金刚石、石墨
C. 红磷和白磷 D. 氧气和臭氧
【答案】A
【解析】
【详解】A、一氧化碳、二氧化碳均是化合物,不是单质,不属于同素异形体,符合题意;
B、金刚石与石墨是由碳元素形成的不同单质,互为同素异形体,不符合题意;
C、红磷与白磷是由磷元素形成的不同单质,互为同素异形体,不符合题意;
D、氧气和臭氧是由氧元素形成的不同单质,互为同素异形体,不符合题意;
故选:A。
13. 不能形成溶液的一组物质是
A. 酒精和碘 B. 二氧化碳和水 C. 泥土和水 D. 食盐和水
【答案】C
【解析】
【详解】A、碘溶于酒精,形成均一、稳定的混合物,属于溶液,故选项A不符合题意;
B、二氧化碳和水反应生成碳酸,形成均一、稳定的混合物,属于溶液,故选项B不符合题意;
C、泥土不溶于水,与水混合形成不均一、不稳定的悬浊液,故选项C符合题意;
D、食盐溶于水,形成均一、稳定的混合物,属于溶液,故选项D不符合题意;
故选:C。
14. 下列说法中正确的是
A. 二氧化碳由一个碳元素和两个氧元素组成 B. 二氧化碳由碳、氧两种元素组成
C. 二氧化碳由碳、氧两种单质组成 D. 二氧化碳分子由碳原子和氧分子构成
【答案】B
【解析】
【详解】A、二氧化碳由碳元素和氧元素组成,元素只讲种类,不讲个数;故选项错误;
B、二氧化碳由碳、氧两种元素组成;故选项正确;
C、二氧化碳分子由碳原子和氧原子构成的;故选项错误;
D、一个二氧化碳分子由一个碳原子和两个氧原子构成;故选项错误;
故选B。
15. 物质的量的符号是
A. n B. mol C. M D. g/mol
【答案】A
【解析】
【详解】物质的量的符号是n,单位是mol,M为摩尔质量,单位为g/mol,表示物质的量的符号是n,故
第4页/共19页
学科网(北京)股份有限公司选A。
16. 有关电解水实验的说法,错误的是
A. 可以证明水由氢元素和氧元素组成
B. 正、负极产生的气体体积比是1:2
C. 用带火星木条检验产生的氧气
D. 证明水分子由一个氢分子和一个氧原子构成
【答案】D
【解析】
【详解】A、电解水生成氢气和氧气,氢气是由氢元素组成,氧气是由氧元素组成,根据元素守恒,水是
由氢、氧元素组成,该选项说法正确;
B、电解水时,正极产生氧气,负极产生氧气,且产生的氧气和氢气的体积比为1:2,则正、负极产生的
气体体积比是1:2,该选项说法正确;
C、氧气能使带火星的木条复燃,则可用带火星木条检验产生的氧气,该选项说法正确;
D、分子是由原子构成的,分子中不含分子,即水分子是由2个氢原子和1个氧原子构成,该选项说法不
正确。
故选D。
17. 以下是人体几种体液的pH,其中碱性最强的是( )
A. 胃液0.9~1.5 B. 胰液7.5~8.0 C. 血浆7.35~7.45 D. 胆汁7.1~7.3
【答案】B
【解析】
【分析】碱性溶液pH>7,数值越大,碱性越强。
【详解】A、胃液pH<7,为酸性,选项A不符合题意;,B中胰液pH为7.5到8.0,C中血浆pH为7.35到
7.45,D中胆汁pH为7.1到7.3,所以可以看出B中pH最大,所以碱性最强,故选B。
【点睛】溶液pH越大,碱性越强,pH越小,酸性越强。
18. 点燃篝火时,通常把木柴架空些,这样做的目的是
A. 加快散热 B. 增大木柴与空气的接触面积
C. 能降低木柴的着火点 D. 提高空气中氧气的含量
【答案】B
【解析】
【详解】将木柴架空,能增大木柴与空气的接触面积,从而使木柴燃烧更旺,故选B。
19. 属于分解反应的是
第5页/共19页
学科网(北京)股份有限公司A. C+O CO B. 2H+O 2HO
2 2 2 2 2
C. CuO+HSO =CuSO +H O D. HCO HO+CO↑
2 4 4 2 2 3 2 2
【答案】D
【解析】
【详解】A、该反应符合“多变一”的特点,属于化合反应,不符合题意;
B、该反应符合“多变一”的特点,属于化合反应,不符合题意;
C、该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应,不符合题意;
D、该反应符合“一变多”的特点,属于分解反应,符合题意。
故选D。
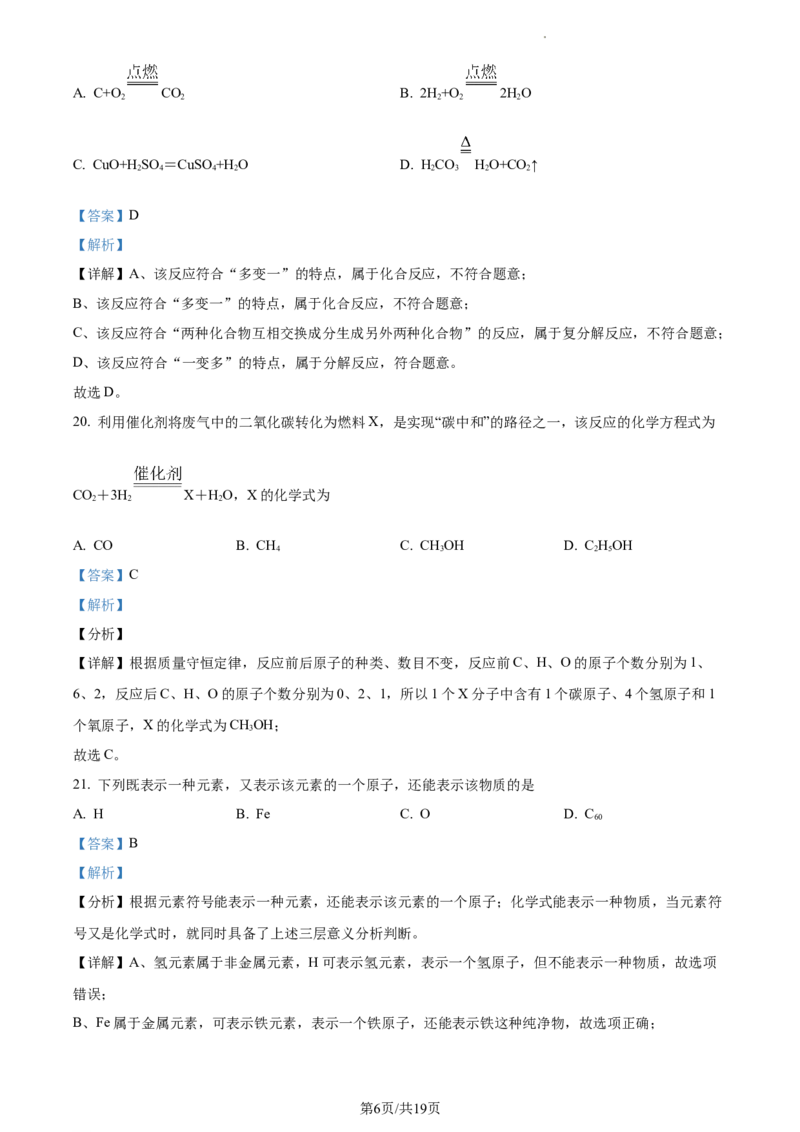
20. 利用催化剂将废气中的二氧化碳转化为燃料X,是实现“碳中和”的路径之一,该反应的化学方程式为
CO+3H X+HO,X的化学式为
2 2 2
A. CO B. CH C. CHOH D. C HOH
4 3 2 5
【答案】C
【解析】
【分析】
【详解】根据质量守恒定律,反应前后原子的种类、数目不变,反应前C、H、O的原子个数分别为1、
6、2,反应后C、H、O的原子个数分别为0、2、1,所以1个X分子中含有1个碳原子、4个氢原子和1
个氧原子,X的化学式为CHOH;
3
故选C。
21. 下列既表示一种元素,又表示该元素的一个原子,还能表示该物质的是
A. H B. Fe C. O D. C
60
【答案】B
【解析】
【分析】根据元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符
号又是化学式时,就同时具备了上述三层意义分析判断。
【详解】A、氢元素属于非金属元素,H可表示氢元素,表示一个氢原子,但不能表示一种物质,故选项
错误;
B、Fe属于金属元素,可表示铁元素,表示一个铁原子,还能表示铁这种纯净物,故选项正确;
第6页/共19页
学科网(北京)股份有限公司C、O属于可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项错误;
D、化学式C ,表示一个C 分子,不是元素符号,故选项错误;
60 60
故选B。
【点睛】本题难度不是很大,考查对元素符号与与化学式含义的理解、掌握及灵活运用进行解题的能力。
22. 物质的化学式与俗称对应错误的是
A. 生石灰:CaO B. 胆矾:CuSO ·5H O
4 2
C. 熟石灰:CaCO D. 干冰:CO
3 2
【答案】C
【解析】
【详解】、生石灰是氧化钙的俗称,其化学式为CaO,故选项A正确;
B、胆矾化学式为CuSO ·5H O,故选项B正确;
4 2
C、熟石灰是氢氧化钙的俗称,其化学式为Ca(OH) ,故选项C错误;
2
D、干冰是固态二氧化碳的俗称,其化学式为CO,故D不正确;
2
故选:B。
23. 粗盐提纯实验中说法正确的是
A. 搭建蒸发装置时要先放置酒精灯
B. 过滤时玻璃棒必须靠在滤纸上方的漏斗壁上以防止滤纸破损
.
C 蒸发时需要将滤液全部蒸干后停止加热
D. 粗盐不能直接放在烧杯中进行称量
【答案】A
【解析】
【详解】A、进行装置组装时要从下到上,从左到右,故搭建蒸发装置时要先放置酒精灯,符合题意;
B、过滤时玻璃棒必须靠在三层滤纸一侧,以防止滤纸破损,不符合题意;
C、蒸发时,应待大部分固体析出时,停止加热,利用余热将其蒸干,不符合题意;
D、粗盐可以直接放在烧杯中进行称量,不符合题意。
故选A。
24. 下列关于溶液的说法正确的是( )
A. 溶液是均一、稳定的混合物
B. 饱和溶液的浓度一定比不饱和溶液的浓度大
C. 澄清、透明的液体一定是溶液
D. 饱和溶液一定不能再继续溶解溶质
【答案】A
【解析】
第7页/共19页
学科网(北京)股份有限公司【详解】A. 溶液是均一、稳定的混合物,此选项正确;
B. 相同温度下,同种物质的饱和溶液的浓度一定比不饱和溶液的浓度大,此选项错误;
C. 澄清、透明的液体不一定是溶液,如水是澄清、透明的液体,但水不是溶液,此选项错误;
D. 该温度下,饱和溶液不能再继续溶解该溶质,还能再继续溶解其它溶质,此选项错误。故选A。
25. 若m克水中含n个氢原子,1摩尔任何物质所含的微粒为N ,则N 为
A A
A. B. C. D.
【答案】D
【解析】
【详解】若m克水中含n个氢原子,则 , ,故选D。
26-30题有1个或2个正确选项
26. 只含游离态氧元素的物质是
A. 氧气 B. 空气 C. 二氧化碳 D. 水
【答案】A
【解析】
【分析】游离态:单质是以游离态形式存在的。只要判断各物质中是否含有单质即可。
【详解】A、氧气是只含有一种元素纯净物,属于单质;故选项正确;
B、空气中含有二氧化碳和水,其中二氧化碳中含有两种元素,属于化合物;水中含有两种元素,属于化
合物;故选项错;
C、二氧化碳中含有两种元素,属于化合物;故选项错;
D、水中含有两种元素,属于化合物;故选项错;
故选A。
27. 下列性质能够区分原子和分子的是
A. 是否能构成物质 B. 分子体积大于原子
C. 原子间有间隙,而分子间没有间隙 D. 在化学变化中是否可以再分
【答案】D
【解析】
【详解】A、原子和分子都能构成物质,不能区分原子和分子;
B、不同物质的分子和原子不能直接比较,因为不管是体积还是质量,有的分子大于原子,有的原子大于
分子,不能区分原子和分子;
C、原子和分子间都有间隙,不能区分原子和分子;
第8页/共19页
学科网(北京)股份有限公司D、在化学变化中分子可以再分,原子不能再分,所以能区分原子和分子。
故选D。
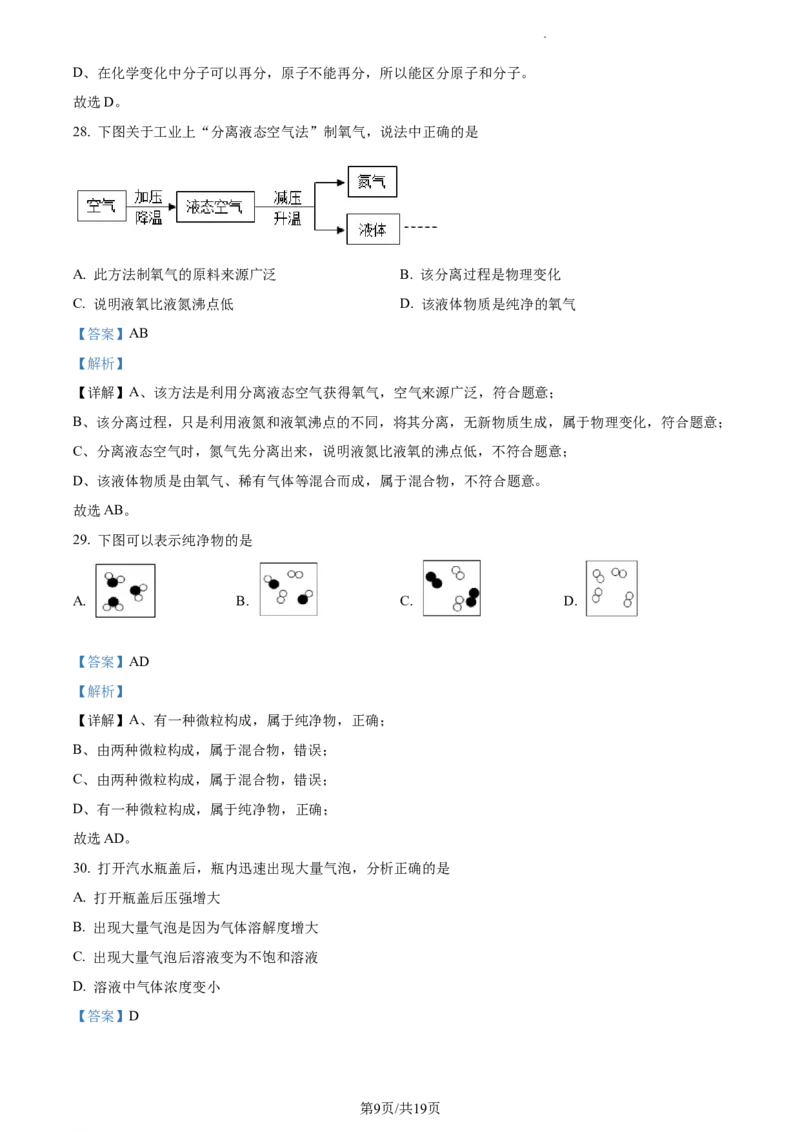
28. 下图关于工业上“分离液态空气法”制氧气,说法中正确的是
A. 此方法制氧气的原料来源广泛 B. 该分离过程是物理变化
C. 说明液氧比液氮沸点低 D. 该液体物质是纯净的氧气
【答案】AB
【解析】
【详解】A、该方法是利用分离液态空气获得氧气,空气来源广泛,符合题意;
B、该分离过程,只是利用液氮和液氧沸点的不同,将其分离,无新物质生成,属于物理变化,符合题意;
C、分离液态空气时,氮气先分离出来,说明液氮比液氧的沸点低,不符合题意;
D、该液体物质是由氧气、稀有气体等混合而成,属于混合物,不符合题意。
故选AB。
29. 下图可以表示纯净物的是
A. B. C. D.
【答案】AD
【解析】
【详解】A、有一种微粒构成,属于纯净物,正确;
B、由两种微粒构成,属于混合物,错误;
C、由两种微粒构成,属于混合物,错误;
D、有一种微粒构成,属于纯净物,正确;
故选AD。
30. 打开汽水瓶盖后,瓶内迅速出现大量气泡,分析正确的是
A. 打开瓶盖后压强增大
B. 出现大量气泡是因为气体溶解度增大
C. 出现大量气泡后溶液变为不饱和溶液
D. 溶液中气体浓度变小
【答案】D
第9页/共19页
学科网(北京)股份有限公司【解析】
【详解】A、汽水是将二氧化碳气体加压之后制成的,打开汽水瓶盖,压强变小,故选项A说法错误;
B、汽水是将二氧化碳气体加压之后制成的,打开汽水瓶盖,压强变小,二氧化碳的溶解度减小,故选项
B说法错误;
C、打开汽水瓶盖,压强变小,二氧化碳的溶解度减小,但仍为常温常压下的饱和溶液,故选项C说法错
误;
D、打开汽水瓶盖,压强变小,二氧化碳的溶解度减小,则浓度减小,故选项D说法正确;
故选:D。
二、填空简答题
31. 元素符号、化学式、化学方程式是国际通用化学语言。
(1)用相应化学语言填空:两个氮分子______;三个氢原子______;氧化铁______。
的
(2)四氧化二氮 化学式是NO,其中“4”的含义是______。
2 4
(3)氢气还原氧化铜,反应的化学方程式是______。
【答案】(1) ①. 2N ②. 3H ③. Fe O
2 2 3
(2)一个四氧化二氮分子中含有4个氧原子
(3)H+CuO Cu+H O
2 2
【解析】
【小问1详解】
化学式前的数字表示分子个数,则两个氮分子的符号为2N;
2
元素符号前的数字表示原子个数,则三个氢原子的符号为3H;
氧化铁中,铁元素的化合价为+3价,氧元素的化合价为-2价,则其化学式为Fe O。
2 3
【小问2详解】
元素符号右下角的数字表示分子中原子个数,则NO 中的“4”表示一个四氧化二氮分子中含有4个氧原子。
2 4
【小问3详解】
氢气能与氧化铜反应生成铜和水,反应的化学方程式为 。
32. 某地区新建水厂,通过混合、絮凝、沉淀、过滤、臭氧活性炭、超滤膜的全新工艺,有望试点自来水
直饮。请回答下列问题:
(1)混合、絮凝、沉淀的目的是将悬浮颗粒沉降。该过程通常加入______促进沉降。
(2)过滤是实验室中常见的操作。使用的主要仪器有铁架台、烧杯、玻璃棒、______等。
第10页/共19页
学科网(北京)股份有限公司(3)臭氧-活性炭联用技术取代了传统氯气的使用,其目的是______。臭氧(O)是一种具有强氧化性的
3
物质,在净水过程中,臭氧转化为氧气,该变化是______(填“化学变化”或“物理变化”)。活性炭用
于净水体现了它具有的性质是______。
(4)超滤膜经常使用醋酸纤维素(C H O)为原料制造。醋酸纤维素含有______种元素,0.1mol
10 16 8
C H O 中含有______个碳原子,氢、氧原子的物质的量之比是______。C H O 中质量分数最大的元素是
10 16 8 10 16 8
______。
【答案】(1)明矾 (2)漏斗
(3) ①. 杀菌消毒 ②. 化学变化 ③. 吸附性
(4) ①. 三##3 ②. 6.02×1023 ③. 2:1 ④. 氧元素##氧##O
【解析】
【小问1详解】
明矾溶于水形成 的胶状物具有吸附性,可以吸附水中悬浮的杂质,加速其沉降;
【小问2详解】
过滤所需的仪器是:铁架台、烧杯、漏斗、玻璃棒;
【小问3详解】
臭氧(O)是一种具有强氧化性的物质,能使蛋白质变性,故目的是:杀菌消毒;
3
臭氧转化为氧气,有新物质生成,属于化学变化;
活性炭结构疏松多孔,具有吸附性,可以吸附水中的色素和异味;
【小问4详解】
由化学式可知,醋酸纤维素含有C、H、O三种元素;
0.1mol C H O 中含有碳原子的个数为:0.1mol×10×6.02×1023=6.02×1023;
10 16 8
氢、氧原子的物质的量之比是:(0.1mol×16):(0.1mol×8)=2:1;
C H O 中C、H、O元素的质量比为:(12×10):16:(16×8)=15:2:16, 氧元素的质量分数最大。
10 16 8
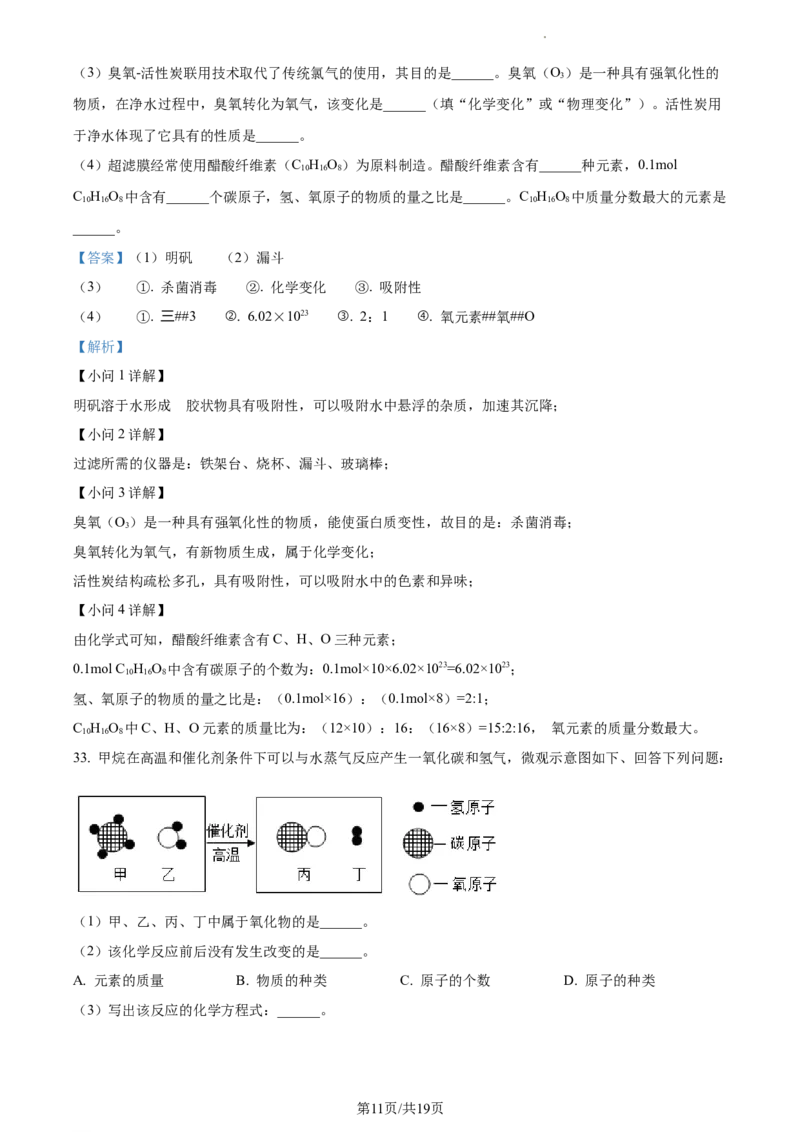
33. 甲烷在高温和催化剂条件下可以与水蒸气反应产生一氧化碳和氢气,微观示意图如下、回答下列问题:
(1)甲、乙、丙、丁中属于氧化物的是______。
(2)该化学反应前后没有发生改变的是______。
A. 元素的质量 B. 物质的种类 C. 原子的个数 D. 原子的种类
(3)写出该反应的化学方程式:______。
第11页/共19页
学科网(北京)股份有限公司【答案】(1)乙、丙 (2)ACD
(3)
【解析】
【小问1详解】
由图示可知,该反应的反应物是甲烷和水,生成物是一氧化碳和氢气,氧化物是两种元素组成含氧元素的
化合物,则水和CO是氧化物,故填:乙、丙;
【小问2详解】
化学变化的实质是分子分成原子,原子再重新组合成新分子的过程,所以在化学反应前后,原子的种类、
数目和质量都不变,元素的种类和质量也不变,物质的总质量不变,物质的种类改变,故选ACD;
【小问3详解】
根据反应的微观示意图分析,该反应的反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式
为 。
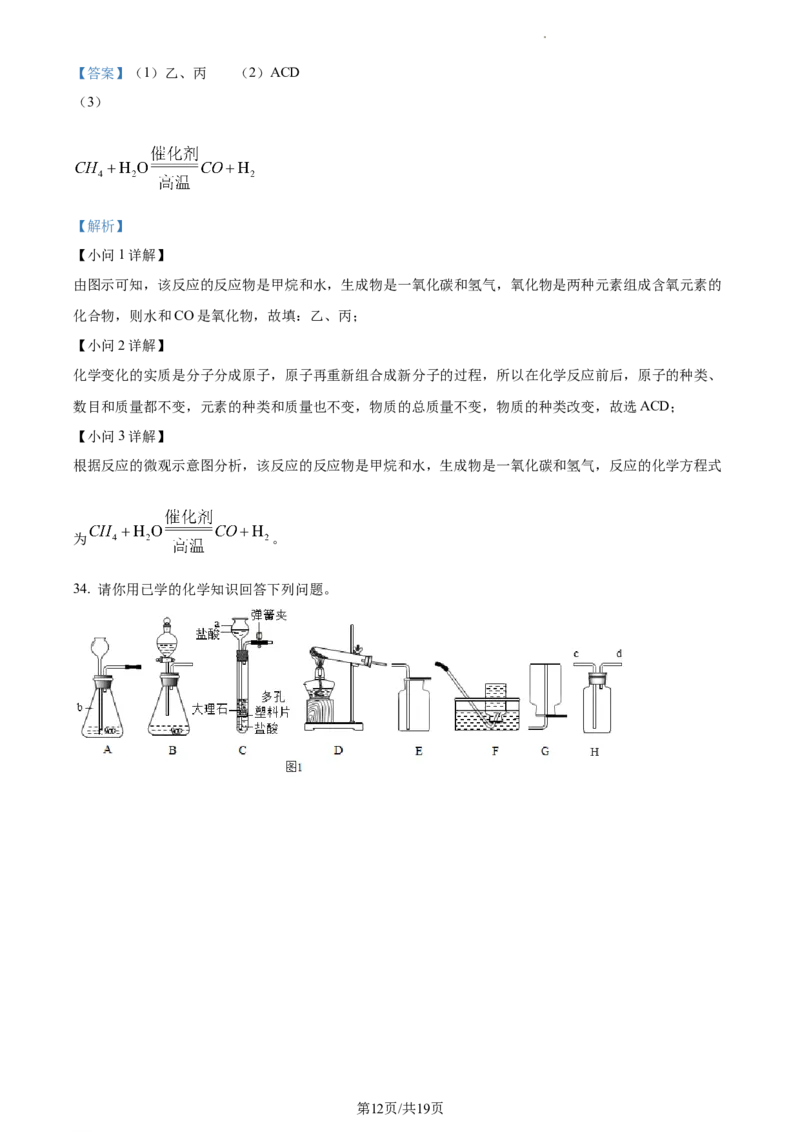
34. 请你用已学的化学知识回答下列问题。
第12页/共19页
学科网(北京)股份有限公司(1)图1中仪器名称a是______;b 是______。
(2)氯酸钾制取氧气,选用的发生装置是______。
(3)实验结束后,A、B、C装置中能实现固液分离的是______。
(4)若用装置B制取氧气,则该反应的化学方程式为______,如气流过快,则进行的操作是______,如
果用图F所示装置收集氧气,是因为氧气具有______且不与水反应的性质,如用H收集二氧化碳,气体应
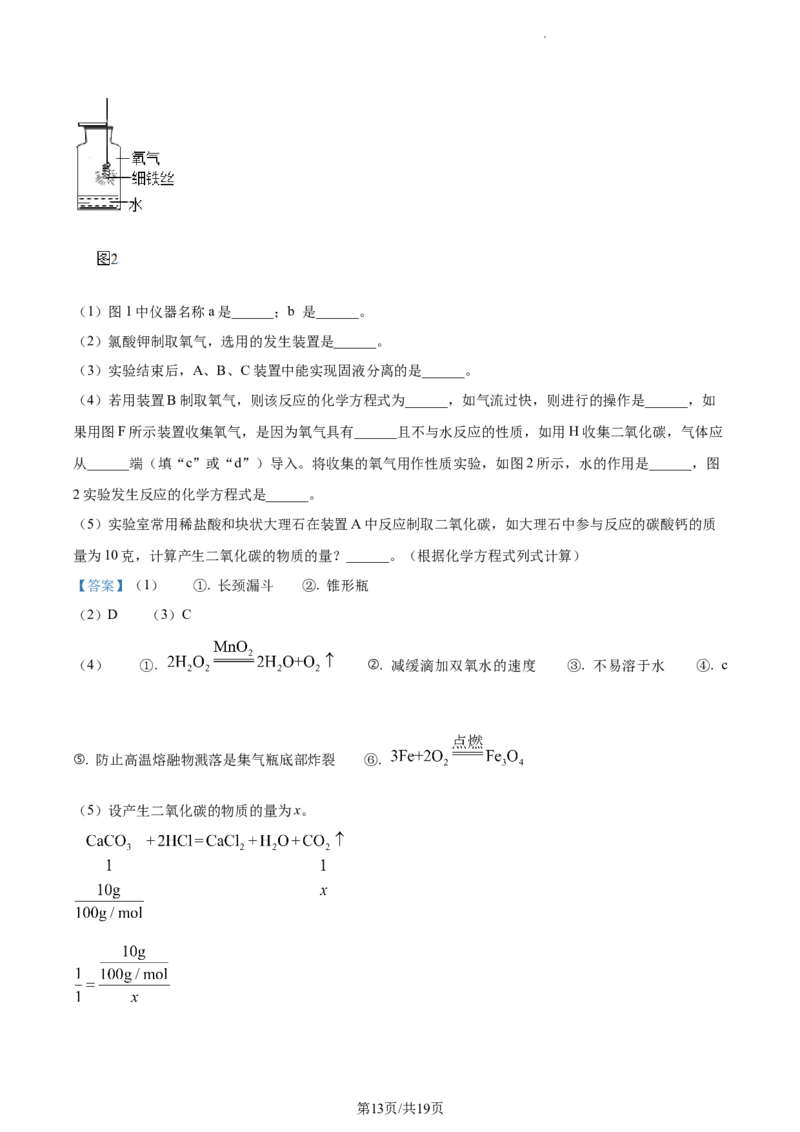
从______端(填“c”或“d”)导入。将收集的氧气用作性质实验,如图2所示,水的作用是______,图
2实验发生反应的化学方程式是______。
(5)实验室常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,如大理石中参与反应的碳酸钙的质
量为10克,计算产生二氧化碳的物质的量?______。(根据化学方程式列式计算)
【答案】(1) ①. 长颈漏斗 ②. 锥形瓶
(2)D (3)C
(4) ①. ②. 减缓滴加双氧水的速度 ③. 不易溶于水 ④. c
⑤. 防止高温熔融物溅落是集气瓶底部炸裂 ⑥.
(5)设产生二氧化碳的物质的量为x。
第13页/共19页
学科网(北京)股份有限公司答:产生二氧化碳的物质的量为0.1mol。
【解析】
【小问1详解】
图1中仪器名称a是长颈漏斗;b 是锥形瓶。
【小问2详解】
氯酸钾在二氧化锰催化作用下加热生成氯化钾和氧气,反应需要加热,选择固体和固体加热装置,则氯酸
钾制取氧气,选用的发生装置是D。
【小问3详解】
装置C含有多孔塑料片,可以控制反应物的接触和分离,进而控制反应的发生和停止,实验结束后,试管
内压强变大,液体进入长颈漏斗中,大理石和盐酸分离,A、B 装置均不能实现固液分离,则A、B、C装
置中能实现固液分离的是C。
【小问4详解】
若用装置B制取氧气,反应在常温下发生,为过氧化氢在二氧化锰催化作用下生成水和氧气,则该反应的
化学方程式为 ,可以通过控制反应物的滴加速率,进而控制反应速率,如气流
过快,则进行的操作是减缓滴加双氧水的速度,排水法收集气体,说明气体难溶于水或不易溶于水,如果
用图F所示装置收集氧气,是因为氧气具有不易溶于水,如用H收集二氧化碳,二氧化碳密度比空气大,
从长管通入,则气体应从c端导入。铁丝在氧气中点燃生成高温熔融物四氧化三铁,放出大量热,则将收
集的氧气用作性质实验,如图2所示,水的作用是防止高温熔融物溅落是集气瓶底部炸裂,图2实验发生
反应的化学方程式是 。
【小问5详解】
见答案。
35. 下列是二氧化碳性质有关实验。
第14页/共19页
学科网(北京)股份有限公司(1)A中加入石蕊试液的目的是______,然后向其中一支试管中通入二氧化碳,溶液变______色,反应
的化学方程式为______;本实验中用两只试管的目的是______。
(2)将一瓶二氧化碳沿烧杯内壁慢慢倒入C烧杯中,可以观察到的现象是______,由此可以得出二氧化
碳的性质是______。
(3)利用装置D、E可证明呼出的气体中含有二氧化碳和水蒸气。D装置内应加入的物质是______;呼出
气体与D、E装置的正确连接顺序是呼出气体→______(填导管口字母代号),确定含有水蒸气的现象是
______,发生反应的化学方程式是______。
【答案】(1) ①. 检验二氧化碳是否与水发生化学反应 ②. 红 ③. CO+H O=HCO ④.
2 2 2 3
对照
(2) ①. 燃着的蜡烛由低到高依次熄灭 ②. 不燃烧、不支持燃烧且密度比空气大
(3) ①. 无水硫酸铜 ②. a→b→d ③. D中白色粉末变蓝 ④. CuSO +5H O=CuSO ·5H O
4 2 4 2
【解析】
【小问1详解】
石蕊溶液遇到酸性物质可以变红,所以加入石蕊的目的是检验二氧化碳是否与水发生化学反应,溶液变成
红色说明二氧化碳与水发生了化学反应生成了碳酸,反应的化学方程式为:CO+H O=HCO,本实验中用
2 2 2 3
两只试管的目的是形成对照实验;
【小问2详解】
由于二氧化碳的密度比空气大,且既不燃烧也不支持燃烧,所以看到的现象是燃着的蜡烛由低到高依次熄
灭;
【小问3详解】
证明呼出的气体中含有二氧化碳和水蒸气,应该先证明水的存在,再证明二氧化碳的存在,顺序不能颠倒,
否则在验证二氧化碳存在时,用到了石灰水,就会干扰水的鉴定,D装置内应该放无水硫酸铜,水会使无
水硫酸铜变蓝,发生反应的化学方程式是:CuSO +5H O=CuSO ·5H O。故填:无水硫酸铜,D中白色粉末
4 2 4 2
变蓝,a→b→d,CuSO +5H O=CuSO ·5H O。
4 2 4 2
36. 下图是初中化学中两个重要实验,请根据所学知识作答。
第15页/共19页
学科网(北京)股份有限公司(1)图1实验:加热前的是操作是______,目的是______,该装置设计的不足之处是______。
(2)图2实验:实验过程中观察到的现象是______,发生反应的化学方程是______。
(3)对图1、2实验的分析正确的是______(填编号)。
a.碳和一氧化碳都具有还原性
b.图2 C中试管口略向下倾斜是为了防止试管炸裂
c.防止液体倒流,都要先将导管移出石灰水,再熄灭酒精灯或喷灯
d.相同质量的氧化铜完全反应后,生成相同质量的二氧化碳
【答案】(1) ①. 先通入一氧化碳 ②. 排尽装置内的空气,防止爆炸 ③. 无尾气处理装置
(2) ①. C中黑色固体变成红色,D中澄清石灰水变浑浊 ②.
(3)ab
【解析】
【小问1详解】
一氧化碳是可燃性气体,点燃前必须验纯,所以实验前要先通入一氧化碳,排尽装置内的空气,防止爆炸;
一氧化碳有毒,不能直接排放到空气中,所以实验装置的最末端要添加尾气处理装置;
【小问2详解】
实验2发生的是碳还原氧化铜,生成铜单质和二氧化碳,反应现象是C中黑色固体变成红色,D中澄清石
灰水变浑浊,反应方程式为 ;
【小问3详解】
a.碳和一氧化碳都能将氧化铜变成铜单质,说明碳和一氧化碳都具有还原性,故a正确;
b.图2 C中试管口略向下倾斜是为了防止试管炸裂,因为加热时会产生水蒸气,如果试管口没向下倾斜,
水蒸气液化回流会使试管炸裂,故b正确;
c.停止加热时,试管内温度降低,压强减小,防止液体倒流,实验2先将导管移出石灰水,再熄灭酒精喷
灯,但是实验1一直通入一氧化碳,不需要这种操作,故C错误;
第16页/共19页
学科网(北京)股份有限公司d.根据化学方程式, 、 ,生成一份二氧化碳时,一
氧化碳要与一份的氧化铜反应,而碳需要两份的氧化铜,故d错误;
故应选ab。
37. 根据NaCl和KNO 的部分溶解度数据,回答下列问题:
3
温度/℃ 0 20 40
.
NaCl 35.7 36.0 366
溶解度g /100g水
KNO 13.3 31.6 63.9
3
(1)0℃时,NaCl的溶解度为______g /100g水;由上述表格可知,影响固体物质溶解性的因素有______。
(写一个)
(2)KNO 和NaCl两种物质的溶解度受温度影响较小的是______,KNO 中混有少量NaCl时,提纯硝酸
3 3
钾的方法是______。
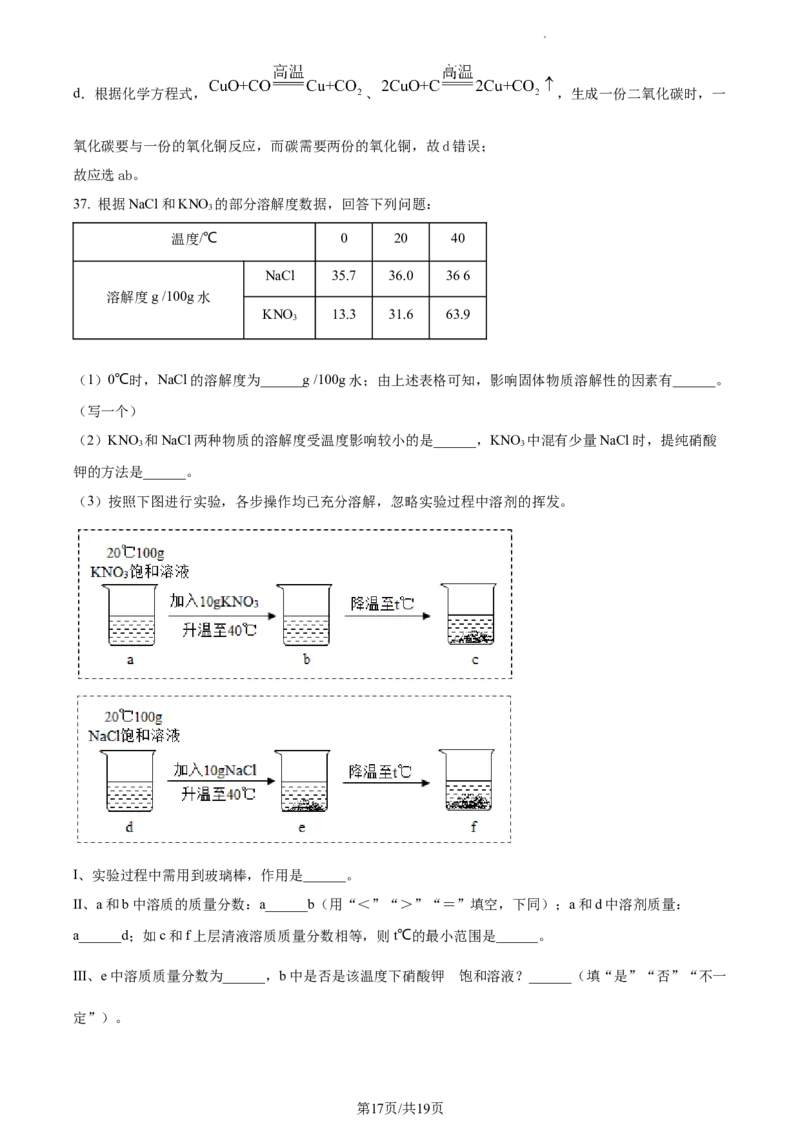
(3)按照下图进行实验,各步操作均已充分溶解,忽略实验过程中溶剂的挥发。
I、实验过程中需用到玻璃棒,作用是______。
II、a和b中溶质的质量分数:a______b(用“<”“>”“=”填空,下同);a和d中溶剂质量:
a______d;如c和f上层清液溶质质量分数相等,则t℃的最小范围是______。
的
III、e中溶质质量分数为______,b中是否是该温度下硝酸钾 饱和溶液?______(填“是”“否”“不一
定”)。
第17页/共19页
学科网(北京)股份有限公司【答案】(1) ①. 35.7 ②. 温度
(2) ①. NaCl ②. 降温结晶
(3) ①. 搅拌,加速溶解 ②. < ③. > ④. 20℃