文档内容
芜湖一中 2024-2025 学年第一学期期中考试
高一化学试卷
命题人: 校对人:
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5
一、选择题(本大题共14小题,每小题3分,共42分。每个小题中只有一个选项是符合
题目要求的,不选、多选、错选均不得分)
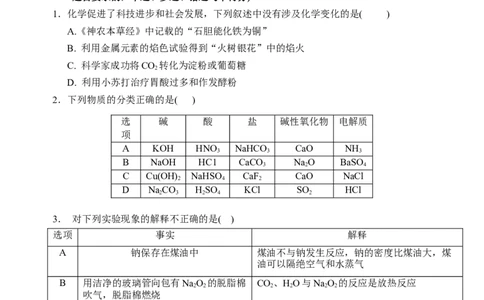
1.化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是( )
A.《神农本草经》中记载的“石胆能化铁为铜”
B. 利用金属元素的焰色试验得到“火树银花”中的焰火
C. 科学家成功将CO 转化为淀粉或葡萄糖
2
D. 利用小苏打治疗胃酸过多和作发酵粉
2.下列物质的分类正确的是( )
选 碱 酸 盐 碱性氧化物 电解质
项
A KOH HNO NaHCO CaO NH
3 3 3
B NaOH HC1 CaCO NaO BaSO
3 2 4
C Cu(OH) NaHSO CaF CaO NaCl
2 4 2
D NaCO HSO KCl SO HCl
2 3 2 4 2
3. 对下列实验现象的解释不正确的是( )
选项 事实 解释
A 钠保存在煤油中 煤油不与钠发生反应,钠的密度比煤油大,煤
油可以隔绝空气和水蒸气
B 用洁净的玻璃管向包有NaO 的脱脂棉 CO、HO与NaO 的反应是放热反应
2 2 2 2 2 2
吹气,脱脂棉燃烧
C 将金属钠取出用滤纸吸干表面煤油, 说明金属钠被氧气氧化得到了黑色产物
在坩埚中加热燃烧,有黑色固体产生
D 钠长期暴露在空气中的产物是NaCO 是钠与空气中的氧气、水和二氧化碳反应的结
2 3
果
4.对下列实验的相关说法错误的是
A.氢氧化铁胶体带正电,做氢氧化铁胶体电泳实验时阴极颜色加深
B.进行焰色试验时,没有铂丝可用无锈铁丝代替进行实验C.实验室中做钠的实验取用后剩余的钠要放回原试剂瓶中
D.葡萄酒中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒
5.氯化钠是一种盐。下列途径,不能得到氯化钠的是
A.金属单质与非金属单质反应 B.酸性氧化物与碱反应
C.酸与碱发生中和反应 D.金属与酸反应
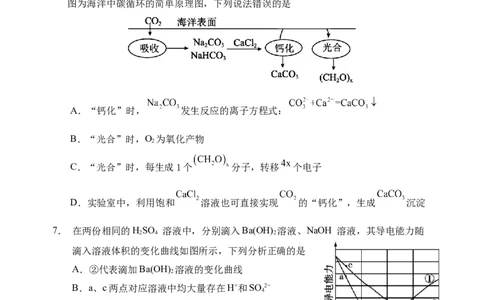
6.海洋碳循环是全球碳循环的重要组成部分,是影响全球气候变化的关键控制环节。下
图为海洋中碳循环的简单原理图,下列说法错误的是
A.“钙化”时, 发生反应的离子方程式:
B.“光合”时,O 为氧化产物
2
C.“光合”时,每生成1个 分子,转移 个电子
D.实验室中,利用饱和 溶液也可直接实现 的“钙化”,生成 沉淀
7. 在两份相同的HSO 溶液中,分别滴入Ba(OH) 溶液、NaOH 溶液,其导电能力随
2 4 2
滴入溶液体积的变化曲线如图所示,下列分析正确的是
A.②代表滴加Ba(OH) 溶液的变化曲线
2
B.a、c两点对应溶液中均大量存在H+和SO 2−
4
C.b点显中性、d 点显酸性
D.e点时,两溶液中OH− 的量相等
8.在稀硫酸中几种离子的转化关系如图所示:
下列说法正确的是A.反应1的氧化剂为Ce4+,还原产物为Mn3+
B.推测不可发生反应:Ce4++Fe2+=Ce3++Fe3+
C.反应3的离子方程式为:Fe3++2I- =I +Fe2+
2
D.氧化性由强到弱的顺序为:Ce4+>Mn3+>Fe3+>I
2
9.一块表面已被缓慢氧化的金属钠,其质量为10.8g,投入100g水中,收集到氢气
0.2g。则原来钠块表面被氧化的钠的质量是( )
A.6.2g B.4.6g C.7.8g D.10.6g
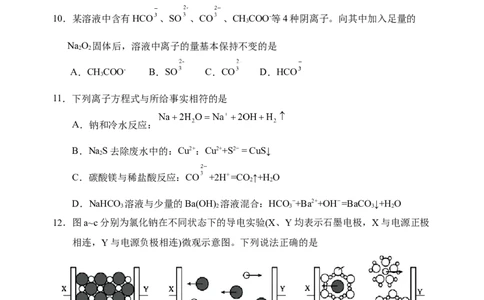
10.某溶液中含有HCO 、SO 、CO 、CHCOO-等4种阴离子。向其中加入足量的
3
NaO 固体后,溶液中离子的量基本保持不变的是
2 2
A.CHCOO- B.SO C.CO D.HCO
3
11.下列离子方程式与所给事实相符的是
A.钠和冷水反应:
B.NaS去除废水中的:Cu2+:Cu2++S2− = CuS↓
2
C.碳酸镁与稀盐酸反应:CO +2H+ =CO ↑+H O
2 2
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO −+Ba2++OH− =BaCO ↓+H O
3 2 3 3 2
12.图a~c分别为氯化钠在不同状态下的导电实验(X、Y均表示石墨电极,X与电源正极
相连,Y与电源负极相连)微观示意图。下列说法正确的是
A.图示中 代表的是水合钠离子
B.氯化钠在不同状态下均能导电C.图b表示在通电的条件下氯化钠产生自由移动的离子
D.由微观示意图类推:金属钠和盐酸反应,主要是钠先和水接触发生反应
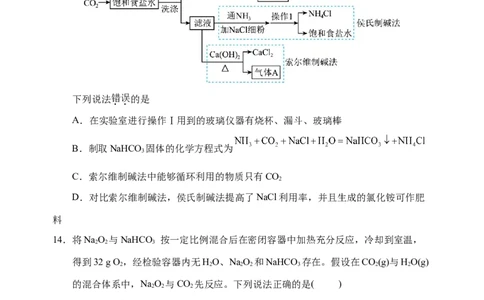
13.索尔维制碱法和侯氏制碱法,两种工艺的差异之一在于对“滤液”的处理方法不同,
流程如图:
下列说法错误的是
A.在实验室进行操作Ⅰ用到的玻璃仪器有烧杯、漏斗、玻璃棒
B.制取NaHCO 固体的化学方程式为
3
C.索尔维制碱法中能够循环利用的物质只有CO
2
D.对比索尔维制碱法,侯氏制碱法提高了NaCl利用率,并且生成的氯化铵可作肥
料
14.将NaO 与NaHCO 按一定比例混合后在密闭容器中加热充分反应,冷却到室温,
2 2 3
得到32 g O,经检验容器内无HO、NaO 和NaHCO 存在。假设在CO(g)与HO(g)
2 2 2 2 3 2 2
的混合体系中,NaO 与CO 先反应。下列说法正确的是( )
2 2 2
A.容器内还剩有CO
2
B.原NaO 与NaHCO 的质量比为13:14
2 2 3
C.产物中NaCO 的质量为106 g
2 3
D.无法求出该容器中发生氧化还原反应的氧化剂和还原剂质量比
二、非选择题(本大题共4小题,共58分)
15.(14分)Ⅰ.胶体金即金溶胶,其具有光吸收性、呈色性和胶体性等特点。免疫胶体
金技术作为胶体金标记物,可实现对抗原抗体的测定。用白磷还原法可制得一种金的分散系,该分散系在临床诊断等方面有着广泛的应用。其操作步骤如下:
a.取20%白磷(记为①)的乙醚溶液0.5 mL,加蒸馏水(记为②)60 mL 。
b.先滴加1%氯化金水溶液(记为③)0.75 mL,再滴加一定浓度的KCO 溶液
2 3
(记为④)0.6 mL ,振荡变成棕红色。
c .加热煮沸至液体变成透明的红色。
d.分离提纯,除去无机溶质。所得分散系中,金颗粒直径在5~12 nm 之间
(1)上述物质①②③④中属于电解质的是____(填序号,下同),除②以外能导电的
是______。
(2)所得分散系属于______,其分散质是________。
(3)所得红色液体______(填“能”或“不能”)继续加热
Ⅱ.把淀粉溶液溶于沸水中,制成淀粉胶体。
(4)鉴别水溶液和胶体可以利用____________。
(5)在淀粉胶体中加入硫酸钠,并装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸
馏水的烧杯里,一段时间后,取出半透膜袋,向烧杯的溶液中滴加氯化钡溶液,
其现象为______________。
16.(10分)某溶液只含Cl 、CO 、SO 、Na 、K 、Mg 六种离子中的某几
种。经实验:
①原溶液 白色沉淀;
②原溶液中加BaCl 溶液不产生沉淀;
2
③原溶液中加AgNO 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问
3
题:
(1)试分析原溶液中一定含有的离子是______________,一定不含有的离子是
_______,可能含有的离子是______________。
(2)有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)
_________,说明理由
_________________________________________________________。
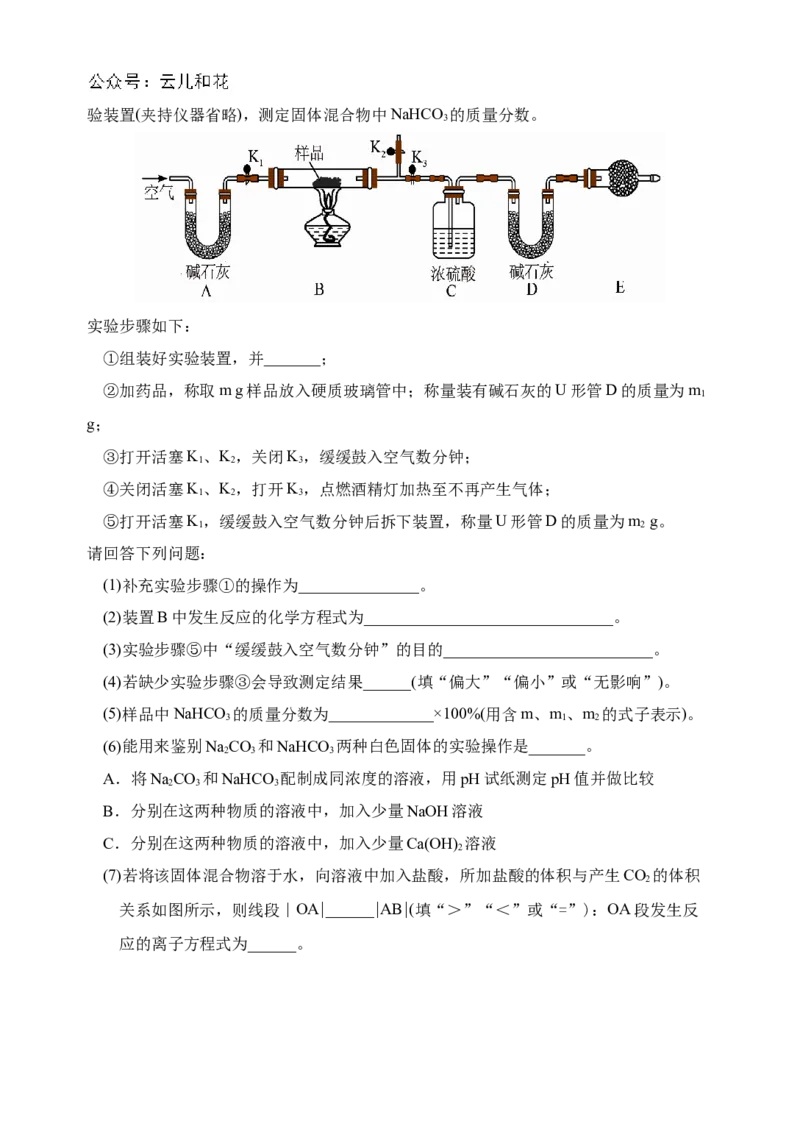
17.(16分)现有一份NaCO 和NaHCO 固体混合物,某化学兴趣小组设计如图所示实
2 3 3验装置(夹持仪器省略),测定固体混合物中NaHCO 的质量分数。
3
实验步骤如下:
①组装好实验装置,并_______;
②加药品,称取m g样品放入硬质玻璃管中;称量装有碱石灰的U形管D的质量为m
1
g;
③打开活塞K、K,关闭K,缓缓鼓入空气数分钟;
1 2 3
④关闭活塞K、K,打开K,点燃酒精灯加热至不再产生气体;
1 2 3
⑤打开活塞K,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为m g。
1 2
请回答下列问题:
(1)补充实验步骤①的操作为_______________。
(2)装置B中发生反应的化学方程式为_______________________________。
(3)实验步骤⑤中“缓缓鼓入空气数分钟”的目的__________________________。
(4)若缺少实验步骤③会导致测定结果______(填“偏大”“偏小”或“无影响”)。
(5)样品中NaHCO 的质量分数为_____________×100%(用含m、m、m 的式子表示)。
3 1 2
(6)能用来鉴别NaCO 和NaHCO 两种白色固体的实验操作是_______。
2 3 3
A.将NaCO 和NaHCO 配制成同浓度的溶液,用pH试纸测定pH值并做比较
2 3 3
B.分别在这两种物质的溶液中,加入少量NaOH溶液
C.分别在这两种物质的溶液中,加入少量Ca(OH) 溶液
2
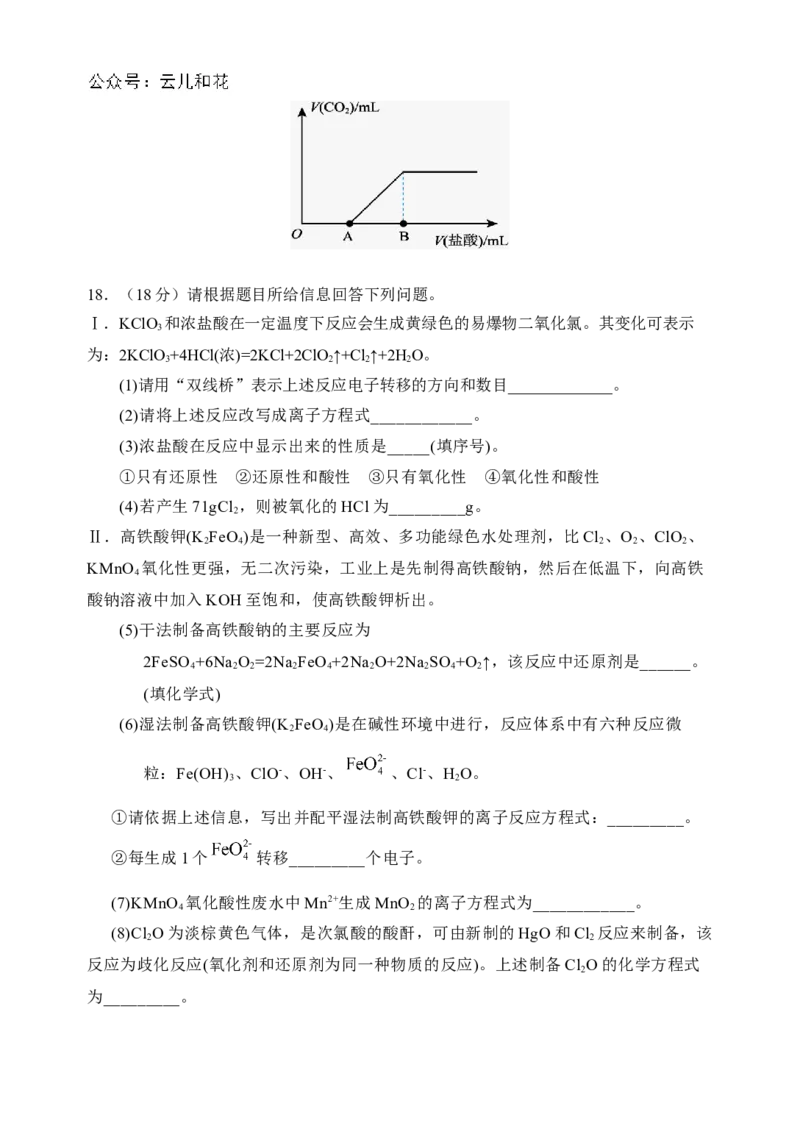
(7)若将该固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生CO 的体积
2
关系如图所示,则线段∣OA∣______∣AB∣(填“>”“<”或“=”):OA段发生反
应的离子方程式为______。18.(18分)请根据题目所给信息回答下列问题。
Ⅰ.KClO 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示
3
为:2KClO+4HCl(浓)=2KCl+2ClO ↑+Cl↑+2H O。
3 2 2 2
(1)请用“双线桥”表示上述反应电子转移的方向和数目_____________。
(2)请将上述反应改写成离子方程式____________。
(3)浓盐酸在反应中显示出来的性质是_____(填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生71gCl ,则被氧化的HCl为_________g。
2
Ⅱ.高铁酸钾(K FeO )是一种新型、高效、多功能绿色水处理剂,比Cl 、O 、ClO 、
2 4 2 2 2
KMnO 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁
4
酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为
2FeSO +6Na O =2Na FeO +2Na O+2Na SO +O ↑,该反应中还原剂是______。
4 2 2 2 4 2 2 4 2
(填化学式)
(6)湿法制备高铁酸钾(K FeO )是在碱性环境中进行,反应体系中有六种反应微
2 4
粒:Fe(OH) 、ClO-、OH-、 、Cl-、H O。
3 2
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:_________。
②每生成1个 转移_________个电子。
(7)KMnO 氧化酸性废水中Mn2+生成MnO 的离子方程式为____________。
4 2
(8)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该
2 2
反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl O的化学方程式
2
为_________。