文档内容
新泰一中北校高一下学期期中考试
化 学 试 题
2025.04
可能用到的相对原子质量:Li7 N14 Mg 24 S 32 Cr52 Cu 64 I 127
第 I 卷(共 40 分)
一、选择题(本题包括 10 小题,每小题 2 分,共 20 分。每小题只有
一个选项符合题意)
1.化学与环境、材料、能源、信息等生产生活息息相关,下列说法正确的是( )
A.“燃煤脱硫”技术有利于我国早日实现“碳达峰、碳中和”
B.“神舟十八号”返回舱使用的耐高温材料包括碳化硅等新型陶瓷
C.研制的高效率钙钛矿太阳能电池能将化学能转化为电能
D.光导纤维具有通信容量大,抗干扰性能强等优点,其主要成分是硅单质
2.下列说法正确的是( )
A.在恒容容器内,反应达到平衡后通入Ar,压强增大,反应速率加快
B.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率
C.l00mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠固体,生成氢气的速率
不变
D.向5mL0.2mol/L的FeCl 溶液中加入几滴同浓度的KI溶液,再加入几滴KSCN
3
溶液,溶液显红色,证明FeCl 与KI的反应是可逆反应
3
3.下列实验中,不能达到实验目的的是( )
A. 用图①装置检验纯碱中含有钾元素 B. 用图②装置可分离得到CCl
4
C. 由装置③分离粗盐中的不溶物 D. 由装置④进行灼烧海带除去有机物
4.碲化镉(CdTe)具有光电转化功能,可用于制造发电玻璃。已知 Te和S位于
52
同一主族。下列叙述错误的是( )
1
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}A. CdTe中Cd呈现+2价 B. Te位于第5周期ⅥA族
C. H Te还原性比HI弱 D. H TeO 的酸性比H SO 弱
2 2 4 2 4
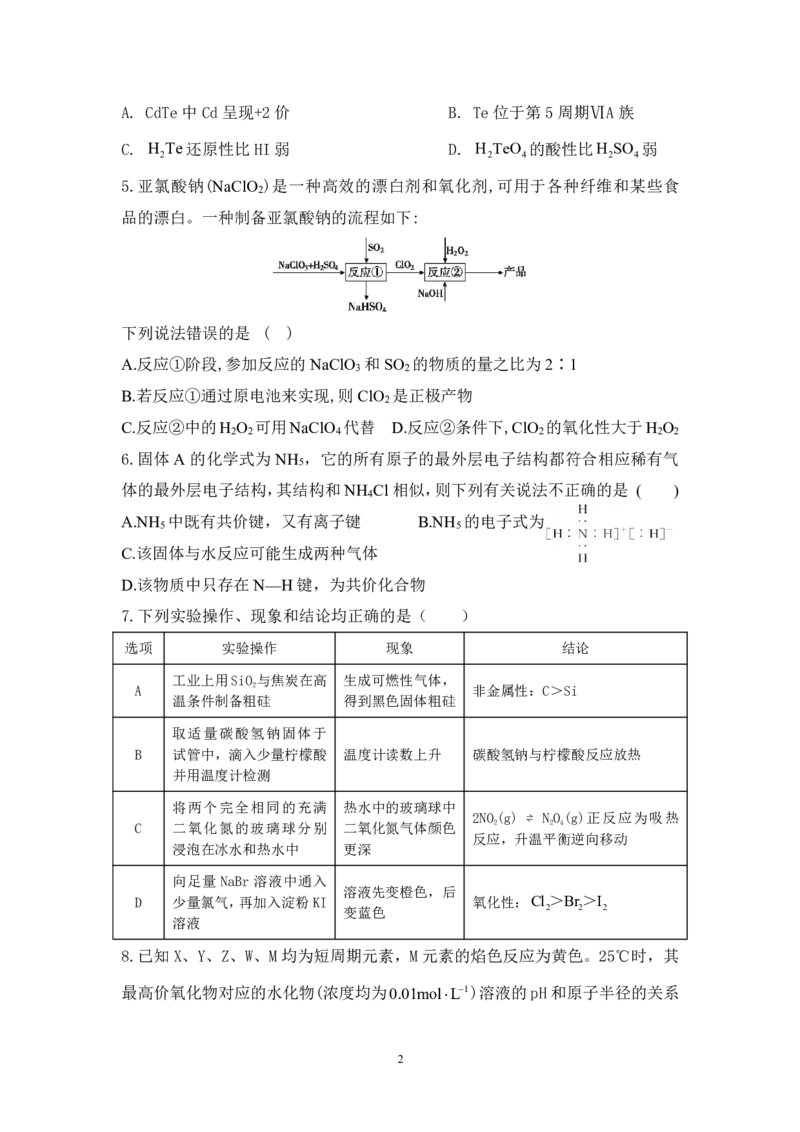
5.亚氯酸钠(NaClO )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食
2
品的漂白。一种制备亚氯酸钠的流程如下:
下列说法错误的是 ( )
A.反应①阶段,参加反应的NaClO 和SO 的物质的量之比为2∶1
3 2
B.若反应①通过原电池来实现,则 ClO 是正极产物
2
C.反应②中的H O 可用NaClO 代替 D.反应②条件下,ClO 的氧化性大于H O
2 2 4 2 2 2
6.固体 A 的化学式为 NH ,它的所有原子的最外层电子结构都符合相应稀有气
5
体的最外层电子结构,其结构和NH Cl相似,则下列有关说法不正确的是 ( )
4
A.NH 中既有共价键,又有离子键 B.NH 的电子式为
5 5
C.该固体与水反应可能生成两种气体
D.该物质中只存在N—H键,为共价化合物
7.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
工业上用SiO 与焦炭在高 生成可燃性气体,
A 2 非金属性:C>Si
温条件制备粗硅 得到黑色固体粗硅
取适量碳酸氢钠固体于
B 试管中,滴入少量柠檬酸 温度计读数上升 碳酸氢钠与柠檬酸反应放热
并用温度计检测
将两个完全相同的充满 热水中的玻璃球中
2NO(g) ⇌ NO(g)正反应为吸热
C 二氧化氮的玻璃球分别 二氧化氮气体颜色 2 2 4
反应,升温平衡逆向移动
浸泡在冰水和热水中 更深
向足量 NaBr 溶液中通入
溶液先变橙色,后
D 少量氯气,再加入淀粉KI 氧化性:Cl>Br>I
变蓝色 2 2 2
溶液
8.已知X、Y、Z、W、M均为短周期元素,M元素的焰色反应为黄色。25℃时,其
最高价氧化物对应的水化物(浓度均为0.01molL1)溶液的pH和原子半径的关系
2
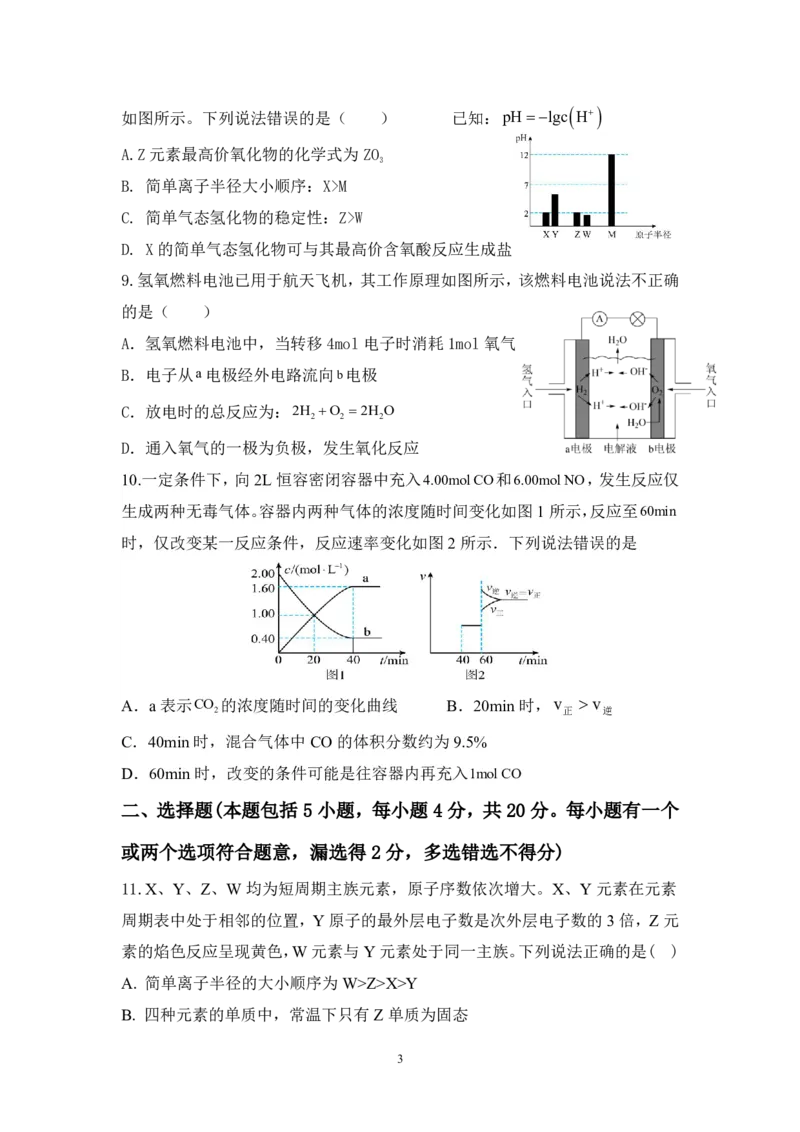
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}如图所示。下列说法错误的是( ) 已知:pH lgc
H
A.Z元素最高价氧化物的化学式为ZO
3
B. 简单离子半径大小顺序:X>M
C. 简单气态氢化物的稳定性:Z>W
D. X的简单气态氢化物可与其最高价含氧酸反应生成盐
9.氢氧燃料电池已用于航天飞机,其工作原理如图所示,该燃料电池说法不正确
的是( )
A.氢氧燃料电池中,当转移4mol电子时消耗1mol氧气
B.电子从a电极经外电路流向b电极
C.放电时的总反应为:2H O 2H O
2 2 2
D.通入氧气的一极为负极,发生氧化反应
10.一定条件下,向2L 恒容密闭容器中充入4.00mol CO和6.00mol NO,发生反应仅
生成两种无毒气体。容器内两种气体的浓度随时间变化如图1所示,反应至60min
时,仅改变某一反应条件,反应速率变化如图2所示.下列说法错误的是
A.a表示CO 的浓度随时间的变化曲线 B.20min 时,v v
2 正 逆
C.40min时,混合气体中CO的体积分数约为9.5%
D.60min时,改变的条件可能是往容器内再充入1mol CO
二、选择题(本题包括 5 小题,每小题 4 分,共 20 分。每小题有一个
或两个选项符合题意,漏选得 2 分,多选错选不得分)
11.X、Y、Z、W 均为短周期主族元素,原子序数依次增大。X、Y元素在元素
周期表中处于相邻的位置,Y原子的最外层电子数是次外层电子数的3倍,Z元
素的焰色反应呈现黄色,W元素与Y元素处于同一主族。下列说法正确的是( )
A. 简单离子半径的大小顺序为W>Z>X>Y
B. 四种元素的单质中,常温下只有Z单质为固态
3
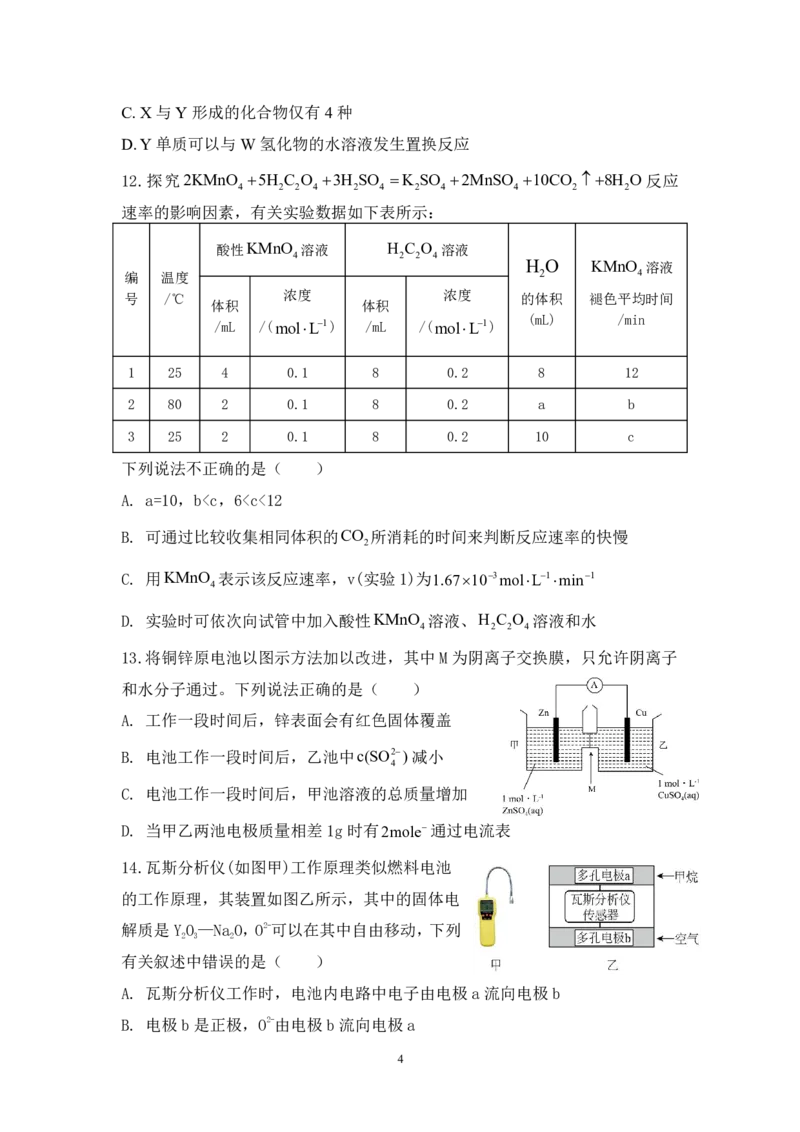
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}C. X与Y形成的化合物仅有4种
D.Y单质可以与W 氢化物的水溶液发生置换反应
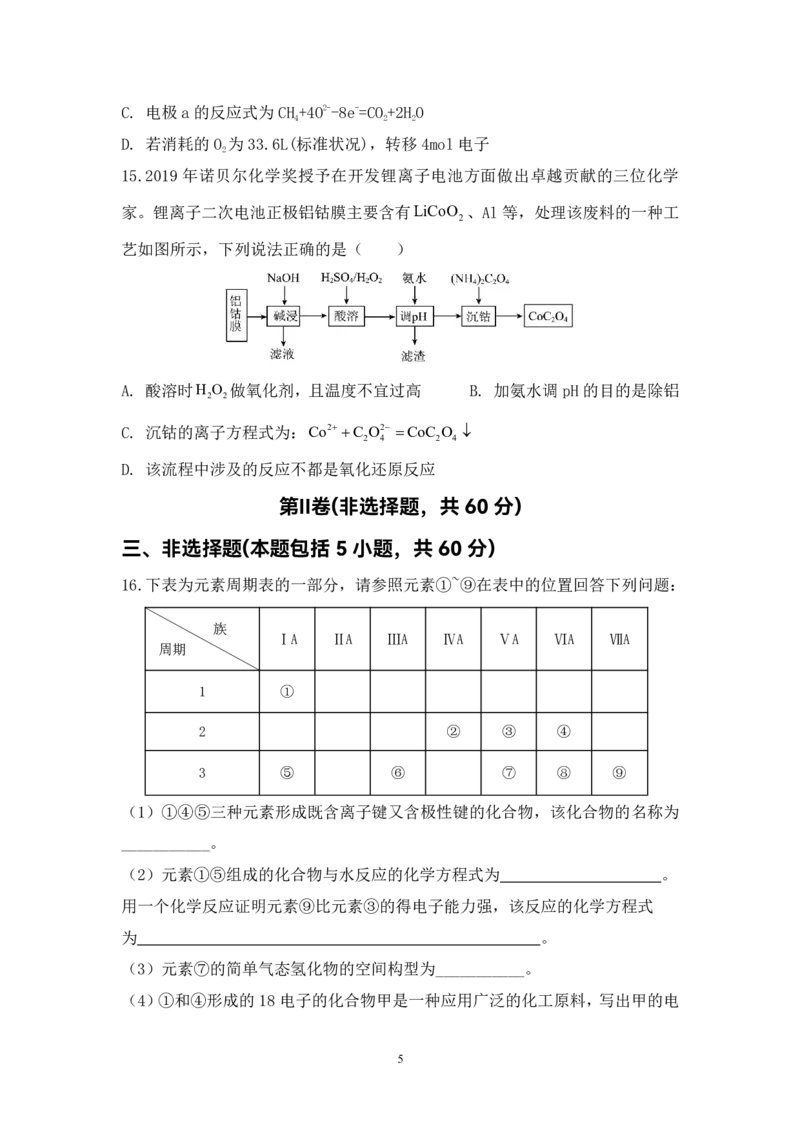
12.探究2KMnO 5H C O 3H SO K SO 2MnSO 10CO 8H O 反应
4 2 2 4 2 4 2 4 4 2 2
速率的影响因素,有关实验数据如下表所示:
酸性KMnO 溶液 H C O 溶液
4 2 2 4
H O KMnO 溶液
编 温度 2 4
号 /℃ 浓度 浓度 的体积 褪色平均时间
体积 体积
(mL) /min
/mL /(molL1) /mL /(molL1)
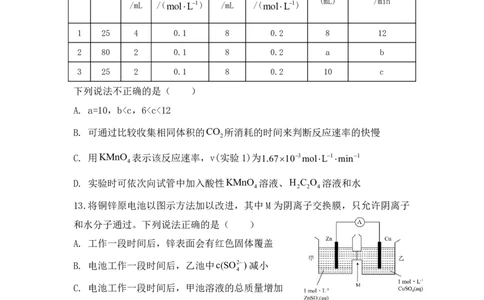
1 25 4 0.1 8 0.2 8 12
2 80 2 0.1 8 0.2 a b
3 25 2 0.1 8 0.2 10 c
下列说法不正确的是( )
A. a=10,b”
正 2 逆 3
“<”“=”或“无法比较”)。
6
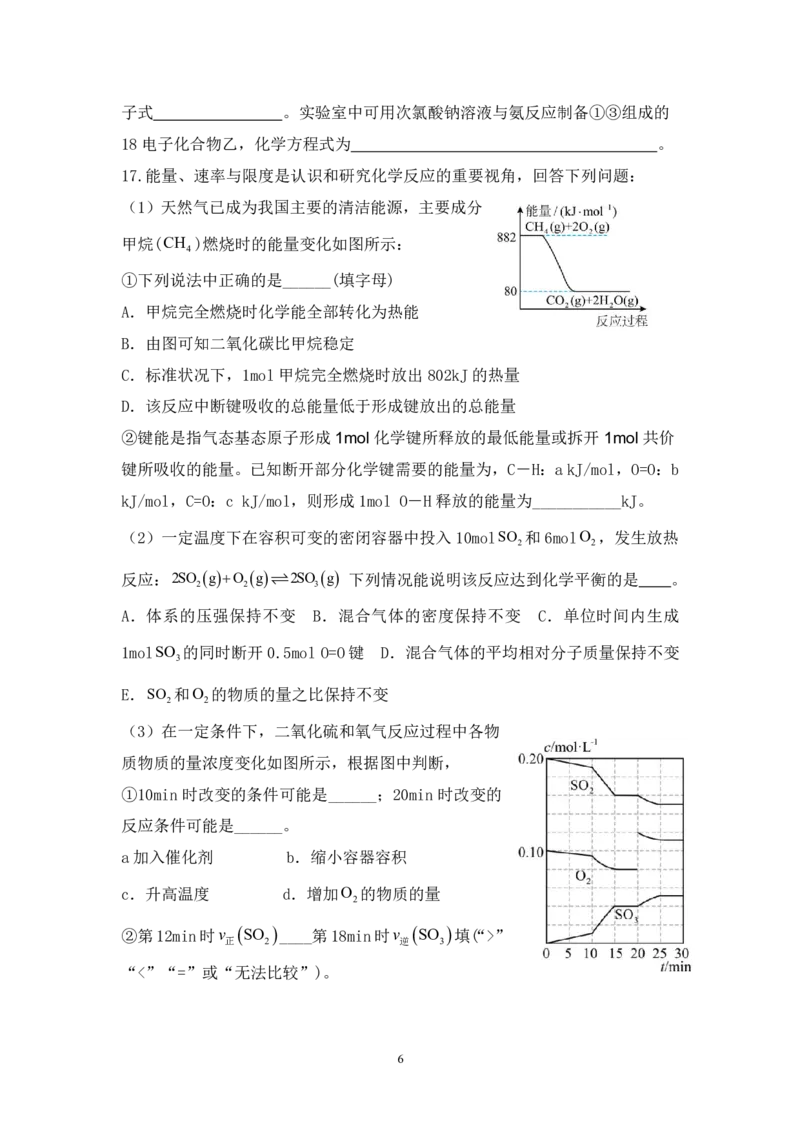
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}18.磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一、采用湿法冶金工
4
艺回收废旧磷酸亚铁锂电池正极片(除LiFePO 外,还含有Al箔、少量不溶于酸
4
碱的导电剂)中的资源,部分流程如下图:
已知:碳酸锂在水中的溶解度随温度的升高而减小。回答下列问题:
(1)“正极碱浸”时,足量NaOH溶液的作用是 (用
离子方程式表示)。
(2)“氧化浸出”时,氧化剂可以选择H O 其作用是 。
2 2
该步操作加热温度不宜过高的原因是 。
(3)最后一步“一系列操作”包括___________、洗涤、干燥。洗涤时最好选用
热水洗涤的原因是 。
(4)工业上将回收的Li CO 、FePO 粉碎与足量炭黑混合高温灼烧再生制备
2 3 4
LiFePO ,写出反应的化学方程式: 。
4
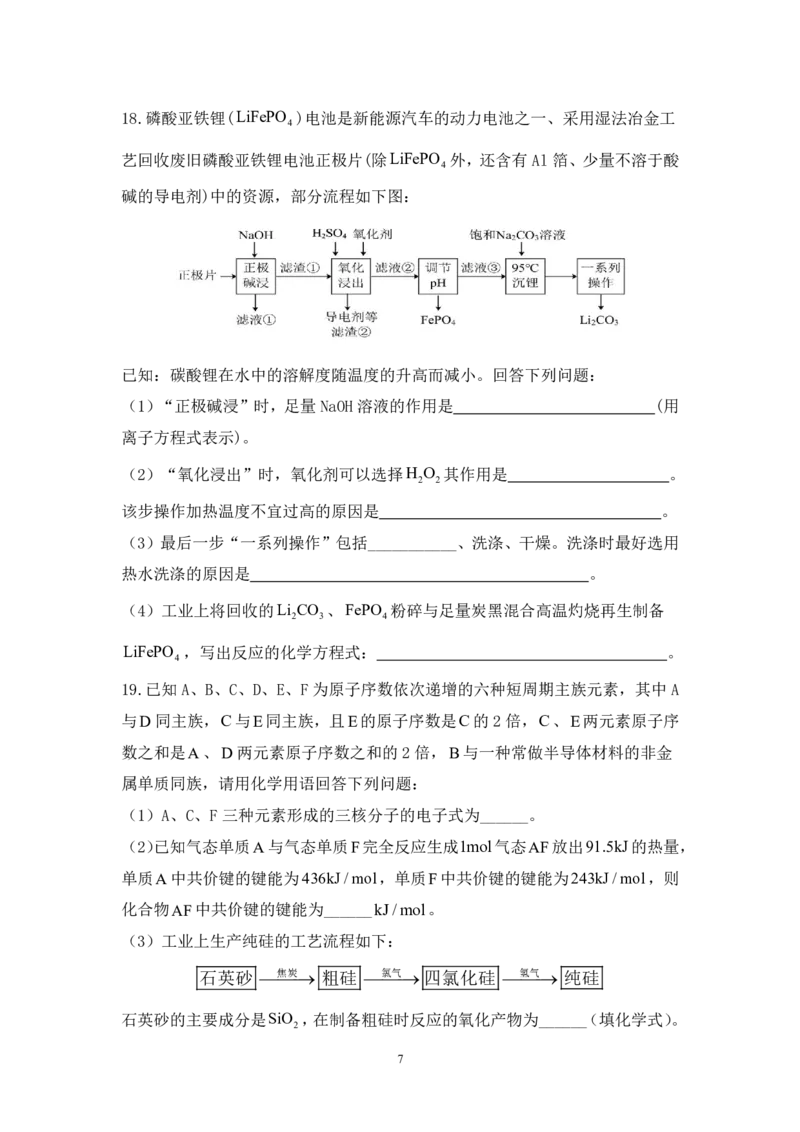
19.已知A、B、C、D、E、F为原子序数依次递增的六种短周期主族元素,其中A
与D同主族,C与E同主族,且E的原子序数是C的2倍,C、E两元素原子序
数之和是A、D两元素原子序数之和的 2倍,B与一种常做半导体材料的非金
属单质同族,请用化学用语回答下列问题:
(1)A、C、F三种元素形成的三核分子的电子式为______。
(2)已知气态单质A与气态单质F完全反应生成1mol气态AF放出91.5kJ的热量,
单质A中共价键的键能为436kJ/mol,单质F中共价键的键能为243kJ/mol,则
化合物AF中共价键的键能为______kJ/mol。
(3)工业上生产纯硅的工艺流程如下:
石英砂 焦炭 粗硅 氯气 四氯化硅 氢气 纯硅
石英砂的主要成分是SiO ,在制备粗硅时反应的氧化产物为______(填化学式)。
2
7
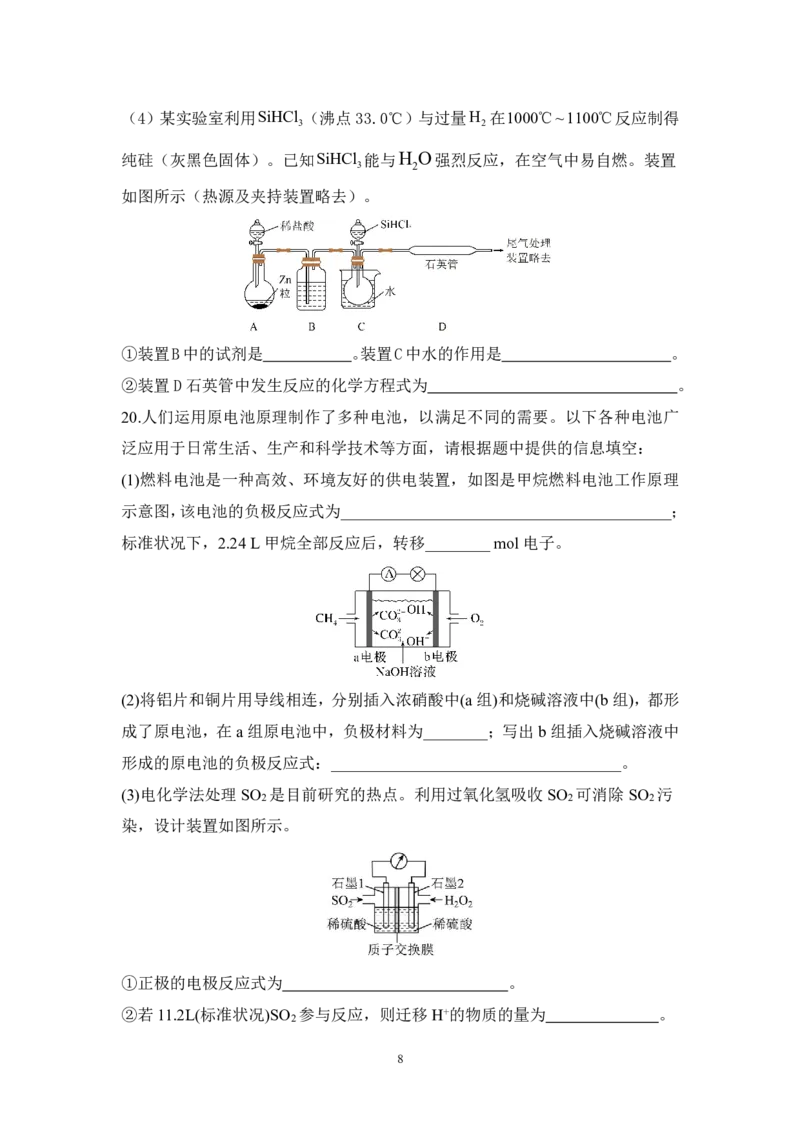
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}(4)某实验室利用SiHCl (沸点33.0℃)与过量H 在1000℃~1100℃反应制得
3 2
纯硅(灰黑色固体)。已知SiHCl 能与H O强烈反应,在空气中易自燃。装置
3 2
如图所示(热源及夹持装置略去)。
①装置B中的试剂是 。装置C中水的作用是 。
②装置D石英管中发生反应的化学方程式为 。
20.人们运用原电池原理制作了多种电池,以满足不同的需要。以下各种电池广
泛应用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空:
(1)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池工作原理
示意图,该电池的负极反应式为_________________________________________;
标准状况下,2.24L甲烷全部反应后,转移________mol电子。
(2)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和烧碱溶液中(b 组),都形
成了原电池,在a组原电池中,负极材料为________;写出b组插入烧碱溶液中
形成的原电池的负极反应式:____________________________________。
(3)电化学法处理SO 是目前研究的热点。利用过氧化氢吸收 SO 可消除SO 污
2 2 2
染,设计装置如图所示。
①正极的电极反应式为 。
②若11.2L(标准状况)SO 参与反应,则迁移H+的物质的量为 。
2
8
{#{QQABZQSxwgCQwBYACZ7KA0lACgmQsJKRJYomxQCUqARLwBNABAA=}#}