AIVEV文献分享丨《Cell Reports Medicine》破解早期癌症检测难题——血浆外囊泡蛋白指纹+智能微流控芯片
2026年4月,澳大利亚昆士兰大学Richard J. Lobb/Matt Trau团队与香港中文大学Andreas Moller团队合作在Cell Reports Medicine上发表了题为Early-stage multi-cancer detection through a plasma extracellular vesicle protein signature的文章,发现并验证了血浆小胞外囊泡上THBS1、NID1、PTX3和VCAN组成的4蛋白标志物组合,并开发了集成纳米剪切微流控与表面增强拉曼散射技术的多重检测设备,该设备能准确区分良性肺结节与早期肺癌,在22种细胞系和764例临床样本中验证了多癌种检测性能,并在前瞻性队列中展现出良好的筛查准确性和临床转化潜力。
研究背景
全球癌症负担持续加重,早期检测是改善患者生存的关键。目前基于循环肿瘤DNA等的液体活检方法在早期癌症检测中的敏感性和特异性仍不理想。小胞外囊泡(sEVs)作为肿瘤细胞释放的纳米级囊泡,携带丰富的蛋白质货物,是极具潜力的非侵入性生物标志物来源,但其临床应用面临异质性、非特异性等挑战,亟需发现可靠的多重标志物以实现精准筛查。
本文亮点
-
通过同基因细胞模型筛选出THBS1、NID1、PTX3和VCAN,并在22种癌细胞系及764例回顾性样本中证实其对9种癌症类型的检测性能优异,且能有效检出I期早期癌症。
-
开发了集成纳米剪切微流控与SERS的多重检测设备,该设备可同时检测sEV上4种蛋白标志物,实现高通量、高灵敏度的原位定量分析,克服了传统方法的复杂性和灵敏度不足问题。
-
在68例因CT发现肺结节的患者中,该设备区分良性病变与早期肺癌的AUC达0.85,阳性预测值85%,展示了作为大规模癌症筛查工具的实际临床潜力。
图文导读
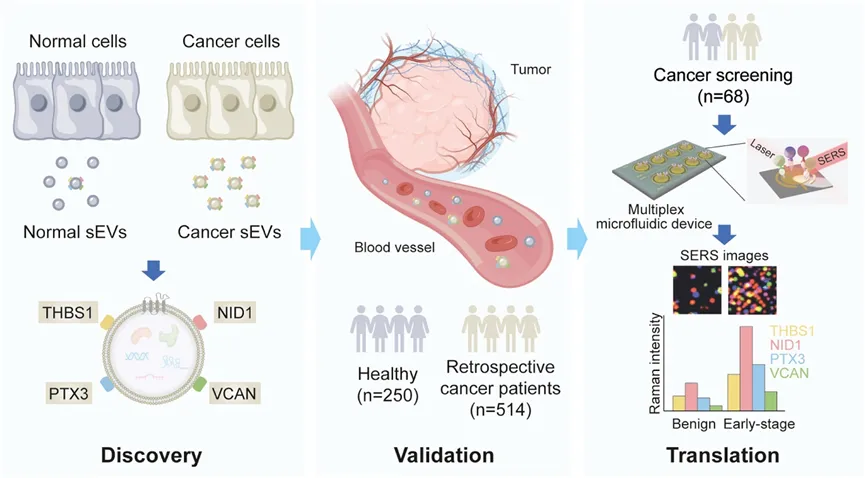
图1(原文 Fig. 1)图注:研究图示总结。 在发现阶段,通过质谱对源自同源HBEC模型的sEVs进行蛋白质组分析,发现了一个4蛋白生物标志物面板(THBS1、NID1、PTX3和VCAN)。该生物标志物面板在ELISA从22个癌细胞系分离出的sEVs中进行了测试。在验证阶段,招募了250名健康个体和514名多癌症患者组成的队列,以评估生物标志物面板的表现。通过ELISA分离并分析了血浆/血清的SVs。在翻译阶段,开发了一种结合SERS的多路复用微流控装置,用于在肺癌筛查环境中同时分析4蛋白生物标志物面板。4种蛋白质的表达水平通过对应拉曼报告的拉曼强度反映。
图片解析:
整体概括了本研究的三大阶段:发现、验证与转化。在发现阶段,研究者利用等基因的人类支气管上皮细胞模型,通过p53敲低和KRAS过表达诱导恶性转化,进而筛选出四种在转化细胞来源的小细胞外囊泡中显著高表达的蛋白——THBS1、NID1、PTX3和VCAN,构成诊断标志物组合。验证阶段中,该四蛋白标志物在22种癌细胞系和764例血浆/血清样本中进行了回测,涵盖9种癌症类型,表现出优异的诊断性能,曲线下面积值达0.91–1.00,并能有效识别I期癌症患者。转化阶段则开发了一种基于微流控和表面增强拉曼散射技术的多通道检测设备,实现对四蛋白标志物的同时检测,并在前瞻性肺结节患者队列中成功区分良性与恶性病变。
图文导读
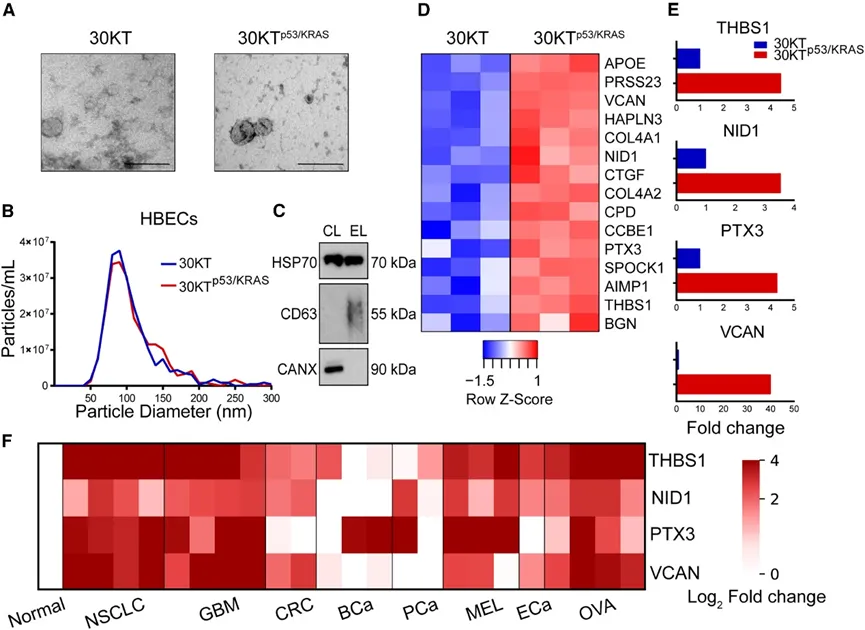
图2(原文 Fig. 2)图注:转化诱导细胞源性sEV蛋白组成的变化。(A) 通过透射电子显微镜评估了分离 sEV 的形态。正常和转化后的 HBEC 衍生 sEV 图像(比例条,200 nm)。(B)利用可调电阻脉冲传感分析从HBEC分离的sEVs,显示大多数sEV的尺寸范围在30至150 nm之间,且转化不会导致sEV分泌增加。(C)HBECs的sEV的western blot显示sEV蛋白HSP70和CD63的存在,且细胞标志物Calnexin缺失。(D) 无标记质谱法鉴定出148种蛋白在转化HBEC(FDR<0.02)衍生的sEV中含量更高,其中15种被标记为细胞外蛋白。(E) 利用ELISA确认了THBS1、NID1、PTX3和VCAN在正常和转化HBECS衍生的sEV中的质谱结果。(F)来自22个癌细胞系的sEV,包括非小细胞肺癌(SKMES1、H1650、HCC4006和H2170)、胶质母细胞瘤(GBM、D54、D270、U87和U118)、结直肠癌(CRC、HT29和SW620)、乳腺癌(BCa、BT549、MDA231和MDA436)、前列腺癌(PCa、PC3和LNCa36) P)、黑色素瘤([MEL]、A375、MAMEL65和SKMEL28)、食管癌([ECa]、OE19)和卵巢癌([OVA]、A2780、CAOV3、IGROV1和OVCAR8)在正常细胞中sEV的平均水平([HBEC] 30KT、HOSE 6.3和HOSE 17)中,THBS1、NID1、PTX3和VCAN的表达明显增加。
图片解析:
展示了通过等基因HBEC模型发现sEV蛋白标志物的核心实验流程。研究发现,经p53/KRAS转化的HBEC细胞所分泌的sEV,在形态、粒径和标志蛋白表达上均符合典型sEV特征。通过质谱分析,研究者鉴定出327个在正常与转化细胞sEV中表达差异显著的蛋白,其中15个为细胞外蛋白,具备作为体液检测靶点的潜力。最终选取THBS1、NID1、PTX3和VCAN四个蛋白,因其在肿瘤进展中具有明确功能,并已被证实可表达于sEV表面,便于抗体捕获。ELISA验证结果显示,这四个蛋白在转化细胞sEV中均显著升高。
图文导读
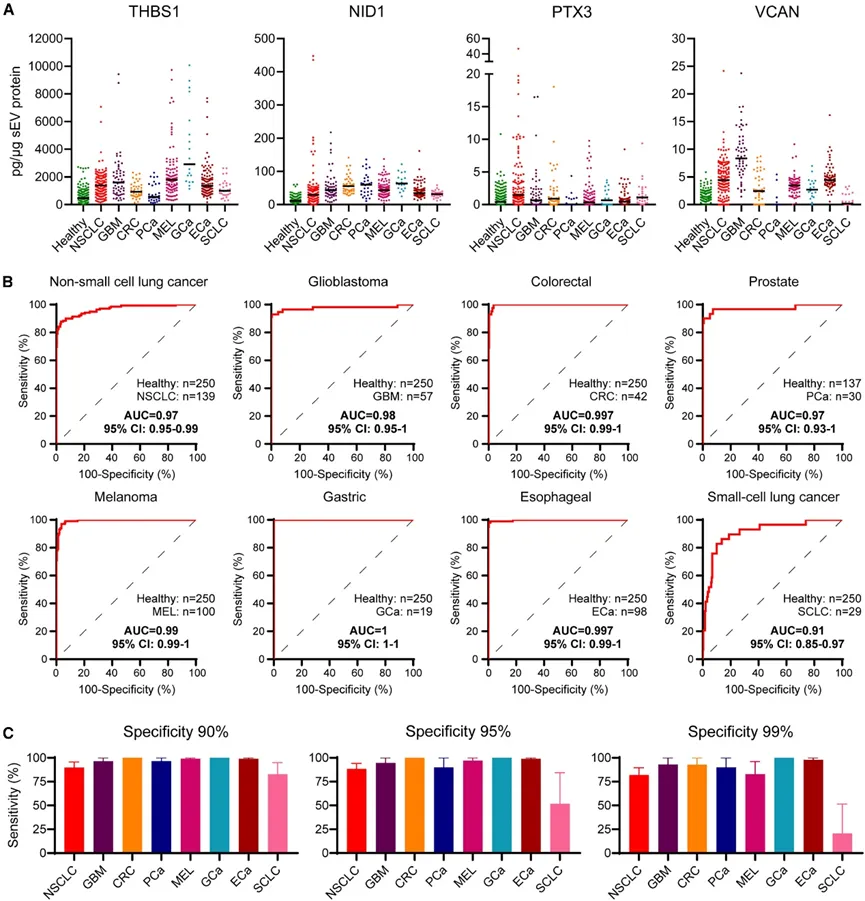
图3(原文 Fig. 3)图注:转化后的sEV特征准确诊断患者血浆中的癌症。(A)癌症患者提取血浆中THBS1、NID1、PTX3和VCAN的表达水平较健康对照组有所提升。样本以三倍计量。点图中的线条表示中位数值。(B)每种癌症类型与健康对照组的ROC分类曲线显示,4蛋白sEV生物标志物组合的诊断能力优异,AUC为0.91–1。(C) 每种癌症类型的诊断性SV特征的敏感性在固定的90%、95%和99%下进行评估。误差条代表95%置信区间。健康(n = 250)、非小细胞肺癌(n = 139)、胶质母细胞瘤([GBM], n = 57)、结直肠癌([CRC], n = 42)、前列腺癌([PCa], n = 30)、黑色素瘤([MEL], n = 100)、胃癌([GCa], n = 19)、食管癌([ECa], n = 98)、小细胞肺癌([SCLC], n = 29)。
图片解析:
该四蛋白标志物在764例临床样本中的诊断性能,与健康对照组相比,癌症患者血浆中THBS1、NID1、PTX3和VCAN的表达水平均显著升高。通过受试者工作特征曲线分析,各癌种的AUC值在0.91至1.00之间,表现出极高的区分能力。在90%、95%和99%的特异性水平下,该标志物组合对各癌种的敏感性均保持较高水平,尤其在非小细胞肺癌、胶质母细胞瘤、结直肠癌、黑色素瘤等癌种中表现突出。图中还涵盖了胃癌、食管癌、小细胞肺癌等较难早期诊断的癌种,验证了该标志物的广谱适用性。该结果表明,基于sEV蛋白的多标志物组合可作为一种高效、非侵入性的血液检测工具,适用于多种癌症的早期筛查。
图文导读
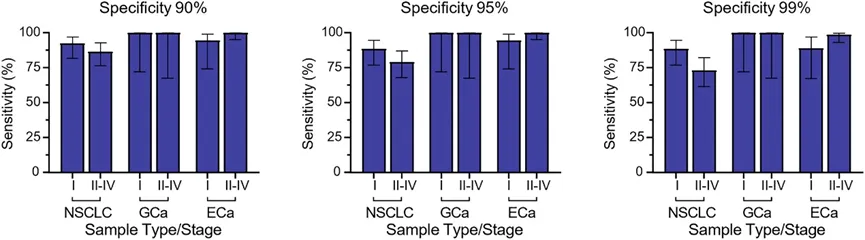
图4(原文 Fig. 4)图注:根据肿瘤分期诊断性SV特征的敏感性。诊断性sEV特征能够诊断NSCLC早期疾病(I期)及晚期疾病(II-IV期),特异性分别为90%、95%和99%,包括非小细胞肺癌(I期,n=52;II-IV期,n=67)、GCa(I期,n=10;II-IV期,n=8)和ECa(I期,n=18;II-IV期n=77)。误差条代表95%置信区间。
图片解析:
重点分析了该四蛋白标志物在早期(I期)与晚期(II–IV期)癌症中的诊断敏感性。在非小细胞肺癌、胃癌和食管癌中,研究者分别评估了在90%、95%和99%特异性下的敏感性表现。结果显示,无论是在I期还是晚期患者中,该标志物组合均能保持较高的敏感性,尤其在NSCLC的I期患者中,敏感性接近晚期水平。这表明该sEV蛋白标志物不仅适用于进展期癌症,也具备检测早期、局部性肿瘤的能力,而早期诊断正是提高癌症生存率的关键。该图还通过误差线展示了95%置信区间,增强了统计可信度。验证了该标志物在早期癌症筛查中的临床潜力,弥补了现有液体活检技术在早期阶段敏感性不足的缺陷。
图文导读
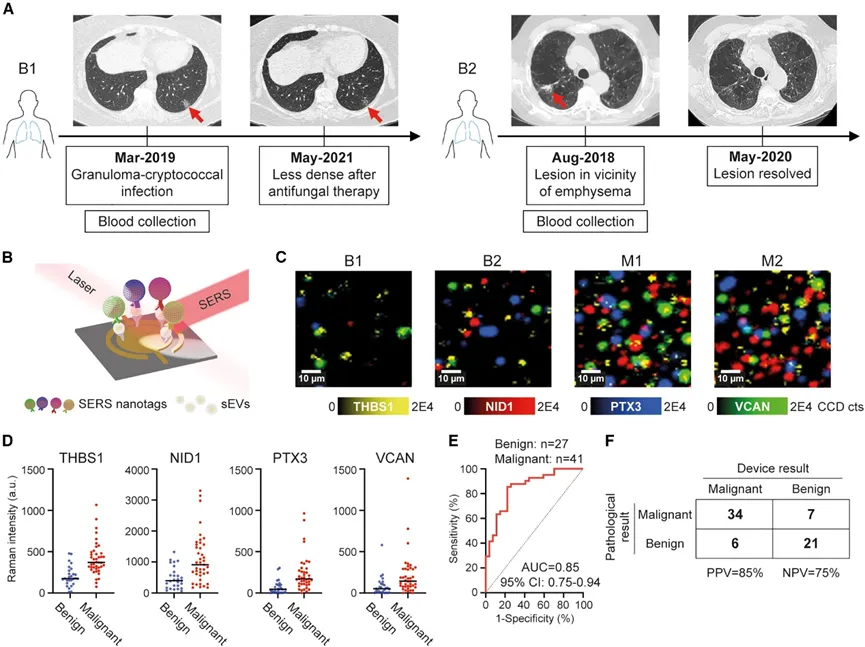
图5(原文 Fig. 5)图注:适用于癌症筛查环境中液体活检检测的多路复用微流控装置评估(A)对2名代表性良性患者B1和B2进行CT影像临床随访。红色箭头表示患者肺部结节。B1患有肉芽肿-隐球菌感染,26个月后病灶密度降低。B2在肺气肿附近有一个病灶,21个月后痊愈。(B)由一对非对称圆形电极组成的多路复用微流控器件示意图。电极与抗THBS1抗体结合,以捕捉癌症源性SVs。携带指定拉曼报告器和配对靶抗体(针对THBS1、NID1、PTX3和VCAN)的SERS纳米标签用于标记捕获的sEV,随后通过SERS定位分析。(C)代表性假色SERS光谱图像,显示早期非小细胞肺癌患者(M1和M2)中THBS1、NID1、PTX3和VCAN的富集,而非良性疾病患者(B1和B2)患者。(D)良性(n=27)和早期NSCLC(n=41)患者中,每种生物标志物THBS1、NID1、PTX3和VCAN的拉曼强度。样本被测量为三份。点阵图中的线代表中位数值。(E)逻辑回归分类的ROC曲线,显示在癌症筛查环境中早期NSCLC病例检测率为0.85,优于良性病例。(F) 多路复用微流控器件的混淆矩阵。
图片解析:
展示了该研究的技术转化核心,一种集成纳米剪切微流控和SERS技术的多通道检测设备,并在68例肺结节患者的前瞻性队列中验证其临床实用性。所有患者均接受CT检查并随后进行活检或长期随访,最终确诊27例为良性病变,41例为早期肺癌。设备通过捕获sEV并同时检测四种蛋白标志物,能够有效区分恶性与良性病变。四蛋白联合分类器的AUC为0.85,阳性预测值为85%,阴性预测值为75%。研究还通过对12例NSCLC患者手术前后血浆样本的纵向分析,发现术后标志物水平显著下降,进一步证实了该标志物与肿瘤存在的相关性。
总结与展望
研究通过等基因细胞模型筛选出THBS1、NID1、PTX3和VCAN四个小细胞外囊泡蛋白标志物,并在764例临床样本中验证了其对多种早期癌症的高灵敏度与特异性。结合微流控-SERS多通道检测设备,研究进一步在前瞻性肺结节患者中准确区分良恶性病变。该策略为无创、规模化癌症早筛提供了可行工具。未来,该技术有望拓展至更多癌种、整合其他生物标志物,并推动临床转化,实现真正意义上的泛癌早期筛查与个体化监测。
DOI:
https://doi.org/10.1016/j.xcrm.2026.102694
原文链接:
https://www.sciencedirect.com/science/article/pii/S2666379126001114
 夜雨聆风
夜雨聆风




